宣痹洗剂中羟基红花黄色素A的含量测定
汤化琪 张志千 汪文琪 李丹丹 夏坤 苏爽 王景红 孙毅坤
1.北京中医药大学中药学院,北京100102;2.中国中医科学院望京医院药学部,北京100102
宣痹洗剂中羟基红花黄色素A的含量测定
汤化琪1张志千1汪文琪1李丹丹1夏坤2苏爽2王景红2孙毅坤1
1.北京中医药大学中药学院,北京100102;2.中国中医科学院望京医院药学部,北京100102
目的测定宣痹洗剂中羟基红花黄色素A的含量。方法采用高效液相色谱法,以羟基红花黄色素A含量为指标,通过正交试验确定正丁醇萃取的最佳条件并测定其含量。结果宣痹洗剂中羟基红花黄色素A的最佳正丁醇萃取条件为正丁醇用量60 mL,萃取4次,每次振摇50 s,各因素影响顺序为正丁醇用量>萃取次数>振摇时间,测得宣痹洗剂中羟基红花黄色素A的含量为0.39μg/mL,平均回收率为97.06%,RSD=1.4%(n=6)。结论本研究建立的正丁醇萃取方法与含量测定方法简便快速、精密度高,可用于该制剂的质量控制。
宣痹洗剂;羟基红花黄色素A;正丁醇萃取;含量测定;高效液相色谱法
宣痹洗剂是由威灵仙、红花等药材经水煎煮制成的复方制剂,具有散寒除湿、活血止痛之功效,临床用于治疗痹症寒湿闭阻、淤血阻络证,症见膝关节疼痛,局部畏恶风寒、活动不利、蹲起困难,下肢沉重,晨僵,舌淡苔白,脉弦;膝关节骨关节炎见上述证候者。红花为本方臣药,是菊科植物红花Carthamus tinctorius L.的干燥花,《本草纲目》中记载红花有“活血、润燥、止痛、散肿、通经”之功效,因此备受国内外学者关注。红花所含成分主要为色素、黄酮类、挥发油、脂肪酸、酚酸等[1-2]。其中羟基红花黄色素A,是红花活血化瘀有效成分之一,其在1993年被Meselhy等人首次分离得到,是红花黄色素的主要成分,《中国药典》2010年版一部规定以其作为红花中的代表性活性成分进行含量测定,多被用于红花相关制剂质量标准的含测指标[3-4]。为保证药品质量,本研究对宣痹洗剂中羟基红花黄色素A的含量测定进行了研究,采用正交设计优化了正丁醇萃取的前处理方法,结果表明,该方法简便、准确、重复性好,可用于该制剂的质量控制。
1 仪器与试药
1.1 仪器
1100型高效液相色谱仪(UV检测器,美国Aglient公司);AE-240型电子天平(瑞士Mettler公司)。
1.2 试药
羟基红花黄色素A对照品(中国食品药品检定研究院,批号:111637-200502);宣痹洗剂样品(批号:121201、121202、121203)由中国中医科学院望京医院制剂中心提供;甲醇为色谱纯,实验用水为纯净水,其他试剂均为分析纯。
2 方法与结果
2.1 色谱条件
采用Waters Symmetry Shiled-RP18(150 mm×4.6 mm,5μm)色谱柱,以0.1%磷酸甲醇-0.1%磷酸(29∶71)为流动相,流速1 mL/min,检测波长403 nm,柱温25℃。
2.2 对照品溶液的制备
精密称取羟基红花黄色素A对照品适量,加25%甲醇制成每1毫升含10.0μg的溶液,摇匀,即得。
2.3 供试品溶液的制备
精密量取样品50.0 mL,置分液漏斗中,加水饱和正丁醇60 mL,振摇萃取4次,每次50 s,分取正丁醇液,蒸干,残渣加25%甲醇使溶解并转移至5 mL棕色量瓶中,加25%甲醇稀释至刻度,摇匀,即得。
2.4 正丁醇萃取方法研究
以羟基红花黄色素A的含量为指标,采用L9(34)正交设计表,以正丁醇用量、萃取次数、振摇时间为考察因素进行正交试验[5-6],正交试验因素水平与结果见表1~3。
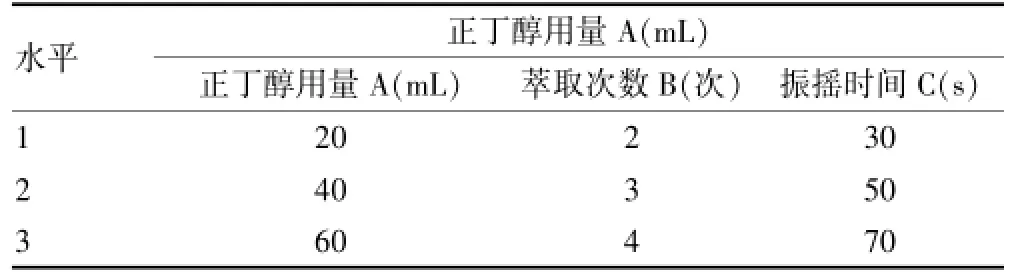
表1 正交试验因素水平表
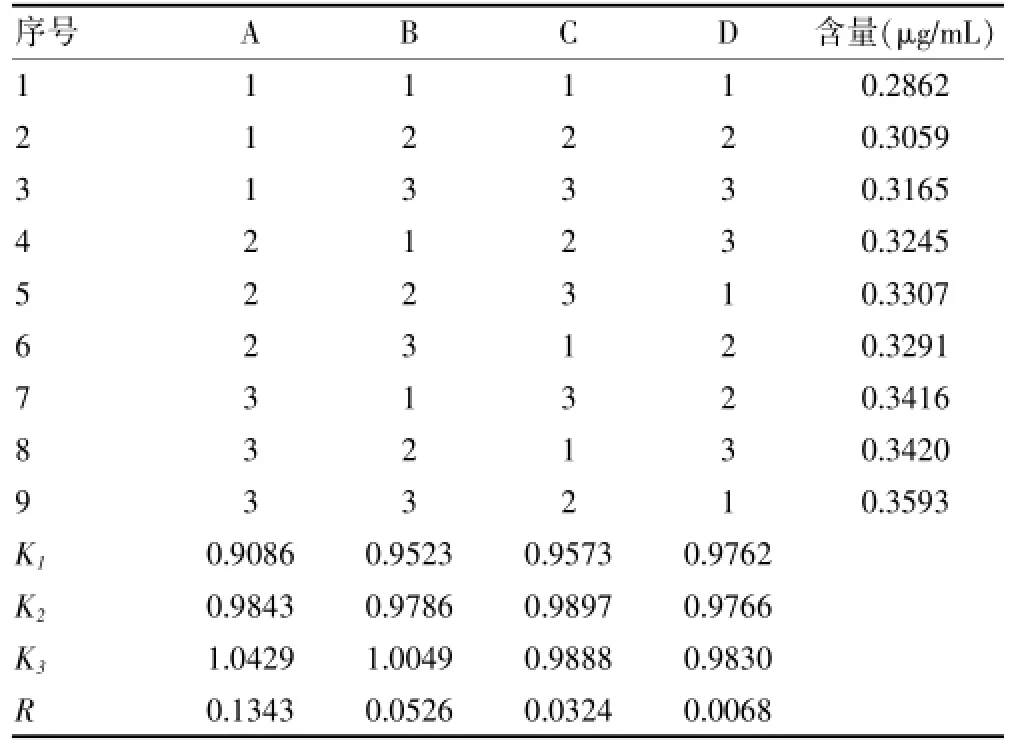
表2 正交试验结果
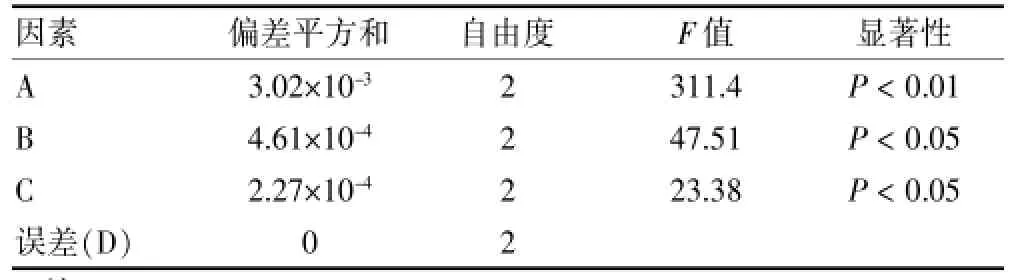
表3 方差分析
由表2可知,正交试验极差R的大小顺序为A>B>C,即影响宣痹洗剂中羟基红花黄色素A得率的各因素主次关系依次为正丁醇用量>萃取次数>振摇时间,其中正丁醇用量对得率的影响极显著,其次为萃取次数与振摇时间,而振摇50 s与振摇70 s的萃取效果基本接近,为节省时间,故选择50 s作为振摇时间,因此确定最佳萃取条件为A3B3C2,即正丁醇用量60 mL,萃取4次,每次振摇50 s。
2.5 阴性样品溶液的制备
按处方比例与工艺制备不含红花的阴性样品,按“2.3”项下方法制备阴性样品溶液。在上述色谱条件下,对照品、样品及阴性样品的液相色谱图见图1。结果表明,样品中其他成分对羟基红花黄色素A的测定无干扰。
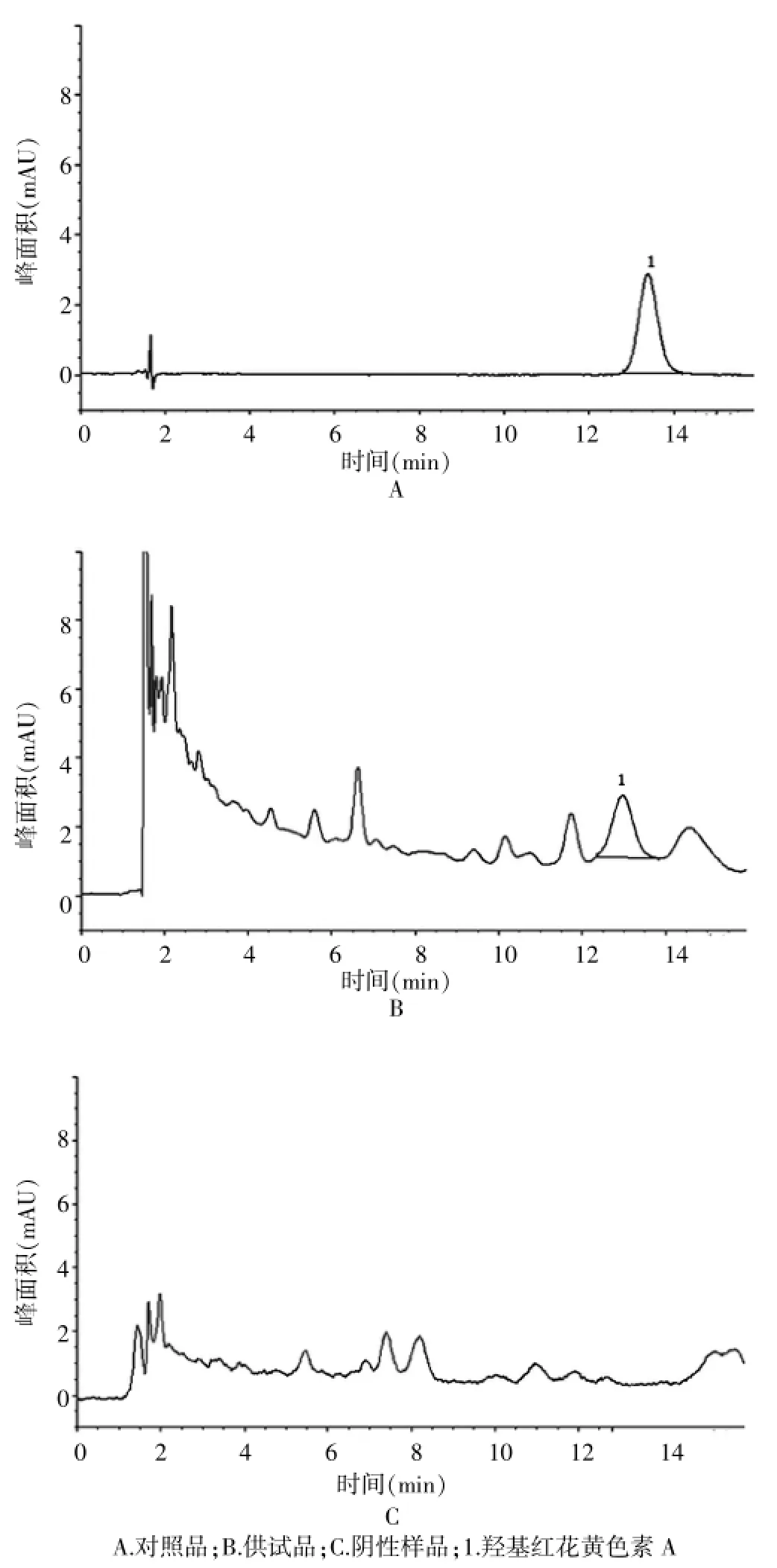
图1 宣痹洗剂高效液相色谱图
3 方法学考察
3.1 线性关系考察
分别精密吸取对照品溶液4、6、8、10、12、14μL,注入高效液相色谱仪,记录峰面积。以进样量X(μg)为横坐标,峰面积Y为纵坐标绘制标准曲线,得回归方程为Y=917.17X+0.16,r=0.9997(n=6)。结果表明,羟基红花黄色素A进样量在0.04~0.14μg范围内线性关系良好。
3.2 精密度试验
精密吸取对照品溶液10μL,连续进样6次,测定峰面积,RSD为1.73%,表明仪器精密度良好。
3.3 重复性试验
精密量取样品6份,分别按“2.3”项下方法,以上述最佳萃取方法制备供试品溶液,并按“2.4”项下色谱条件进样20μL,测定峰面积,计算含量。结果羟基红花黄色素A的平均含量为0.3757μg/mL,RSD为2.0%,表明该方法重复性良好。
3.4 稳定性试验
取同一供试品溶液,分别于制备后0、2、4、6、8、10、12、24 h进样20μL,测得峰面积的RSD为1.8%,结果表明供试品溶液在24 h内基本稳定。
3.5 加样回收率试验
精密量取已知含量(0.3757μg/mL)的同批样品25 mL共6份,分别置分液漏斗中,精密加入对照品溶液(10.02μg/mL)各1.0 mL,分别按“2.3”项下方法,以上述最佳萃取方法制备供试品溶液,按“2.4”项下色谱条件进样20μL,计算回收率,结果见表4。
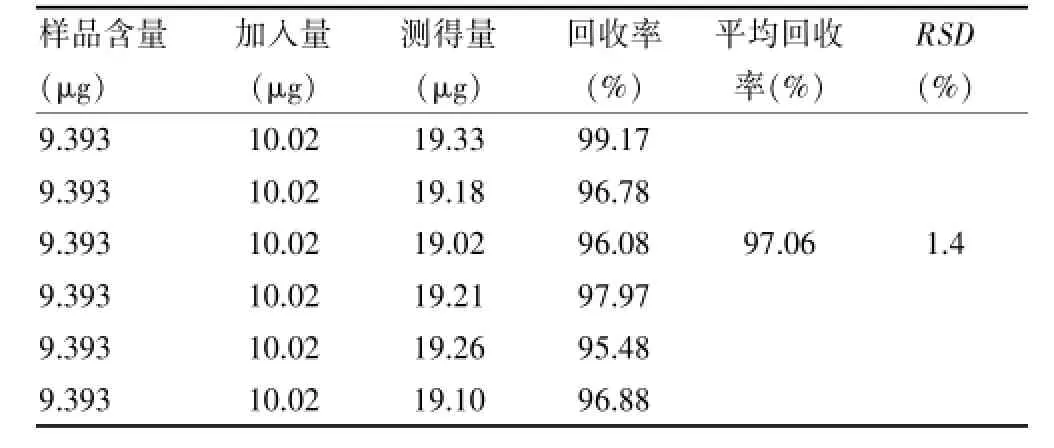
表4 加样回收率试验结果
3.6 样品测定
取不同批次样品5份,分别按“2.3”项下方法,以上述最佳萃取条件制备供试品溶液,按“2.4”项下色谱条件进样20μL,以外标法计算得到其中羟基红花黄色素A的含量为0.39μg/mL,RSD为1.5%。
4 讨论
羟基红花黄色素A是红花中主要成分之一,具有活血化瘀、通脉止痛等功效。现代研究表明,羟基红花黄色素A可以扩张冠状动脉、改善心肌缺血,降低血压,保护脊髓出血/再灌注损伤,具有抗凝、抗血小板聚集和血管再通作用,能有效缓解不稳定性心绞痛(UA)、降低纤维蛋白原浓度、清除自由基、控制心绞痛的发作及向心肌梗死的转化、抗疲劳及耐缺氧等药理作用。
目前,羟基红花黄色素A的提取、分离以及纯化工艺得到了很大的改进,且其在红花中含量的定量分析方法先进,体内的药物代谢方式也已明确。且其多项药理作用虽然已有报道,但仍然是国内外研究的热点,一方面是其在靶细胞及分子水平的作用机制尚有待于进一步深入探究;另一方面是与其他中药活性组分的配伍所产生的新疗效及其作用机制需要在分子、细胞、整体动物多个层次予以系统揭示。因此,这就需要对不同制剂中羟基红花黄色素A的提取、分离、纯化等处理手段以及含量测定进行进一步深入的研究。
正交试验设计和分析方法是目前最常用的工艺优化试验设计和分析方法,是部分因子设计的主要方法。正交试验以概率论、数理统计和实践经验为基础,利用标准化正交表安排试验方案,并对结果进行计算分析,最终迅速找到优化方案,是一种高效处理多因素优化问题的科学计算方法。正交设计法就是利用正交表处理多因素多水平试验的一种科学方法。该法能以尽可能少的试验次数,获得最满意的试验结果,筛选出最佳试验条件,找出影响试验结果的主要因素,从而为在医药科学研究中多因素多水平问题提供了科学的、合理的解决途径,并日益广泛地应用于中药研究中。在工艺条件的优选工作中具有广阔的应用前景,只是在用正交设计法探讨工艺条件时,受测试指标及所选因素、水平的影响很大,这样选择科学合理的测试指标、因素、水平就成了整个实验的重要步骤,对能否获得最佳工艺参数具有重要意义。
本研究以宣痹洗剂为载体,以羟基红花黄色素A含量为考察指标,采用正交试验优化得到正丁醇最佳萃取条件为:正丁醇用量60 mL,萃取次数4次,振摇时间50 s,并测得其中羟基红花黄色素A的含量为0.39μg/mL。
在羟基红花黄色素A含量测定研究中,参照《中国药典》2010年版及相关文献[7-12],对流动相选择与比例、柱温、检测波长等因素进行了考察。因干扰峰的存在,对流动相进行调整,经比较选定0.1%磷酸甲醇-0.1%磷酸(29∶71)为流动相时最佳。羟基红花黄色素A是具有单查耳酮苷类结构的化合物,极性较强,且呈酸性,在流动相中加入少量磷酸以抑制其离解,可改善其峰形及分离效果。
刘亮等[5]的研究结果表明,振摇时间对萃取效果无显著性影响,而本研究结果却发现振摇时间对萃取效果有显著影响,这可能是因为振摇时间太短,样品溶液不能与正丁醇充分混合,从而影响萃取效果所造成。而本研究结果亦显示振摇时间为50 s与70 s时萃取效果接近,这可能是振摇50 s时样品即与正丁醇充分混合,故选择50 s作为最佳萃取时间,在节省时间的同时,达到了最佳萃取效果。
通过预实验比对发现,如未进行正丁醇萃取,宣痹洗剂中其他成分对羟基红花黄色素A的干扰明显,无法进行含量测定,从而进行萃取,而正丁醇萃取宣痹洗剂中羟基红花黄色素A的过程是利用羟基红花黄色素A与杂质在水与正丁醇2种互不相溶的溶剂中的溶解度或分配系数之间的差异,通过多次分配而实现分离[13],而羟基红花黄色素A在水饱和正丁醇中具有较大溶解度,所以本试验用水饱和的正丁醇作为纯化萃取的溶剂,具有纯化效果好,操作简便,用时短等优点。且羟基红花黄色素A是具有单查耳酮苷类结构的化合物[14-15],其分子结构中具有不稳定基团,在提取、分离、纯化过程中易发生氧化、水解、聚合等反应,将使其结构、药理作用等发生变化[16]。
宣痹洗剂为北京中医药“十病十药”入选项目,临床效果显著,但仍缺少相应质量控制标准,尤其是对其中主成分的含量测定方法尚无相关研究,本研究对其中羟基红花黄色素A的含量测定方法进行了研究,为该药的质量控制提供了理论参考。
[1]郭宇飞,申丹,杨洪军.含红花中药组方规律分析[J].中国中医杂志,2014,39(11):2144-2148.
[2]姜华.羟基红花黄色素A对大鼠脑缺血-再灌注损伤的保护作用及机制[J].中药材,2013,36(3):462-464.
[3]张国霞,王维波,陈德道,等.红花中羟基红花黄色素A的加速稳定性研究[J].中国实验方剂学杂志,2014,20(15):86-88.
[4]何春龙,王焕芸,莎日娜.HPLC法测定清热八味散中羟基红花黄色素A的含量[J].现代中药研究与实践,2014,28(1):69-72.
[5]刘亮,杜江,姚丽,等.苗药观音草正丁醇萃取工艺的研究[J].中国民族民间医药,2011,20(20):5-6.
[6]陈建平,王金辉,汤化琪,等.蒙药瞿麦中多糖超声提取工艺研究及含量测定[J].中南药学,2013,11(4):264-267.
[7]国家药典委员会.中国药典[S].一部.北京:中国医药科技出版社,2010:141.
[8]王焕芸,冯欣,武娜.RP-HPLC测定七味葡萄散中羟基红花黄色素A的含量[J].中国新药杂志,2010,19(16):1465-1467.
[9]杨红,陈岳蓉,刘海青.RP-HPLC测定骨筋丸胶囊中羟基红花黄色素A、落干酸和龙胆苦苷的含量[J].药物分析杂志,2014,34(3):423-427.
[10]张建业,陈星,孙云峰,等.RP-HPLC法同时测定新生化颗粒中羟基红花黄色素A、阿魏酸和甘草酸铵[J].中成药,2014,36(2):310-313.
[11]赵国英,袁秀荣,李玲,等.鹿红颗粒中黄芪甲苷和羟基红花黄色素A的含量测定[J].中国实验方剂学杂志,2014,20(6):40-43.
[12]何梅凤,吴伟,邓新国,等.HPLC法测定兔房水中羟基红花黄色素A[J].中成药,2014,36(7):1558-1560.
[13]丁越,张彤,陶建生,等.正丁醇萃取技术制备高纯度栀子苷的工艺研究[J].中国新药杂志,2012,21(14):1596-1599.
[14]童文,孙佩,杨晓,等.红花花色与羟基红花黄色素A的相关性初探[J].西南农业学报,2011,24(1):101-104. [15]唐红,舒华,周文飞,等.红花中羟基红花黄色素A的纯化工艺研究[J].广州化工,2014,(15):67-69,79.
[16]杨小虎,王丹丹,朱彦,等.羟基红花黄色素A的现代研究新进展[J].湖南中医药大学学报,2013,33(3):102-106.
Content determination of Hydroxy Safflor Yellow A in Xuanbi Lotion
TANGHuaqi1ZHANGZhiqian1WANGWenqi1LIDandan1XIAKun2SUShuang2WANGJinghong2SUNYikun1
1.School of Materia Medica,Beijing University of Chinese Medicine,Beijing 100102,China;2.Department of Pharmaceutical,Wangjing Hospital of China Academy of Chinese Medical Sciences,Beijing 100102,China
ObjectiveTo determine the content of Hydroxy Safflor Yellow A(HSYA)in Xuanbi Lotion.MethodsThe content of HSYA,measured by HPLC,was used as the evaluation index to determine the optimum N-butanol extraction condition by orthogonal experiment.ResultsThe content of HSYA in Xuanbi Lotion was 0.39μg/mL,the average recovery rate was 97.06%,RSD=1.4%(n=6),which was determined in the optimum extraction condition of 60 mL N-butanol,extracting for 4 times,shaking 50 s every time,and the effect order of the three factors was volume of N-butanol>extraction times>shaking time.ConclusionThe method of N-butanol extraction and content determination established by this study is convenient,rapid and precise,which can be used to control the quality of Xuanbi Lotion.
Xuanbi Lotion;Hydroxy Safflor Yellow A;N-butanol extraction;Content determination;HPLC
R284.2
A
1673-7210(2015)04(c)-0129-04
2015-01-19本文编辑:卫轲)
北京中医药“十病十药”研发项目(编号SBSY 2013-003)。
汤化琪(1992.11-),男,北京中医药大学2014级药物分析专业在读硕士研究生。
王景红(1965.9-),女,主任药师,中国中医科学院望京医院药学部处长;研究方向:医院药学、临床药学、医院制剂。孙毅坤(1965.1-),男,博士,教授,北京中医药大学中药学院中药分析系主任;研究方向:药效物质基础及药品质量控制。

