精准肝切除在肝中叶肿瘤切除中的应用
张新俊,王晓云,王彦坤,陈 磊,胡 磊,高 波
(1.云南省第一人民医院肝胆外科,昆明 650032;2.昆明医科大学临床实训中心,昆明 650041)
精准肝切除在肝中叶肿瘤切除中的应用
张新俊1,王晓云1,王彦坤1,陈 磊1,胡 磊1,高 波2△
(1.云南省第一人民医院肝胆外科,昆明 650032;2.昆明医科大学临床实训中心,昆明 650041)
目的 评价精准肝切除在肝中叶肿瘤切除中的临床应用价值。方法回顾分析云南省第一人民医院36例肝中叶肿瘤患者,其中24例肝中叶肿瘤患者(精准肝切除组)应用精准肝切除手术方法行肝中叶切除,另外8例(Pringle组)行Pringle法阻断快速切除。比较两组不同手术方式患者的临床资料。结果精准肝组与Pringle组比较,术后凝血酶原时间、总胆红素比较差异无统计学意义(P>0.05);手术时间、术中出血、术后谷草转氨酶、谷丙转氨酶、并发症发生率、围术期病死率比较差异有统计学意义(P<0.05)。其中精准肝切除组未发生与本术式相关的并发症。结论精准肝切除术是解决肝中叶肿瘤肝内“手术高危区”解剖的安全、有效的方法。
肝切除术;肝肿瘤;精准肝切除;肝中叶切除
随着肝切除技术的不断完善和进步,尤其在成人活体肝移植技术的推动下,精准肝切除技术得到蓬勃发展。云南省第一人民医院肝胆外科自2009年开展精准肝中叶切除术,效果满意,现作如下经验探讨。
1 资料与方法
1.1 一般资料 选择2009~2012年间肝中叶肿瘤患者32例,其中男21例,女11例,年龄23~65岁。全组Child分级A级,吲哚氰氯15 min滞留率(ICGR 15 min)均小于10%,自终末期肝病模型(MELD)评分均小于10分。其中原发性肝癌9例,高位胆管癌7例(Bithmus分级Ⅳ级),肝血管瘤10例,胆囊癌6例(Neven′s分级Ⅳ级)。其中应用精准肝切除24例肝中叶肿瘤患者(精准肝切除组)。另外8例行Pringle法阻断快速切除(Pringle组)。
1.2 方法
1.2.1 术前评估 精准肝中叶切除手术方法要求术前最精确的评估包括:(1)患者完善的螺旋CT检查,CT血管造影术(CTA)检查,然后根据重建的肝动脉、门静脉、肝静脉片进行评估;(2)评估肝内肿瘤和肝内结构的CTA影像学关系,了解肿瘤占据的肝段、与周围血管的关系、是否有重要血管的侵犯;(3)评估肝脏拟切除后是否损伤剩余左右肝的正常功能;(4)术中精细操作,注意辨别肝外、肝内重要的地标性血管,避免损伤;(5)建立术后精确管理理念等外科治疗全过程[1]。本组病例均经过术前CTA精确评估,具备一定的手术条件。
1.2.2 手术方法 精准肝切除手术手术方案:(1)是否需要行局部肝叶、肝段的血流阻断。(2)仔细解剖第一肝门,其中Ⅳb段、Ⅴ段切除选择不阻断;Ⅷ段切除也选择不阻断;Ⅴ、Ⅷ段切除选择肝右前叶肝动脉、门静脉右前支阻断;Ⅳ、Ⅴ、Ⅷ段切除选择先阻断肝右前动脉、门静脉右前支,待右侧肝离断基本完成后,再阻断肝左动脉(或左内叶动脉,大概有30%左肝动脉在肝外分出左外和左内动脉)、门静脉左支。有左肝静脉侵犯的患者,行扩大左半肝切除,Ⅴ、Ⅷ段肝静脉与下腔静脉重建;有右肝静脉侵犯的患者,在术前评估左肝剩余肝体积够患者代偿者,行肝中叶和肝Ⅶ段切除,肝右后静脉与下腔静脉重建。(3)术中精细解剖操作:用超声吸引刀切开肝实质,2 mm以内的肝内脉管(Glisson)结构和1 mm以内的静脉用电刀烧灼,其余用钛夹或丝线结扎,明确的小出血点用5-0 Prolene线缝闭。拟切肝的地标血管应充分显露,最后用4-0 Prolene线缝闭。术中应注意控制中心静脉压在8 mm Hg左右,减少出血[2]。(4)标本切除后,肝断面均开放,有利于肝脏的再生修复,但应仔细检查肝断面是否存在出血、漏胆,然后用止血纱布覆盖肝断面,肝断面留置引流管充分引流。高位胆管癌患者因肝外胆管已切除,应于肝断面行二级胆管整形,行高位胆-肠吻合。手术步骤见图1(a、b、c 3例典型患者)。

2 结 果
精准肝切除组均采用精准肝切除成功实施肝中叶肿瘤切除,其中1例行扩大左半肝切除;Pringle组行肝中叶肿瘤切除1例,扩大左半肝切除3例,扩大右半肝切除1例,Ⅳ、Ⅴ段部分切除3例。患者术后围术期死亡1例,急、慢性肝功能衰竭和腹水发生4例,术后胆漏2例,腹腔脓肿4例,无出血再次手术。精准肝切除组与Pringle组比较,术后凝血酶原时间(PT)、总胆红素(TBIL)比较差异无统计学意义(P>0.05);手术时间、术中出血、术后谷草转氨酶(AST)、谷丙转氨酶(ALT)、并发症发生率、围术期病死率比较差异有统计学意义(P<0.05),见表1、2。
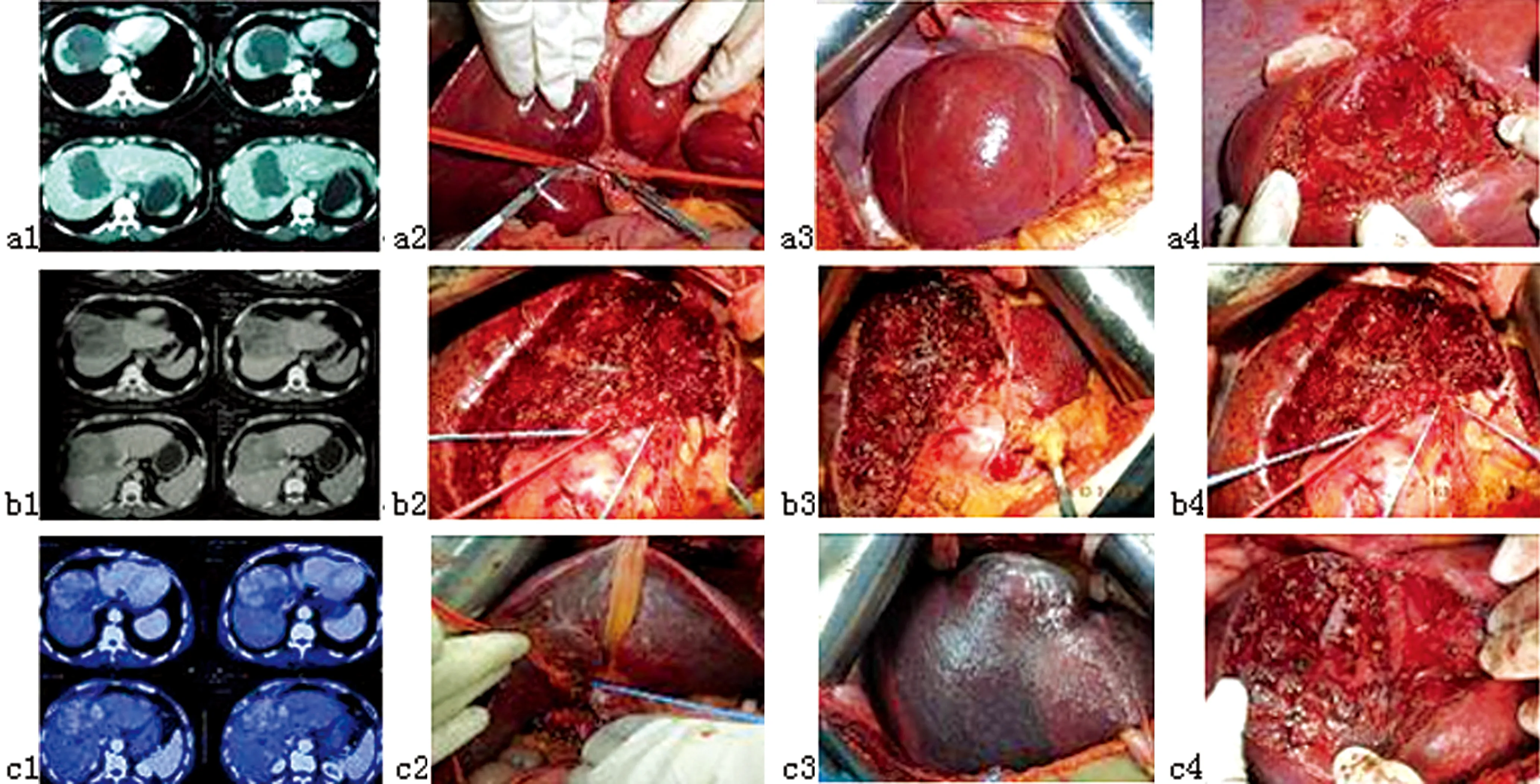
a1~c1:患者术前CT显示肿瘤位于肝脏Ⅴ,Ⅷ段;a2~c2:术中解剖右肝蒂;a3~c3:术中选择性阻断右前叶血供后显示;a4~c4:切除肿瘤后肝切面显示。
图1 3例肝脏中叶肿瘤患者精准肝切除手术方法图解

表1 精准肝切除组与Pringle组肝中叶肿瘤切除患者的术中和术后情况比较
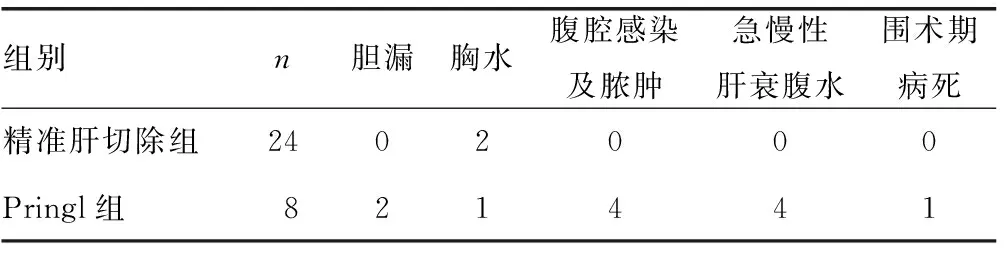
表2 精准肝切除组与Pringle组肝中叶肿瘤切除患者的术后并发症比较(n)
3 讨 论
3.1 肝中叶切除的困难与危险 肝中叶是肝左内叶和右前叶的总称,按照Couinaud分段,包括肝第Ⅳ、Ⅴ、Ⅷ段。肝中叶切除因为其复杂的肝内解剖结构,手术切除技术难度较大。如果处理不当可能术中大出血危及患者的生命,也有可能损伤保留的肝脏血管和胆管,从而影响剩余的肝脏功能,或者引起其他胆道并发症,诱发胆道狭窄、肝功能衰竭或小肝综合征,甚至造成患者死亡[3]。因此,术中控制出血、减少因肝血流阻断造成的热缺血和再灌注损伤是肝切除手术成功的关键[4]。
3.2 肝中叶切除的手术方式比较 肝中叶所占据肝脏的位置决定了肝中叶肿瘤切除的手术的复杂性,手术风险极高,被称为肝脏手术的十足雷区[5]。本组病例研究显示,通过术前精确评估,选择正确的手术方式十分必要。(1)精准肝中叶切除:该术式术前需精确评估肝脏的储备功能、肿瘤的位置、是否侵犯周围的重要血管。如需要行扩大的半肝切除,残余的肝脏功能需最大限度保护,残余肝体积是否够患者代偿,决定了手术的成败和患者的预后。术中充分游离第一肝门后,应用CTA指导前入路行肝中叶肿瘤切除。(2)常规第一肝门阻断的肝中叶切除:本术式第一肝门阻断需分次进行,每次持续15~20 min,间隔开放第一肝门5 min。因肝中叶手术操作复杂,持续时间长,对肝脏的损伤大,而且出血量大,术后易出现并发症、慢性肝功能衰竭,甚至造成患者死亡[6-7]。精准肝中叶切除最突出的优点在于最大限度地保留剩余肝脏的有效功能,通常比扩大的半肝切除多保留约35%的肝脏组织,有利于术后患者的尽早恢复,这对于合并有肝硬化的患者尤为重要。肝中叶切除需要有两个断面离断肝实质,创面较大,往往涉及第一、二、三肝门解剖结构,且在肿瘤切除过程中保证残余两侧肝脏的正常出入肝血流及胆管功能。肝创面有的学者主张对拢缝合,减少术后并发症。但这又对残余的肝脏血供和静脉回流造成不良影响[8],因此,创面就必须完全敞开。这就是肝中叶切除的难点。然而,常规的手术方法无法全面准确地解决这个问题,探寻新的手术方法显得尤为重要。通过对本组病例总结分析,作者认为精准肝中叶切除是肝中叶肿瘤切除的最佳手术方式。
3.3 精准肝中叶切除的应用前景 通过对本组病例临床资料的总结显示,精准肝切除是理论基础研究与技术操作的完美结合。明显较过去提高了肝中叶肿瘤的切除率。精准肝切除需要术前精确地进行肝内肿瘤﹑病变部位和肝内结构的影像学定位、评估,剩余肝脏体积的测定,肝脏储备功能的评估,术中不阻断或选择性阻断拟切除肝组织的入肝血流,应用CUSA刀等精细手术器械精细离断肝实质,精细处理肝断面[9-11]。精准肝切除与传统肝切除的不同和优势是它需要术前精确的影像学判断,指导解剖性前入路切肝途径,并对肝储备功能精确测定,剩余肝体积准确判断,不阻断肝血流或选择性地阻断拟切除的肝脏叶或段的血流,避免了剩余肝组织的热缺血损伤和再灌注损伤,同时,对肝内解剖的熟悉加仔细处理肝断面,可以最大限度地保留肝内重要的解剖结构,保证残余肝脏的正常功能,减少并发症。更重要的是手术者掌握足够的手术技巧[12]。在我国合并有肝硬化的肝肿瘤患者居多,扩大的半肝切除往往需要切除大约60%~85%的肝脏,这将大大增加术后肝功能衰竭的发生率和病死率[13-14]。而当较大的恶性肿瘤位于肝中叶时,必须决定采用保留一侧肝脏的半肝或扩大半肝切除术,还是保留两侧肝脏组织的肝中叶切除术。使用精确肝中叶切除既做到了有效、安全地切除肝脏肿瘤,又避免了术中大出血,并且做到了最大限度地保留了剩余肝脏的功能、减少了术后并发症、缩短了住院时间、提高了肝中叶肿瘤患者的手术切除率和生存率。本组病例资料说明精准肝切除是肝中叶切除可行之选,值得进一步推广。
[1]董家鸿.肝细胞癌治疗理念与策略的转变[J].中华消化外科杂志,2009,8(2):85-87.
[2]彭俊华.低中心静脉压在肝叶切除中的应用[J].中国误诊学杂志,2009,11(22):5382-5383.
[3]窦科峰,张巍.极量肝切除的技术思考[J].中国实用外科杂志,2008,28(9):736-739.
[4]张成武.复杂肝切除术的术前准备和术中处理[J].肝胆胰外科杂志,2013,2(1):1-4.
[5]戴朝六,彭松林,贾昌俊,等.中央区肝癌肝切除的手术体会[J].中国医学科学院学报,2008,30(4):460-464.
[6]Nanashima A,Tobinaga S,Abo T,et al.Left hepatectomy accompanied by a resection of the whole caudate lobe using the dorsally fixed liver-hanging maneuver[J].Surg Today,2011,41(3):453-458.
[7]Liu P,Qiu BA,Bai G,et al.Choice of approach for hepatectomy for hepatocellular carcinoma located in the caudate lobe:isolated or combined lobectomy?[J].World J Gastroenterol,2012,18(29):3904-3909.
[8]杨甲梅,陆炯炯.肝中叶切除术的评估与手术技巧[J].中国实用外科杂志,2010,30(8):672-673,690.
[9]吴健雄,钟宇新,荣维淇,等.选择性血流阻断配合超声乳化吸引刀切除中央型肝肿瘤[J].中华普通外科杂志,2008,23(12):907-910.
[10]Qiu Y,Zhu X,Zhu R,et al.The clinical study of precise hemihepatectomy guided by middle hepatic vein[J].World J Surg,2012,36(10):2428-2435.
[11]严广,黄志华,葛新国,等.中央型原发性肝癌42例外科治疗体会[J].中华普通外科杂志,2011,26(1):68-69.
[12]Dai WD,Huang JS,Hu JX.Isolated caudate lobe resection for huge hepatocellular carcinoma (10 cm or greater in diameter)[J].Am Surg,2014,80(2):159-165.
[13]Beard RE,Hanto DW,Gautam S,et al.A comparison of surgical outcomes for noncirrhotic and cirrhotic hepatocellular carcinoma patients in a Western institution[J].Surgery,2013,154(3):545-555.
[14]Torzilli G,Montorsi M,Del Fabbro D,et al.Ultrasonographically guided surgical approach to liver tumours involving the hepatic veins close to the caval confluence[J].Br J Surg,2006,93(10):1238-1246.
验交流·
10.3969/j.issn.1671-8348.2015.23.030
云南省卫生科技计划项目(2009NS013)。
张新俊(1968-),副主任医师,硕士,主要从事肝胆、胰、脾临床科研教学研究。
△通讯作者,E-mail:gbzhxw@sohu.com。
R657.3;R735.7
B
1671-8348(2015)23-3252-03
2015-02-12
2015-07-28)

