一种C50Cl10富勒烯氯化物新的生成机理的密度泛函理论计算
甘佐华 陈姝璇 谭 凯(厦门大学化学化工学院,固体表面化学国家重点实验室,福建省理论与计算化学重点实验室,福建厦门361005)
一种C50Cl10富勒烯氯化物新的生成机理的密度泛函理论计算
甘佐华 陈姝璇 谭 凯*
(厦门大学化学化工学院,固体表面化学国家重点实验室,福建省理论与计算化学重点实验室,福建厦门361005)
过去广泛接受#271C50Cl10是由#271C50空笼直接氯化得到.我们通过研究拓扑结构弄清了C50富勒烯之间的相互关系.利用密度泛函理论(DFT)计算从最稳定C50富勒烯#270C50出发,通过氯化和Stone-Wales(SW)转变获得#271C50Cl10.结果表明:氯化后最终产物是热力学最有利的,并且在有氯存在下,SW转变的活化能垒会降低.这些结果可以解释目前的相关实验事实,暗示了#270C50空笼先氯化得到不同#270C50氯化物,再进行两次SW旋转的路径,由于活化能垒更低因而是一条更为可行的路线.
密度泛函理论;Stone-Wales转变;氯化
1 引言
自从Ih对称性富勒烯C601被发现并被大量制备以来,其衍生物的化学及物理研究迅速发展.其中氯化富勒烯因其可作为进一步衍生化的中间体并具有一系列奇异的物理和化学性质吸引了许多科学家的关注,在许多领域有着潜在的应用前景. 2004年Xie等2利用电弧放电合成分离出C50Cl10后,相当多氯化富勒烯被陆续制备和表征.3-8近年来,实验上发现一系列含氯环境下通过Stone-Wales(SW)旋转而获得的不满足独立五元环原则(non-IPR)的氯化富勒烯,包括#1809C60Cl8,9#1804C60Cl12,10#18917C76Cl24,11#39173C82Cl2812和#283794C102Cl2013等.由于SW转变过程无法从实验观测,开展相应的理论研究就显得非常必要.Ioffe等11利用密度泛函理论(DFT)方法研究了C76富勒烯氯化物和它们之间的结构转变过程,得到从IPR#19150C76Cl24出发经过七步SW旋转获得#18917C76Cl24.Yang等13也利用DFT方法预测了从IPR#341061C102Cl20出发可以经过两次SW旋转,得到最终的产物#283794C102Cl20.最近,甘利华等14对C60及其衍生物的SW旋转过程进行了密度泛函理论水平的计算,结果揭示#1809C60Cl8和#1804C60Cl12等C60富勒烯衍生物可能是先衍生化后再经过SW旋转异构化形成得到.
©Editorial office of Acta Physico-Chimica Sinica
尽管2004年实验上成功合成了#271C50Cl10,2但是关于它形成机理依然不清楚.公认的观点认为它是由富勒烯空笼#271C50捕获氯稳定而成,然而是否存在其它路径而获得C50Cl10呢?这个问题过去还没有人探讨过.Lu等15使用B3LYP方法对271种C50异构体及氯化物进行了计算,结果显示具有D3对称性的序号为270的C50是它的基态结构,同时包括#271C50,#266C50,#264C50,#262C50和#260C50都是亚稳态结构.Zhao16和Tian17的研究小组也分别用半经验方法与不同的DFT方法获得了相似的结果,证实富勒烯空笼#270C50是最稳定的结构.因而本文将使用DFT方法对C50氯化物进行计算研究,探索SW旋转异构化生成#271C50Cl10的过渡态,弄清氯化过程的反应机制.
2 模型与计算方法
C50的空笼及氯化物的几何结构优化和电子结构性质在Dmol3模块18,19中采用Perdew-Burke-Ernzerhof(PBE)20及加极化的全电子双数值基组(DNP)进行计算.对于SWT的过渡态能垒,采用完全线性同步转变(LST)/二次同步转变(QST)方法21进行无对称性限制的搜索.以上方法的可靠性已经在先前关于富勒烯的一系列研究中得到验证.为了估计C50氯化物的热力学稳定性,我们计算了氯化反应(式(1))的氯化能(ΔECl),如公式(2)所示.
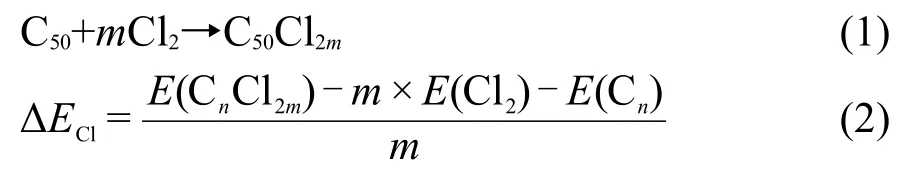
上式中,ΔECl定义为产物(氯化富勒烯)的能量减去反应物(空笼和Cl2)的能量,然后再除以加成的Cl2的个数.同时为了对比不同类型泛函的差异,我们也使用了Gaussian 09软件包22的B3LYP/6-31G*杂化泛函23计算C50异构体的电子能量和HOMO-LUMO能隙.
需要提到的是,这些C50异构体之间的图论连通性是相互关联的,可以通过不超过三次的C―C键旋转而互相转化.图1所示为#271C50、#270C50、#266C50、#264C50、#263C50、#262C50和#260C50之间相互转化的SW旋转示意图.
3 结果与讨论
3.1 C50氯化富勒烯的结构和能量
计算了这几种C50富勒烯氯化物的能量及结构(氯化数2m小于14),每个富勒烯氯化物都搜索了几十个异构体.图2所示为能量最低的C50富勒烯氯化物的结构.
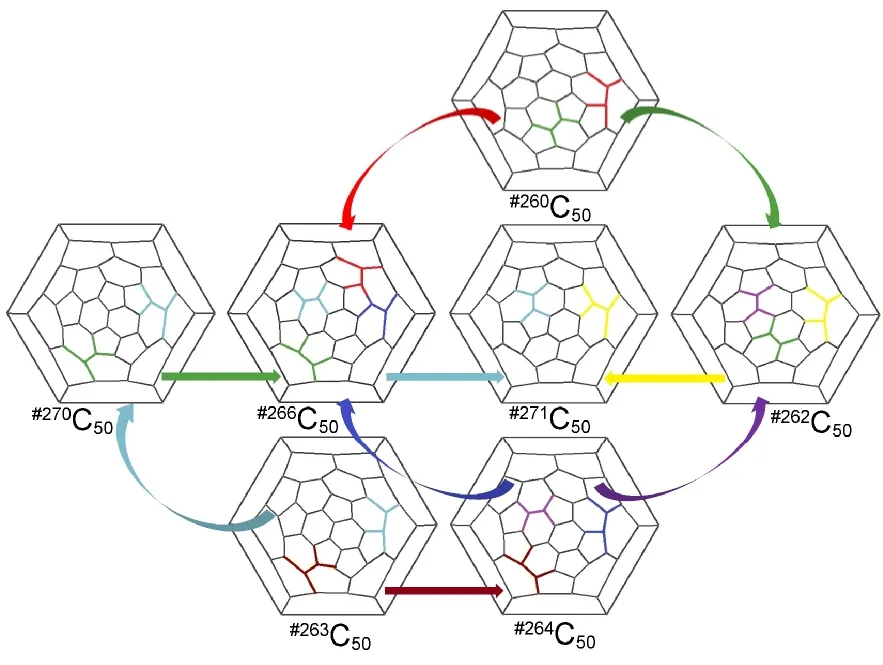
图1 #271C50、#270C50、#266C50、#264C50、#263C50、#262C50和#260C50之间相互转化的SW旋转示意图Fig.1 SW rearrangement between C50fullerene isomers#271C50,#270C50,#266C50,#264C50,#263C50,#262C50,and#260C50
表1给出了PBE/DNP水平下优化后不同氯化数目的最稳定氯化物的相对能量、氯化能、HOMOLUMO能隙等结果.从表1数据中可以看出#270C50是C50中能量最低的结构,而#271C50则比它要高16.54 kJ· mol-1.这一结果与前人的理论计算的结果是一致的.与B3LYP/6-31g*的计算结果相比,#271C50则比它要高23.32 kJ·mol-1.因此,虽然泛函不同,PBE和B3LYP方法都能给出一致的结果.在所有氯化富勒烯中,#271C50氯化物都是能量上最稳定的.以#270C50碳笼为例,#270C50Cl2比#271C50Cl2高48.53 kJ·mol-1,而当10个Cl原子加成上后,#270C50Cl10比#271C50Cl10高207.67 kJ·mol-1.同时,我们比较了这些C50富勒烯的氯化能.结果显示共同的趋势:氯化的过程是一个放热反应,是能量有利的过程.这就告诉我们当富勒烯空笼在电弧放电条件下生成,在有氯的环境下更倾向于先氯化,而不是先进行SW转变.这也与甘利华等14的14C60研究结果是相一致的.从热力学有利的角度,从#270C50氯化生成#270C50Cl10,然后经过SW转变生成#271C50Cl10具有最大的热力学稳定性.因而下一步我们将考虑这个SW转变的过程.
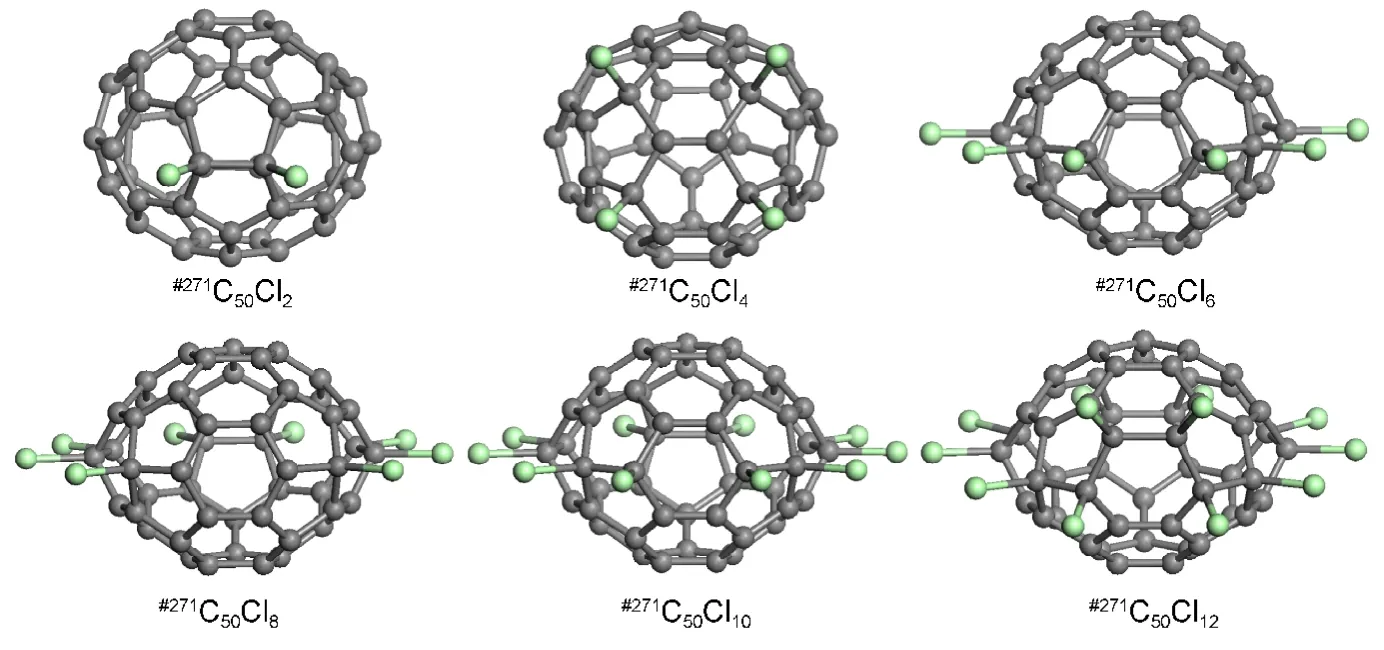
图2 PBE/DNP水平下优化最低能量的C50Cl2m(2m=2-12)的结构Fig.2 Optimized structures of the lowest energy C50Cl2m(2m=2-12)at the PBE/DNPlevel
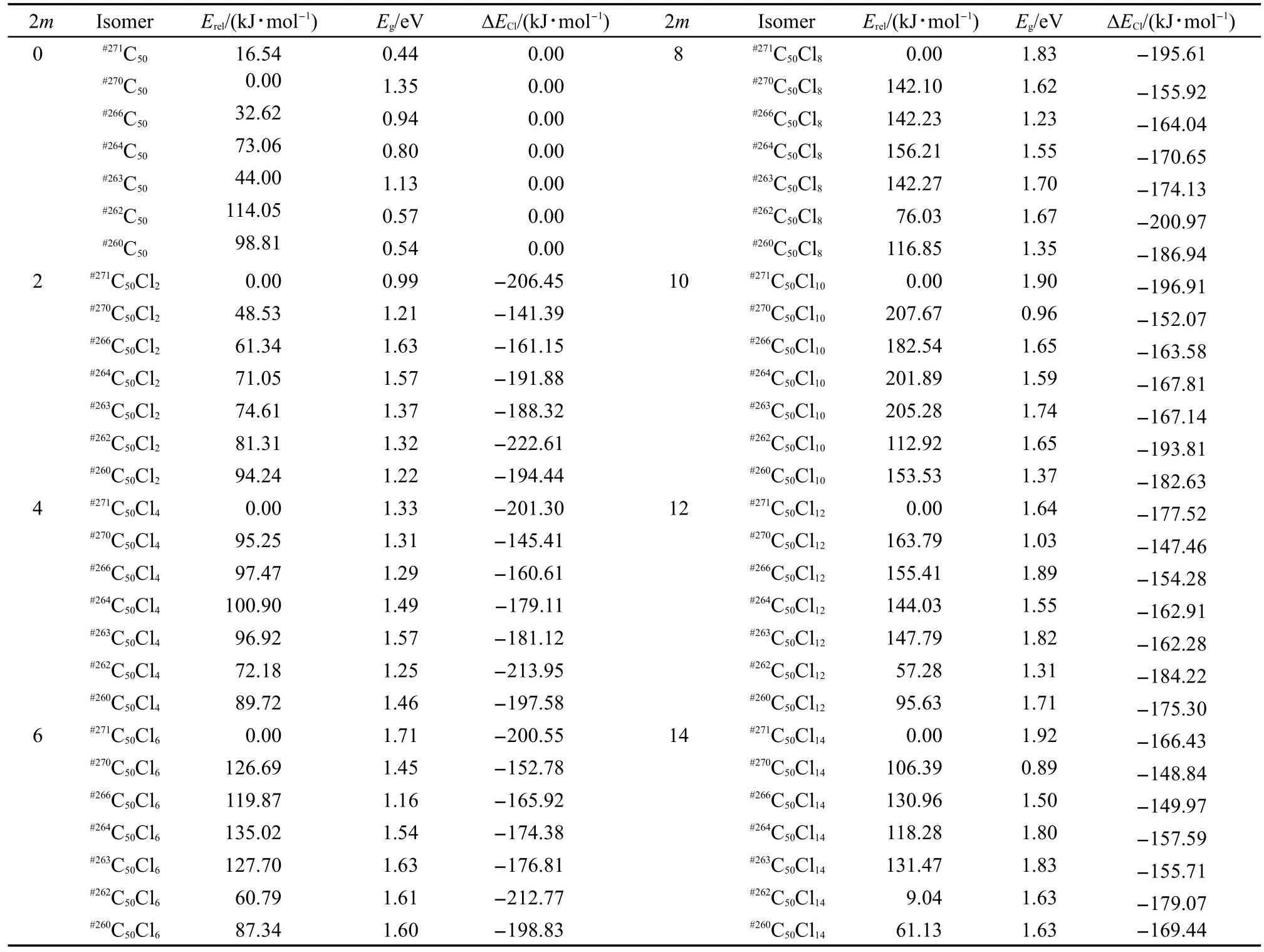
表1 PBE/DNP水平下优化后的最稳定C50Cl2m(2m=0-14)异构体的相对能量(Erel),HOMO-LUMO能隙(Eg)和氯化能(ΔECl)Table 1 Relative energies(Erel),HOMO-LUMO gap(Eg),and chlorinated energy(ΔECl)of the most stable isomers of C50Cl2m(2m=0-14)optimized at the PBE/DNP level
3.2 C50富勒烯氯化物间Stone-Wales转变
富勒烯空笼的SW旋转反应需要较高的能量,反应能垒大概在5-7 eV之间.我们用PBE/DNP计算了#270C50通过两次SW旋转生成#271C50,获得的活化能垒分别为574.43 kJ·mol-1(5.95 eV)和564.80 kJ· mol-1(5.85 eV).之前的理论计算报道了在富勒烯空笼上加成氯原子或者氢原子,其SW旋转能垒会降低.考虑到#270C50Cl10到#271C50Cl10具有最大的热力学稳定性,我们首先计算了#270C50Cl10➝#266C50Cl10➝#271C50Cl10的SW旋转活化能,包括有氯重排和无氯重排的情况.计算结果如图3所示,对于没有氯的重排#270C50Cl10➝#266C50Cl10和#266C50Cl10➝#271C50Cl10的SW旋转活化能分别为451.76和445.06 kJ·mol-1.与对应的空笼SW旋转活化能相比,分别降低了122.67和 119.74 kJ·mol1.而有氯重排的情况下,#270C50Cl10➝#266C50Cl10和#266C50Cl10➝#271C50Cl10的SWT旋转活化能分别为393.98和365.09 kJ·mol-1.与空笼相比,分别降低了180.45和199.71 kJ·mol-1.而且容易发现有氯重排的情况下,SW旋转的活化能比没有氯重排的情况下要低.
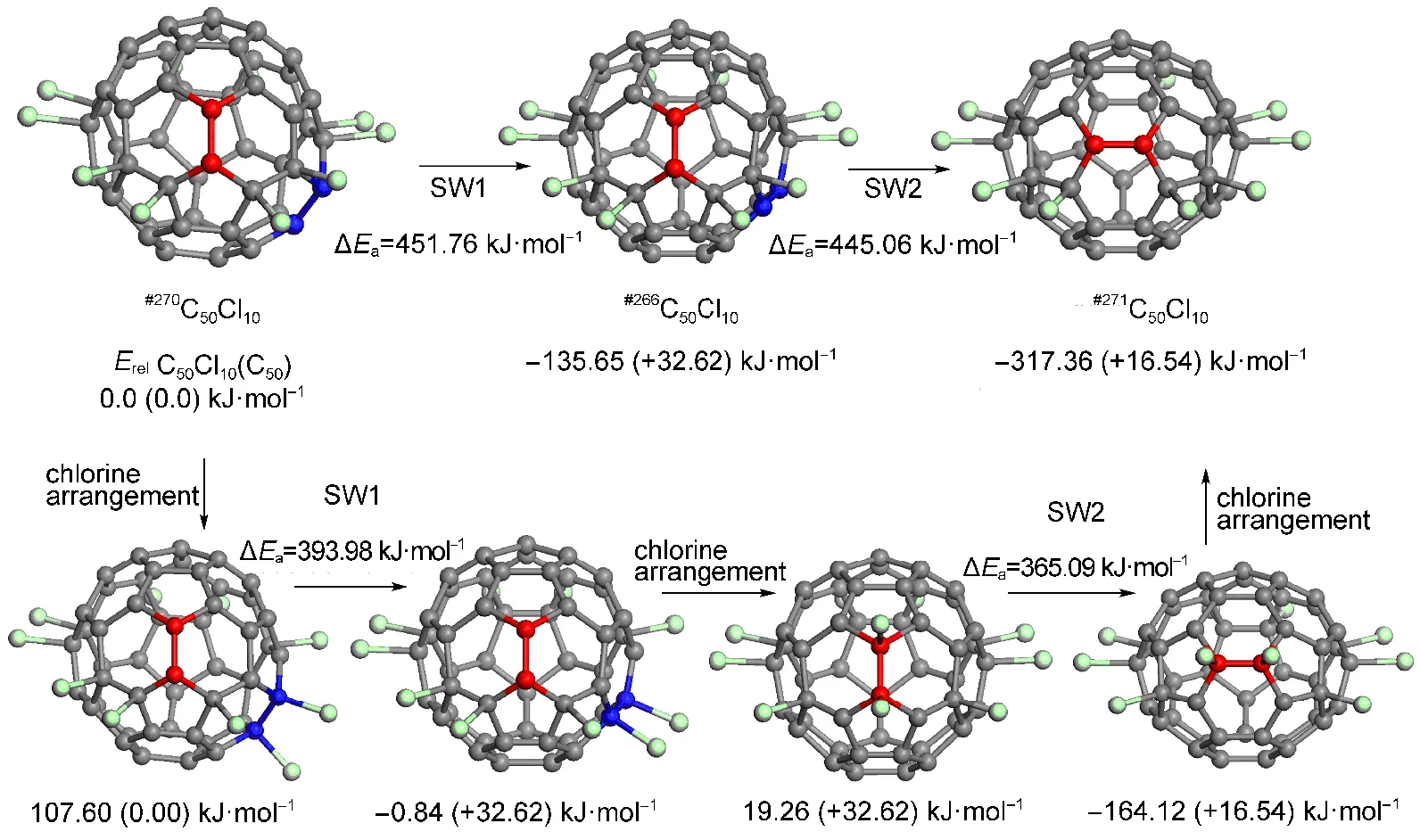
图3 #270C50Cl10➝#266C50Cl10➝#271C50Cl10的SW旋转Fig.3 SW transformation from the#270C50Cl10into#271C50Cl10through#266C50Cl10
进一步,我们考查了加成氯原子个数对SW旋转活化能的影响.同样对于#270C50Cl2m➝#266C50Cl2m➝#271C50Cl2m(2m=2-8,12),计算了它们的SW旋转活化能.
从表2可以看出,不管有没有氯重排,SW旋转活化能都比空笼降低,最低的活化能仅为290.6 kJ· mol-1;同时,进行SW旋转时,第一次旋转和第二次旋转的活化能差异很小.并且反向旋转比正向旋转活化能大,即富勒烯衍生化过程中,趋向于生成#271C50的方向旋转,氯化度不会改变SW旋转的结果.
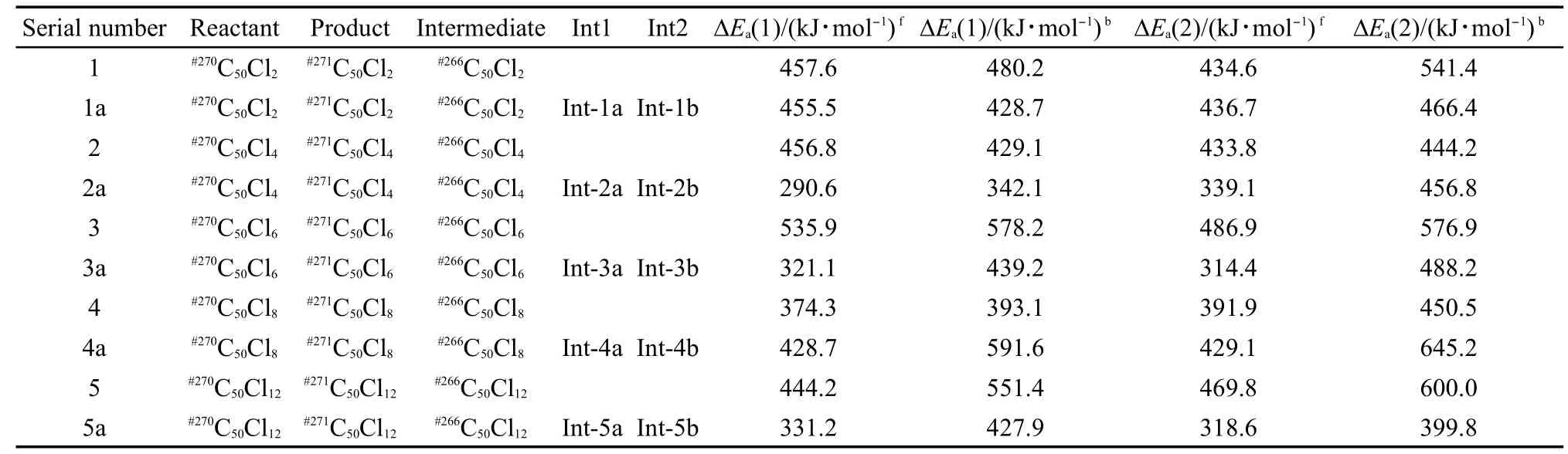
表2 PBE/DNP水平下计算的两次SW旋转活化能Table 2 Two SW activated energy barriers calculated at the PBE/DNPlevel
以上结果显示,在从#270C50空笼生成#271C50Cl10富勒烯衍生物形成过程中,一条高度可能的路径是,#270C50空笼首先氯化,得到不同#270C50氯化物,这些#270C50氯化物进行两次SW旋转,最终获得#271C50氯化物,这些#271C50氯化物通过重排而获得热力学和动力学上最稳定的结构#271C50Cl10.
4 结论
对富勒烯衍生物#271C50Cl10的的另一条形成机理进行了密度泛函理论水平的计算.结果显示,#271C50Cl10可以通过能量更稳定的#270C50空笼氯化得到.#270C50空笼先氯化,得到不同#270C50氯化物,再进行两次SW旋转的路径由于活化能垒更低因而是一条更为可行的路线.这些结果很好地解释了实验现象,揭示了富勒烯衍生物新的形成机理.
(1) Kroto,H.W.;Heath,J.R.;O'Brien,S.C.;Curl,R.F.;Smalley, R.E.Nature1985,318,162.doi:10.1038/318162a0
(2) Xie,S.Y.;Gao,S.;Lu,X.;Huang,R.B.;Wang,C.R.;Zhang, X.;Liu,M.L.;Deng,L.S.;Zheng,L.S.Science2004,304,699.doi:10.1126/science.1095567
(3) Tan,Y.Z.;Li,J.;Zhu,F.;Han,X.;Jiang,W.S.;Huang,R.B.; Zheng,Z.;Qian,Z.Z.;Chen,R.T.;Liao,Z.J.;Xie,S.Y.;Lu, X.;Zheng,L.S.Nat.Chem.2010,2,269.doi:10.1038/ nchem.549
(4) Wang,C.R.;Shi,Z.Q.;Wan,L.J.;Lu,X.;Dunsch,L.;Shu,C. Y.;Tang,Y.L.;Shinohara,H.J.Am.Chem.Soc.2006,128,6605.doi:10.1021/ja0567844
(5) Tan,Y.Z.;Liao,Z.J.;Qian,Z.Z.;Chen,R.T.;Wu,X.;Liang, H.;Han,X.;Zhu,F.;Zhou,S.J.;Zheng,Z.;Lu,X.;Xie,S.Y.; Huang,R.B.;Zheng,L.S.Nat.Mater.2008,7,790.doi: 10.1038/nmat2275
(6) Kuvychko,I.V.;Streletskii,A.V.;Popov,A.A.;Kotsiris,S.G.; Drewello,T.;Strauss,S.H.;Boltalina,O.V.Chem.Eur.J.2005,11,5426.
(7) Troshin,P.A.;Lyubovskaya,R.N.;Ioffe,I.N.;Shustova,N.B.; Kemnitz,E.;Troyanov,S.Z.Angew.Chem.Int.Edit.2005,44,234.
(8) Troyanov,S.I.;Shustova,N.B.;Ioffe,I.N.;Turnbull,A.P.; Kemnitz,E.Chem.Commun.2005,72.
(9) Weng,Q.H.;He,Q.;Liu,T.;Huang,H.Y.;Chen,J.H.;Gao,Z. Y.;Xie,S.Y.;Lu,X.;Huang,R.B.;Zheng,L.S.J.Am.Chem. Soc.2010,132,15093.doi:10.1021/ja108316e
(10) Chen,R.T.;Zhou,S.J.;Liang,H.;Qian,Z.Z.;Li,J.M.;He, Q.;Zhang,L.;Tan,Y.Z.;Han,X.;Liao,Z.J.;Weng,W.Z.; Xie,S.Y.;Huang,R.B.;Zheng,L.S.J.Phys.Chem.C2009,113,16901.doi:10.1021/jp902325w
(11) Ioffe,I.N.;Mazaleva,O.N.;Chen,C.;Yang,S.F.;Kemnitz,E.; Troyanov,S.I.Dalton Trans.2011,40,11005.doi:10.1039/ c1dt10256g
(12) Ioffe,I.N.;Mazaleva,O.N.;Sidolov,L.N.;Yang,S.F.;Wei, T.;Kemnitz,E.;Troyanov,S.I.Inorg.Chem.2012,51,11226.
(13) Yang,S.F.;Wei,T.;Wang,S.;Ignateva,D.V.;Kemnitz,E.; Troyanov,S.I.Chem.Commun.2013,49,7944.doi:10.1039/ c3cc44386h
(14) Gan,L.H.;Wen,R.Sci.Sin.Chim.2014,44,345.[甘利华,文 蓉.中国科学:化学,2014,44,345.]
(15) Lu,X.;Chen,Z.F.;Thiel,W.;Schleyer,P.v.R.;Huang,R.B.; Zheng,L.S.J.Am.Chem.Soc.2004,126,14871.doi:10.1021/ ja046725a
(16) Zhao,X.J.Phys.Chem.B2005,109,5267.doi:10.1021/ jp0452610
(17) Tian,W.Q.;Feng,J.K.;Wang,Y.A.;Aoki,Y.J.Chem.Phys.2006,125,094105.doi:10.1063/1.2335436
(18) Delley,B.J.Chem.Phys.1990,92,508.doi:10.1063/1.458452
(19) Delley,B.J.Chem.Phys.2000,113,7756.doi:10.1063/ 1.1316015
(20) Perdew,J.P.;Burke,K.;Ernzerhof,M.Phys.Rev.B1992,45,13244.doi:10.1103/PhysRevB.45.13244
(21) Henkelman,G.;Jónsson,H.J.Chem.Phys.2000,113,9978. doi:10.1063/1.1323224
(22) Frisch,M.;Trucks,G.;Schlegel,H.B.;et al.Gaussian 09,Revision A.02;Gaussian Inc.:Wallingford,CT,2009.
(23) Lee,C.;Yang,W.;Parr,R.G.Phys.Rev.B1988,37,785.doi: 10.1103/PhysRevB.37.785
Alternative Formation Mechanism of C50Cl10Fullerene Chloride Based on Density Functional Theory Calculations
GAN Zuo-Hua CHEN Shu-Xuan TAN Kai*
(State Key Laboratory of Physical Chemistry of Solid Surfaces&Fujian Provincial Key Laboratory of Theoretical and Computational Chemistry,College of Chemistry and Chemical Engineering,Xiamen University, Xiamen 361005,Fujian Province,P.R.China)
#271C50Cl10is widely postulated to be a direct chlorination product of cage#271C50.We suggest an alternative formation mechanism of#271C50Cl10,based on the topological relationship of these C50fullerenes. Density functional theory(DFT)calculations of the proposed cage transformation pathway in the chlorination of C50were performed.The proposed pathway is stimulated by chlorination-promoted fullerene cage transformation,with a low activation barrier.DFT calculations of the Stone-Wales(SW)transformation pathways revealed that the thermodynamically favored rearrangement of other C50chlorofullerene into#271C50Cl10requires a lower activation energy than that of the pristine carbon cage.This suggested that it is a more effective pathway of chlorinating C50to#271C50Cl10.
Density functional theory;Stone-Wales transformation;Chlorination
O641
10.3866/PKU.WHXB201411172www.whxb.pku.edu.cn
Received:September 23,2014;Revised:November 15,2014;Published on Web:November 17,2014.
∗Corresponding author.Email:ktan@xmu.edu.cn;Tel:+86-592-2182826.
The project was supported by the National Natural Science Foundation of China(21273177)and National Key Basic Research Program of China (973)(2011CB808504).
国家自然科学基金(21273177)和国家重点基础研究发展规划项目(973)(2011CB808504)资助

