痰热清注射液辅助治疗恶性肿瘤并肺部感染的有效性及安全性评价*
周 华汪成琼田应彪陈 灵肖 政△
(1.遵义医学院附属医院遵义医学院循证医学中心,循证医学教育部网上合作研究中心遵义医学院分中心,贵州 遵义 563003;2.遵义医学院附属医院,贵州 遵义 563003)
·研究报告·
痰热清注射液辅助治疗恶性肿瘤并肺部感染的有效性及安全性评价*
周 华1,2汪成琼1田应彪2陈 灵2肖 政1△
(1.遵义医学院附属医院遵义医学院循证医学中心,循证医学教育部网上合作研究中心遵义医学院分中心,贵州 遵义 563003;2.遵义医学院附属医院,贵州 遵义 563003)
目的系统评价痰热清注射液辅助治疗恶性肿瘤并肺部感染的有效性与安全性。方法系统检索CBM、CNKI、维普、万方、Pubmed及Embase数据库,采用Cochrane协作网RCT质量评价标准评价纳入研究质量,Meta分析提取数据。结果1)纳入8个RCT,恶性肿瘤并肺部感染662例,纳入研究质量一般;2)与单一抗生素比较,Meta分析合并RR值包括临床痊愈[RR=1.45,95%CI(1.10,1.91)],临床显效[RR=1.24,95% CI(1.04,1.48)]及总体疗效[RR=1.19,95%CI(1.06,1.33)],两组差异有统计学意义(P=0.02)。3)与双抗生素比较,临床痊愈[RR=0.91,95%CI(0.75,1.11)]、临床显效[RR=0.88,95%CI(0.66,1.19)]、临床有效[RR= 1.45,95%CI(0.63,3.30)]及临床总体疗效[RR=0.97,95%CI(0.90,1.04)],两组差异无统计学意义(P=0.42)。结论本研究表明痰热清注射液辅助治疗恶性肿瘤并肺部感染的临床疗效优于单抗生素,与二联抗生素疗效相当。
痰热清注射液 抗生素 恶性肿瘤 肺部感染 Meta分析
恶性肿瘤患者因长期接受放化疗、手术和侵入性治疗而易并发肺部感染,其预后差,疾病负担重[1-3]。抗生素治疗常因病原菌耐药性及多重耐药而失败,致使临床决策困难[4-5]。中医药在抗感染治疗中有直接抗菌、消除炎症及增强机体抗病能力等重要作用。痰热清注射液具有清热、化痰及解毒之力,常辅助抗生素防治各种感染性疾病,但其有效性和安全性各研究报道存在差异,致使临床选择困难[6-7]。因此本研究系统评价痰热清注射液辅助治疗恶性肿瘤并肺部感染的有效性及安全性,为科学制订恶性肿瘤并肺部感染治疗策略提供依据。现报告如下。
1 材料与方法
1.1 检索策略
1.2 选取标准
纳入标准为1)研究对象为恶性肿瘤并肺部感染(排除单独以某器官或系统肿瘤为研究对象文献)。2)研究类型为随机对照试验(RCT)。3)试验组为痰热清注射液辅助治疗,即常规使用敏感抗生素的基础上加痰热清注射液。4)对照组单纯使用敏感单或双抗生素治疗。5)结局指标如下。(1)临床疗效。用药第7~14日,根据临床症状有无改善、体征有无好转评定治疗反应,有效者继续治疗,无效者调整治疗方案,归入无效。用药第7~14日根据症状、体征及胸部X线变化归入痊愈、显效和有效。痊愈:体温正常,症状和体征消失,胸片肺部炎症吸收,血、痰病原菌培养转阴。显效:体温正常,症状、阳性体征基本消失,胸片肺部炎症大部吸收。有效:症状体征有好转,胸片肺部炎症有所吸收。无效:体温正常或高于正常,症状、体征无变化或加重,胸片肺部炎症未吸收。总体疗效:包括有效、显效及痊愈。(2)不良反应。排除标准:重复文献、无关文献、会议摘要、普通综述、报告信息不准确、统计数据无法应用者。
1.3 纳入文献质量评价
按Cochrane系统评价手册质量评价标准评价纳入研究方法学质量。包括:1)是否应用随机方法;2)是否做到分配隐藏;3)是否采用盲法;4)基线是否可比;5)其他偏倚,如评价RCT的方法学质量。针对每个纳入研究,对上述5条作出“是”(该试验发生各种偏倚的可能性最小)、“否”(该试验有发生偏倚的高度可能性)和“不清楚”(缺乏相关信息或偏倚情况不确定)评价。“是”为2分,“否”为0分,“不清楚”为1分,总评分最高为10分。
1.4 文献筛选与质量评价
由2名评价员(周华和汪成琼)根据纳入、排除及质量评价标准,独立筛选及评价文献,筛选与评价分歧通过与第三方讨论解决(肖政)。
1.5 资料提取及统计分析
依据PICO原则 (P为研究对象,I为干预措施,C为研究对照,O为研究结果)设计资料提取表格,提取纳入研究基本情况(作者、发表时间、患者来源、病例数、试验组、对照组及研究设计),研究结果包括临床疗效及不良反应等。采用RevMan5.3进行Meta分析,连续变量用均数差(MD)或标准化均数差(SMD),二分类变量采用相对危险度(RR)及其95%CI进行描述。各研究间异质性检验采用χ2检验,若不存在异质性或异质性较小 (I2<50%,P>0.1),采用选择固定效应模型(Fixed effects model)计算合并效应量;如异质性检验结果显示各研究间存在异质性(P≤0.1,I2≥50%),分别采用固定效应模型交替随机效应模型进行Meta分析,其结果的一致性好,说明无明显异质性来源,则采用随机效应模型 (Random effects model)进行合并分析。合并研究超过10个,采用漏斗图分析发表偏移。
2 结 果
2.1 文献检索与筛选结果
共检索到文献855篇,包括CBM(n=335篇),CNKI(n=115篇),维普 (n=161篇),万方 (n=233篇),Pubmed(n=4篇),Embase(n=7篇)。首先,阅读题目排除重复文献452篇,阅读摘要,排除会议摘要11篇,无关文献329篇,综述9篇,阅读全文后排除不符合纳入标准文献46篇,最后纳入8篇随机对照研究 (如图1)。

图1 文献检索及筛选结果
2.2 纳入研究基本特征 见表1。本研究纳入2005-2011年间7个省8个RCT研究,恶性肿瘤并肺部感染662例。痰热清注射液辅助治疗组345例,单纯使用抗生素组317例。采用临床疗效及不良反应等指标评价疗效。结果表明各研究中痰热清注射液辅助治疗恶性肿瘤并肺部感染治疗效果报道不一。
2.3 纳入研究质量特征 见表2。纳入8个研究,其质量基本特征分布如下:纳入研究整体质量一般,1个研究质量为7分,4个研究质量6分,3个研究5分,平均积分为5.92分。仅1篇文献说明随机方法,其余7篇仅描述随机2字,均未说明盲法和分配隐藏;5篇基线一致,3篇为不清楚;均未说明其他偏倚。结果表明纳入研究质量一般,尤其是随机方法、分配隐藏及盲法部分描述不清楚。

表1 纳入研究文献基本特征

表2 纳入研究质量基本特征
2.4 痰热清临床使用特征
见表3。纳入8个研究,痰热清注射液辅助治疗肺部感染使用特征分布(如)如下:痰热清注射液静脉注射,使用剂量主要为20 mL辅助用药,每日1次,7~10 d为1个疗程,而兰丙欣等[11]用30 mL,单丽珠等[6]用药14 d为1个疗程。结果表明痰热清注射液辅助治疗治疗恶性肿瘤并肺部感染常20 mL辅助用药,每日1次,7~10 d为1个疗程。
2.5 临床疗效评价
依据临床疗效评价标准,对痰热清注射液辅助治疗的临床疗效分为5个等级包括临床无效、有效、显效、痊愈及总体疗效,依据纳入文献特征分别评价如下。
2.5.1 临床痊愈 纳入6个研究,500例患者。1)痰热清注射液辅助单抗生素组与单抗生素组比较的5个研究,痰热清注射液辅助单抗生素组225例,单抗生素组195例,研究结果间同质性好,固定效应模型分析表明临床痊愈在两组间有统计学差异 [RR=1.45,95%CI(1.10,1.91),P=0.009],结果表明痰热清注射液辅助抗生素组临床痊愈率优于对照组。2)痰热清注射液辅助单抗生素组与双抗生素组比较的1个研究,痰热清注射液辅助单抗生素组40例,双抗生素组40例,统计学分析表明临床痊愈在两组间无统计学差异 [RR= 0.91,95%CI(0.75,1.11),P=0.37],痰热清注射液辅助单抗生素组与双抗生素组的临床痊愈相当。

表3 痰热清注射液使用基本特征
2.5.2 临床显效 纳入6个研究,534例患者,2个比较方案。1)纳入痰热清注射液辅助单抗生素组与单抗生素组比较的5个研究,痰热清注射液辅助单抗生素组252例,单抗生素组228例,研究结果间同质性较好,固定效应模型分析表明临床显效在两组间有统计学差异 [RR=1.24,95%CI(1.04,1.48),P=0.02],结果表明痰热清注射液辅助单抗生素组临床显效率优于对照组。2)纳入与双抗生素组比较的1个研究,痰热清注射液辅助单抗生素组28例,双抗生素组26例,统计学分析表明临床显效在两组间无统计学差异 [RR= 0.88,95%CI(0.66,1.19),P=0.42],痰热清注射液辅助单抗生素组与双抗生素组的临床显效相当。

图2 两组临床治愈比较的Meta分析
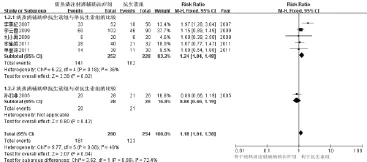
图3 两组临床显效比较的Meta分析

图4 两组临床有效比较的Meta分析
2.5.3 临床有效 纳入8个研究,662例患者,2个比较方案。1)纳入痰热清注射液辅助单抗生素组与单抗生素组比较的6个研究,痰热清注射液辅助单抗生素组277例,单抗生素组251例,研究结果间同质性较好,固定效应模型分析表明临床显效在两组间无统计学差异[RR=0.91,95%CI(0.62,1.33),P=0.61],结果表明痰热清注射液辅助抗生素组临床有效率与对照组相当。2)与双抗生素组比较的2个研究,痰热清注射液辅助单抗生素组68例,双抗生素组66例,研究结果间同质性较好,固定效应模型分析表明临床有效在两组间无统计学差异 [RR=1.45,95%CI(0.63,3.30),P= 0.38],痰热清注射液辅助单抗生素组与双抗生素组的临床有效相当。
2.5.4 总体疗效 纳入8个研究,670例患者,2个比较方案。1)纳入痰热清注射液辅助单抗生素组与单抗生素组比较的6个研究(如图5),痰热清注射液辅助单抗生素组277例,单抗生素组251例,研究结果间同质性较差,随机效应模型分析表明临床总体疗效在两组间有统计学差异[RR=1.19,95%CI(1.06,1.33),P= 0.003],结果表明痰热清注射液辅助抗生素组临床总体疗效优于对照组。2)纳入与双抗生素组比较的2个研究(如图6),痰热清注射液辅助单抗生素组68例,双抗生素组66例,研究结果间同质性较好,固定效应模型分析表明临床总体疗效在两组间无统计学差异[RR=0.97,95%CI(0.90,1.04),P=0.43],痰热清注射液辅助单抗生素组与双抗生素组的临床总体疗效相当。

图5 痰热清注射液辅助单抗生素与单抗生素总体疗效比较的Meta分析

图6 痰热清注射液辅助单抗生素与双抗生素总体疗效比较的Meta分析
2.6 不良反应
纳入7个研究描述不良反应,4个研究报道无不良反应,3个研究报道局部静脉疼痛2例[12];轻微头痛、心悸各1例,胃肠道反应2例[13];颜面潮红1例[7]。结果表明痰热清注射液辅助治疗恶性肿瘤并肺部感染存在一定程度并发症,各并发症影响相对较轻。
2.7 发表偏移与异质性分析
发表偏移分析,各Meta分析纳入研究均为超过10个,因此未做发表偏移分析。异质性分析:为降低纳入研究异质性,本研究严格按照制定的统一纳入和排除标准,以确保纳入研究临床上的同质性;痰热清注射液辅助单抗生素与单抗生素总体比较的Meta分析的异质性较高,排除临床异质性后,采用随机效应模型及固定效应模型交替分析表明Meta分析结果稳定性较好,结果可靠。结果表明本次Meta分析结果评估较客观,可靠性及可信度较高。
3 讨 论
本研究纳入2005至2011年间7个省8个RCT研究,恶性肿瘤并肺部感染662例,系统分析表明痰热清注射液辅助治疗恶性肿瘤并肺部感染的常用剂量为20 mL,每日1次,连续用7~10 d为1个疗程。Meta分析表明与单抗生素相比,痰热清注射液辅助单抗生素能显著改善恶性肿瘤并肺部感染患者的临床痊愈、显效及总体疗效率。而与双抗生素相比,痰热清注射液辅助单抗生素组的临床疗效包括痊愈、显效、有效及总体疗效均与双抗生素对照组相当。研究提示痰热清注射液辅助治疗能增强抗感染疗效,并可能减少抗生素种类及剂量。研究提示痰热清注射液能清除细菌[14-16],降低胸科术后、COPD急性加重期、创伤性急性肺损伤等患者血清白细胞介素-6(IL-6)、白细胞介素-8(IL-8)、肿瘤坏死因子-α(TNF-α)等炎性介质水平[17-19],提示痰热清注射液具有抗感染及改善炎症功效。抗生素为恶性肿瘤并肺部感染常规治疗手段,而非规范使用抗生素为耐药及二重感染的重要原因。本研究Meta分析提示痰热清注射液辅助治疗能减少抗生素用量。研究表明,痰热清注射液可能降低二重感染发生率[20],因此可能对预防滥用抗生素性二重感染及耐药、提高抗感染治疗的安全性等具有重要价值。纳入7个研究描述不良反应,3个研究报道局部静脉疼痛2例[12];轻微头痛、心悸各1例,胃肠道反应2例[13];颜面潮红1例[7],提示相关不良反应轻微,安全性较好。纳入研究整体质量一般,纳入研究随机及盲法等描述不清,严重影响研究结果可信度。大部分合并指标同质性好,仅辅助单抗生素与单抗生素总体比较的Meta分析的异质性较高,排除临床异质性后,采用随机效应模型及固定效应模型交替分析表明Meta分析结果稳定性较好,科学性较好,结果可靠。纳入研究未做发表偏倚分析。综合分析表明本次Meta分析稳定性及科学性较好,结果可靠,纳入研究数量较少,但质量不高。
综上,本研究表明痰热清注射液辅助治疗恶性肿瘤并肺部感染的临床疗效优于单一抗生素,与二联抗生素疗效相当;可能对预防滥用抗生素性二重感染及耐药,提高抗感染治疗的安全性等具有重要价值。但纳入研究证据数量较少及质量不高,建议临床慎用,同时设计高质量、规范的随机对照试验予以证实其疗效及安全性。
[1] Andalib A,Ramana-Kumar AV,Bartlett G,et.al.Influence of postoperative infectious complications on Long-Term survival of lung cancer patients:a population-based cohort study[J]. Journal of Thoracic Oncology.2013,8(5):554-561.
[2] Lee JO,Kim DY,Lim JH,et al.Risk factors for bacterial pneumonia after cytotoxic chemotherapy in advanced lung cancer patients[J].Lung Cancer,2008,62(3):381-384.
[3] 王廷祥,饶远权,刘杏娥.肺癌患者化疗期间感染相关危险因素分析[J].中华医院感染学杂志,2014,24(4):887-888,891.
[4] 高彩凤,褚金龙,李骏,等.中西医结合治疗恶性血液病肺感染的疗效观察[J].中国综合临床,2009,25(7):721-723.
[5] Zhan P,Suo LJ,Qian Q,et al.Chlamydia pneumoniae infection and lung cancer risk:a meta-analysis[J].Eur J Cancer,2011,47(5):742-747.
[6] 单丽珠,张鹤.中药联合抗生素治疗晚期恶性肿瘤合并肺感染临床观察:附38例分析[J].中华实用中西医杂志,2011,24(4):4-5.
[7] 李瑜英.痰热清注射液治疗恶性肿瘤合并肺部感染疗效观察[J].医学信息:中旬刊,2011,24(8):4008-4009.
[8] 孙羽非.痰热清注射液治疗肿瘤化疗后并发肺部感染的疗效观察[J].中国医学研究与临床,2005,3(8):45.
[9] 赵宏亮,王鹏远,李伟,等.痰热清联合抗生素治疗肿瘤患者肺部感染[J].医药论坛杂志,2005,26(21):60.
[10]李燕妃,许德明,赵小琼,等.痰热清与头孢他啶合用治疗癌症合并肺部感染52例[J].第四军医大学学报,2007,28(17):1623-1623.
[11]兰丙欣.痰热清注射液治疗恶性肿瘤患者化疗后并发肺部感染[J].中国实用医刊,2009,36(20):87-88.
[12]李云霞,沈丽达,邓明佳.痰热清注射液治疗恶性肿瘤肺部感染102例临床观察[J].云南中医中药杂志,2009,30(5):21-22.
[13]刘小男,杨晓秋,陈其彬,等.痰热清注射液对晚期肿瘤患者肺部感染抗炎及镇痛作用观察[J].中国中医急症,2009,18(7):1031,1099.
[14]闵存云,刘和强.痰热清注射剂治疗急性上呼吸道感染的临床疗效观察[J].中成药,2006,28(5):678-679.
[15]宋志香,芦苇,陈亮,等.痰热清与万古霉素治疗耐甲氧西林金黄色葡萄球菌性肺炎及其耐药性研究[J].中华医院感染学杂志,2009,19(14):1861-1863.
[16]潘莉娜,李新忠,李欣科.痰热清注射液对呼吸机相关性肺炎高热患者C反应蛋白和感染参数的影响[J].中国实验方剂学杂志,2013,19(23):298-301.
[17]喻秋平,万于华,周学亮,等.痰热清对胸科术后患者血清炎性细胞因子影响的研究[J].实用中西医结合临床,2011,11(2):36-37.
[18]韦思尊,陈斯宁,冯原.痰热清注射液对慢性阻塞性肺疾病急性加重期患者细胞因子和肺功能影响的研究[J].中国中医急症,2011,20(9):1402-1403.
[19]阳世雄,赵永亮,曾建业,等.痰热清注射液对创伤性急性肺损伤患者细胞因子表达的影响[J].中国中医急症,2010,19(7):1087-1088.
[20]李穗晖,梁艳菊,黎玉辉,等.痰热清注射液联合抗生素治疗肺癌化疗后合并肺部感染临床观察痰热清注射液对创伤性急性肺损伤患者细胞因子表达的影响[J].中国中医急症,2012,21(7):1131-1132.
Efficacy and Safety of Tanreqing Injection in Adjuvant Treatment for the Pulmonary Infection after Ma-lignant Tumors:A Meta-analysis
ZHOU Hua,WANG Chengqiong,TIAN Yingbiao,et al. Evidence-Based Medicine Center;MOE Virtual Research Center of Evidence-based Medicine at Zunyi Medical College,Affiliated Hospital of Zunyi Medical College,Guizhou,Zunyi 563003,China
Objective:To systematically evaluate the efficacy and safety of Tanreqing injection in adjuvant treatment for the pulmonary infection after malignant tumors.Methods:All related studies in CBM,CNKI,VIP,Wanfang,Pubmed and Embase were retrieved,and their quality were evaluated by Cochrane scale and analyzed all data with meta-analysis.Results:1)Eight RCTs involving 662 malignant tumors patients with pulmonary infection were included,with general methodological quality in most trials.2)Compared with one antibiotic,the merged RR values and their 95%CI of Meta-analysis for clinical cure,marked effectiveness and overall effect were as follows:1.45(1.10,1.91),1.24(1.04,1.48)and 1.19(1.06,1.33)and these were statistically significant.3)Compared with two antibiotic,the merged RR values and their 95%CI of Meta-analysis for clinical cure,marked effectiveness,effectiveness and overall effect were as follows: 0.91 (0.75,1.11),0.88(0.66,1.19),1.45(0.63,3.30)and 0.97(0.90,1.04)and these were no statistically significant.Conclusions:Our study shows that the clinical efficacy of Tanreqing injection with one antibiotic is more than the one antibiotic and is similar to two antibiotics to the pulmonary infection after malignant tumors.
Tanreqing injection;Antibiotics;Malignant tumors;Pulmonary infection;Meta-analysis
R730.59
A
1004-745X(2015)06-0969-05
10.3969/j.issn.1004-745X.2015.06.012
国内外主要数据库:中国生物医学文献数据库(CBM)、中国学术期刊
总库(CNKI)、维普中文科技期刊全文数据库 (VIP)、万方数据库(wanfang)、Pubmed及Embase(建库至2014年6月)。中文检索词:痰热清注射液、痰热清、癌、Ca及肿瘤。英文检索词: “Tanreqing,Tanreqing injection[Mesh],Neoplasms”[Mesh]、Carcinoma、Cancer及tumors。1)中文检索式:主题(痰热清注射液+痰热清)*主题(癌+ Ca+肿瘤)。2)英文检索式:(Tanreqing OR Tanreqing injection[Mesh])AND(Neoplasms[Mesh]OR Carcinoma、Cancer OR tumors)。检索方式:由2名检索员(周华和汪成琼)独立采用主题词与自由词相结合计算机辅以手工检索数据,根据检索结果修正完善,尽可能全面地收集符合纳入标准的文献,无语种限制。
2015-01-24)
贵州省哲学社会科学规划基金资助(14GZYB58);遵义医学院博士启动基金(F-617)
△通信作者(电子邮箱:zy426f@163.com)

