铁(Ⅲ)-磺基水杨酸光度法测定柚肉中的VC
梁奇峰,吴适涛
(嘉应学院化学与环境学院,广东梅州514015)
维生素 C(VC)又名抗坏血酸(ascorbic acid),是一种重要的营养物质和药物,具有防止坏血病、预防心血管病等生理功能。VC广泛存在于新鲜水果、蔬菜中,测定VC的含量具有实际意义。目前,VC含量的测定方法较多,主要有碘量法[1-2]、分光光度法[3-5]、电位滴定法[6]、高效液相色谱法[7]等。
本文利用Fe(Ⅲ)-磺基水杨酸体系褪色光度法,测定了梅县沙田柚果肉中VC的含量。该法的测定原理是磺基水杨酸与Fe3+在pH为2~3生成1∶1的紫红色的稳定配合物,加入VC后,将Fe3+还原成Fe2+,使溶液中Fe3+的浓度减少,紫红色配合物的浓度随之减少,溶液褪色,用分光光度计测定溶液反应前后吸光度分别记为A0、A,其吸光度变化为ΔA=A0-A,吸光度差ΔA与VC浓度在一定的浓度范围内呈良好的线性关系,据此可以进行样品中VC含量的测定[5]。该法操作方便,测定灵敏度高,测定结果与碘量法接近,可以推广应用。
1 材料与方法
1.1 仪器与试剂
722sp型可见分光光度计:上海棱光技术有限公司;AE系列电子天平:梅特勒-托利多仪器上海有限公司;800B离心机:上海安亭科学仪器厂制造。
抗坏血酸:天津市福晨化学试剂工厂;磺基水杨酸、高氯酸:广州化学试剂厂;铁铵矾[NH4Fe(SO4)2·12H2O]:广东光华化学有限公司;以上试剂均为分析纯。
抗坏血酸标准溶液(500μg/mL):准确称取0.0500 g抗坏血酸于50 mL烧杯中,用12 mL 10%的盐酸溶液溶解,再转移到100 mL棕色容量瓶中,用蒸馏水定容,摇匀备用。Fe3+标准溶液(0.01 mol/L):准确称取1. 2055 g铁铵矾[NH4Fe(SO4)2.12H2O]于 50 mL 的烧杯中,加入10.00 mL 6 mol/L的盐酸,水浴加热溶解,转移到250 mL容量瓶中,用蒸馏水定容,摇匀备用。磺基水杨酸溶液(0.01 mol/L):准确称取1. 0910 g磺基水杨酸于50 mL的烧杯中,加适量蒸馏水溶解,转移至500 mL的容量瓶中,摇匀备用。高氯酸溶液(0.1 mol/L):准确量取2.10 mL高氯酸于250 mL容量瓶中,用蒸馏水定容至,摇匀备用。
1.2 样品来源及样品溶液的配制
1.2.1 样品来源
实验所用梅县沙田柚均直接购自当地水果批发市场。
1.2.2 样品溶液的配制
选择保存较好的沙田柚,剥皮去核,将果肉混匀,称取适量果肉样品(质量25 g左右)于研钵中,加入10 mL 10%的盐酸,迅速研磨成浆,用蒸馏水洗涤研钵,将浆状样品和洗涤液一并移入250 mL容量瓶中,用蒸馏水稀释至刻度,充分混合后离心15 min,取上清液作测定用。
1.3 测定方法
分别取Fe3+标准溶液1.00 mL,磺基水杨酸溶液5.00 mL,高氯酸溶液2.00 mL于2个50 mL容量瓶中,其中一个容量瓶再准确加入一定体积的抗坏血酸标准溶液或柚肉样品溶液,定容,摇匀。20 min后,以二次蒸馏水为空白,用1 cm比色皿,在502 nm波长下测定两份溶液的吸光度分别为A0和A,吸光度差ΔA=A0-A,绘制ΔA与加入的抗坏血酸的浓度标准工作曲线,并测定出沙田柚果肉中VC的含量。
2 结果与讨论
2.1 测定波长的选择
按照1.3方法,测定Fe(Ⅲ)-磺基水杨酸体系在400 nm~750 nm范围的吸收曲线,如图1所示,确定最大吸收波长为502 nm,故选择该波长为测定波长。
2.2 酸度的选择

图1 Fe(Ⅲ)-磺基水杨酸体系吸收曲线Fig.1 Absorption curve of Iron(Ⅲ)-sulfosalicylic acid system
磺基水杨酸-铁(Ⅲ)体系在强酸性条件下呈紫红色,在pH为2~3的溶液中,Fe3+离子与磺基水杨酸发生显色反应,生成的1∶1的紫红色稳定配合物;pH为4~9时,生成1∶2的红色螯合物;pH为9~11.5时,生成1∶3的黄色螯合物;pH大于12时,有色螯合物将被破坏而生成Fe(OH)3沉淀[5]。同时VC在中性或者碱性条件下易被氧化分解。为了保证显色体系较高的灵敏性和实验的准确性,溶液保持强酸性,故用0.1 mol/L高氯酸溶液调节溶液pH为2~3。
2.3 高氯酸溶液用量的选择
按照1.3方法,改变高氯酸溶液的体积,测定反应体系的吸光度变化值ΔA,绘制ΔA~V(高氯酸)的吸收曲线如图2。

图2 高氯酸溶液用量的选择Fig.2 Choice of perchloric acid volume
从图2可知,当加入2.00 mL高氯酸溶液时ΔA达到最大值,故高氯酸溶液用量为2.00 mL。
2.4 Fe(Ⅲ)标准溶液用量的选择
按照1.3方法,改变Fe3+标准溶液体积,测定反应体系的吸光度变化值ΔA,绘制ΔA~V(Fe3+溶液)的吸收曲线如图3所示。
从图3可知,当加入1.00 mL Fe3+标准溶液时ΔA最大,随后ΔA随Fe3+溶液体积增加变化不大,故Fe3+标准溶液用量为1.00 mL。
2.5 磺基水杨酸溶液用量的选择
按照1.3方法,改变磺基水杨酸溶液的体积,测定反应体系的吸光度变化值ΔA,绘制ΔA~V(磺基水杨酸)的吸收曲线如图4所示。

图3 Fe(Ⅲ)标准溶液用量的选择Fig.3 Choice of Fe(Ⅲ)volume

图4 磺基水杨酸溶液用量的选择Fig.4 Choice of sulfosalicylic acid volume
从图4可知,当加入5.00 mL磺基水杨酸时ΔA值较大,随着磺基水杨酸的量的增加ΔA变化不大,故磺基水杨酸溶液的用量为5.00 mL。
2.6 稳定性
按照实验方法,在室温下测定反应体系在不同时间的吸光度变化值ΔA与反应时间t的关系如图5所示。
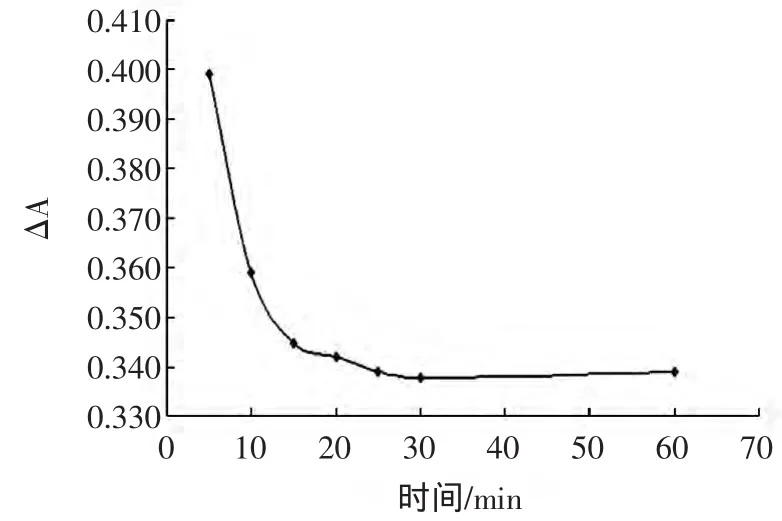
图5 反应时间的选择Fig.5 Choice of reaction time
由图5可知,体系在30 min~60 min内ΔA基本不变,故本实验选择反应时间为30 min即可。
2.7 标准工作曲线
按照实验方法,在Fe(Ⅲ)-磺基水杨酸体系中准确加入不同体积的抗坏血酸标准溶液,测定反应前后吸光度变化值ΔA,并绘制ΔA~CVc标准工作曲线如图6所示。
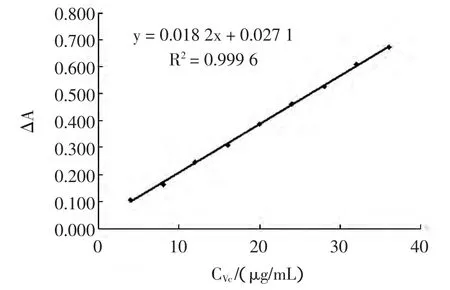
图6 标准工作曲线Fig.6 Standard working curve
从图 6 可知,在质量浓度为 4 μg/mL~37 μg/mL 范围内,吸光度之差ΔA(y)与抗坏血酸浓度CVc(x)呈较好的线性关系,其线性回归方程为y=0. 0182x+0. 0271,相关系数 r=0. 9996。
连续测定空白溶液吸光度11次,测定相对标准偏差σ=0.005。取置信系数k=3,按上述线性回归方程,其斜率S=0. 0182 mL/μg,则该方法检出限D为0.824 μg/mL(D=kσ/S)。
2.8 沙田柚果肉中VC含量的测定
准确移取5.00 mL沙田柚果肉样品溶液于25 mL容量瓶中,按照实验方法,测定体系吸光度的变化值ΔA,从标准曲线中求出相对应的VC含量,计算出沙田柚果肉中VC的含量。平行测定5次,结果与碘量法对比见表1。
分别准确移取处理好的沙田柚果肉样品溶液5.00 mL于5个25 mL容量瓶中,加入1.00 mL抗坏血酸标准溶液后,按照上述实验方法,测定加标回收率,结果见表1。

表1 梅县沙田柚果肉中VC含量的测定(n=5)Table 1 Determination results of Vitermin C in Shatian pomelo pulp and recoveries of the method(n=5)
3 结论
对Fe(Ⅲ)-磺基水杨酸体系褪色光度法测定VC含量的实验条件进行了优化,利用该法测得梅县沙田柚果肉VC的含量为97.92 mg/100 g,测定相对标准偏差为1.1%,测定回收率为95.6%~98.9%(n=5)。该法方法简单易行,测定结果与碘量法相近。
[1] 中华人民共和国药典委员会.中华人民共和国药典二部[M].北京:化学工业出版社,2000:792
[2] 叶青,江志波.酸碱滴定法与碘滴定法测定维生素C[J].理化检验-化学分册,2007,43(5):410-412
[3] 陆茜,陈凤群,万昆.紫外分光光度法测定维生素C含量[J].江汉大学学报:自然科学版,2005,33(2):68-69
[4] 蔡卓,黄富嵘,梁信源,等.重铬酸钾分光光度法测定药片中维生素 C[J].广西大学学报:自然科学版,2008,33(3):289-296
[5] 马红燕,高瑞,孙雪花,等.磺基水杨酸-铁(Ⅲ)体系光度分析法测定维生素C的研究[J].化学试剂,2009,31(8):619-621
[6] 陈秋丽,甘振威,张娅婕,等.电位滴定法测定深色蔬菜和水果中的维生素C[J].吉林大学学报:医学版,2004(5):11-14
[7] 姜波,范圣第,刘长建.菠萝中维生素C的高效液相色谱分析[J].大连民族学院学报,2003,5(1):52-53

