氰基丙烯酸盐增强口腔石膏模型强度的研究
魏焱 高原 吕锦 王斌 刘劲松
1.成都市第一人民医院口腔科,成都 610041;2.温州医科大学附属口腔医院口腔修复科,温州 325027
石膏材料广泛应用于医学、牙科学、建筑业和艺术行业,但较差的机械性能限制了其使用。在口腔医学领域,石膏模型材料主要被用于制作口腔软硬组织的阳模,能够再现口腔软硬组织的解剖形态,是义齿加工的依据。因此石膏模物理机械性能的稳定性与义齿的修复质量有着密切的关系,其强度和耐磨性能会影响修复体的制作精度,甚至修复效果。为了提高修复体制作的精度以满足口腔患者日益增长的修复需求,研究者们尝试用多种方法来提高口腔模型材料的强度和耐磨性能。有学者[1]将具有较高强度的树脂材料引入到牙科领域以代替石膏材料。然而,环氧树脂类材料由于自身尺寸精确性不足限制了其应用。Craig等[2]描述了在石膏材料中用硅胶或可溶性树脂代替水的方法。但是该法由于其不可预测的凝固膨胀系数难以在牙科领域推广。还有学者尝试通过在石膏模型表面涂覆薄层硬化剂,如氰基丙烯酸盐、环氧树脂、苯乙烯丙烯酸或合成树脂来提升石膏模型的强度和耐磨性。这种方法由于价格低廉、操作简便,适合在牙科实验室广泛应用和发展[3-6]。然而,最近的纳米印痕试验和扫描电镜(scanning electron microscope,SEM)观察表明石膏硬化剂只在石膏模型表面附着了很薄的一层,渗透十分有限,难以有效改善材料强度[7]。
氰基丙烯酸盐虽然已被应用于牙科领域的石膏材料,但是其仅仅局限于被用作表面保护剂[4]和修复性粘接材料[8]。如果能够将其深入渗透到石膏材料中,则可能通过氰基丙烯酸盐的自凝作用这一优势将石膏晶体凝结而增加强度。本文拟探索一种用氰基丙烯酸盐强化石膏材料的简易方法,并证实了其对石膏材料强度的增强作用。
1 材料和方法
1.1 溶液制备及黏度测定
将氰基丙烯酸正丁酯(Sicomet 6000;Sichel-Werke GmbH公司,德国)加入三氯甲烷液体中(Merck KgaA公司,德国),制成20%和30%的溶液,同时加入对苯二酚(Merck Schuchardt OHG公司,德国)以稳定溶液、抑制自凝。溶液的黏度用应力控制流变仪(Haake RheoStress 1,Thermo Scientific公司,美国)检测,该仪器带有一个圆锥(60 mm直径,1°角)和平板,在20 ℃条件下,切变速率在60 s内从1 000 s-1下降到200 s-1。仪器用蒸馏水校准,溶液在制备后即刻、24 h及48 h后分别作检测。
1.2 样本制备
本实验所用的石膏为3型牙科石膏(Gypsum公司,美国),系硫酸钙在125 ℃及高压锅内蒸汽压力下加热脱水制得[9]。牙科石膏按照产品说明书在真空条件下混合,注入模具,凝固2 h,然后打磨成35 mm×4 mm×4 mm尺寸的长条形共90个样本,随机分成3组,即对照组(未浸润氰基丙烯酸正丁酯溶液)、20%组和30%组(两个实验组,分别浸润20%和30%氰基丙烯酸正丁酯溶液),最后所有样本用1 200号金刚砂纸抛光。所有样本经超声清洁后在室温下干燥24 h。用低速切削机在样本上预先制备深度约1.8 mm的缺口。将两组石膏样品分别浸润于两种不同浓度的氰基丙烯酸盐8 h,于室温下干燥12 h。然后用特制的压缩空气驱动带有固定刀片的循环运动机将缺口切削锋利,并再向深处延伸100~200 μm。缺口的最终长度用装有物镜测微计(Olympus公司,日本)的光学显微镜(YS2-H,Nikon公司,日本)进行测量,达到1 μm的精确度。为了尽量减少切口钝化效应,测量每个缺口末端两侧以确保其直径小于10 μm。
1.3 纳米压痕试验
纳米压痕试验采用纳米级压痕试验系统(UMIS-2000,CSIRO公司,澳大利亚)。将样本固定在一个并联机器的金属底座上,安装有样本的基座上有磁铁以保证其与UMIS系统间足够的接触。样本的弹性模量和硬度采用经校准的Berkovich硬度计压头在20 mN的固定加载下测定。36个压痕以6×6阵列的形式排列在抛光面上,每个压痕间相距50 μm以避免邻近压痕残余应力的影响。两个实验组的样本采用与上述相同的方法。所有压痕试验均在标准实验室环境下进行(23 ℃±1 ℃,50%±5%相对湿度)。
1.4 抗压强度及布氏硬度测试
该实验亦在标准实验室条件下进行。用抗压强度试验机测试试件的抗压强度,实验所用加荷速率为7 kN·min-1,直至试件压缩断裂。记录所施最大力(F),按公式计算每一件试件最大强度(S),S=F/314,单位为MPa。
用布洛维硬度计(HBRX-187.5型,济南方圆试验仪器有限公司)测量石膏的布氏硬度,压球直径10.0 mm,实验力2 452 N,保持力时间60 s,分别从实验组和对照组中取10件样品,每件样品取5个不同的部位各打1个点进行测量,点与点之间间隔1 cm,记录压痕直径并读出布氏硬度值,最后取其平均值。
1.5 双轴强度
在标准实验室环境下,采用环夹具带有活塞的英斯特朗万能试验机(Model 3369,Instron公司,美国)进行检测,卡头速度为0.5 mm·min-1。样本盘的直径分别为10、8、3 mm以支持活塞的圆盘和尖端。记录最大负载以计算双轴挠曲强度σF。
1.6 断裂韧性
采用标准单边切口梁法测定断裂韧性(K1c)。用万能试验机(Model 3369,Instron公司,美国)对制备的样本进行三点弯曲形式的加载,支持跨度为30 mm,卡头速度为0.5 mm·min-1,直至材料断裂。每个实验组制备5个样本。
1.7 能量色散X线光谱仪(energy dispersive X-ray spectroscopy,EDX)检测
为了分析石膏表面变化,石膏样品断面喷金后用电镜带有的EDX(JEOL 6700 FESEM,JEOL公司,美国)检测材料表面元素。
1.8 数据分析
采用OriginPro 8软件对实验结果进行分析,均值间的差异采用方差分析(ANOVA),组间比较采用one-way ANOVA(带有Tukey post-hoc比较),P<0.05为差异有统计学意义。
2 结果
2.1 氰基丙烯酸正丁酯溶液黏度测定结果
黏性测定表明该溶液为牛顿流体,48 h内黏性小幅上升,但在室温下仍接近水(图 1)。在室温下存放1周后,30%的溶液因过于黏稠而难以使用。
2.2 石膏机械性能
两个实验组与对照组相比具有较高的弹性模量、双轴强度、断裂韧性、抗压强度和布氏硬度(P<0.05);其中,20%组改善石膏的双轴强度、断裂韧性、抗压强度和布氏硬度分别达39%、30%、63%、18%。但两个实验组间差异无统计学意义(P>0.05)(表1)。

图1 稀释氰基丙烯酸盐溶液制备48 h内的黏度Fig 1 Records of viscosities of the diluted cyanoacrylate solutions with 48 h of operation
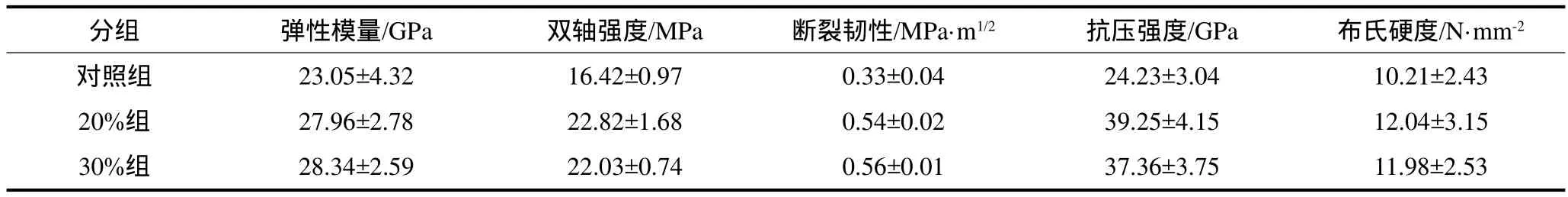
表1 对照组、20%组和30%组石膏的机械性能Tab 1 Mechanical properties among control group, 20% group and 30% group
2.3 EDX检测结果
EDX检测结果见图2。由图2可见,对照组材料包括氧、硫、钙峰,与石膏一致。实验组的石膏样本具有更高的碳峰。
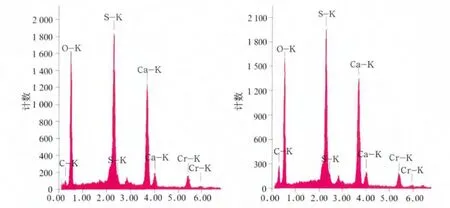
图2 EDX检测结果Fig 2 The results of EDX spectra
3 讨论
石膏模型是制作各种修复体的工作模型,它是制作各种精密的修复体的基础。它必须能够再现口腔软硬组织的解剖形态,同时要有一定的抗弯强度。如果石膏模型抗弯强度不足,模型在脱模时可能会折断;在义齿制作的过程中也可能会发生断裂。有学者[10]经过研究发现,石膏模型的抗弯强度是有限的,当遇到长窄的牙体需要预备取模、灌模时更为明显。石膏模型材料的物理机械性能与所制作修复体的精度也紧密相关,它会影响修复体的制作精度乃至成败。
本实验测定了稀释的氰基丙烯酸盐溶液的黏性,为本实验选择合适浓度的氰基丙烯酸盐溶液做准备。结果表明该稀释的溶液为牛顿流体,48 h内黏性小幅上升,而更高浓度的氰基丙烯酸盐由于其自凝作用导致溶液黏性短时间内快速增加而难以实施。在室温下存放1周后,30%的溶液因过于黏稠而难以使用。考虑到流变仪部件可能因此被粘连而没有测量溶液的黏性。黏性的改变可能源于氰基丙烯酸盐的自凝作用,其与空气中的微量水接触即能通过阴离子聚合机制发生聚合[11]。进一步研究证实pH值、温度以及其他因素均能影响聚合作用[12],表明该溶液只能现用现配,配置好后密闭容器内保存48 h内即应用完,加工温度也应严格控制,因为温度过高可能加速聚合作用,过低则会增加溶液黏性。
不同氰基丙烯酸盐浓度实验组和对照组的机械性能(包括纳米压痕弹性模量、双轴强度、断裂韧性、抗压强度和布氏硬度)检测结果显示:实验组与对照组相比具有较高的弹性模量、双轴强度、断裂韧性、抗压强度和布氏硬度;浸润20%氰基丙烯酸盐溶液的石膏比浸润30%氰基丙烯酸盐溶液的石膏的双轴强度、抗压强度和布氏硬度均高。这个结果比之前报道的类似材料中采用环氧树脂浸润法效果更为显著[5]。分散的纳米压痕弹性模量数据是由于材料的多孔特性造成的,类似于He等[13]关于羟磷灰石的报道。
EDX分析结果显示对照组材料的氧、硫、钙峰与石膏基本一致。实验组石膏样本的断裂表面中心具有更高的碳峰,提示氰基丙烯酸盐从样本中渗透。而实验材料的其他性质,包括耐水性、尺寸稳定性以及表面耐磨性等仍需进一步的研究加以证实。
综上所述,本研究的方法不但经济实用,操作简便,而且能有效的提高石膏模型材料的机械性能,使其能够承受牙科修复体制作过程中的载荷,为提高口腔模型材料的强度提供了参考依据。该方法制作的实验材料的耐水性、尺寸稳定性以及表面耐磨性等仍需进一步的研究。
[1]Prisco R, Cozzolino G, Vigolo P. Dimensional accuracy of an epoxy die material using different polymerization methods[J]. J Prosthodont, 2009, 18(2):156-161.
[2]Craig RG, Powers JM. Restorative dental materials[M]. St.Louis: Mosby Inc., 2002:1-584.
[3]Fukui H, Lacy AM, Jendresen MD. Effectiveness of hardening films on die stone[J]. J Prosthet Dent, 1980, 44(1):57-63.
[4]Ghahremannezhad HH, Mohamed SE, Stewart GP, et al.Effects of cyanoacrylates on die stone[J]. J Prosthet Dent,1983, 49(5):639-646.
[5]Sanad ME, Combe EC, Grant AA. Hardening of model and die materials by an epoxy resin[J]. J Dent, 1980, 8(2):158-162.
[6]Harris PE, Hoyer S, Lindquist TJ, et al. Alterations of surface hardness with gypsum die hardeners[J]. J Prosthet Dent,2004, 92(1):35-38.
[7]He LH, van Vuuren LJ, Planitz N, et al. A micro-mechanical evaluation of the effects of die hardener on die stone[J]. Dent Mater J, 2010, 29(4):433-437.
[8]Hasan RH. The effect of microwave disinfection on tensile strength of dental gypsum[J]. Al-Rafidain Dent J, 2008, 8(2):213-218.
[9]McCabe JF, Walls AWG. Applied dental materials[M]. Oxford: Blackwell Publishing Ltd, 2009:1-303.
[10]Derrien G, Sturtz G. Comparison of transverse strength and dimensional variations between die stone, die epoxy resin, and die polyurethane resin[J]. J Prosthet Dent, 1995,74(6):569-574.
[11]Pepper DC. Kinetics and mechanisms of zwitterionic polymerizations of alkyl cyanoacrylates[J]. Polym J, 1980, 12(3):629-635.
[12]Behan N, Birkinshaw C. The mechanism of polymerization of butyl cyanoacrylate in aqueous dispersions[J]. Colloid Polymer Science, 2000, 21(13):884-886.
[13]He LH, Standard OC, Huang TT, et al. Mechanical behavior of porous hydroxyapatite[J]. Acta Biomater, 2008, 4(3):577-586.

