Castleman病继发副肿瘤性天疱疮和系统性红斑狼疮一例
吴玮 范瑞强 罗家胜 秦晓民
Castleman病继发副肿瘤性天疱疮和系统性红斑狼疮一例
吴玮 范瑞强 罗家胜 秦晓民
患者男,47岁。反复口腔溃疡1年余,全身水疱9个月余。体检:口腔内见多处溃疡面,唇黏膜见片状糜烂面、黄色或黑褐色痂皮和嘴角浸渍发白,张口困难;鼻孔黏膜交界处、眼睑缘和阴茎冠状沟见黄褐色痂和脱痂后的淡红斑;躯干、四肢见散在红斑和水疱,大疱疱壁紧贴皮肤、部分破裂,基底潮红,类似多形红斑样改变,部分疱壁浑浊,见白色药痂黏着或黑色痂皮,尼氏征阴性;10指(趾)甲周见皱缩的水肿性暗红斑。水疱组织病理和皮损直接免疫荧光检查符合天疱疮诊断。纵隔肿瘤组织病理和免疫组化符合Castleman病(透明血管型)伴滤泡树突细胞增生。实验室检查:血清补体C3下降以及抗核抗体、抗核小体抗体、dsDNA抗体均阳性。诊断: Castleman病、副肿瘤性天疱疮、系统性红斑狼疮。用小剂量泼尼松和硫唑嘌吟治疗2个月后皮疹完全消退,免疫抑制药物缓慢减量,治疗6个月后,患者自行停用免疫抑制药物改为中药治疗,皮疹发展为中毒性表皮坏死松解症,最后死亡。该病在肿瘤切除后免疫抑制药物需维持一段较长时间,否则可导致皮疹反复或加重。
巨淋巴结增生;副肿瘤性天疱疮;红斑狼疮,系统性
Castleman病是一种良性的淋巴细胞增生性肿瘤,又称巨大淋巴滤泡增生,可引起特征性黏膜及皮肤损害,表现与天疱疮相似的病理和免疫荧光,也可出现结缔组织病的一系列表现。现报告 1例 Castleman病继发副肿瘤性天疱疮(paraneoplastic pemphigus)和系统性红斑狼疮(SLE)。
一、病历资料
患者男,47岁,反复口腔溃疡1年余,全身反复水疱9个月余。患者于1年前发热后口腔出现多处疼痛性溃疡,诊治不详,无好转,2个月后龟头上也出现糜烂和疼痛,曾到某口腔医院诊治,诊断为白塞病,治疗后(具体不详)龟头糜烂好转,但口腔溃疡仍反复。就诊前9个月,双手掌出现散在的红斑和水疱,伴瘙痒,之后四肢和躯干多处出现红斑和水疱,瘙痒剧烈。患者一直用中药煎剂治疗,病情反复。就诊前20天皮疹增多,全身出现水疱、糜烂和结痂,口腔溃疡加重,逐渐波及到双唇、鼻黏膜和眼睑缘,溃疡表面结痂,张口受限,遂到我院,查血常规、Trust试验、HIV抗体均正常,予抗过敏药物效果不佳。拟诊天疱疮于2012年8月18日收入我科。发病以来患者体重减轻10 kg,无关节疼痛和发热,家族中无类似病史。既往史:否认高血压、糖尿病、肾病、肝炎、肺结核等病史,否认药物过敏史。5年前曾行胸部CT检查提示右上纵隔一直径约2 cm的肿物,考虑为肿大淋巴结,未作处理。
体检:体温37℃,脉搏80次,呼吸24次,血压120/80 mmHg (1 mmHg=0.133 kPa)。精神疲惫,消瘦。全身浅表淋巴结未及肿大,心肺腹无明显异常。皮肤科情况:双侧颊黏膜、上颚黏膜、舌边缘见多处溃疡面;唇黏膜见片状糜烂面、渗出、黄色或黑褐色痂皮和嘴角浸渍发白,张口困难;鼻孔黏膜交界处、眼睑缘和阴茎冠状沟见浆痂和脱痂后的淡红斑;躯干、四肢见散在红斑和水疱,大疱疱壁紧贴皮肤、部分破裂,基底潮红,类似多形红斑样改变,部分疱液浑浊,见白色药痂黏着或黑色痂皮,尼氏征阴性;10指(趾)甲周见皱缩的水肿性暗红斑。见图1~3。
实验室检查:白细胞5.5×109/L,嗜酸性粒细胞0.12、计数1×109/L,血红蛋白119 g/L(参考值135~175 g/L)。免疫功能6项(2次结果相似):IgM 2.48 g/L(0.4~2.3 g/L),C3 0.43 g/L(0.9~1.8 g/L)、CH50 20 U/m(l23~46 U/ml),C4正常。自身免疫抗体(2次结果相似):抗ANA抗体1∶1 000、均质型,抗组蛋白抗体弱阳性,抗核小体抗体阳性,抗dsDNA抗体(++),重组Ro-52弱阳性。总IgE 632.4 IU/ml (0~200 IU/ml);EB病毒抗体VCA-IgA阳性,EB病毒早期抗体EA-IgA阴性。血细胞沉降率19 mm/1 h;白蛋白31.4 g/L (40~55 g/L)。尿粪常规、肝功能、凝血4项、肺癌3项、前列腺癌标抗体、血管炎3项(抗PR3、MPO、GBM抗体)、CA242、CA199、癌胚抗原、甲胎蛋白、类风湿因子、C反应蛋白均正常。结核抗体、天疱疮抗体和类天疱疮抗体均阴性。X线胸片:右上纵隔肿块5 cm×6 cm×7 cm。胸部CT(图4):右前上纵隔内见一团状软组织肿块影,边界清楚,大小7.2 cm× 5.9 cm×9.6 cm,考虑:右前纵隔内肿块,巨淋巴结增生可能,心包少许积液;双肺散在少许炎症,双肺上叶多发性肺大泡。背部水疱组织病理检查(图5):轻度角化过度,部分基底细胞层上水疱,部分为棘层内水疱,水疱内见棘刺松解细胞,真皮浅层及血管周围散在淋巴细胞和嗜酸性粒细胞浸润;直接免疫荧光:棘细胞间IgG(±)、C3(++)(图6),基底膜带IgG(+), IgA和IgM均为阴性。符合天疱疮组织病理改变。
二、治疗经过
根据皮损组织病理和免疫荧光,结合临床和实验室检查,拟诊副肿瘤性天疱疮、Castleman病?SLE。给予丙种球蛋白5 g静脉注射每日1次,用5 d,泼尼松25 mg/d,于同年9月12日在胸外科行右上前纵隔肿物切除术,并清除颈部淋巴结20个。纵隔肿物病理检查:包膜完整,表面灰红,质地细腻。肿瘤组织中可见结节状成分和弥漫生长成分:结节状成分为生发中心萎缩伴透明变的淋巴滤泡,周边套区小淋巴细胞增生,围绕生发中心呈同心圆样排列,可见毛细血管穿透套区并长入生发中心(图7);弥漫生长区由梭形至卵圆形细胞构成,排列呈束状、席纹状,瘤细胞核卵圆形或长梭形,核仁小,核膜薄,瘤细胞异形性不明显,梭形细胞间见均匀粉染沉积,间质淋巴细胞、浆细胞及组织细胞反应明显,局部见多核巨细胞。免疫组化结果:CD3、CD5、CD7、CD20、PaX-5、CD21、CD23均阳性,CD15、CD30、TdT、SMA、CD35均阴性;散在浆细胞CD38、CD138阳性,血管CD34阳性;符合Castleman病(透明血管型)伴滤泡树突细胞增生及间质硬化。另见淋巴结20个,呈反应性增生改变。最后确诊为Castleman病(透明血管型)、副肿瘤性天疱疮、SLE。术后继续予泼尼松25 mg每日1次,4周后皮肤糜烂面大部分消退,腋下和胸壁仍有水疱和糜烂面,唇黏膜和口腔内仍有糜烂和疼痛,影响进食,加服硫唑嘌吟50 mg每日2次,治疗4周后皮疹和黏膜糜烂基本消失。12月6日自身抗体结果:ANA 1∶320均质型,抗组蛋白抗体、抗核小体抗体、抗dsDNA、重组Ro-52均阴性;IgM 3.51 g/L,C3 0.61 g/L、CH50、C4正常。2013年1月,复查胸部CT未见异常,黏膜溃疡和皮疹无复发,糖皮质激素和免疫抑制剂逐渐减量。同年3月,患者突然自行停用泼尼松和硫唑嘌吟,改为纯中药治疗,1周后口腔溃疡复发,全身出现散在水疱,坚持仅服中药治疗,1个月后出现中毒性表皮坏死松解症样皮疹。胸片:右上肺前段、右中肺纤维灶,未除外左肺上叶支气管扩张并感染,未见纵隔肿物。自身抗体: ANA 1∶3 200,dsDNA(-),补体C3 0.51。最后死于感染性多器官功能衰竭。
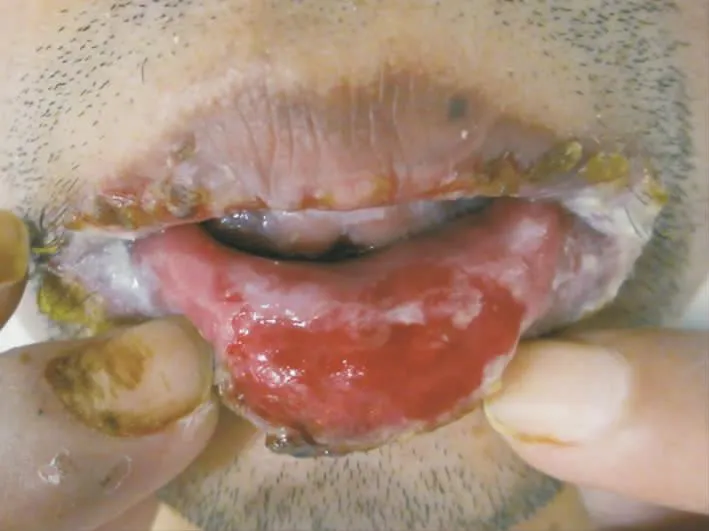
图1 患者唇黏膜见糜烂面、渗出、黄色或黑褐色痂皮,口角浸渍发白

图2 10指甲周见皱缩的水肿性暗红斑

图3 趾甲周见水肿性暗红斑,右足背和小腿暗红斑,见糜烂面和水疱

图4 胸部CT:右前上纵隔内见团状软组织肿块影,边界清楚
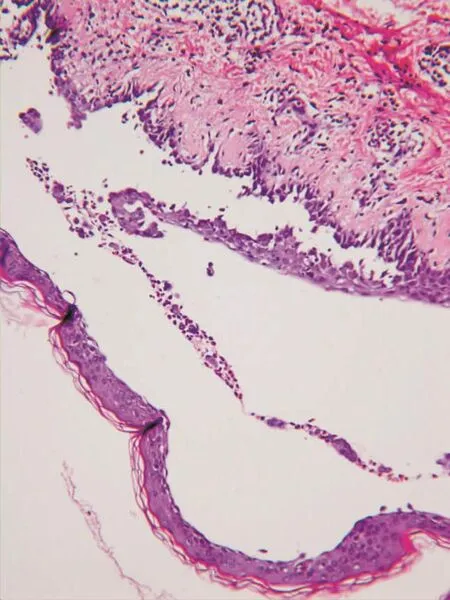
图5 皮损组织病理:表皮内水疱,棘层松解细胞,真皮浅层及血管周围散在淋巴细胞和嗜酸性粒细胞浸润(HE×200)

图6 直接免疫荧光:C3棘细胞间沉积(HE×200)

图7 小血管长入生发中心,内皮细胞增生,生发中心透明变,周围小淋巴细胞呈洋葱皮样排列(HE×200)
三、讨论
Castleman病是一种病因不明的良性淋巴结增生性疾病,可累及淋巴结区域的任何部位,以胸部纵隔淋巴结最常见,其次是颈部、腋下、腹部和腹股沟等部位。该患者5年前行胸部CT曾发现右上纵隔处有1处直径约2 cm的肿大淋巴结,逐渐增大到直径6 cm,说明Castleman病是一个良性增生过程,对于无症状的深部肿大淋巴结是否需早期切除是个值得探讨的问题。根据组织病理学Castleman病分为3种类型:透明血管型、浆细胞型、混合型。本例患者根据临床表现、胸部CT和病理结果提示为单中心透明血管型Castleman病[1]。Castleman病的治疗方法和疗效与其分型和继发的疾病有关,对于单中心型首选手术切除肿瘤。2005年朱学骏等[2]报告对于伴发副肿瘤性天疱疮的单中心型Castleman病患者早诊断、早切除肿瘤是成功治疗副肿瘤性天疱疮的关键。本例患者也采取了相同的治疗方法,并在纵隔肿瘤切除后取得较好的短期疗效,但用小剂量糖皮质激素和硫唑嘌吟治疗6个月后患者突然停用转而改服中药煎剂,出现中毒性表皮松解症样皮疹,最后死亡。
副肿瘤性天疱疮并发的肿瘤很多,在中国以Castleman病为最常见[3]。王亮春等[4]对Castleman肿瘤组织细胞进行培养及鉴定培养细胞上清液中抗体成分,发现Castleman肿瘤组织能够分泌抗体,且抗体性质与血液中的抗体性质基本相同。Tey等[5]曾报道Castleman病可能始发于暴露于表皮表位的界面皮炎,从淋巴肿块释放出来的IL-6激活了分子模拟和表位扩展,导致自身抗体的产生。皮损形态的多样性可能与疾病发展过程中以细胞免疫还是体液免疫介导为主有关,各种皮疹可同时共存,也可由一种皮疹发展成另一种皮疹,当表现为松弛性大疱时类似寻常型天疱疮和落叶型天疱疮,这些大疱可能发展为大面积表皮剥脱,类似于中毒性表皮坏死松解症[6]。Kim等[7]报道1例患SLE1年的41岁患者,出现难治性口腔溃疡和躯干部暗红斑,皮肤病理活检提示天疱疮样改变,影像学检查发现腹膜后巨大肿块,病理活检提示为透明血管型Castleman病,切除肿瘤后SLE的自身抗体组蛋白抗体转阴,ds-DNA抗体明显下降,与本例非常相似。
总之,需要强调的是,Castleman病导致副肿瘤性天疱疮和SLE,与结缔组织病之间的因果关系还需进一步研究,同时强调与Castleman病相关的副肿瘤性天疱疮在肿瘤切除后,免疫抑制药物应用需维持一段很长的时间,否则容易导致皮疹的反复和加重。
志谢广州医学院附属第一医院病理科付欣鸽教授
[1]Wen X,Jiang X.Paraneoplastic pemphigus in association with Castleman disease of the pararenal retroperitoneum[J].J Dermatol,2012,39(7):662-664.
[2]朱学骏,王京,陈喜雪,等.伴发副肿瘤性天疱疮的Castleman瘤:附10例报告[J].中华皮肤科杂志,2005,38(12):745-747.
[3]Zhu X,Zhang B.Paraneoplastic pemphigus[J].J Dermatol,2007,34(8):503-511.
[4]王亮春,陈喜雪,赵俊郁,等.副肿瘤性天疱疮伴发Castleman肿瘤分泌致病相关抗体的初步研究[J].中华皮肤科杂志,2004,37(2):74-76.
[5]Tey HL,Tang MB.A case of paraneoplastic pemphigus associated with Castleman′s disease presenting as erosive lichen planus[J]. Clin Exp Dermatol,2009,34(8):e754-e756.
[6]Yong AA,Tey HL.Paraneoplastic pemphigus[J].Australas J Dermatol,2013,54(4):241-250.
[7]Kim KJ,Cho CS,Choi JJ.Pararenal retroperitoneal Castleman′s disease mimicking systemic lupus erythematosus[J].Int J Rheum Dis,2010,13(3):e20-e25.
2014-03-10)
(本文编辑:吴晓初)
Castleman′s disease with secondary paraneoplastic pemphigus and systemic lupus erythematosus:a case report
Wu Wei,Fan Ruiqiang,Luo Jiasheng,Qin Xiaomin.Department of Dermatology,Guangdong Provincial Hospital of Traditional Chinese Medicine,Guangzhou 510120,China
Wu Wei,Email:wuwei1350187@126.com
A 47-year-old man presented with recurrent oral ulcerations for more than 1 year and generalized vesicles for 9 months.Physical examination revealed multiple oral ulcers,patchy labial erosions with yellow or dark brown crusts,maceration and blanching of the angle of mouth resulting in difficulty in mouth opening. Cinnamomeous crusts were seen on the nasal limen,palpebral margin and coronary sulcus of penis,with pale red macules after decrustation.Diffuse erythematous patches and bullae were present on the trunk and extremities.The walls of bullae tightly clung to the skin,and some bullae were ruptured,leaving an erythematous and moist surface and giving an erythema multiforme-like appearance;some bullae were turbid and covered with adherent drugcontaining white crusts or black crusts.Nikolsky′s sign was negative.Shrinking,edematous dark-red patches were seen in periungual regions of all the fingers and toes.Histologic biopsy and direct immunofluorescence examination ofbullous lesions confirmed a diagnosis ofparaneoplastic pemphigus (PNP).Histopathologicaland immunohistochemical findings from the mediastinal tumor were consistent with Castleman′s disease(hyalinevascular type)with proliferation of follicular dendritic cells.Laboratory examination revealed a decrease in serum complement C3 and the presence of antinuclear,anti-nucleosome and anti-dsDNA antibodies.The final diagnosis included Castleman′s disease,PNP and systemic lupus erythematosus.After 2 months of treatment with low-dose prednisone and azathioprine,skin lesions completely regressed.Then,the dose of prednisone and azathioprine was tapered.Six months later,the patient himself suddenly withdrew prednisone and azathioprine,and began to take traditional Chinese medicine;thereafter,the lesions developed into toxic epidermal necrolysis(TEN),and the patient died finally.This case demonstrates that immunosuppressive therapy should be maintained for a long period of time in patients with Castleman′s disease after tumor removal,otherwise,skin lesions may recur or get worse.
Giant lymph node hyperplasia;Paraneoplastic pemphigus;Lupus erythematosus,systemic
10.3760/cma.j.issn.0412-4030.2014.10.020
510120广州,广东省中医院皮肤科
吴玮,Email:wuwei1350187@126.com

