几种三维镧系配位聚合物的合成、结构表征及其性质测定
邵彩云,王力册,卢世杉,许珍焕,刘梦岩,徐 杨,刘 流,杨立荣*
(1.河南大学 化学化工学院,河南 开封 475004;2.中原石化实业有限公司,河南 濮阳 457000)
近年来,金属-有机框架物(Metal-Organic-Frameworks,MOFs)因具有孔径可调控、结构多样及易于功能化等特性引起了研究人员的广泛兴趣.经过十多年的研究,人们已经合成并表征了大量结构新颖且具有多种功能的配位聚合物[1-3].其功能主要包括:气体分子与小分子有机蒸气的吸附与分离、多相催化、多相分离、分子与离子交换、手性识别与分离、分子磁性质、发光与非线性光学性质、电学性质等[4-11].镧系元素具有较大的离子半径和较好的亲核力,具有较高的配位数,易于形成具有特殊性质的配位聚合物.氨三乙酸有三种配位离子存在形式、高的对称性、丰富的配位方式和有利于形成螺旋结构的配合物等优点[12-14].本文作者以氨三乙酸为配体,运用水热合成法制备并表征了4个配位聚合物:[Sm(NTA)(H2O)]n、[Gd(NTA)(H2O)]n、[Dy(NTA)(H2O)]n和[Er(NTA)(H2O)]n.
1 实验部分
1.1 仪器与试剂
所用试剂氨三乙酸、氢氧化钾、硝酸钐、硝酸钆、硝酸镝和硝酸铒等均为分析纯.红外光谱的测定用德国Bruker VERTEX70型傅立叶变换红外分光光度仪,用KBr压片,在范围内400~4 000cm-1测定;用Perkin-Elmer 240C型元素分析仪进行C、H、O元素分析;单晶结构测定是在室温条件下使用Bruker Smart CCD型X-ray单晶衍射仪进行测试;热重分析使用Perkin-Elmer TGA7热重分析仪,程序升温速率10K/min,氮气流速40mL/min;荧光分析在室温下进行,采用以450W的氙气灯作为激发光源的F-7000FL荧光光谱仪.磁化率的测定是在2~300K的温度下使用Quantum Design MPMS-5仪进行测定.
1.2 X射线单晶衍射结构分析
在296(2)K下用单色化的石墨Mo Kα射线(λ=0.071 073nm)为激发光源,收集强度数据使用的是Bruker Smart CCD单晶衍射仪,采用ω/2θ扫描方式.用SADABS程序对收集到的数据进行吸收校正[15].用直接法解出配合物的结构,运用全矩阵最小二乘法对非氢原子坐标和各向异性温度因子进行精修,用SHELXTL程序[16]进行全部的计算.将配合物的主要晶体学数据进行分类并列于表1中,选取与中心金属离子有关的键长数据列于表2以及氢键数据列于表3.
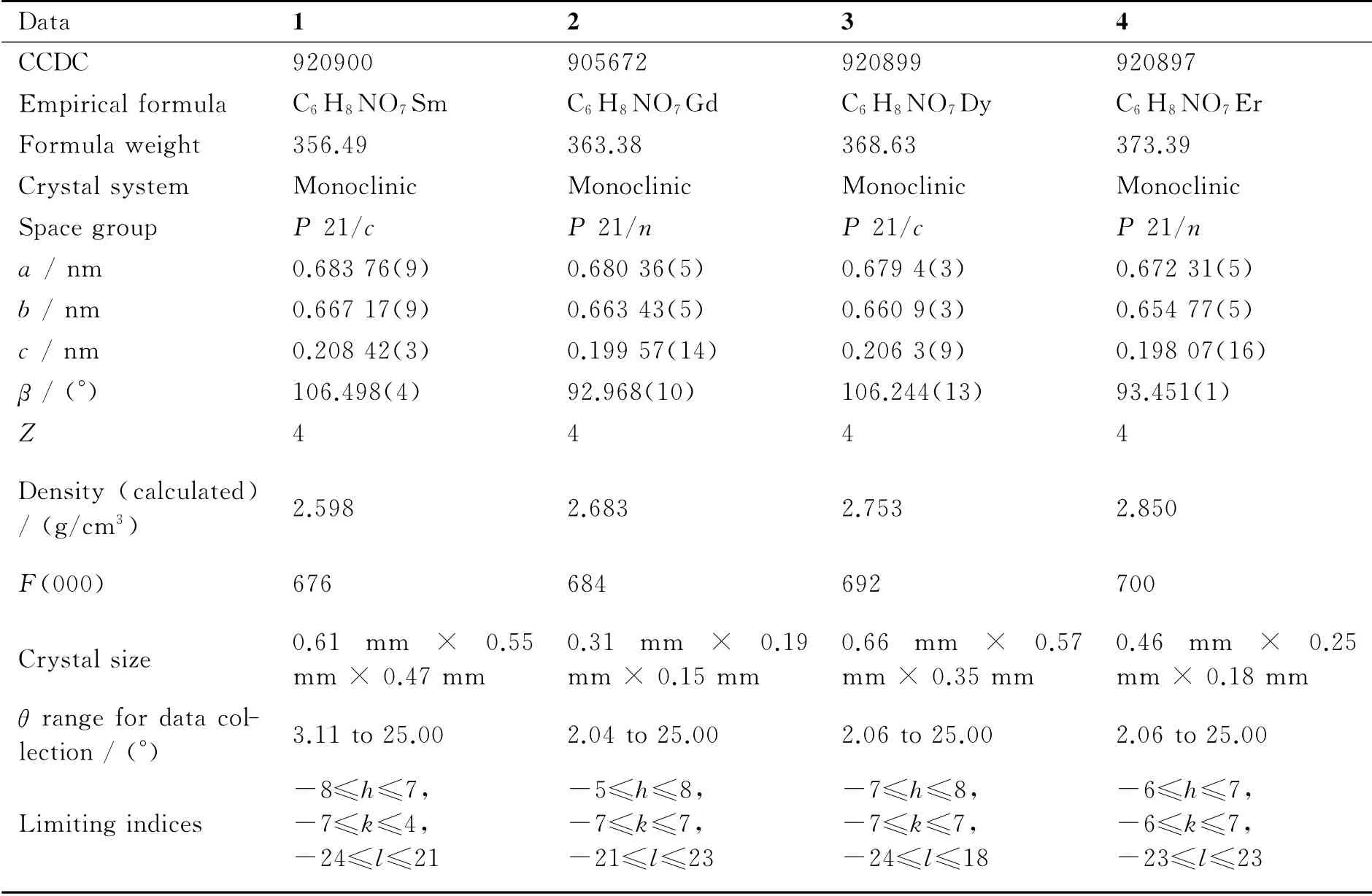
表1 配合物1-4的主要晶体数据Table 1 Crystal data and structure refinement parameters in 1-4
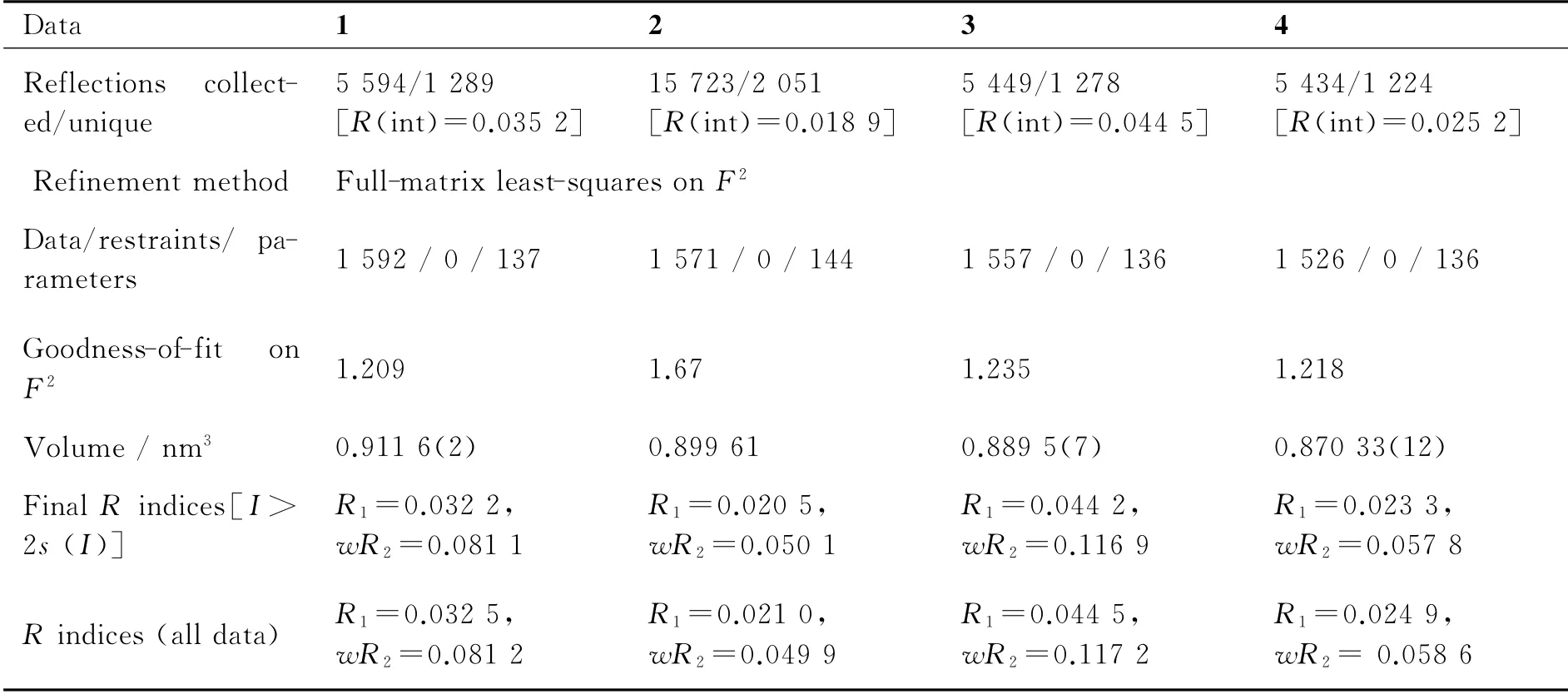
续表1
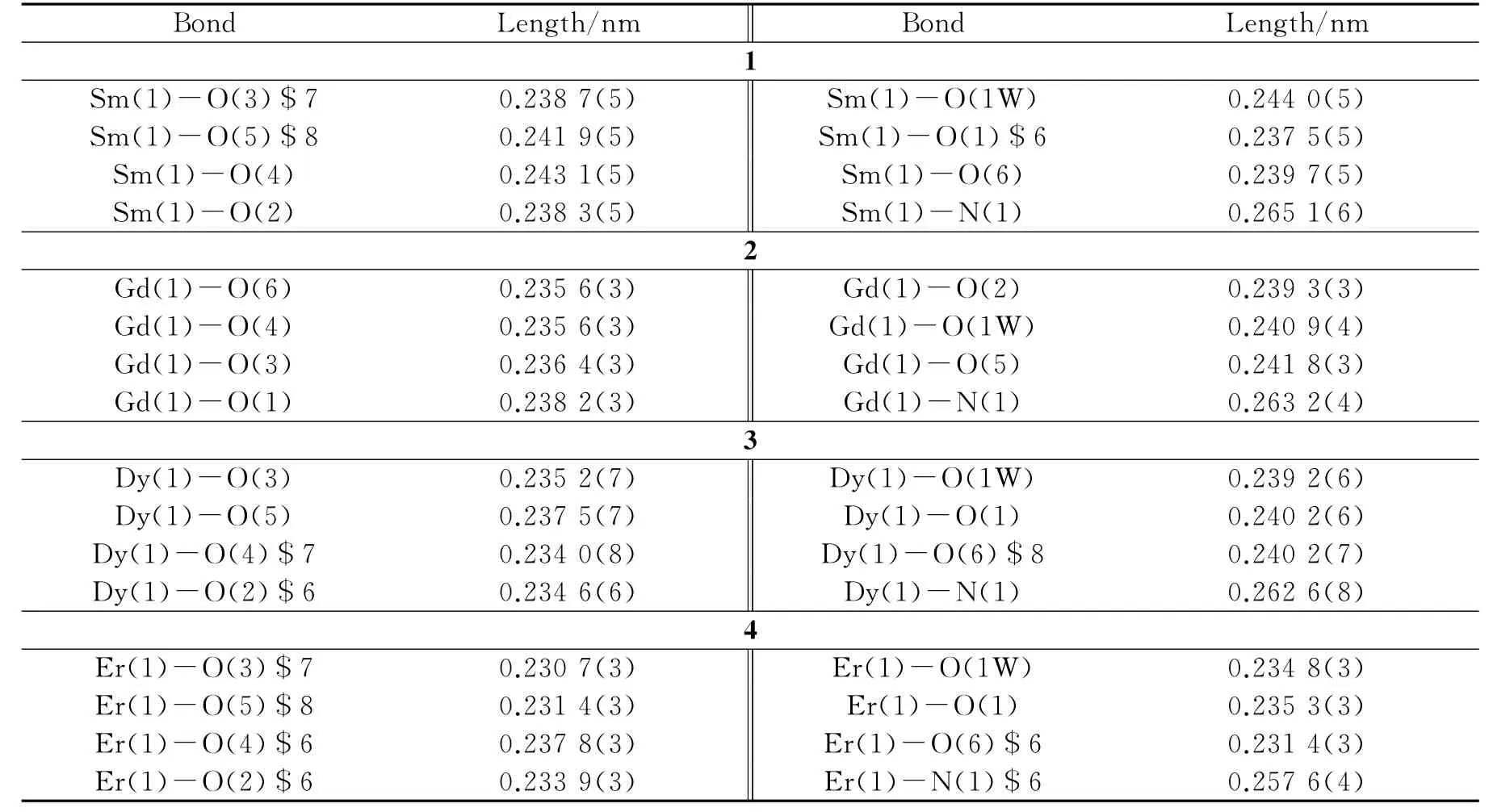
表2 配合物1-4的部分键长Table 2 Selected bond length in 1-4
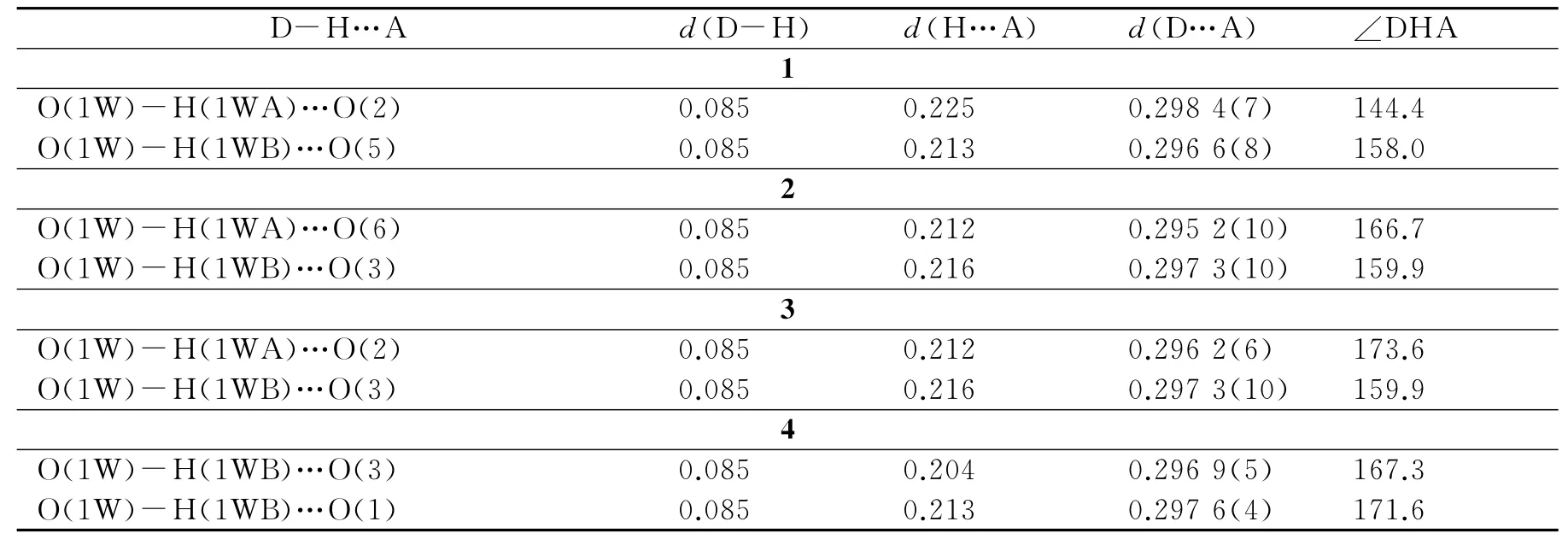
表3 配合物1-4的氢键数据Table 3 Hydrogen bond in 1-4
1.3 配合物的合成
[Sm(NTA)(H2O)]n(1)的合成:将0.2mmol的H3NTA和0.6mmol Sm(NO3)3·6H2O溶于10mL水中,在室温下用1mol/L的氢氧化钾调节混合溶液pH至5,搅拌30min.将上述溶液转移至25mL的聚四氟乙烯内衬中,并将其装入反应釜中,在160℃温度条件下反应4d,自然冷却至室温得到淡黄色晶体,产率为42.3%.元素分析数据为C6H8NO7Sm,理论值(%):C,20.22;H,2.16;N,3.93;实验值(%):C,20.42;H,2.02;N,3.57.FT-IR(KBr,cm-1)ν:3 318(br),1 634(s),1 611(s),1 478(w),1 421(s),1 389(m),1 334(m),1 312(w),1 269(w),1 246(w),1 134(w),1 023(w),987(w),969(w),954(w),934(m),914(w),773(w),729(w),695(m),654(w),566(w),493(w),438(w).
[Gd(NTA)(H2O)]n(2)的合成:2的合成与1相似,将Sm(NO3)3·6H2O换成Gd(NO3)3·6H2O,反应物的物质的量之比、反应条件不变.得到无色晶体,产率为43.5%.元素分析数据为C6H8NO7Gd,理论值(%):C,19.84;H,2.22;N,3.85;实验值(%):C,20.12;H,2.43;N,3.76.FT-IR(KBr,cm-1)ν:3 247(br),1 658(s),1 598(s),1 488(w),1 469(s),1 379(m),1 345(m),1 331(w),1 299(w),1 246(w),1 156(w),1 053(w),978(w),933(w),926(m),749(w),799(w),673(m),634(w),612(w),555(w),516(w),443(w).
[Dy(NTA)(H2O)]n(3)的合成:3的合成与1相似,将Sm(NO3)3·6H2O换成Dy(NO3)3·6H2O,反应物的物质的量之比、反应条件不变.得到无色晶体,产率为41.6%.元素分析数据为C6H8NO7Dy,理论值(%):C,19.55;H,2.19;N,3.80;实验值(%):C,19.63;H,2.08;N,3.62.FT-IR(KBr,cm-1)ν:3 387(br),2 954(w),1 659(s),1 628(s),1 468(w),1 428(s),1 387(m),1 338(m),1 315(w),1 265(w),1 227(w),1 123(w),1 019(w),989(w),968(w),949(w),927(m),913(w),756(w),738(w),699(m),654(w),623(w),569(w),523(w),467(w),432(w).
[Er(NTA)(H2O)]n(4)的合成:4的合成与1相似,将Sm(NO3)3·6H2O换成Er(NO3)3·6H2O,反应物的物质的量之比、反应条件不变.得到淡黄色晶体,产率为37.8%.元素分析数据为C6H8NO7Er,理论值(%):C,19.30;H,2.16;N,3.75;实验值(%):C,20.24;H,2.59;N,3.46.FT-IR(KBr,cm-1)ν:3 456(br),2 954(w),1 667(s),1 614(s),1 458(w),1 429(s),1 383(m),1 334(m),1 313(w),1 267(w),1 228(w),1 143(w),1 014(w),967(w),945(w),914(w),762(w),734(w),679(m),622(w),603(w),586(w),543(w),459(w).
2 结果与讨论
2.1 配合物的红外光谱
配合物1-4不溶于CH3COCH3,CH3CH2OH,CH3OH,CH3CN和THF,微溶于DMSO,DMF和H2O中,红外光谱与元素分析与单晶衍射结果相符.经过分析这些数据可以得出配体H3NTA和稀土金属离子Sm(III)、Gd(III)、Dy(III)和Er(III)分别形成了配位键.在438~695cm-1(1)、443~673cm-1(2)、478~692cm-1(3)和459~679cm-1(4)处的微弱吸收归属于Ln-O振动吸收峰.在这四个配位聚合物的红外数据中可以看到有很宽并且很强的峰3 318(1)、3 247(2)、3 421(3)和3 456(4)cm-1,可归属于水分子的羟基吸收峰[17].在1 634~1 611cm-1(1)、1 658~1 598cm-1(2)、1 656~1 612cm-1(3)和1 667~1 624 cm-1(4)范围内强吸收峰归属于配体H3NTA的COO-的伸缩振动吸收.在1 700cm-1处都没有吸收,表明H3NTA完全去质子化形成了NTA3-,并和相应的金属离子发生了配位[18].
2.2 配合物的结构描述及镧系收缩
结构分析表明,配合物1-4属同晶型同构.以配合物[Er(NTA)(H2O)]n(4)为例来描述该类配合物的结构特征.Er(III)的配位环境如图1a所示,中心原子采取N1O7的配位模式形成十二面体几何构型,三个氧原子(O(2)、O(4)和O(6))和一个N原子来自同一个氨三乙酸分子,另外四个氧原子分别来自三个氨三乙酸分子和一个配位水分子.氨三乙酸分子的配位模式如图1b所示,每个氨三乙酸分子都与四个Er(III)相连接,连接模式是μ4-(η4-N,O,O1,O2)O3,O4,O5.Er-ONTA的键长范围是0.231 4(3)~0.237 8(3)nm,Er-OW键长为0.234 8(4)nm,Er-ONTA的平均键长比Er-OW短,Er-N键长是0.257 5(4)nm.键长数据和相关文献中镧系配位聚合物是一致的[19-21].

图1 a.Er(III)的配位环境;b.NTA3-的配位模式Fig.1 a.Coordination environment of Er(III);b.Coordination mode of NTA3-
在配合物中,基本单元为菱形四面体构筑块Er8C14O28,体积为0.660 7nm×0.672 3nm×0.654 8 nm,夹角分别是119.70°和60.30°(图2b).中空的菱形四面体由八个Er原子通过O-C-O连接而成,可以容纳半径为0.285 0nm的球体.如图2c和2d所示,基本单元菱形四面体沿c轴方向无限延伸形成2D层状结构,相邻的2D层之间经由氢键组装成为3D结构.如图2e所示,在配合物4中存在两种氢键,分别是O(1W)-H(1WB)…O(3)和O(1W)-H(1WB)…O(1).有关数据见表3.
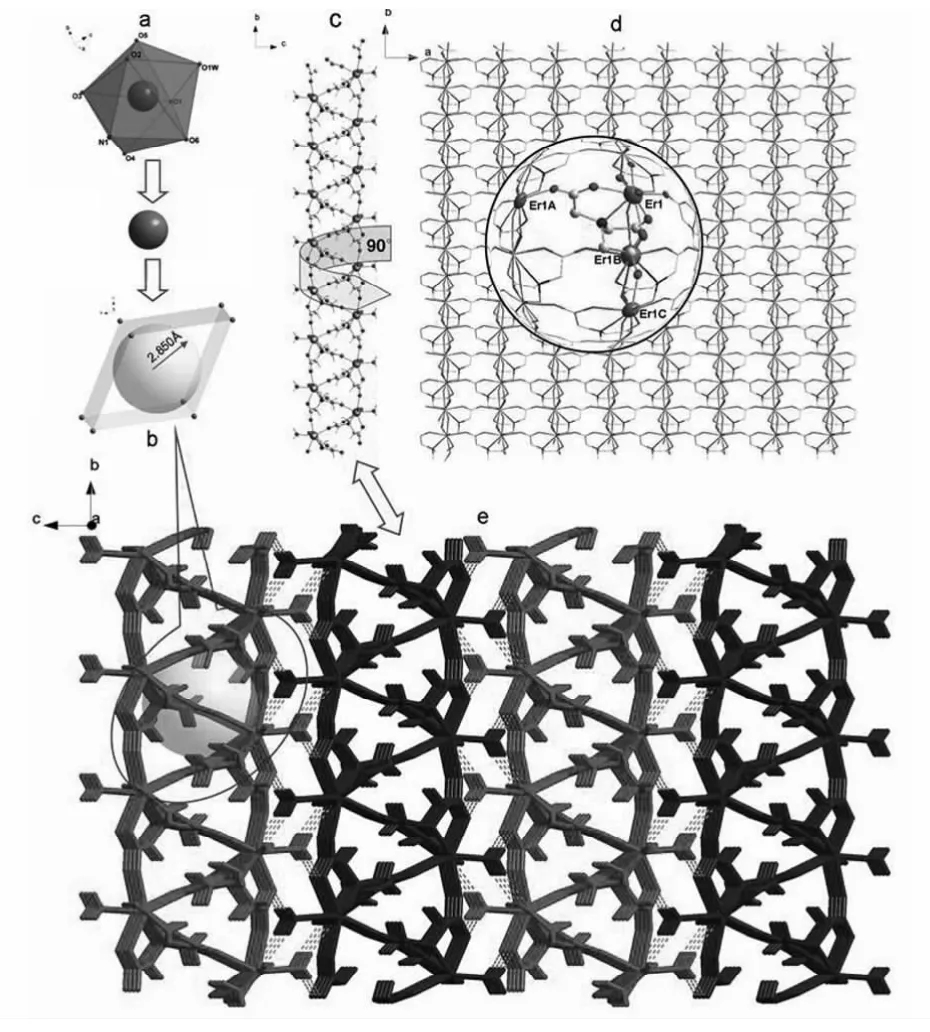
图2 a.以Er(III)为中心的多面体结构;b.配位聚合物4的基本结构单元Er8C14O28;c.a轴方向2D面;d.c轴方向2D面;e.a轴方向3D结构Fig.2 a.Highlight of the coordination polyhedra for crystallographically independent Er(III)ion;b.Er8C14O28 building block in 4;c.2Dplane of 4 viewed froma-axis;d.2Dplane of 4 viewed fromc-axis;e.Hydrogen bonding interactions in 4 presenting 3Dnetwork viewed froma-axis
对配合物1-4的键长数据分析表明该系列配聚物具有镧系收缩效应.如表4所示,配合物1-4的Ln-OW,Ln-OC,Ln-N和Ln…Ln的平均键长随着核电荷数递增而逐渐减小.
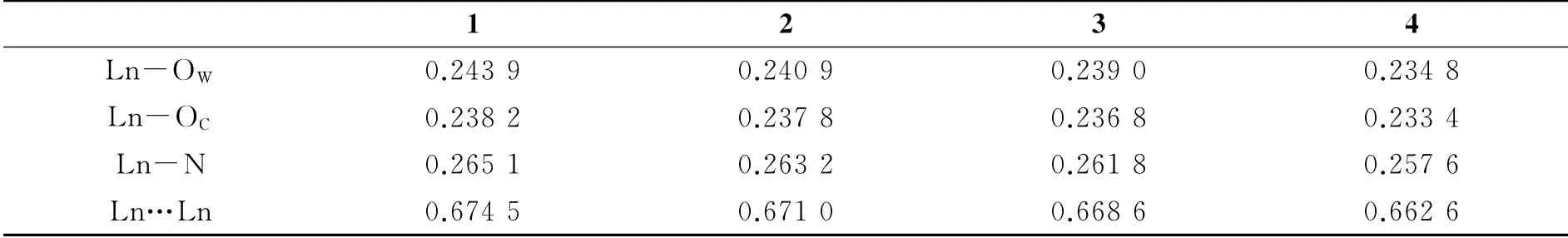
表4 配合物1-4的(平均)键长和距离Table 4 Comparison of the corresponding distances(average)in 1-4 /nm
2.3 配合物的磁性
在2.0~300K范围内测量了1以温度为变量的磁化率,χM-χMT曲线如图3所示.χM-1服从居里外斯定律,即χM=C/(T-θ)(Sm:52~300K),Weiss常量θ是-189.485K,Curie常量C是0.430cm3·mol-1·K.温度为300K时,χMT=0.297cm3·mol-1·K(1.540μB),低于理论值1.172cm3·mol-1·K(3.061μB)(Sm(III),SSm=5/2,g=2/7).连续降温至52K,χMT的值平稳地逐渐减少.以上数据和χMT相对于温度的曲线表明1呈现反铁磁性特征.
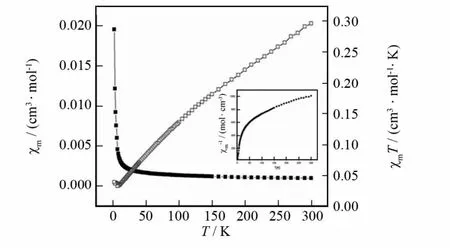
图3 配合物1的χM和χMT曲线,插入1的χM-1曲线Fig.3 Thermal variation ofχMandχMTfor 1.Insert:Plot of thermal variation ofχM-1for 1
2.4 配合物的荧光性能
将2溶于去离子水配制成1×10-4mol/L的溶液,向其中添加不同浓度的Mn2+、Cd2+、Pb2+、Hg2+和Cu2+,测定添加金属离子后对2的荧光强度及发射峰位置的影响,实验结果见图4.当加入2倍量的Hg2+(HgCl2)时,配合物2在532nm(激发波长为287nm)处的荧光强度由90a.u.增大至约1 000a.u.,发射峰的位置没有改变,其荧光强度增加了10倍多.如图4E所示,当向2中添加上述其他金属离子时,配合物2的荧光强度变化不显著.实验结果表明,配合物2对Hg2+具有荧光选择性.

图4 添加金属离子后2的荧光光谱Fig.4 Emission spectra of 2 at room temperature in the presence of metal ions
2.5 配合物的热重分析
从热重曲线(图5)中可以看出,配合物3热分解分为两个阶段进行.第一阶段在260~355℃,配合物3失重5.82%,失去的是配位水,理论值为6.07%;第二阶段在379~1 000℃,配合物3失重43.70%,归属为氨三乙酸的分解.残重为48.18%,残余物为Dy2O3,与理论值50.60%相符合.
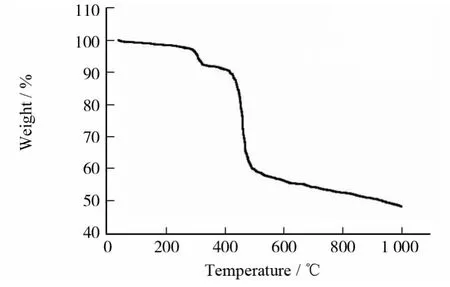
图5 配合物3的TG曲线Fig.5 TG curves of complex 3
3 结论
水热条件下合成了一系列同晶同构的稀土配位聚合物,它们通过基本结构单元Ln8C14O28形成2D层状结构,2D结构又通过氢键堆积成3D结构;该系列配合物存在镧系收缩效应;配合物1呈现出反铁磁性,配合物2对Hg2+具有较好的荧光选择性.
[1]YAGHI O M,O′KEEFFE M,OCKWIG N W,et al.Reticular synthesis and the design of new materials[J].Nature,2003,423(6941):705-714.
[2]DHAKSHINAMOORTHY A,GARCIA H.Metal-organic frameworks as solid catalysts for the synthesis of nitrogen-containing heterocycles[J].Chem Soc Rev,2014,43:5750-5765.
[3]MCKINLAY A C,BO X,WRAGG D S,et al.Exceptionalbehavior over the whole adsorption-storage-delivery cycle for NO in porous metal organic frameworks[J].J Am Chem Soc,2008,130(31):10440-10444.
[4]CHENW T,FUKUZUMI S.Ligand-dependent ultrasonic-assistant self-assemblies and photophysical properties of lanthanide nicotinic/isonicotinic complexes[J].Inorg Chem,2009,48(8):3800-3807.
[5]MA M L,CAN C J,ZANG S Q.Syntheses,structures,tunable emission and white light emitting Eu3+and Tb3+doped lanthanide metal-organic framework materials[J].Dalton Trans,2013,42(29):10579-10586.
[7]WU J Y,YEH T T,WEN Y S,et al.Unusual robust luminescent porous frameworks self-assembled from lanthanide ions and 2,2′-bipyridine-4,4′-dicarboxylate[J].Cryst Growth Des,2006,6(2):467-473.
[8]SILVA P,ANANIAS D,BRUNO S M,et al.Photoluminescent metal-organic frameworks-rapid preparation,catalytic activity,and framework relationships[J].Eur J Inorg Chem,2013,2013(32):5576-5591.
[9]GEIβLER D,LINDEN S,LIERMANN K,et al.Lanthanides and quantum dots as Förster resonance energy transfer agents for diagnostics and cellular imaging[J].Inorg Chem,2013,53(4):1824-1838.
[10]PERRIER M,KENOUCHE S,LONG J,et al.Investigation on NMR relaxivity of nano-sized cyano-bridged coordination polymers[J].Inorg Chem,2013,52(23):13402-13414.
[11]KANETOMO T,ISHIDA T.Preparation and characterization of[Gd(hfac)3(DTBN)(H2O)](DTBN=di-t-butyl nitroxide)ferromagnetic Gd3+-Gd3+super-superexchange[J].Chem Commun,2014,50:2529-2531.
[12]STARYNOWICZ P.Europium(II)complexes with nitrilotriacetic acid(NTA)[J].Polyhedron,2003,22(20):2761-2765.
[13]WANG J,ZHANG X D,ZHANG Y,et al.Coordinate structures of PrIII,GdIII,TmIII,and YbIII complexes with nitrilotriacetic acids[J].J Struct Chem,2004,45(1):114-123.
[14]KANG J G,KANG H J,JUNG J S,et al.Crystalstructures and luminescence properties of[Ln(NTA)2H2O]3-complexes(Ln=Sm3+,Eu3+,Gd3+,Tb3+,Ho3+,and NTA=nitrilotriacetate)[J].Bull Korean Chem Soc,2004,25(6):852-858.
[15]SHELDRICK G M.SADABS software for empirical absorption correction[CP].University of Göttingen,1996.
[16]SHELDRICK G M.SHELXTL V5.1software reference manual[CP].Bruker AXS Inc,Madison,1997.
[17]LI X F,HAN Z B,CHENG X N,et al.Studies on the radii dependent lanthanide self-assembly coordination behaviors of a flexible dicarboxylate ligand[J].Inorg Chem Comm,2006,9(11):1091-1095.
[18]LIU M S,YU Q Y,CAI Y P,et al.One-,two-,and three-dimensional lanthanide complexes constructed from pyridine-2,6-dicarboxylic acid and oxalic acid ligands[J].Cryst Growth Des,2008,8(11):4083-4091.
[19]YANG L R,WU L Z,ZHANG H M,et al.Synthesis,structure and luminescent recognition properties of cerium(IV)coordination polymers based on pyridine-2,6-dicarboxylic acid[J].Dyes Pigments,2013,99(2):257-267.
[20]YANG L R,LIU L,WU L Z,et al.A series of 3Disomorphous lanthanide coordination polymers based on flexible dicarboxylate ligand:Synthesis,structure,characterization,and properties[J].Dyes Pigments,2014,105:180-191.
[21]刘 流,刘冰冰,吴兰枝,等.一种新型三维配位聚合物的合成以及表征和磁性测定[J].化学研究,2013,24(5):448-453.

