兽用抗寄生虫药莫奈太尔的研究进展
梁先明,李亚菲,曾振灵∗
(1.中国兽医药品监察所,北京 100081;2.华南农业大学,广州 510642)
寄生虫感染是危害畜禽生产和畜牧业发展的重要疾病,其防治以药物为主。抗药性是畜禽寄生虫病防治中面临的日益严峻的问题,因此寻找和开发新的抗寄生虫药尤为必要。莫奈太尔(Monepantel,MNP)是诺华动物保健公司研发的一种新型氨基乙腈衍生物类驱虫药。莫奈太尔口服液(商品名ZOLVIX®)2009年9月首先在欧洲批准上市,用于治疗和控制羊肠道蠕虫感染。随后,该药在澳大利亚、新西兰和巴西等国家上市。国外已有大量研究表明该药具有较好的驱虫效果,国内尚未对该药进行系统研究和相关报道。本文就莫奈太尔的理化性质、药代动力学及药效学等研究现状进行了介绍,以期为该药在我国兽医临床上的合理应用以及开展相关研究提供参考。
1 理化性质
莫奈太尔的化学名称为:N-[(1S)-1-氰基-2-(5-氰基-2-三氟甲基-苯氧基)-1-甲基-乙基]-4-三氟甲基磺酰基-苯甲酰胺。CAS登记号:887148-69-8,分子式是C20H13F6N3O2S,分子量为473.39,化学结构式见图1。

图1 莫奈太尔的化学结构式
莫奈太尔物理性质:白色粉末,在水中几乎不溶(20 ℃时,小于0.1 mg/L),微溶于丙二醇(6.9 g/L)和正辛醇(7.3 g/L),溶于乙醇(60.7 g/L),易溶于二氯甲烷(175 g/L)和聚乙二醇(156.1 g/L)。 在pH 7.0条件下,辛醇/水分配系数logP值为3.0。
莫奈太尔主要有A、B两种晶型,A晶型熔点125℃,B晶型熔点142~149℃,其中B晶型为优势晶型,A晶型在一定条件下可以转化为B晶型。莫奈太尔结构中有一个手型中心,S构型为有效构型,在甲醇中的比旋度为-32°。诺华动物保健有限公司上市的ZOLVIX®,为2.5%的莫奈太尔口服溶液,剂量为绵羊每kg体重2.5 mg,相当于1 mL。莫奈太尔的合成方法[1]如图2所示。
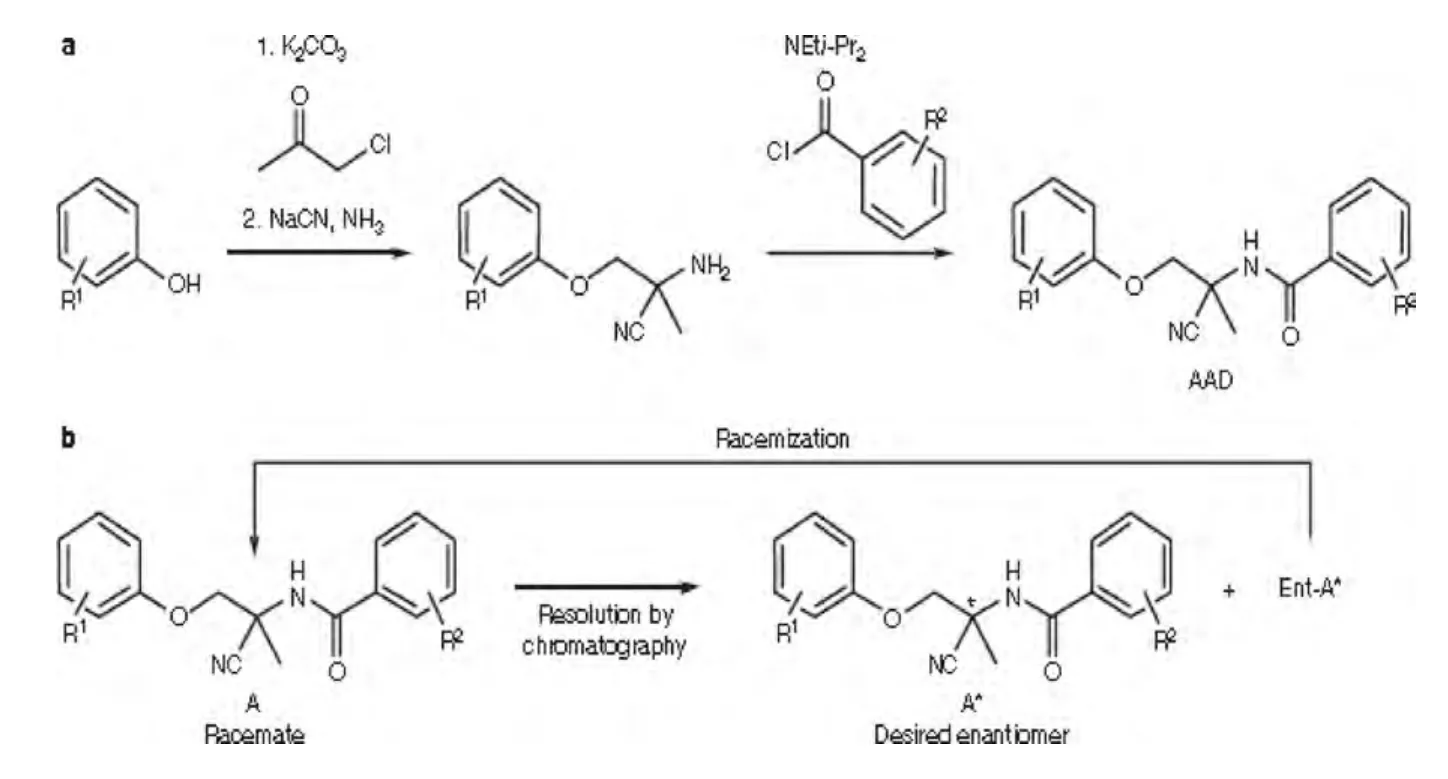
图2 氨基乙腈衍生物类合成路线图(Nature,2008)
2 药代动力学研究
2.1 在羊体内的药动学 莫奈太尔在绵羊体内代谢快,生物利用度低。Karadzovska等[2]对杂交绵羊单剂量经口给予莫奈太尔 1、3、10 mg/kg体重,或静脉注射给予1 mg/kg体重的莫奈太尔或莫奈太尔砜(MNPSO2),收集静脉给药组和经口给药3 mg/kg组的粪便,测定血液和粪便中的莫奈太尔及其砜型代谢产物,观察莫奈太尔及其砜型代谢产物的峰浓度(Cmax)和达峰时间(Tmax),计算 AUC(药-时曲线下面积)、MRT(平均滞留时间)和 t1/2(消除半衰期)等药动学参数。结果表明,静脉给药后,莫奈太尔浓度在 48 h后低于定量限(LOQ,3 ng/mL),总体血浆清除率(Cl)相对较高(1.5 L·kg-1·h-1),稳态时分布容积(Vss) 为7.4 L/kg。约4%的药物在粪便中以莫奈太尔原型形式排泄,大约94%为砜型代谢产物,其中27%的砜型代谢物在粪便中排泄,其余进一步代谢。莫奈太尔砜经静脉给药后,稳态时的分布容积(31.2 L/kg)高于莫奈太尔,但是总体血浆清除率大约为莫奈太尔 1/5(0.3 L·kg-1·h-1),半衰期为105 h。经口给药后,莫奈太尔浓度在96 h下降至3 ng/mL(LOQ)。砜型代谢产物浓度在1 h内升至高于LOQ。从大约4 h开始,砜型代谢产物超过原型药物。尽管莫奈太尔的绝对生物利用度只有31%,但是莫奈太尔口服或静注后形成砜的量大致相同(口服与静注的AUC0-∞比值为94%)。这种差异可能是由于首过效应引起,这也表明莫奈太尔口服效果好。
Lifschitz等[3]报道,以 2.5 mg/kg 的推荐剂量对22只健康的罗姆尼羊(Romney Marsh lamb)灌服莫奈太尔(Zolvix®),给药后48 h,血浆中MNP的含量较低,砜型代谢物的含量要显著高于MNP,且在血浆中维持的时间较长(长达9 d)。在肝脏和胆汁中,MNP代谢较高,砜型代谢物MNPSO2的含量明显高于原型药物。在第一个48 h内,MNP在皱胃内容物的含量在2000~4000 ng/g,砜型代谢物也可以检测到,但是含量明显比原型药物低。在肠道的不同部位,MNP的含量差异较大,从 56 ng/g到4200 ng/g,但是MNPSO2的含量明显高于皱胃中的含量(199~677 ng/g)。 整体而言,MNP 和 MNPSO2在黏膜组织中的含量要比组织内容物的含量低。不同的黏膜部位,MNP和MNPSO2在皱胃和十二指肠黏膜中的浓度要比回肠和盲肠中的含量高。莫奈太尔及其代谢物在不同组织中的蓄积浓度与它高效的抗虫效果有关。
欧洲药物审评局(European Medicine Agency,EMA)报告[4]显示,在大鼠和绵羊体内用14C标记的莫奈太尔研究MNP的吸收、分布、代谢和排泄。经口给药后,莫奈太尔快速吸收并快速氧化为砜,莫奈太尔在1 d内达到血药峰浓度,接着缓慢氧化和裂解为可以通过粪便和尿液排泄的代谢物,进入血液后半衰期约为5 d,绵羊中观察到的所有代谢产物也可在大鼠中观察到。该药主要通过粪便排泄,但尿液中也有排泄。
Lucie Stuchlíková 等[5-6]研究了莫奈太尔在绵羊的体内、体外代谢特点。他们将MNP与绵羊肝细胞共同孵育后,在肝细胞中鉴定了5个Ⅰ相代谢物和4个Ⅱ相代谢物。MNP在肝细胞中的生物转化有氧化、羟基化、硫酸化、糖基化,此外还伴随有水解和乙酰化并与谷胱甘肽结合等反应。体内代谢产物与体外代谢有明显不同,Lucie Stuchlíková等在绵羊粪便和尿液中共发现13种代谢物,其中有7种代谢产物与体外代谢研究中完全不同,在肝细胞中代谢的产物也并不能在粪便和尿液中完全检测到。此外,他们通过比较MNP在敏感与耐药的线虫的生物转化发现,在线虫体内的酶系统主要通过氧化和水解反应使MNP发生生物学转化,且MNP在耐药的线虫体内,形成的代谢物种类较多。
2.2 其他因素对药动学影响 Barry C Hosking等[7]报道了品种、年龄和性别对莫奈太尔在绵羊体内药动学的影响,发现雄性动物中莫奈太尔砜的AUC(0~504 h)比雌性动物的大,具有明显的统计学差别。品种对一些重要的药动学参数影响较大。对于研究中用到的美利奴(Merino)羊比多塞特(Dorset)羊,不管是莫奈太尔原型还是其砜型代谢物,尽管AUC无统计学差异,但是美利奴羊比多塞特羊的 Cmax高,且美利奴羊的达峰时间也要短。Hosking等[8]研究了不同给药方式对莫奈太尔药动学的影响,发现对于莫奈太尔及其代谢物,口服给药比直接瘤胃给药、皱胃给药的Cmax和AUC大,这些药动学特点与临床上推荐的口服给药治疗效果密切相关。
3 药效学研究
3.1 作用机制 莫奈太尔属氨基乙腈衍生物类驱虫药,特定地作用于线虫特有的烟碱乙酰胆碱受体亚科ACR-23蛋白,具有快速、高效和渗透性神经肌肉效应,通过引起体壁肌肉过度收缩导致咽前部麻痹、痉挛性收缩并最终死亡,可以有效杀灭耐受其他类别药物的线虫。由于哺乳动物中没有该受体,因此莫奈太尔对除线虫之外的其他有机体均表现为低毒性。
3.2 药物剂量研究
3.2.1 剂量确定 Hosking 等[9]分别用 1.25、2.5 和5.0 mg/kg体重的莫奈太尔治疗人工感染线虫的绵羊,通过计算虫卵数来观察不同剂量的治疗效果。试验发现,2.5和5.0 mg/kg的莫奈太尔可以高效地杀灭第四期肠道线虫,而低剂量只有中度的杀虫效果,最终认为2.5 mg/kg对控制绵羊的肠道线虫是一个比较合适的剂量。Ronald Kaminsky等[10]也通过比较1.25、2.5和5.0 mg/kg的剂量对绵羊肠道主要的线虫的杀虫率,认为2.5 mg/kg的剂量对控制绵羊胃肠道线虫的有效率可达93%以上。
3.2.2 剂量确认 Hosking等[11]通过9个试验,对莫奈太尔进行剂量确认研究。他们对绵羊感染13种胃肠道线虫幼虫,以2.5 mg/kg体重的莫奈太尔给以治疗发现,该剂量的莫奈太尔除了对匙形细颈线虫(Nematodirus spathiger)和微管食道口线虫(Oesophagostomum venulosum)的杀虫率变化较大,对其它种属的线虫均有较好的杀虫效果,满足相关要求,且动物耐药良好,未观察到副作用。
Heinz Sager等[12]对自然感染或人工感染处于成虫期的肠道线虫的绵羊按2.5 mg/kg体重口服给予莫奈太尔,评价莫奈太尔的治疗效果。研究发现,不管对于自然感染还是人工感染线虫,除了对个别线虫如微管食道口线虫和羊鞭虫的杀虫率较低,莫奈太尔对大部分的肠道线虫的杀虫率均可达92%以上。
3.2.3 田间试验 2007年,Jones等[13]在苏格兰、英格兰和法国开展的多中心、单盲、随机对照田间试验证明了莫奈太尔的有效性。他们选用杂交品种的6周~10岁、12~52 kg各种绵羊2300只绵羊(901只用于驱虫药活性和安全性研究,其余1399只仅用于安全性评价)。第0天,对每个中心的100只绵羊采集粪样,随机选择75只绵羊通过传统投药枪按2.5 mg/kg莫奈太尔给予ZOLVIX,剩余25只绵羊作为空白不给药对照。第7天,采集粪样,用于虫卵计数和粪培养(用于幼虫分化),区分为细颈线虫和非细颈圆线虫虫卵。所有组的莫奈太尔驱虫药活性均高于98%,且虫卵计数减少具有显著性差异。给药组的绵羊未见不良反应。
3.3 其他临床研究 莫奈太尔对线虫有较好的杀虫效果,对已产生耐药的线虫亦有效。Stein等[14]研究了莫奈太尔对捻转血矛线虫以及背带线虫第四期幼虫的抑制效果。结果表明,当绵羊以2.5 mg/kg的剂量口服给药,莫奈太尔对捻转血矛线虫的有效率为99.7%,对背带线虫的有效率可达99.8%。Ramage等[15]报道了莫奈太尔对自然感染的第四期背带线虫的效果,对静止期和繁殖期的线虫,杀虫率分别为99.7%和99.3%。Ronald Kaminsky等[16]用多重耐药的虫株(耐苯并咪唑类药物、左旋咪唑以及大环内酯类药物)感染绵羊后,按照推荐剂量和给药方式给药[莫奈太尔2.5 mg/kg体重;得曲太尔(derquantel)2.0 mg/kg体重和阿维菌素0.2 mg/kg体重合用],比较了莫奈太尔、得曲太尔和阿维菌素联合用药对多重耐药虫体的杀虫效果。结果表明,莫奈太尔对多重耐药虫体有较好的杀虫效果,尤其对蛇形毛圆线虫(Trichostrongylus colubriformis)和捻转血矛线虫,其杀虫效果可达99.9%;得曲太尔和阿维菌素联合用药对蛇形毛圆线虫的杀虫效果与莫奈太尔一致,但是对捻转血矛线虫幼虫的效果明显不如莫奈太尔,仅有18.3%。
4 靶动物的安全性研究
4.1 耐受性研究 Malikides等[17]研究了莫奈太尔对靶动物的耐受性。他们将56只断奶的美利奴(Merino)羔羊(12~15周,28只母羊,28只去势羊)随机分为4组,分别口服给予1倍推荐最大剂量(3.75 mg/kg)、3 倍 (11.25 mg/kg) 或 5 倍(18.75 mg/kg)的莫奈太尔,对照组给予生理盐水。共给药3周,8次。给药当天每2 h观察一次羔羊,持续10 h,非给药天检查两次。给药前后通过颈静脉采集血样,进行血液学、临床化学和凝血参数测定。同时对每只羔羊尸检,收集器官/组织样品,用于组织病理学检查。研究发现,在试验期间,所有羔羊均未死亡,生长和行为正常。各组的饲料和水消耗没有差异,未见明显的病理学或组织病理学变化。该研究表明,口服给予莫奈太尔耐受性良好,对动物无特异性影响。
4.2 生殖毒性研究 Malikides等[18]也观察了莫奈太尔对山羊的生殖毒性。28只健康的美利奴(Merino)公羊随机分成两组,其中一组口服给予3倍推荐最大剂量(11.25 mg/kg)的莫奈太尔,每隔5 d给药一次,共给药63 d,另外一组给予生理盐水作为对照。试验发现,给药组的山羊与对照组表现无差异,均生长正常。给药组山羊的体温、粪便颜色、血液内红细胞、白细胞也无明显变化。除了天冬氨酸转氨酶、碱性磷酸酶的活性及肌酸酐的浓度有差异外,其它的生化指标也与对照组无明显差异。此外,对照组山羊的生殖能力也不受药物影响。这说明动物能耐受高剂量的莫奈太尔,即使连续口服高剂量的药物,对动物的生殖能力等也无影响。
5 残留
目前,EMA规定的每日允许摄入量(ADI)为0.03 mg/kg 体重或每人(60 kg)1800 μg/d。 根据莫奈太尔在绵羊体内的代谢研究,莫奈太尔快速代谢为砜,被进一步缓慢代谢,因此,EMA规定莫奈太尔砜是残留标示物。欧盟、瑞士、澳大利亚、新西兰、南非、乌拉圭、阿根廷、巴西和日本建立了最高残留限量(MRLs)标准(表1)。

表1 莫奈太尔在羊各组织中的残留标示物及最高残留限量
粮农组织/世界卫生组织联合食品添加剂专家委员会(JECFA)根据在小鼠观察到的最大无作用剂量为 1.8 mg/(kg 体重·d),推荐 ADI为0.02 mg/kg体重,在绵羊体内的残留标示物为莫奈太尔砜,推荐的 MRLs 标准分别为:肌肉 300 μg/kg,脂肪 5500 μg/kg,肝脏 3000 μg/kg,肾脏 700 μg/kg,已到食品法典委员会(CAC)制定残留限量标准程序的第七步,待CAC大会审议。
6 结语
莫奈太尔作为新型抗虫药,其良好的抗虫效果,已在兽医临床上得到了肯定,尤其是对已产生耐药性的线虫具有较好的效果。由于该药不易产生耐药性且毒性低,莫奈太尔在今后动物体内寄生虫疾病的防治中发挥重要作用。相信随着研究的深入,该药在兽医临床的应用具有更加广阔的前景。
[1]Kaminsky R,Ducray P,Jung M,et al.A new class of anthelmintics effective against drug-resistant nematodes[J].Nature, 2008,452(7184): 176-180.
[2]Karadzovska D,Seewald W,Browning A,et al.Pharmacokinetics of monepantel and its sulfone metabolite, monepantel sulfone,after intravenous and oral administration in sheep[J].Journal of Veterinary Pharmacology and Therapeutics, 2009, 32 (4):359-367.
[3]Lifschitz A,Ballent M,Virkel G,et al.Accumulation of monepantel and its sulphone derivative in tissues of nematode location in sheep:Pharmacokinetic support to its excellent nematodicidal activity[J].Veterinary Parasitology, 2014, 203(1/2): 120-126.
[4]EMA.Committee for Medicinal Products for Veterinary Use(EMA/CVMP /741250/2011 ) [ DB/OL ].http://www.ema.europa.eu/docs/en_GB/document_library/Maximum_Residue_Limits_-_Report/3013 /05 /WC500143639.pdf.
[5]Stuchlíková L, Jirásko R, Vokrˇál Ⅰ, et al.Investigation of the metabolism ofmonepantelin ovine hepatocytes by UHPLC/MS/MS [ J].Analytical and Bioanalytical Chemistry,2013, 405(5): 1705-1712.
[6]Stuchlíková L, Jirásko R, Vokrˇál Ⅰ, et al.Metabolic pathways of anthelmintic drug monepantel in sheep and in its parasite(Haemonchus contortus)[J].Drug Testing and Analysis, 2014,
[7]Hosking B C, Kaminsky R, Sager H, et al.The effect of sheep breed, age, and gender on the pharmacokinetics and efficacy of monepantel, an amino-acetonitrile derivative[J].Parasitology Research, 2010, 106(2): 367-375.
[8]Hosking B C,Stein P A,Karadzovska D,et al.Effect of route of administration on the efficacy and pharmacokineticsofan experimental formulation of the amino-acetonitrile derivative monepantel in sheep[J].Veterinary Record, 2010, 166(16):490-494.
[9]Hosking B C,Stein P A,Mosimann D,et al.Dose determination studies for monepantel, an amino-acetonitrile derivative, against fourth stage gastro-intestinal nematode larvae infecting sheep[J].Veterinary Parasitology, 2008, 157(1): 72-80.
[10]Kaminsky R,Mosimann D,Sager H,et al.Determination of the effective dose rate for monepantel(AAD 1566) against adult gastro-intestinal nematodes in sheep[J].International Journal for Parasitology, 2009, 39(4): 443-446.
[11]Hosking B C,Dobson D P,Stein P A,et al.Dose confirmation studies for monepantel, an amino-acetonitrile derivative, against fourth stage gastro-intestinal nematode larvae infecting sheep[J].Veterinary Parasitology, 2009, 160(3): 251-257.
[12]Sager H, Hosking B, Bapst B, et al.Efficacy of the aminoacetonitrile derivative, monepantel, against experimental and natural adult stage gastro-intestinal nematode infections in sheep[J].Veterinary Parasitology, 2009, 159(1): 49-54.
[13]Jones M D,Hunter R P,Dobson D P,et al.European field study of the efficacy and safety of the novel anthelmintic monepantel in sheep[J].Veterinary Record, 2010, 167(16): 610-613.
[14]Stein P A, Rolfe P F, Hosking B C.The control of inhibited fourth-stage larvae of Haemonchus contortus and Teladorsagia spp.in sheep in Australia with monepantel[J].Veterinary Parasitology, 2010, 169(3): 358-361.
[15]Ramage C,Bartley D J,Jackson F,et al.The efficacy of monepantel against naturally acquired inhibited and developing fourth-stage larvae of Teladorsagia circumcincta in sheep in the United Kingdom[J].Veterinary Parasitology, 2012, 186(3): 528-531.
[16]Kaminsky R,Bapst B,Stein P A,et al.Differences in efficacy of monepantel,derquantel and abamectin against multi-resistant nematodes of sheep[J].Parasitology Research, 2011, 109(1):19-23.
[17]Malikides N,Helbig R,Roth D R,et al.Safety of an aminoacetonitrile derivative (AAD), monepantel, in weaned lambs following repeated oral administration[J].New Zealand Veterinary Journal, 2009, 57(1): 10-15.
[18]Malikides N,Helbig R,Mahoney R,et al.Reproductive safety of an amino-acetonitrile derivative (AAD), monepantel, in rams following repeated oraladministration [J].New Zealand Veterinary Journal, 2009, 57(1): 16-21.

