依达拉奉对中、重型颅脑损伤患者脑水肿及预后的影响
李 凯,周 杰,车万民,宋丽梅,赵全华,董 涛
(中国中医科学院望京医院神经外科,北京,100102)
随着现代社会工业、交通业、建筑业的飞速发展,意外事故导致创伤的事故发生率逐渐增多,其中创伤性颅脑损伤(TBI)是常见的、且死亡率和致残率最高的意外损伤之一。有关TBI的机制研究中提示脑水肿是造成患者死亡和残疾的主要原因,脑水肿可引起细胞肿胀、改变细胞代谢内环境等使颅内压明显升高,同时组织血流灌注减少,甚至形成脑疝压迫脑干呼吸、循环中枢而危及生命[1-2]。依达拉奉可通过清除氧自由基、减少水通道蛋白表达等作用减轻脑水肿。本研究观察了依达拉奉治疗中、重度TBI脑水肿的临床疗效,现报告如下。
1 资料与方法
1.1 一般资料
选取2011年2月—2014年2月在中国中医科学院望京医院住院治疗的124例中、重型TBI脑水肿患者,所有患者均经头颅CT等检查确诊为脑水肿,发病后12 h内就诊,且格拉斯哥昏迷量表(GCS)<8分;排除伴有其他严重脏器损伤、伴有影响GCS评分的神经系统疾病者。124例患者随机分成治疗组63例,对照组61例。治疗组中男39例,女24例;年龄19 ~68 岁,平均(45.23 ±4.67)岁。对照组中男37例,女24例;年龄21~65岁,平均(44.23±5.17)岁。2组性别、年龄等一般资料无显著差异(P>0.05),具有可比性。
1.2 方法
对照组给予抗感染、止血、脱水、营养支持等常规治疗;治疗组在此基础上给予依达拉奉注射液30 mg(江苏先声药业有限公司,国药准字H20031341)加入0.9%氯化钠溶液100 mL中静脉滴注,2次/d。2组均治疗14 d,并随访6个月。
1.3 观察指标
观察治疗前及治疗后第3、7、14、28天的脑水肿面积、治疗第28天的GCS评分及随访6个月后的Glasgow预后评分(GOS)。脑水肿面积依据头颅CT所示脑水肿最大层面的长×宽进行测算。
2 结果
2.1 2组治疗前后脑水肿面积比较
2组治疗前脑水肿面积无显著差异(P>0.05);治疗后第3、7天面积均较治疗前显著扩大(P<0.01),至第7天达高峰,组间比较无显著差异(P>0.05);治疗后第14、28天2组脑水肿面积较前均显著减小(P<0.01),治疗组显著小于对照组(P <0.01)。见表1、图1。
表1 2组治疗前后脑水肿面积变化比较() cm2

表1 2组治疗前后脑水肿面积变化比较() cm2
与治疗前比较,**P <0.01;与对照组比较,##P <0.01。
组别 例数 治疗前 第3天 第7天 第14天 第28天治疗组 63 19.81 ±0.52 26.04 ±0.42** 34.41 ±0.54** 12.45 ±0.48**## 4.36 ±0.33**##对照组 61 19.75±0.44 26.11±0.46** 34.56 ±0.34** 18.75±0.46** 11.37±0.67**
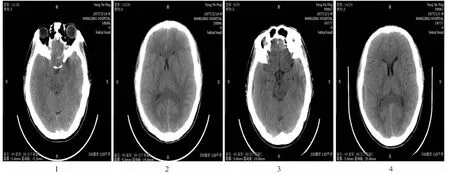
图1 高空摔伤患者头颅CT变化
2.2 2组治疗前后GCS评分比较
治疗组与对照组治疗前GCS评分分别为(7.23±0.65)、(7.36 ±0.60),2 组比较无显著差异(P>0.05);治疗第28天,2组评分分别为(13.45 ± 1.42)、(10.75 ± 1.38),均较治疗前显著升高(P<0.01);治疗组显著高于对照组(P <0.01)。
2.3 随访情况
随访6个月后,分别对2组进行GOS评分测定,治疗组良好27例(42.86%)、中度残疾18例(28.57%)、重度残疾7 例(11.11%)、植物生存 6例(9.52%)、死亡 5 例(7.94%);对照组良好 15例(24.59%)、中度残疾 19 例(31.15%)、重度残疾7 例(11.48%)、植物生存 13 例(21.31%)、死亡7例(11.48%)。治疗组评分良好率显著高于对照组(P <0.05)。
3 讨论
TBI患者多伴随不同程度的脑水肿,其主要危害是机械性压迫脑组织,导致颅内压增高,甚至引发脑疝,最终导致患者残疾或死亡。传统分子学机制认为,TBI患者发生脑水肿的机制主要包括:钙超载是脑神经元水肿死亡的最后共同途径;细胞膜钠-钾-ATP酶活性减退;活性氧或氧自由基损害;兴奋性氨基酸的神经毒作用;细胞内乳酸酸中毒致细胞内水肿[3]。近年来,有研究[3-5]表明水通道蛋白(AQPs)是影响水肿进展的关键因素,其中水通道蛋白-4(AQP-4)是脑内表达最多的亚型,抑制其表达可减少脑水肿面积、改善脑内神经功能。严重TBI发生后数小时内脑血流量急剧下降,引起广泛性脑血管扩张及脑血流过度灌注,导致其自动调节机制丧失,加重脑组织缺血、水肿。中、重度TBI患者病情危重,常出现呼吸道分泌物增加,引发气道梗阻,肺通气量减少,导致脑组织缺氧,此时脑组织无氧代谢增加会产生大量的酸性代谢产物,增加血脑屏障通透性,从而加重脑组织水肿。此外,重度TBI患者体内会产生大量的氧自由基,引发严重细胞及血管损伤,因此,清除氧自由基无疑有助于减轻患者脑水肿的病情,故本研究采用依达拉奉治疗TBI患者的脑水肿。依达拉奉作为一种广谱的自由基清除剂,药理研究表明其减轻脑水肿的可能机制为:①依达拉奉能够抑制黄嘌呤氧化酶和次黄嘌呤氧化酶的活性,刺激前列环素的生成,减少炎症介质白三烯,减轻脑水肿及继发性缺血损伤,从而抑制迟发性神经元死亡,保护作用明显[6-7];② 依达拉奉可直接清除羟基,有效抑制脂质自由基的生成,并有效抑制自由基介导的蛋白质核酸不可逆的破坏作用等机制发挥减轻脑水肿的功能;③依达拉奉可抑制AQP-4的表达,从而有减轻脑水肿的作用[8]。贺震民等[9]研究表明,依达拉奉能有效清除TBI后体内的大量自由基,减轻脑水肿严重程度,改善患者预后。周路球等[10]研究发现,轻度低温联合依达拉奉早期应用于重型TBI患者,可显著降低颅内压,疗效优于常规治疗或单纯轻度低温治疗者。
本研究结果表明,2组在治疗初期,即第3、7天脑水肿面积均较治疗前显著扩大(P<0.01),提示在TBI初期脑水肿达到高峰;第14天起见到显著疗效,第14、28天2组脑水肿面积显著减小(P<0.01),治疗组显著小于对照组(P<0.01),提示加用依达拉奉的患者脑水肿减退效果更显著。治疗第28天,2组GCS评分均较治疗前显著升高(P<0.01);治疗组显著高于对照组(P<0.01);随访6个月后,治疗组GOS评分良好率显著高于对照组(P<0.05),表明依达拉奉可促进患者神经功能恢复,显著改善预后,提高生存质量,降低病死率及致残率,与上述报道一致。
[1]Kammersgaard L P,Linnemann M,Tibk M.Hydrocephalus following severe traumatic brain injury in adults.Incidence,timing,and clinical predictors during rehabilitation[J].NeuroRehabilitation,2013,33(3):473.
[2]Honeybul S,Ho K M.Long-term complications of decompressive craniectomy for head injury[J].Journal of neurotrauma,2011,28(6):929.
[3]Fazzina G,Amorini A M,Marmarou C R,et al.The protein kinase C activator phorbol myristate acetate decreases brain edema by aquaporin 4 downregulation after middle cerebral artery occlusion in the rat[J].Journal of neurotrauma,2010,27(2):453.
[4]Skjolding A D,Holst A V,Broholm H,et al.Differences in distribution and regulation of astrocytic aquaporin 4 in human and rat hydrocephalic brain[J].Neuropathology and applied neurobiology,2013,39(2):179.
[5]Filippidis A S,Kalani M Y S,Rekate H L.Hydrocephalus and aquaporins:lessons learned from the bench[J].Child's Nervous System,2011,27(1):27.
[6]Wang G,Su J,Li L,et al.Edaravone alleviates hypoxia-acidosis/reoxygenation-induced neuronal injury by activating ERK1/2[J].Neuroscience letters,2013,543:72.
[7]Zhou F,Chen G,Zhang J.Edaravone reduces brain oedema and attenuates cell death after intracerebral haemorrhage in mice[J].Brain Injury,2009,23(4):353.
[8]何远东,卞立松,许亮,等.依达拉奉预处理对大鼠脑损伤后细胞毒性脑水肿的影响[J].脑与神经疾病杂志,2013,21(4):305.
[9]贺震民,蔡青.依达拉奉治疗重型颅脑损伤的临床观察[J].海南医学,2009,20(6):68.
[10]周路球,马真,纠智松,等.轻度低温联合依达拉奉治疗提高重型颅脑损伤疗效[J].中华神经医学杂志,2013,12(8):815.

