螃蟹甲内生真菌Chaetosphaeronema sp.的化学成分研究
温欣,张大为,郭顺星,王春兰
螃蟹甲内生真菌sp.的化学成分研究
温欣,张大为,郭顺星,王春兰
100193 北京,中国医学科学院北京协和医学院药用植物研究所分析中心
研究一株来源于藏药螃蟹甲内生真菌 PHY-24 的化学成分。
采用麦麸培养基,对内生真菌 PHY-24 进行放大培养,通过硅胶柱色谱、MCI 柱色谱、ODS 柱色谱、Sephadex LH-20 柱色谱、高效液相色谱等对其发酵液中的化学成分进行分离纯化,利用 NMR、MS 等波谱方法进行化学成分的结构鉴定,并测定这些成分抗 HIV-1 整合酶链转移反应活性。
从内生真菌 PHY-24 发酵液的乙酸乙酯提取部分分离并鉴定了 4 个化合物,分别是:integrastatin B(1)、2-乙酰基-3,5-二羟基-苯乙酸(2)、curvulin(3)、O-methylcurvulinic acid(4)。其中化合物(1)和(2)具有抗 HIV-1 整合酶链转移反应活性,其 IC50分别为 6.22 和 75.1 μmol/L。
4 个化合物均为从此属真菌中首次分得,其中化合物(1)、(2)具有抗 HIV-1 整合酶链转移反应活性。化合物(2)的活性为首次报道。
内生真菌; 化学成分; 螃蟹甲
内生真菌是指那些在其生活史中某一段时期生活在植物组织内,对植物组织没有引起明显病害症状的真菌,包括在其生活史中的某一阶段营表生的腐生真菌和对宿主暂时没有伤害的潜伏性病原真菌和菌根菌[1]。尽管内生真菌广泛存在于自然界中,但很长时间内没有被重视。直到 1993 年,美国科学家 Stierle 等[2]从红豆杉的内生真菌中分离得到了具有抗癌活性的紫杉醇,内生真菌代谢产物的重要性才逐渐被发掘。因存在于宿主植物内,内生真菌可以产生与宿主植物相同或相近的代谢产物,有时也能产生新的天然产物,成为天然产物的又一大资源库[2-3],而且内生真菌具有易培养、培养条件可控、产量较高的特点。国内外已有大量文献报道了从植物内生真菌中分离得到多种活性化合物[4]。本科室从螃蟹甲中分离并鉴定了内生真菌 PHY-24(sp.),并测定其发酵产物具有良好的抗 HIV-1 整合酶链转移反应活性[5]。基于上述背景,本研究对其发酵产物化学成分进行研究。
1 材料与方法
1.1 材料
1.1.1 菌株 螃蟹甲内生真菌sp. 菌株由中国医学科学院药用植物研究所生物中心分离保藏,由本科室张大为鉴定。
1.1.2 仪器 Varian unity 600 型核磁共振仪为美国 Varian 公司产品;AGZAB 2F 型质谱仪为英国 VG 公司产品;Waters 600 高效液相色谱仪、XBridge C18 分析型色谱柱(4.6 mm × 150 mm,5 μm)、XBridge C18 制备色谱柱(18 mm × 150 mm,4 μm)为美国 Waters 公司产品;Phenomenex Synergi Hydro-RP C18 分析型色谱柱(4.6 mm × 250 mm,5 μm)、Phenemonex Hydro 制备色谱柱(21.20 mm × 250 mm,4 μm)为美国 Phenomenex公司产品;Pump Manager C-615 中压色谱柱为瑞士 Buchi 公司产品。
1.1.3 试剂 分析纯石油醚、乙酸乙酯、二氯甲烷、甲醇、丙酮购自北京化工厂;色谱纯甲醇购自美国Burdick & Jackson 公司;薄层色谱硅胶板 GF254、柱色谱硅胶 H、300 ~ 400 目硅胶、200 ~ 300 目硅胶均购自青岛海洋化工厂;Sephadex LH-20 购自美国Pharmacia 公司;核磁试剂(CDCl3、CD3OD、氘代试剂作为内标)购自美国Sigma 公司。
1.2 方法
1.2.1 放大发酵 按照每升麦麸培养基含 30 g 麦麸、20 g葡萄糖、1.5 g MgSO4·7H2O、3 g KH2PO4的配方制备培养基。从平板 PDA 培养基上挑取 PHY-24 菌块接种到装有 150 ml 麦麸培养基的 250 ml 三角瓶中,采用摇床振荡培养 2 ~ 3 d,摇床转速控制在 120 r/min,培养温度设定为 25 ℃。将培养好的 PHY-24 菌种液每瓶转接至装有 2.5 L 麦麸培养基的 5 L 三角瓶中,采用摇床振荡培养 17 ~ 18 d,摇床转速控制在 120 r/min,培养温度设定为 25 ℃。每一批次的 PHY-24 放大发酵物为 10 L,共得发酵物 30 L。
1.2.2 提取分离 用尼龙布分离 PHY-24 发酵液和菌丝体。发酵液加入 1 倍体积乙酸乙酯,萃取浓缩得乙酸乙酯提取物 20 g。取10 g提取物采用硅胶柱色谱纯化,以石油醚:乙酸乙酯(5:1),二氯甲烷:甲醇(10:1),甲醇进行梯度洗脱,共得14 流分。Fr8(0.8 g)经 Sephadex LH-20(甲醇)及制备HPLC(90% 甲醇-水,流速 8 ml/min)得化合物 1(31 mg)。另取 10 g 提取物采用 MCI 柱色谱纯化,以甲醇-水不同比例梯度洗脱,共得 9 流分。Fr3(0.21 g)析出晶体,经重结晶得化合物 2(27 mg)。Fr4(0.35 g)经 HPLC 制备(55% 甲醇-水,流速 10 ml/min)得化合物 3(22 mg)和化合物 4(34 mg)。
1.2.3 抗 HIV-1 整合酶链转移反应活性测定 参照 He 等[6]建立的 HIV-1 整合酶链转移反应活性检测方法。反应在 96 孔透明微孔板中进行。用1 × 反应缓冲液(25 mmol/L 哌嗪-1,4-二乙磺酸、10 mmol/L β-巯基乙醇、0.1 g/L BSA、5% 无菌甘油、20 mmol/L MnCl2)100 μl 洗板一次。加入 5 μl 用 DMSO 配制的待测样品(阳性对照组为 50 mmol/L 的黄芩素,阴性对照组为溶剂 DMSO)至微孔板中,与整合酶在 2 × 反应缓冲液中 37 ℃温育 20 min。加入 1.5 pmol/L 供体 DNA 和 15 pmol/L 靶 DNA 底物,混匀后 37 ℃反应 2 h。加入 1.5 μl 链霉亲和素磁珠和 51.5 μl 结合缓冲液[10 mmol/L Tris-HCl,pH 7.6,2 mol/L NaCl,20 mmol/L EDTA,0.1%(w/v)吐温 20]彻底振荡混匀,20 ℃孵育15 min,每隔 5 分钟振荡混匀一次。将微孔板置于板式磁珠收集器静置 90 s,弃上清液。用 100 μl TBST(含 0.1% Tween 20 的Tris-HCl 缓冲盐溶液)洗磁珠 3 次。加入100 μl 用 TBST 按照 1:5000 稀释的碱性磷酸酶标记的地高辛抗体,振荡混匀后于 37 ℃孵育 30 min。100 μl TBST 洗磁珠 3 次,将磁珠转移到新的微孔板中。加入 100 μl 显色底物缓冲液(6.7 mmol/L 对硝基苯磷酸二钠、0.1 mol/L Na2CO3、2 mmol/L MgCl2,pH 9.5),避光显色30 min。用酶标仪测定 405 nm 处的吸光值(405)。用以下公式计算药物对肿瘤细胞的抑制率,并通过非线性拟合计算 IC50。

抑制率 =A阴性对照-A样品× 100% A阴性对照-A阳性对照
2 结果
2.1 结构鉴定
化合物 1:棕色粉末(TCM),ESI-MS m/z:403 [M+H]+。1H-NMR(CDCl3,600MHz)δ:1.94(3H,s,H-19),2.20(3H,s,H-18),3.81(3H,s,H-21),3.82(3H,s,H-22),7.11(1H,s,H-7),7.21(1H,s,H-13),10.29(1H,s,H-20)。13C-NMR (CDCl3,600 MHz)δ:25.58(C-19),26.07(C-18),56.26(C-21),56.48(C-22),77.40(C-10),97.04(C-2),101.57(C-7),105.41(C-13),120.00(C-8),120.01(C-3),120.99(C-11),125.62(C-12),139.31(C-4),139.34(C-16),139.87(C-15),140.59(C-5),146.97(C-14),147.51(C-6),190.41(C-20),193.18(C-9)。与文献[7]数据基本一致,故鉴定为integrastatin B(图 1A)。
化合物 2:白色粉末(MeOH),ESI-MS m/z:211 [M+H]+。1H-NMR(MeOH,600MHz)δ:6.27(1H,d,J = 2.4,H-8),6.21(1H,d,J = 2.4,H-6),3.65(2H,s,H-2),2.52(3H,s,H-2')。13C-NMR(MeOH,600MHz)δ:206.15(C-1'),175.27(C-1),161.91(C-7),161.03(C-5),137.94(C-3),120.58(C-4),l12.03(C-8),102.71(C-6),40.79(C-2),32.38(C-2')。与文献[8-9]数据基本一致,故鉴定为curvulin acid,即 2-乙酰基-3,5-二羟基苯乙酸(图 1B)。
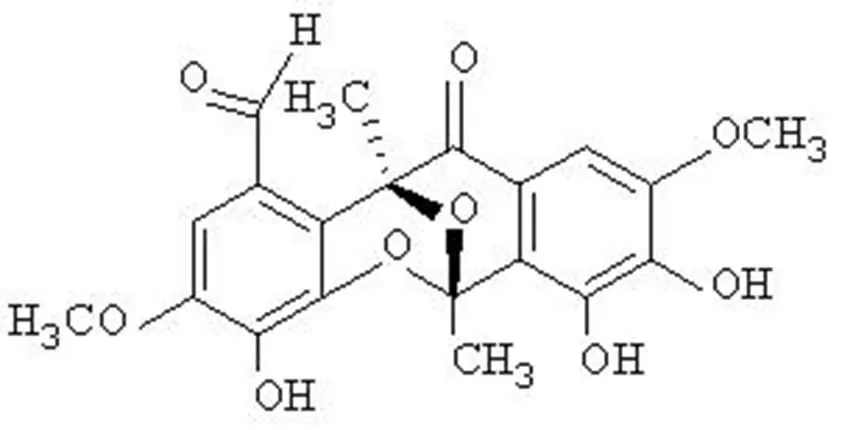
图 1 化合物 1(A)和 2(B)结构式
Figure 1 The molecular structures of compound 1 (A) and 2 (B)
化合物 3:无色片状结晶(MeOH),ESI-MS m/z:239[M+H]+。参考文献[9]鉴定为curvulin。
化合物 4:白色粉末(MeOH 或 DMSO),ESI-MS m/z:225[M+H]+。与文献[9]数据基本一致,故鉴定为 O-methylcurvulinic acid。
2.2 HIV-1 整合酶链转移反应抑制剂筛选
采用高通量 ELISA 方法测定了化合物的抗 HIV-1 整合酶链转移反应活性。结果表明,化合物 1、2 具有抗 HIV-1 整合酶链转移反应活性,IC50分别为 6.22 和 75.1 μmol/L。其余 2 个化合物均无此活性。
3 讨论
从藏药螃蟹甲内生真菌 PHY-24 发酵产物乙酸乙酯提取物中分离得到 4 个化合物,均为sp. 中首次分得。这 4 个化合物文献报道仅从微生物中得到[7-12]。到目前为止,integrastatin B 报道具有抗 HIV-1 整合酶活性,其 IC50为 2.5 μmol/L[7];curvulin acid 未见任何活性报道;curvulin、O-methylcurvulinic acid 仅被报道为植物毒素,可致马齿苋和多刺苋菜黑斑病[10]。
对上述化合物进行抗 HIV-1 整合酶链转移反应活性筛选,结果显示化合物 1 具有明显的抗 HIV-1 整合酶链转移反应活性,其 IC50为6.22 μmol/L,与文献[7]报道基本一致;化合物 2 的抗 HIV-1 整合酶链转移反应活性较微弱,其 IC50为 75.1 μmol/L,为本文首次报道。
目前,针对 PHY-24菌株活性代谢产物的研究仍在继续,以期发现其他的活性成分。
[1] Stone JK, Bacon CW, White JF Jr. An overview of endophytic microbes: endophytism defined//Bacon CW, White JF Jr. Microbial Endophytes. New York: Marcel Dekker, 2000:3-29.
[2] Stierle A, Strobel G, Stierle D. Taxol and taxane production by Taxomyces andreanae, an endophytic fungus of Pacific yew. Science, 1993, 260(5105):214-216.
[3] Li WK, Hu ZB. Endophytes and naural medicine. Chin J Nat Med, 2005, 3(4):193-199. (in Chinese)
黎万奎, 胡之璧. 内生菌与天然药物. 中国天然药物, 2005, 3(4): 193-199.
[4] Zhou SL, Chen SL, Tan GH, et al. Advances in studies on endophytic fungal natural products. J Fungal Res, 2008, 6(4):234-239, 244. (in Chinese)
周松林, 陈双林, 谭光宏, 等. 内生真菌天然活性产物的研究进展. 菌物研究, 2008, 6(4):234-239, 244.
[5] Zhang DW, Zhao MM, Chen J, et al. Isolation, idetification and anti-HIV-1 integrase activity of culturable endophytic fungi from Tibetan medicinal plant Phlomis younghusbandii Mukerjee. Acta Pharm Sinica, 2013, 48(5):780-789. (in Chinese)
张大为, 赵明明, 陈娟, 等. 西藏药用植物螃蟹甲可培养内生真菌的分离、鉴定及抗HIV-1整合酶链转移活性研究. 药学学报, 2013, 48(5):780-789.
[6] He HQ, Ma XH, Liu B, et al. A novel high-throughput format assay for HIV-1 integrase strand transfer reaction using magnetic beads. Acta Pharmacol Sin, 2008, 29(3):397-404.
[7] Singh SB, Zink DL, Quamina DS, et al. Integrastatin: structure and HIV-1 integrase inhibitory activities of two novel racemic terracyclic aromatic hererocycles produced by two fungal species. Tetrahedron Lett, 2002, 43:2351-2354.
[8] Li LL, Chen JP, Kong LY. Chemical constituents of monascus anka. Chin Pharm J, 2006, 41(15):1131-1133. (in Chinese)
李丽莉, 陈杰鹏, 孔令义. 安卡红曲的化学成分研究. 中国药学杂志, 2006, 41(15):1131-1133.
[9] Coombe RG, Jacobs JJ, Watson TR. Constituents of some Curvularia species. Aust J Chem, 1968, 21(3):783-788.
[10] Kenfield D, Hallock Y, Clardyb J, et al. Curvulin and O-Methylcurvulinic acid: Phytotoxic metabolites of Drechslera indica which cause necroses on purslane and spiny amaranth. Plant Sci, 1989, 60(1):123-127.
[11] Kamal A, Khan MA, Qureshi AA. Studies in the biochemistry of micro-organisms—II: Constitution of curvulin, curvulinic acid and curvulol, metabolic products of Curvularia siddiqui. Tetrahedron, 1963, 19(1):111-115.
[12] Crawley GC. Isolation of three new isochroman-3-one metabolites from Oidiodendron rhodogenurn Robak. J Chem Soc, Perkin Trans 1, 1981:221-223.
Chemical constituents of an endophytic fungussp. fromMukerjee
WEN Xin, ZHANG Da-wei, GUO Shun-xing, WANG Chun-lan
To study the chemical constituents of an endophytic fungus PHY-24 (sp.) from Tibetan medicinal plantsMukerjee.
PHY-24 culture was scaled-up using wheat bran medium. The chemical constituents from the fermentation broth of the strain PHY-24 were isolated and purified by silica gel, MCI, ODS and Sephadex LH-20 column chromatography, and their chemical structures were identified by analysis of MS and NMR. Bioactivities of the constituents were tested with anti-HIV-1 integrase strand transfer reaction.
Four compounds were separated and identified from the fermentation broth, including integrastatin B, curvulin acid, curvulin, O-methylcurvulinic acid. Integrastatin B and curvulin acid have anti-HIV-1 activity with IC50being 6.22 μmol/L and 75.1 μmol/L, respectively.
The four compounds were firstly obtained from thegenus, with integrastatin B and curvulin acid having anti-HIV-1 integrase strand transfer reaction activity. The activity of curvulin acid was firstly reported.
Endophytic fungus; Chemical constituents;Mukerjee
WANG Chun-lan, Email: wangchunlan2006@163.com
10.3969/cmba.j.issn.1673-713X.2014.06.007
王春兰,Email:wangchunlan2006@163.com
2014-04-17
Author Affiliation: Analysis Center, Institute of Medicinal Plant Development, Chinese Academy of Medical Sciences & Peking Union Medical College, Beijing 100193, China

