鲑鱼降钙素新型注射用温度敏感原位凝胶系统的构建及评价
丁维明,李艳芳,李桂玲
鲑鱼降钙素新型注射用温度敏感原位凝胶系统的构建及评价
丁维明,李艳芳,李桂玲
100050 北京,中国医学科学院北京协和医学院医药生物技术研究所制剂室(丁维明、李桂玲);100191 北京大学第三医院中心实验室(李艳芳)
构建鲑鱼降钙素新型注射用温度敏感原位凝胶系统并对其胶凝特性和降血钙效应进行评价。
以泊洛沙姆 F127 为主要基质材料,复合使用泊洛沙姆 F68,制备鲑鱼降钙素注射用温度敏感原位凝胶给药系统,以胶凝温度、胶凝时间、流变学、质构特性为考察指标,对该凝胶系统性质进行评价;采用大鼠眼眶取血,钙显色法监测体内血清钙离子浓度,对该凝胶系统降血钙效应进行研究。
所制备的鲑鱼降钙素注射用温度敏感原位凝胶的胶凝温度为(35.3 ± 1.3)℃,胶凝时间为(108.3 ± 5.5)s,在 25 ℃条件下为流动的液体,原位凝胶的黏度和黏滞力极低,方便注射给药,当温度增至 37 ℃时能够迅速发生相转变,黏度和黏滞力等质构特性数据显著增加,成为具有一定胶凝强度的半固体;大鼠降血钙效应结果显示,该给药系统具有明显的缓释作用,其 24 h 时血钙浓度明显低于普通注射剂组,相对于普通注射剂的药理活性为 138.6%。
温度敏感原位凝胶用于鲑鱼降钙素的注射给药,是一种很有潜力的递送系统。
降钙素; 泊洛沙姆; 温度敏感原位凝胶
鲑鱼降钙素(salmon calcitonin,sCT)是由32 个氨基酸组成的活性肽,可维持血中钙离子平衡和抑制破骨细胞活性,从而对有效降低血钙和促进骨骼对钙的吸收起着关键作用[1],具有作用稳定、副作用小等特点,在临床上广泛应用于预防和治疗骨质疏松、骨折、变形性骨炎、高血钙等多种疾病[2-3]。然而,sCT 生物半衰期较短,需反复给药,不利于骨质疏松患者的长期治疗,因此,sCT 的缓释制剂受到广泛关注。
温度敏感原位凝胶是指高分子材料以溶液状态给药后,利用材料受热反向胶凝的性质,在用药部位对温度刺激产生响应,发生分散状态或构象的可逆转化,形成半固体状的药物储库[4]。该给药系统有诸多优点,如分剂量准确、给药方便、缓释或控释性、定位靶向性、增加药物稳定性、提高药物生物利用度等。注射用温度敏感原位凝胶近年来研究较多,它是将可注射用的高分子材料及其他适宜辅料制成温度敏感原位凝胶,以液体状态局部注射于人体内部,在注射部位胶凝形成三维网状结构的半固体状药物储库,随材料的不断溶蚀、降解而释放药物,达到长期缓释的目的。其载体材料的选择至关重要[5]。温度敏感型非离子表面活性剂泊洛沙姆 F127 对某些难溶性药物有很好的溶解性,系统载药量充足,体内可降解,生物相容性好,且其非特异性抗黏附特性可阻止蛋白和细菌附着,从而有效防止感染发生,是一种优良的温敏载体材料[6-7]。
为延长 sCT 作用时间、提高疗效、降低给药次数以提高患者顺应性,本文以泊洛沙姆F127 为主要基质材料,复合使用泊洛沙姆 F68,制备了 sCT 注射用温度敏感原位凝胶制剂。对该凝胶系统的胶凝温度与胶凝时间、流变学特性、质构特性以及大鼠局部注射给药后的释放和降血钙效应进行了研究,为蛋白多肽类药物选择可注射缓释给药系统提供了依据。
1 材料与方法
1.1 材料
1.1.1 试剂 鲑鱼降钙素由上海延长生化公司提供;泊洛沙姆 F127 和 F68 由德国 BASF 公司提供;其他试剂均为分析纯。
1.1.2 仪器 RCT basic 加热磁力搅拌器购自德国 Ika 公司;黏度计、TC-502D 恒温水浴、R/S+ 流变仪及 CT3 质构分析仪均购自美国 Brookfield 公司;E200 恒温水浴购自德国 Lauda公司。
1.1.3 实验动物 SD 雄性大鼠 15 只,体重180 ~ 210 g,合格证号:SYXK(京)2011-0039,由北京维通利华实验动物技术有限公司提供。
1.2 方法
1.2.1 sCT 温度敏感原位凝胶的制备 称取处方量的sCT,加入注射用水使溶解并制成 10 μg/ml 的溶液,然后向其中加入处方量的泊洛沙姆 F127 和 F68,磁力搅拌使其分散均匀,然后于 4 ℃条件下冷藏放置 24 h,使充分溶胀,得到无色澄明的溶液,过 0.22 μm 微孔滤膜,即得。
1.2.2 胶凝温度与胶凝时间的考察 采用转子法测定体系的胶凝温度[8]。将样品置加热磁力搅拌器中,自室温开始,控制升温速度 0.5 ℃/min,同时以 1.5 cm × 0.6 cm 磁性转子搅拌,速率 100 r/min,磁性转子完全停止转动时的温度即为胶凝温度;将样品置 37 ℃恒温水浴中,仍采用上述转子和搅拌速度,记录磁性转子完全停止转动所用时间,即为胶凝时间。
1.2.3 流变学特性考察 采用R/S+ 流变仪(恒温水浴控温)考察体系的流变学特性。分别考察25 ℃和 37 ℃恒温条件下剪切力随剪切速率变化的规律,并绘制流变曲线。
1.2.4 质构特性考察 将样品于37 ℃恒温条件下放置约 30 min,待其充分胶凝后,以 CT3 质构分析仪测定其胶凝强度和黏附性能[9]。测定条件为:探头模具 TA5,触发点负载 0.2 g,预测试速度2 mm/s,测试速度 0.5 mm/s,返回速度 0.5 mm/s,穿透距离 10 mm。
1.2.5 大鼠降血钙效应的研究[10]取 SD 雄性大鼠随机分为 3 组,每组 5 只,分别作为空白对照组、sCT 普通注射液组和 sCT 注射用温度敏感原位凝胶组。给药途径为皮下注射。两个给药组 sCT 的剂量均为 5.0 μg/kg,空白对照组给予等体积的生理盐水,实验前 12 h 禁食,可自由饮水。给药前自大鼠眼眶取血约 0.5 ml 作为对照,给药后分别于 0.5、1.0、1.5、2.0、3.0、4.0、5.0、6.0 及 8.0 h 自大鼠眼眶取血 0.5 ml,6149 ×离心 15 min,取血清,按文献[11-12]方法测定血钙浓度:
⑴试液配制:按文献方法,分别配制钙储备液(1.0 × 103μg/ml 钙离子溶液)、邻甲酚酞络合剂(OCPC)试液(OCPC 32.5 mg、8-羟喹啉 1.1 g、浓盐酸 7.5 ml,以去离子水稀释至 500 ml)、二乙胺试液(二乙胺42 ml,以去离子水稀释至1000 ml)。量取 OCPC 试液、二乙胺试液、甲醇,按 3:3:2 比例配成钙显色液,超声混合 5 min(临用前配制,室温避光放置 1 h 后使用)。
⑵标准曲线绘制:精密吸取上述钙储备液 1.0、2.0、3.0、4.0、5.0、6.0 ml,分别置 25 ml量瓶中,以去离子水稀释至刻度,制得 40、80、120、160、200 及 240 μg/ml 的系列浓度钙标准溶液,分别吸取 40 μl,向其中加入钙显色液 5 ml,混合均匀后立即于 570 nm 波长处测定吸收度。以钙离子浓度()对吸收度值()进行线性回归。
⑶回收率与精密度:分别吸取 40、80 及120 μg/ml 的钙标准溶液 40 μl,向其中加入大鼠空白血清 40 μl,然后按“标准曲线绘制”项下方法处理并测定 570 nm 波长处吸收度值,于 1 d 内重复测定 6 次,计算回收率和日内差。
⑷大鼠血清中钙离子浓度测定:吸取大鼠血清样品每份 40 μl,加入钙显色剂 5 ml,混合均匀后,立即于 570 nm 波长处测定其吸收度值。以标准曲线方程计算血清钙离子浓度。
⑸数据处理:以给药前大鼠血清钙离子浓度作为 100%,各时间点降血钙百分率计算公式为:
降血钙百分率 F(%)=T/0× 100%
T和0分别为 T 时间及给药前的大鼠血清钙离子浓度。以降血钙百分率(F%)对时间(T)作图,得降血钙百分率-时间曲线。以梯形法计算曲线上面积AAC0 ~ 24 h。相对药理活性 RPA 由下述公式计算:
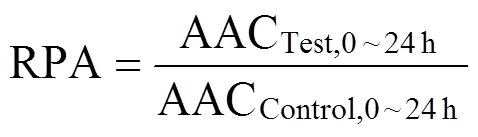
1.3 统计学处理
采用 SPSS13.0 统计学软件进行数据分析,各组间比较采用检验,以< 0.05 为差异有统计学意义。
2 结果
2.1 处方优化
参考本课题组以前在温度敏感原位凝胶方面的研究工作结果[13],初步确定 sCT 温度敏感原位凝胶的基本处方组成为泊洛沙姆 F127(约 20%)及泊洛沙姆 F68(约 1.2%)。之前的原位凝胶基质中还加入了羟丙基甲基纤维素 K4M(HPMC K4M),以调节胶凝温度和凝胶强度,但 HPMC 的溶胀需要加热且过程缓慢,因此凝胶制备需要较长时间,而 sCT 为多肽类药物,热稳定性不佳,且长时间放置也不利于其稳定,因此本处方组成中去掉 HPMC K4M,通过调节泊洛沙姆 F127 和 F68 的浓度来调节合适的胶凝温度。经处方筛选,得到最佳处方组成为:泊洛沙姆 F127 浓度19%,泊洛沙姆 F68 浓度 1.6%。
2.2 胶凝温度
以转子法测定 sCT 温度敏感原位凝胶的胶凝温度为(35.3 ± 1.3)℃,该胶凝温度可较好地满足以液体状态局部注射给药和在体迅速胶凝的要求。
2.3 胶凝时间
以转子法测定 sCT 温度敏感原位凝胶的胶凝时间为(108.3 ± 5.5)s。说明该原位凝胶局部注射后 2 min 以内即可于给药部位形成凝胶,有利于其缓释效果的发挥。
2.4 流变学特性
按最优化处方制备的 sCT 温度敏感原位凝胶,其流变学曲线见图 1。由图可见,在 25 ℃(室温)条件下原位凝胶的剪切力与切变速率呈线性关系,即黏度不随切变速率改变而改变,表明此温度下的原位凝胶具备牛顿流体特性,流动性好,便于制备和转移、吸取、注射等操作,容器残留量小。而当温度升至37 ℃(体温)时,黏度迅速增至很高,其流变曲线存在一屈服值,提示进入体内的凝胶不会因运动或体位变化产生凝胶的挤压与摩擦而发生流动,容易保持一定形状,作为凝胶贮库,有利于缓释效果的发挥。
2.5 质构特性
本研究中,按最优化处方制备的 sCT 温度敏感原位凝胶质构特性考察结果见图 2 和表 1。测定参数定义如下:硬度:第 1 个压缩循环的正峰峰值;凝胶强度:压缩总正峰面积;黏性:压缩的负峰面积,代表探头从样品中离开时的难易程度;黏滞力:第 1 次压缩负峰的峰值。由表 1 结果可知,在 25 ℃条件下,原位凝胶的黏性和黏滞力极低,表明其具备溶液的特性,而基本不表现凝胶的特性;当温度增至 37 ℃时,所有质构特性数据显著增加,表明该温度下形成了具有较高凝胶强度和黏性的凝胶,推测其不易迅速被体液溶蚀,而能在一段较长的时间内保持半固体状态,发挥凝胶骨架的作用,缓慢释放其中所包载的药物。
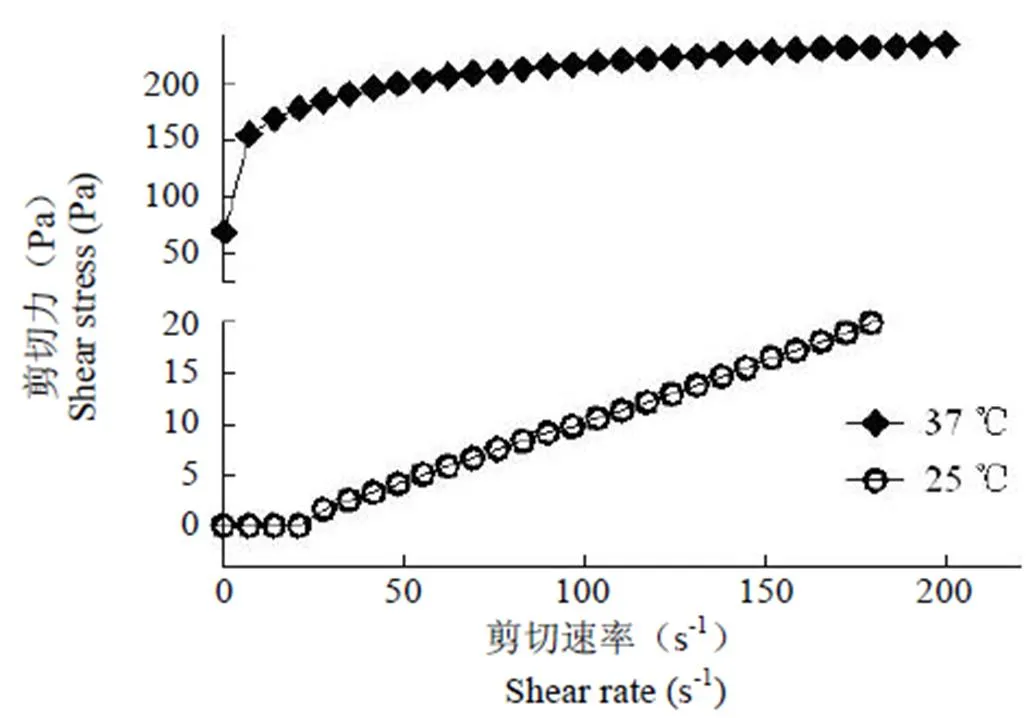
图 1 鲑鱼降钙素温度敏感原位凝胶的流变学曲线
Figure 1 Rheogram of thermosensitivegel loading salmon calcitonin
2.6 降血钙效应
2.6.1 标准曲线的制作及回收率与精密度考察 以钙离子浓度()对吸收度值()进行线性回归得标准曲线方程为= 0.0026+ 0.0312(2= 0.9981);平均回收率为(98.4 ± 2.6)%、(99.4 ± 1.5)% 和(98.6 ± 2.5)%,日内差 RSD 为 2.6%、1.5% 和 2.5%。
2.6.2 大鼠降血钙效应 由图 3 可见,sCT 普通注射液组 1 h 时血钙浓度明显下降,3 h 时血钙浓度达最低值,随后血钙浓度随时间迅速回升;而温敏原位凝胶组血钙浓度下降速率比普通注射液组低,其谷浓度显著高于普通注射液组(< 0.01),表明其最大降血钙能力相对较弱,这可能与原位凝胶中药物初始释放速率低于普通注射液有关。但温敏原位凝胶组的血钙浓度回升速度比注射剂缓慢,在 6 h 和 8 h 产生显著性差异(< 0.05),且其24 h 时血钙浓度明显低于注射剂组,最终计算出温敏原位凝胶组相对于普通注射剂组的相对药理活性为 138.6%。结果表明,温敏原位凝胶制剂维持降血钙的作用时间长于普通注射剂,具有较好的缓释效果,与普通注射液相比,可获得更加平缓且持久的降血钙效应。
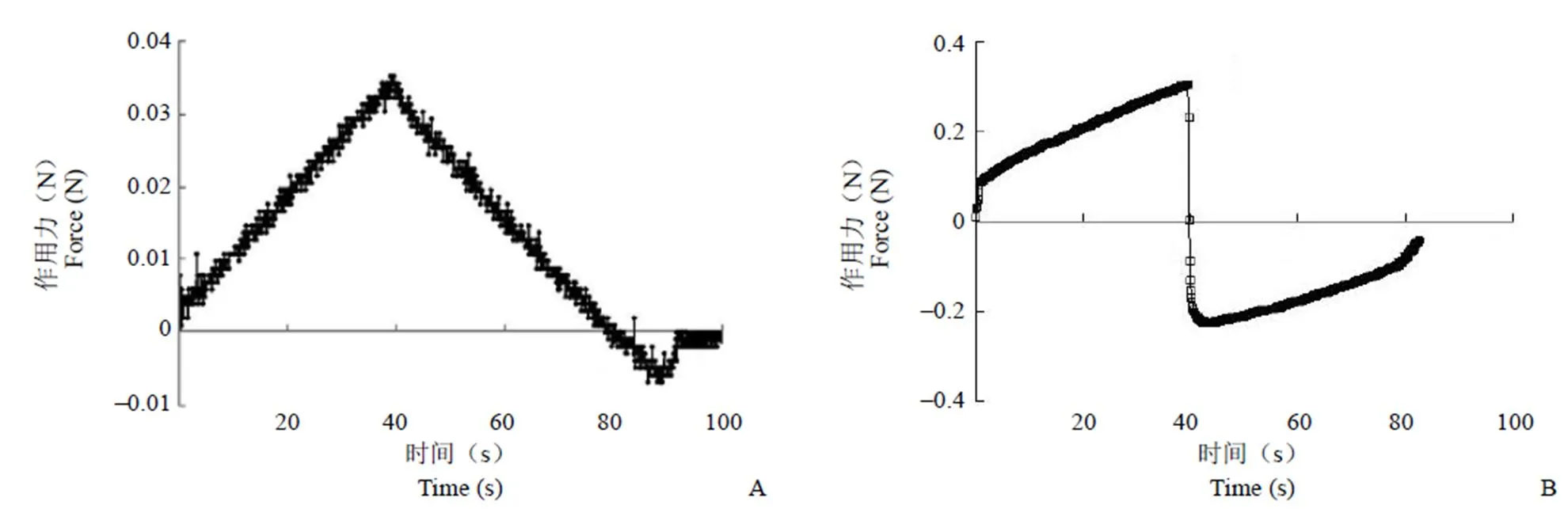
图 2 鲑鱼降钙素温度敏感原位凝胶不同温度下的质构特性曲线(A:25 ℃;B:37 ℃)
Figure 2 Texture profiling of thermosensitivegel loading salmon calcitonin at different temperatures (A: 25 ℃; B: 37 ℃)
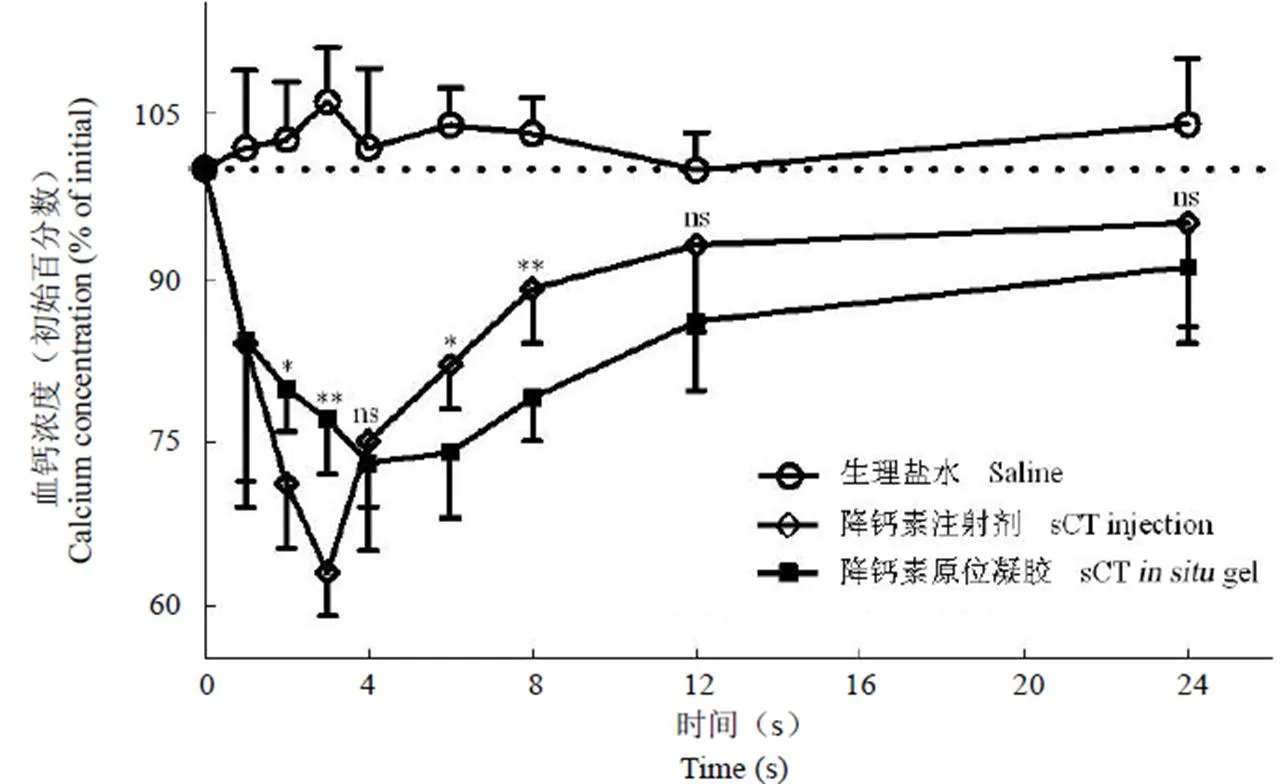
图 3 鲑鱼降钙素普通注射液组及温度敏感原位凝胶组大鼠单剂量给药(5.0 μg/kg)后的血钙水平曲线(与普通注射剂组相比,*P < 0.05;**P < 0.01;nsP > 0.05)
Figure 3 Serum calcium level profiles after S.C. administration of salmon calcitonin (sCT) injection andgel to rats at a single dose of 5.0 μg/kg (n = 5) (Compared with sCT injection,*< 0.05;**< 0.01;ns> 0.05)
3 讨论
胶凝温度是衡量温度敏感原位凝胶系统是否构建成功的关键指标之一。胶凝温度是否适宜需从两方面综合考虑:在体外正常贮存条件下应为流动性较好的液体,以方便给药和分剂量准确;而在体温下又能够迅速形成具有足够胶凝强度的凝胶。温敏原位凝胶的胶凝温度 T 以略低于体温(30 ~36 ℃)为宜。若 T 过低,则室温较高时可能发生胶凝,从而给凝胶的制备和使用带来困难;T 过高,则无法保证在体温条件形成凝胶,或形成凝胶的速度过慢、强度过低等,从而导致缓释效果不理想。单纯泊洛沙姆 F127 水溶液的 T 偏低;泊洛沙姆 F68 本身不具有受热反向胶凝性质,但 F68 的加入可显著升高 F127 溶液的 T 值。因此,本文将泊洛沙姆 F127 与 F68 复合使用作为温敏凝胶的载体材料,以调节适宜的胶凝温度。泊洛沙姆 F127 是最常用的温度敏感原位凝胶载体材料,当其浓度达 18% 以上时,才会出现受热反向胶凝的现象,浓度进一步增加,可以提高其凝胶强度,从而提高缓释效果。制剂中常用的 F127 浓度为 15% ~ 25%。文献报道泊洛沙姆的毒性很低,因其易溶于水,生物相容性也大大优于不溶性的缓释凝胶基质[14-15]。本文制剂中使用的泊洛沙姆 F127 浓度为 19%,推测其安全性和生物相容性良好。
测定胶凝时间的目的是考察温敏原位凝胶在人体平均温度下,从溶液状态转变为凝胶状态所需要的时间。理想的注射用温敏原位凝胶,在以溶液状态进入人体后,应能够迅速于给药部位(原位)胶凝,形成半固体药物储库。因此,胶凝时间越短越好。如果胶凝时间过长,则凝胶形成过程太慢,给药后一段时间内,系统在给药部位仍以液体状态存在,往往会产生较为严重的初始突释效应。由于试验所测得的胶凝时间较短,且测定温度的差异也会对胶凝时间产生影响,因此,为尽可能减小测量误差,不同凝胶样品测定前的起始温度应一致,恒温时应保持相同温度,计时方法也应相同。
流变学特性是原位凝胶非常重要的评价指标[16]。对于注射用温敏原位凝胶,希望其在体外时黏度较低,为流动性很好的液体,用细小针头就能顺利注射;而在体温下黏度迅速增加,形成凝胶。本文所制备的 sCT 温敏原位凝胶能够较好地符合这一要求。目前,对注射用温敏原位凝胶的黏度范围尚无统一规定,根据经验,溶液能够被顺利注射,且能够有效形成凝胶即可。但随着注射用温敏原位凝胶研究的深入,必将会建立起统一的黏度范围标准。
在大鼠血清钙离子浓度测定试验中,血液中存在的镁离子可能干扰试验结果,本文通过加入 8-羟喹啉的方法来掩蔽镁离子的影响。干扰试验表明,按照文中的 8-羟喹啉加入量,镁离子的干扰可完全被掩蔽,测定结果不受镁离子的影响。另外,动物试验中,空白对照组(注射生理盐水)的大鼠血钙浓度也有一定波动,是因为血液中的钙是内源性物质,钙离子浓度随时间波动属动物的正常生理现象,该波动幅度较小,不影响对制剂降血钙效应的测定和评价。
[1] Sinswat P, Tengamnuay P. Enhancing effect of chitosan on nasal absorption of salmon calcitonin in rats: comparisonwith hydroxypropyl- and dimethyl-beta-cyclodextrins. Int J Pharm, 2003, 257(1-2):15-22.
[2] Chesnut CH 3rd, Azria M, Silverman S, et al. Salmon calcitonin: a review of current and future therapeutic indications. Osteoporos Int, 2008, 19(4):479-491.
[3] de Paula FJ, Rosen CJ. Back to the future: revisiting parathyroid hormone and calcitonin control of bone remodeling. Horm Metab Res, 2010, 42(5):299-306.
[4] Abashzadeh Sh, Dinarvand R, Sharifzadeh M, et al. Formulation and evaluation of an in situ gel forming system for controlled delivery of triptorelin acetate. Eur J Pharm Sci, 2011, 44(4):514-521.
[5] Ghahremankhani AA, Dorkoosh F, Dinarvand R. PLGA-PEG-PLGA tri-block copolymers as in situ gel-forming peptide delivery system:effect of formulation properties on peptide release. Pharm Dev Technol, 2008, 13(1):49-55.
[6] Zhang L, Parsons DL, Navarre C, et al. Development and in-vitro evaluation of sustained release Poloxamer 407 (P407) gel formulations of ceftiofur. J Control Release, 2002, 85(1-3):73-81.
[7] Talasaz A, Ghahremankhani A, Moghadam S, et al. In situ gel forming systems of Poloxamer 407 and hydroxypropyl cellulose or hydroxypropyl methyl cellulose mixtures for controlled delivery of vancomycin. J Appl Polym Sci, 2008, 109(4):2369-2374.
[8] Yong CS, Choi JS, Quan QZ. Effect of sodium chloride on the gelation temperature, gel strength and bioadhesive force of poloxamer gels containing diclofenac sodium. Int J Pharm, 2001, 226(1-2):195- 205.
[9] Deng LJ, Li GL, Ding WM, et al. Preparation and quality control of thermosensitive in situ gel of penciclovir for ophthalmic use. Chin J Antibiot, 2010, 35(6):457-461. (in Chinese)
邓丽娟, 李桂玲, 丁维明, 等. 喷昔洛韦眼用温度敏感原位凝胶的制备及质量控制. 中国抗生素杂志, 2010, 35(6):457-461.
[10] Qian DM, Shen GQ, Ke RL. Biological assay of calciton in by blood calcium determination in rats. Chin J Pharmaceutical Analysis, 1994, 14(3):30-34. (in Chinese)
钱德明, 沈根全, 柯若伦. 用大鼠血钙法测定降钙素生物效价的探讨. 药物分析杂志, 1994, 14(3):30-34.
[11] Wang Y, Chen SQ, Wu Q, et al. Determination of calcium in human blood by spectrophotomery. J Anhui Univ (Nat Sci), 1996, 20(1):68- 73. (in Chinese)
王玉, 陈世卿, 吴琼, 等. 邻甲酚酞络合酮分光光度法测定血清钙. 安徽大学学报(自然科学版), 1996, 20(1):68-73.
[12] Fan Y, Li X, Zhou Y, et al. Improved intestinal delivery of salmon calcitonin by water-in-oil microemulsions. Int J Pharm, 2011, 416(1): 323-330.
[13] Ding WM, Li M, Li GL, et al. Thermosensitive in situ gel of boanmycin hydrochloride for injection. Acta Pharm Sinica, 2011, 46(6):727-732. (in Chinese)
丁维明, 李眉, 李桂玲, 等. 盐酸博安霉素注射用温度敏感原位凝胶的研究. 药学学报, 2011, 46(6):727-732.
[14] Nasir F, Iqbal Z, Khan A, et al. Development and evaluation of pluronic- and methylcellulose-based thermoreversible drug delivery system for insulin. Drug Dev Ind Pharm, 2013, Aug 29.
[15] Ibrahim el-SA, Ismail S, Fetih G, et al. Development and characterization of thermosensitive pluronic-based metronidazole in situ gelling formulations for vaginal application. Acta Pharm, 2012, 62(1):59-70.
[16] A-sasutjarit R, Sirivat A, Vayumhasuwan P. Viscoelastic properties of Carbopol 940 gels and their relationships to piroxicam diffusion coefficients in gel bases. Pharm Res, 2005, 22(12):2134-2140.
Preparation and characterization of a novel injectable thermosensitivegel containing salmon calcitonin
DING Wei-ming, LI Yan-fang, LI Gui-ling
To prepare the thermosensitivegel of salmon calcitonin for injection and evaluate the characteristics and hypocalcemic effect.
Poloxamer F127 and poloxamer F68 were used to prepare the thermosensitive gel of samon calcitonin. The characteristics of the gel, such as gelation temperature, gelation time, rheological behavior and texture characteristics, were evaluated. Blood samples were drawn from orbit in rats, and coloration methods were used to monitor serum calcium ion concentration in order to studydrug release and the hypocalcemic effect.
The gelation temperature of the salmon calcitonin-loadedgel was (35.3 ± 1.3)℃, and the gelation time was (108.3 ± 5.5) s. Thegel, a fluid solution at 25 ℃, became semisolid quickly at 37 ℃ due to the fact the viscosity and mechanical parameters such as gel strength for gel was enhanced at 37 ℃. Thegel loading sCT clearly decreased serum calcium level in rats over a longer period of time as compared with the conventional injection indicating sustained characteristic, and produced 138.6% hypocalcemic efficacy relative to common injection.
The thermosensitivegel delivery system may be a promising candidate for injectable sustained delivery of salmon calcitonin.
Calcitonin; Poloxamer; Thermosensitive in situ gel
LI Gui-ling, Email: liguiling1999@163.com
10.3969/cmba.j.issn.1673-713X.2014.03.007
“重大新药创制”国家科技重大专项(2012ZX09301002-001)
李桂玲,Email:liguiling1999@163.com
2013-12-02
Author Affiliations:Formulation Laboratory, Institute of Medicinal Biotechnology, Chinese Academy of Medical Science & Peking Union Medical College, Beijing 100050, China (DING Wei-ming, LI Gui-ling); Medical Research Center, Peking University Third Hospital, Beijing 100191, China (LI Yan-fang)

