免疫渗滤法检测血液及尿液HIV抗体的应用评价
王 倩,杨志东,崔 晨,尚 红
(中国医科大学附属第一医院检验科,辽宁 沈阳 110001)
人类免疫缺陷病毒(human immunodeficiency virus,HIV)是获得性免疫缺陷综合症(acquired immune deficiency syndrome,AIDS)的病原体。自美国1981年诊断出首例AIDS以来,HIV在全球范围内迅速播散,我国AIDS疫情处于总体低流行,特定人群和局部地区高流行的态势[1-3]。目前,HIV抗体检测是临床诊断HIV感染的主要依据,但静脉采血筛查HIV抗体为有创操作,而且容易造成医务人员职业暴露感染,应用无创采集的尿液、唾液等样本检测HIV抗体容易被受试者接受,且能够降低职业暴露的风险。北京万泰生物药业公司HIV1+2型抗体诊断试剂盒(免疫渗滤法)可以快速检测尿液及血浆标本中HIV抗体,本研究采用对照试验方法,评价该试剂盒的临床检测性能,现将结果报告如下。
1 材料与方法
1.1 材料
1.1.1 研究对象 沈阳地区背景清晰的受试人员200例:中国医科大学艾滋病研究所确诊的HIV阳性感染者80例(蛋白免疫印迹法确证HIV抗体阳性),AIDS高危人群40例,健康体检人群80例。
1.1.2 实验试剂 考核试剂HIV1+2型血液、尿液抗体诊断试剂盒(免疫渗滤法)由北京万泰生物药业股份有限公司提供,参考试剂HIV抗体诊断试剂盒(ELISA法)购自法国生物梅里埃公司,免疫印迹法HIV抗体检测试剂盒购自新加坡MP生物医学亚太有限公司。
1.2 方法
1.2.1 标本采集 采集研究对象的血液及尿液标本,血液标本按临床采血技术规范要求抽取静脉血3~5 mL,离心留取血浆备用;尿液标本采集随机尿3~5 mL,及时送检。
1.2.2 检测方法 严格按照试剂说明书进行操作,应用参考试剂检测研究对象的血浆样本,应用考核试剂分别检测同一研究对象的血浆及尿液标本,确保考核试剂每次试验均为有效试验,考核试剂与参考试剂检测结果不一致时应对考核试剂的检测结果进行复检,并经蛋白免疫印迹法确认。
1.2.3 结果判读 根据考核试剂说明书要求,对照点不显色,检测点无论显色与否,结果均判定为无效(图1);对照点显色,检测点不显色,结果判定为阴性(图2);对照点显色,检测点显色,结果判定为阳性(图3)。

图1 无效结果Fig.1 The invalid result

图2 阴性结果Fig.2 The negative result

图3 阳性结果Fig.3 The positive result
1.2.4 统计学分析 计算考核试剂与参考试剂检测的阳性符合率、阴性符合率、总符合率与Kappa值,Kappa值与一致性强度关系见表1。

表1 Kappa值与一致性强度关系Table 1 Kappa value and consistency intensity
2 结果与分析
2.1 血浆样本HIV抗体检测情况
考核试剂与参考试剂结果均显示80例临床确诊的HIV阳性感染者及2例艾滋病高危人群HIV抗体阳性。考核试剂与参考试剂检测结果相比较,阳性符合率 100.00%,阴性符合率100.00%,总符合率 100.00%,Kappa 值 1.00,一致性强度为最强(表2)。
2.2 尿液样本HIV抗体检测情况
考核试剂检测结果显示,55例临床确诊的HIV阳性感染者及1例艾滋病高危人群尿液HIV抗体阳性。考核试剂与参考试剂检测结果相比较,阳性符合率68.29%、阴性符合率100.0%、总符合率87.00%,Kappa值 0.72,一致性强度为高度(表3)。
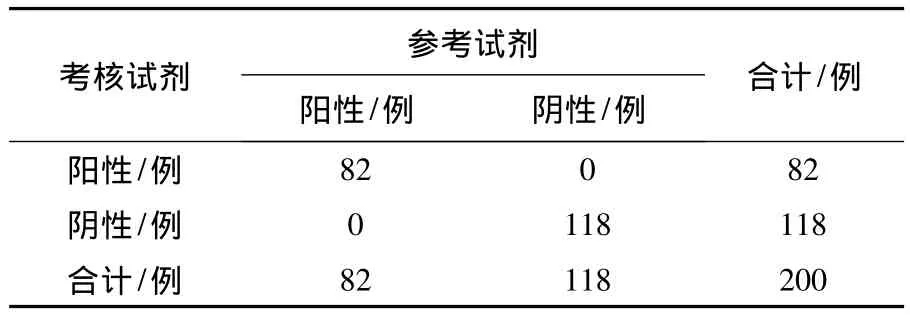
表2 血浆样本HIV抗体检测结果Table 2 HIV antibody results of plasma samples

表3 尿液样本HIV抗体检测结果Table 3 HIV antibody results of urine samples
3 讨论
研究显示,HIV感染者不仅血液含有HIV抗体,其尿液、唾液、泪液、精液及阴道分泌物中均含有HIV抗体[4-6]。尿液标本最易获得且采集具有无损伤性,其HIV抗体与血液抗体平行,主要为IgG。国外上世纪末已有尿液HIV抗体的检测报道,国内近年开始有尿液HIV抗体的检测技术研究[7-8]。万泰药业公司生产的免疫渗滤法HIV抗体诊断试剂盒可用于检测血液及尿液标本中HIV-1及HIV-2抗体,本研究以法国生物梅里埃公司HIV抗体诊断试剂盒(ELISA法)为参照,评估考核试剂万泰药业公司HIV1+2型抗体诊断试剂盒的临床检测性能。
对平行采集的200例背景清晰的受试者血浆及尿液标本应用考核试剂检测,并与参考试剂检测结果进行比较。结果显示,考核试剂检测血浆HIV抗体与参考试剂相比较,阳性符合率、阴性符合率和总符合率均达到100%,Kappa值1.00,检测结果一致性强度为最强;考核试剂检测尿液HIV抗体与参考试剂相比较,阳性符合率68.29%,阴性符合率100%,总符合率87.00%,Kappa值0.72,检测结果一致性强度为高度。
本研究显示,尿液HIV抗体检测敏感性较血液标本略低,200例受试者中,25例临床确诊的HIV阳性感染者和1例血液HIV抗体阳性(经蛋白免疫印迹法确认)的AIDS高危人群,尿液标本经考核试剂检测并复检后HIV抗体均阴性,分析原因:①受试者尿液HIV抗体浓度低于血液标本,与血浆相比,尿液的黏度很低,流过检测卡的速度显著增加,从而使抗原抗体结合的反应时间缩短;②尿液中的化学物质如无机盐、蛋白质、酸碱度等可以影响免疫反应中抗原抗体的反应活性,降低反应的敏感度;③大量摄入液体或服用利尿剂等化学药物影响尿液HIV抗体的阳性检出率[8]。此外,有研究报道[9],尿液存贮时间延长可导致假阴性结果的产生。因此,尿液采集后应尽快检测。
综上所述,免疫渗滤法HIV抗体诊断试剂盒对血浆样本检测性能优越,并适合尿液标本的HIV抗体检测,由于尿液标本采集具有无创伤性且容易获得,大大降低了医务人员职业暴露的风险。免疫渗滤法较传统ELISA法操作简便、快速,尤其适合基层医院及大规模样本HIV抗体筛查。
[1]De Cock KM,Jaffe HW,Curran JW.The evolving epidemiology of HIV/AIDS[J].AIDS,2012,26(10):1205-1213.
[2]卫生部新闻办公室.介绍中国艾滋病疫情现状[J].首都公共卫生,2010,4(1):1.
[3]李建彬,陈斌,米志强,等.以HIV-15'LTR为靶点的药物筛选细胞模型的构建[J].微生物学杂志,2011,31(6):96-100.
[4]Taye B,Woldeamanuel Y,Kebede E.Diagnostic detection of human immunodeficincy virus type-1 antibodies in urine,Jimma Hospital,south west Ethiopa[J].Ethiop Med J,2006,44(4):363-368.
[5]Delaney KP,Branson BM,Uniyal A,et al.Performance of an oral fluid rapid HIV-1/2 test:experience from four CDC studies[J].AIDS,2006,20(12):1655-1660.
[6]Fouda GG,Yates NL,Pollara J,et al.HIV-specific functional antibody responses in breast milk mirror those in plasma and are primarily mediated by IgG antibodies[J].Journal of Virology,2011,85(18):9555-9567.
[7]谭卓,黄云坚,倪崖,等.垂直流免疫印迹法检测尿液HIV-1抗体的技术研究[J].国际流行病学传染病学杂志,2008,35(2):86-88.
[8]赵立庆,雷素萍,李连学,等.ELISA法检测尿液中HIV-1抗体的研究分析[J].中国艾滋病性病,2003,9(5):276-277.
[9]Almeda J,Casabona J,Matas L,et al.Evaluation of a commercial enzyme immunoassay for HIV screening in urine[J].Eur J Clin Microbiol Infect Dis,2004,23(11):831-835.