纳米TiO2/ZSM-5型催化剂的制备及其光催化应用研究进展
孙家伟,刘娜,翟尚儒,安庆大
(大连工业大学轻工与化学工程学院,辽宁 大连 116034)
近年来,TiO2光催化剂因其对气态和液态污染物都有大幅度的降解作用而受到研究者的广泛关注[1]。随着研究者大量研究发现,TiO2光催化剂不仅具有较好的光敏性和光稳定性,而且还具有无毒、无害、无腐蚀性、可重复使用等特性;在操作方面,光催化反应具有反应条件温和、设备结构简单、操作条件易控制等优点[2-5]。与体相 TiO2相比,纳米TiO2颗粒有利于提高光子产率,具有更高的光催化活性。但纳米TiO2颗粒因粒径小、表面能量高而极易团聚,进而对有机物的吸附量下降,使其光催化效率受到限制[6-7]。研究发现,选择具有一定吸附能力的多孔材料作载体,将TiO2负载其上,不仅可起到分散、稳固纳米TiO2颗粒的作用,也利于在实际应用中催化剂的回收[8];载体的吸附作用可使液相或气相体系中低剂量有机底物在催化剂表面富集,增大底物与光催化剂的接触概率,借此提高有机物的降解速率[12,19-21]。目前,用于负载 TiO2的载体主要有玻璃[9]、不锈钢[10]、氧化铝[11]、活性炭[12]、碳纳米管[13]、介孔分子筛MCM-41[14]和沸石[15,16-22]等。在众多载体中,ZSM-5型分子筛因其较高的比表面积、较高的吸附性能、带电框架结构、良好的热稳定性及环境友好等特性使其成为最合适的载体之一[23]。鉴于此,本文系统地归纳了纳米TiO2/ZSM-5及金属阳离子改性后的 M-纳米TiO2/ZSM-5的不同制备方法,不同催化剂对不同有机染料降解的作用机理,并对其未来对水质、土壤、大气中有机污染物降解的应用前景作了展望。
1 纳米 TiO2/ZSM-5光催化剂的制备及其光催化应用
目前,纳米 TiO2/ZSM-5的常见制备方法是溶胶-凝胶法、浸渍法,最新的制备方法是水热合成法,而固体间相互结合法的报道较少。
1.1 溶胶-凝胶法制备纳米TiO2/ZSM-5光催化剂及其应用
2007年,Panpa等[25]利用溶胶-凝胶法,以TiOSO4为前体,结合 Sakthivel等[24]所使用的方法合成pH值为6、含硫酸根离子的TiO2溶胶溶液,与ZSM-5混合搅拌形成凝胶,从而制成纳米TiO2/ZSM-5。制备流程图如图1[25]。
Panpa 等[25]通过对甲基蓝溶液的光催化降解实验研究表明,TiO2负载量为20%时,在紫外光照射与硫酸根离子的协同作用下,纳米 TiO2/ZSM-5展现出更高的催化效率,同商业P25相比,二者的光催化效率几乎相同。制备过程中使用硫酸根离子作为一种强絮凝剂能增加染料分子沉降在催化剂表面的数量,进而增加染料分子的吸附量,从而增加光催化效率。

图1 复合物纳米TiO2/ZSM-5制备的流程图[25]
虽然Panpa等[25]成功合成了纳米TiO2/ZSM-5,但是其光催化效率并不理想,且仍有部分作用机理尚未进行深入研究,不过在其处理纺织染料方面有潜在的应用。
2010年,Zainudin等[26]首先利用 Gennequin等[27]报道的溶胶-凝胶法合成纳米 TiO2,再将四异丙醇钛、乙醇、水分别按照 1∶2∶5 的比例混合制成溶胶-凝胶液,经80 ℃ 干燥24 h制成纳米TiO2,再将制成的纳米 TiO2同 ZSM-5、硅凝胶混合,使用磁力搅拌器搅拌 30 min,干燥后使用马弗炉在600 ℃下煅烧 3 h制成新型纳米 TiO2/ZSM-5(SNTZS)。通过降解苯酚溶液测试其光催化效率,实验研究表明,SNTZS的最佳合成质量比为纳米TiO2∶ZSM-5∶硅胶凝胶∶硅胶溶胶=1∶0.6∶0.6∶1,在234 nm紫外光照射3 h条件下,光催化剂对50 mg/L的苯酚溶液的降解率达到 90%。而德固赛公司生产的P25在同样条件下对苯酚的降解率只有67%,相比而言,SNTZS的光催化活性要远远高于德固赛公司生产的 P25,其原因主要是前者能够创造出更多的空穴电子对[28],并且能够有效地抑制空穴电子对的复合,进而增加了光催化效率。
Zainudin 等[26]研制的 SNTZS型光催化剂具有较大的比表面积、较低的电子空穴复合率、较高的晶体质量、良好的光催化稳定性以及可循环利用等诸多优点,使得其在紫外光照射下对苯酚的降解率取得了显著的成效。然而 SNTZS光催化剂对可见光利用率较低,对电子和空穴的捕捉能力也无法令人满意。总的来说,结合 SNTZS所制成的催化剂已经使纳米 TiO2/ZSM-5型光催化剂的研究获得了重大的突破。
由于溶胶-凝胶法中所用的原料首先被分散到溶剂中而形成低黏度的溶液,因此就可以在很短的时间内获得分子水平的均匀性,在形成凝胶时,反应物之间很可能是在分子水平上被均匀地混合,进而TiO2能均匀地分散到ZSM-5表面,并且反应温度低,反应容易进行。但是溶胶-凝胶法也存在某些问题: 通常整个溶胶-凝胶过程所需时间较长(主要指陈化时间),常需要几天;还有就是凝胶中存在大量微孔,在干燥过程中又将会逸出许多气体及有机物,并产生收缩。
1.2 浸渍法制备纳米TiO2/ZSM-5光催化剂及其应用
2005年,Mohamed等[29]使用浸渍法合成出纳米 TiO2/ZSM-5,他们将 Na-ZSM-5[30]与含一定量TiCl4的乙醇溶液混合搅拌,所得产物经 110 ℃干燥6 h,再经550 ℃煅烧6 h制成。他们通过降解EDTA 来考察纳米 TiO2/ZSM-5的光催化效率,研究表明,在紫外光照射下,TiO2的负载量为2%时,pH值为7时EDTA的降解率达到99%。此方法操作简单,对EDTA的光催化效果较好,为EDTA的降解开辟了一条新的路径。
2009年,Huang等[31]通过浸渍法将钛酸四丁酯缓慢加入 H-ZSM-5和乙醇的悬浮液中,再将蒸馏水加入到上述悬浮液中搅拌1 h,再经过 90 ℃ 干燥 12 h 和不同温度下煅烧 3 h 制成纳米 TiO2/ZSM-5。在臭氧辅助作用及紫外光照射条件下,通过对乙醛气体的光催化氧化降解实验研究表明,TiO2的负载量为 20%时光催化剂催化活性最高,其中臭氧不仅能够作为电子的接收者,还能产生OH·,因此 O3辅助下大大增加了纳米TiO2/ZSM-5的光催化活性,进而提高了光催化效率。O3的作用机理如式(1)~式(9)[31]。

Huang 等[31]用浸渍法合成的纳米 TiO2/ZSM-5具有较强的吸附性能和较高的光催化活性,尤其是他们首次采用 O3和紫外光共同辅助来进行光催化反应,取得了令人满意的效果。但是在紫外光下照射下反应能耗较高,反应成本较大。此制备方法的完善及作用机理还有待于继续研究。
2010年,Mahadwad等[32]同样通过浸渍法制备出纳米TiO2/ZSM-5。他们先将ZSM-5浸入到水中90 min,再与TiO2溶胶混合搅拌1 h,将混合液在50 ℃下干燥2~3 h,再将其放入120 ℃ 烘箱中过夜,再经450 ℃ 煅烧11~12 h 制成TiO2/ZSM-5。通过对RB-5染料的光催化降解实验研究表明,将TiO2浸渍在 ZSM-5表面能够在比较温和的反应条件下进行,在紫外光照射下,TiO2的负载量为 20%时对RB-5的降解率达到最大,并且在同样条件下,TiO2/ZSM-5对RB-5的光催化效率要高于商业P25对RB-5的光催化效率。虽然TiO2/ZSM-5的光催化活性强于P25,但是其对降低污水中COD没有达到令人满意的效果。
浸渍法制备 TiO2/ZSM-5具有较高的活性组分利用率、生产方法简单、生产能力高、成本低等优点。但是干燥过程会导致活性组分的迁移,导致TiO2的负载量下降。
1.3 水热合成法制备纳米TiO2/ZSM-5光催化剂及其应用
2010年,Khatamian 等[33]利用水热合成法将5 mL四丁基氢氧化胺与 5 mL无水乙醇混合搅拌1 h,再向混合液中加入 5.56 mL四乙基钛酸酯和 30 mL蒸馏水,混合后在80 ℃温度下加热1 h,再加入1 g ZSM-5粉末形成白色凝胶,继续搅拌 1 h,将所有产品放入聚四氟乙烯内衬的反应釜中在180 ℃烘箱内反应4天,得到白色悬浮液在25 ℃下干燥,然后于400 ℃煅烧3 h制成 TiO2/ZSM-5。通过对棕NG的染料降解实验研究表明,水热合成法制备的纳米TiO2/ZSM-5在紫外光照射下对棕NG染料的降解率要远远高于同样条件下商业 P25对棕 NG 染料的降解率。原因是水热合成法 TiO2能更好地分布在ZSM-5外表面的同时,分子筛内部孔道也吸附了一定量TiO2,进而抑制了TiO2的大量凝聚,使得纳米 TiO2/ZSM-5光催化剂更易产生空穴电子对,进而提高了光催化效率[34]。纳米TiO2/ZSM-5与商业P25、ZSM-5的光催化效率对比如图2。
水热合成法合成的TiO2/ZSM-5催化效率较高,但是其设备要求高、技术难度大、成本高、安全性能差等缺点制约了使用该方法来扩大化生产TiO2/ZSM-5的可行性。
1.4 固体间结合法制备纳米TiO2/ZSM-5光催化剂及其应用
除上述3种方法外,由于其他方法的报道较少,制备的光催化剂的催化性能较低,所以本文只列举固体间结合法来进行综述。

图2 反应 30 min催化剂的活性比较[33]
Mohamed等[29]使用固体间结合法在氮气环境下将 ZSM-5预处理后与TiO2(锐钛矿)在室温下机械混合,所得固体在550 ℃煅烧6 h 制得光催化剂。
Mohamed 等[29]通过对 EDTA 的降解率来考察光催化剂的光催化效率。研究表明,在紫外光照射下,用固体间结合法制得的催化剂对 EDTA 具有一定降解性能,降解率能够达到 75%。对比其他方法制备的光催化剂,催化效果不够理想。
2 金属离子改性纳米 TiO2/ZSM-5光催化剂的制备及其应用
金属离子改性后的纳米 TiO2/ZSM-5主要有两种形式:①纳米 TiO2/M-ZSM-5型和②M-纳米TiO2/ZSM-5型,其中 M 离子的引入目前主要采用离子交换法和水热合成法两种方法。而纳米 TiO2负载的方法主要有浸渍法、溶胶-凝胶法以及水热合成法。所以针对①和②的不同类型会有不同的制备方法与之对应。
2.1 纳米TiO2/M-ZSM-5型光催化剂的制备及应用
2.1.1 水热合成法与溶胶-凝胶法
2009年,Guo等[35]利用正丁胺为模板剂,通过水热合成法用 Na+对 H-ZSM-5进行改性,首先得到 NaZSM-5。然后使用一种改进的溶胶-凝胶法,将含有饱和吸水量的 NaZSM-5加入到钛酸四丁酯与无水乙醇组成的混合液中,其中钛酸四丁酯水解所需要的水分由分子筛的缓释作用所提供,这种改进的溶胶-凝胶法能够抑制 TiO2凝胶的聚合。通过对甲基橙的光催化降解实验研究表明,Na+的改性不会影响TiO2在分子筛上的分布,而会影响分子筛上质子的活性,进而对分子筛吸附甲基橙分子的量产生影响,当Na+负载量在1.1%时,催化剂对甲基橙的吸附效果最佳,进而光催化效率最高。其中,催化剂上的强酸性位点会抑制甲基橙分子的吸附,中等酸性位点有利于甲基橙分子的可逆吸附。其机理如图3所示[35]。
Guo 等[35]首次使用改进的溶胶-凝胶法,利用分子筛的缓释作用水解钛酸四丁酯,使得 TiO2在分子筛上的分布更加均匀,团聚作用减弱,进而提高了光催化效率,但是制备出的光催化剂在可见光下光催化效率较低,有待于通过进一步工作提高。
2.1.2 浸渍法与离子交换法
2012年1月,Yuan等[36]利用浸渍法和离子交换法成功地制备出纳米TiO2/M-ZSM-5(M=Zn,Cu,Mn),他们将金属离子盐溶液与H-ZSM-5进行离子交换首先合成M-ZSM-5,再向M-ZSM-5与乙醇组成的悬浮液中加入钛酸四丁酯,再加入一定量的水使钛酸四丁酯水解成二氧化钛浸渍在 M-ZSM-5的表面,从而制备出纳米TiO2/M-ZSM-5(M=Zn,Cu,Mn)。在臭氧辅助条件下,对乙醛气体的降解实验研究表明,M-ZSM-5中金属阳离子作为臭氧的氧化活性位点在相对稳定的状态下吸附乙醛分子,提高了反应的催化氧化率,并且光催化产生的截流子不但与H2O和O2反应,还同臭氧反应,所以在紫外-臭氧共同作用下,纳米TiO2/M-ZSM-5显著提高了光催化降解乙醛的效率。进一步研究发现,Zn、Cu、Mn 3种金属离子中,使用Mn离子改性后纳米TiO2/Mn-ZSM-5的光催化效率最高,主要是因为Mn离子分解O3的能力要强于Zn、Cu离子,从而获得更好的光催化效率,如图4[36]。

图3 HZSM-5和 TiO2/1.1%Na-HZSM-5复合光催化剂的可逆吸附[35]

图4 乙醛的降解率[36]
上述方法合成的光催化剂对提高污染性气体降解率这一难题提供了可靠的解决途径,对比之前的研究有了更突出的进展。
2.1.3 湿式浸渍法
2012年 8月,Wang 等[37]利用湿式浸渍法将Ni(NO3)2和 Ti(SO4)2溶液与ZSM-5混合搅拌10 h,所得固体经过60 ℃ 真空干燥5 h 后再放入马弗炉内煅烧3 h,制成TiO2/Ni-ZSM-5催化剂。通过对柴油的脱硫降解实验研究表明,在反应温度为60 ℃,反应压强为0.1 MPa,空间速率为1 h−1,催化剂同柴油比率为 1.5时,柴油中 TH、BT、DBT、4,6-DMDBT 的最佳去除率分别达到了 99.8%、98.6%、99.8%和 99.5%,其中催化剂对噻吩(TH)的催化降解率最高。作用机理分析如下:TiO2和NiO 的带隙能分别为3.2 eV和3.5 eV,导致二者的带隙结构和产生电子能力有所不同,由于NiO的费米能级高于 TiO2,NiO 导带产生的电子会转移到TiO2的导带上,相对应的 TiO2价带产生的空穴会转移到 NiO 的价带,从而使得TiO2中的空穴电子对有效地分离,提高了光催化效率。
Wang 等[37]使用湿式浸渍法合成的光催化剂首次应用于去除柴油中的硫化合物,取得了令人满意的效果。
2.2 M-纳米 TiO2/ZSM-5型光催化剂的制备及其应用
2.2.1 溶胶-凝胶法与光沉淀法
2006年,杨海明等[38]采用溶胶-凝胶法和光沉淀法制备了 Pt-纳米TiO2/ZSM-5催化剂,研究了铂修饰对催化剂吸附性能的影响,考察了催化剂在日光照射下对氨氮的氧化,并以紫外光作为对比。结果表明,铂的修饰显著提高了催化剂的吸附能力,还可提高催化剂在日光照射条件下对氨氮的氧化效率和总氮去除率。实验结果表明,在太阳光照射、空气曝气条件下,反应 2 h 氨氮去除率达 50.1%,总氮去除率达 31. 8%。此法制备的催化剂在日光照射下有脱除水体氨氮和总氮的效果,但是二者的降解效果都没有达到一个理想的预期,此法有待于进一步研究。
2.2.2 溶胶-凝胶法与离子交换法
2008年,Ökte 和Yilmaz[39]先通过溶胶-凝胶法以醇盐为前体合成了纳米TiO2/ZSM-5[40-41],再通过离子交换法将钇离子负载到纳米 TiO2/ZSM-5上制备出Yi-纳米TiO2/ZSM-5[42]。通过对甲基橙的光催化降解实验研究表明,初始浓度为3.27 mg/L的甲基橙溶液,在紫外光照射条件下照射 4 h,TiO2的负载量为 40%,钇离子负载量为 28%时,甲基橙的降解率达到 97.3%。研究发现,钇离子的引入使得光催化效率有了明显的提高是因为钇离子对电子的吸引,从而抑制了空穴电子对的复合。图5是甲基橙光催化反应机理图[39]。
同年,他们课题组[43]经过进一步研究,使用上述方法合成出 0.28%La-40%纳米 TiO2/ZSM-5,其对甲基橙光催化机理如图6。
2009年,该课题组[44]继续研究,用同样的方法制备出 0.28%Ce-40%纳米 TiO2/ZSM-5,并将其与0.28%La-40%纳米 TiO2/ZSM-5进行光催化性能比较,二者都显示出较高的光催化效率,但 0.28%La-40%TiO2/ZSM-5的光催化效率较高。

图5 甲基橙的催化降解路径模拟[39]

图6 甲基橙光催化降解的简易路线图[43]
该课题组还成功地将 Ce、La、Yi等离子负载到纳米 TiO2/ZSM-5上,由于金属离子对电子的吸引作用,抑制了空穴电子对的复合,提高了光催化效率,但在可见光照射下的光催化效果无法令人满意,有待于进一步的研究。
2010年,夏凤丽等[45,46]同样使用溶胶-凝胶法制备出Sm3+掺杂TiO2(摩尔分数为0.9%)负载在ZSM-5上的催化剂,制成的 Sm-纳米 TiO2/ZSM-5通过对甲基橙溶液的降解实验研究表明,Sm 掺杂可以改善催化剂的吸附性能,提高TiO2催化剂的光催化活性。在催化剂浓度为1~5 g/L变化时,甲基橙的降解率随着催化剂浓度增加而逐渐增大,降解率从 50%增加到 85%。甲基橙的初始浓度在 10~50 mg/L 时,随着初始浓度增大,光催化降解速度减小。溶液 pH 值对甲基橙降解影响显著,酸性溶液有利于甲基橙的光催化降解。对于Sm在催化剂中的作用机理,Xu等[47]通过进一步研究证明有以下两点原因:①稀土元素具有f电子,对有机污染物有较强的吸附作用,并且部分Sm元素以Sm2O3富集在TiO2表面,Sm2O3能提高催化剂表面吸附能力,从而提高TiO2光催化效率;②Sm3+的半径(96.4 nm)远大于 Ti4+的离子半径(68 pm),无法取代晶格位置上的Ti4+[48],可能进入晶格内部成为间隙原子引起 TiO2晶格膨胀,从而引起氧缺陷捕获光生空穴;Sm3+是可变价元素,Sm3+/Sm2+标准还原电位为−1.55 V,容易在二氧化钛表面发生氧化还原反应,也可捕获电子或空穴[49]。共同作用短时间里捕获空穴和电子,大大加强了空穴电子对的有效分离,因而提高了光催化活性。
2.2.3 水热合成法
2012年,Khatamian 等[50]利用水热合成法制备出 M-纳米 TiO2/ZSM-5(M=Fe或 Ni),并且在可见光照射下催化降解黄GX溶液来比较 Fe-纳米TiO2/ZSM-5和 Ni-nanaTiO2/ZSM-5的光催化效率,结果显示前者的光催化效率要高于后者。实验研究表明,在可见光照射 15 min后,Fe-纳米TiO2/ ZSM-5对染料GX的降解率达到接近 100%,其原因归结为以下两点:①Fe 和 Ni 的d轨道重叠效应;②Fe3+对空穴和电子的吸收作用[51]。其作用机理如式(10)~式(13)[50]。
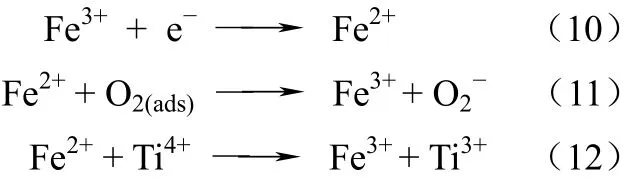

Khatamian等[50]使用水热合成法合成的催化剂突破了在可见光照射下能够发生光催化反应这一瓶颈,使得纳米 TiO2/ZSM-5型光催化剂的研究进入了新的阶段。
3 结 语
近年来,以纳米 TiO2/ZSM-5为主体的光催化剂受到研究人员的广泛关注,在理论研究、制备方法和应用探索等方面均取得较大进展,这对光催化技术的学术研究和产业挖掘有重大意义,有助于多功能复合材料在环境和化工领域发挥更大的作用。
目前制备纳米 TiO2/ZSM-5为主体的光催化剂方法主要有溶胶-凝胶法、浸渍法和水热合成法3种方法,比较3种方法可以得到如下结论。
(1)溶胶-凝胶法具有反应温度低、反应相对简单等优点,但其反应周期较长、干燥过程中孔道会发生收缩等缺点限制了溶胶-凝胶法的进一步发展。
(2)浸渍法制备的纳米TiO2/ZSM-5具有较高的活性组分利用率、生产方法简单、生产能力高、成本低等优点。但是干燥过程会导致活性组分的迁移,导致 TiO2的负载量下降,分散不均匀。
(3)水热合成法制备的催化剂光催化性能较高,但是其设备结构复杂、生产技术难度大、成本高、安全性能差等缺点制约了使用该方法来扩大化生产纳米TiO2/ZSM-5的可行性。
但是上述 3种方法均存在对可见光利用率较低、纳米TiO2颗粒在载体上分散不均匀、无法更好地抑制空穴电子对复合等复杂问题,严重制约了纳米 TiO2/ZSM-5为主体的光催化剂的进一步发展,所以解决以上问题就成为未来研究纳米 TiO2/ZSM-5为主体的光催化剂的重要突破口。近来,水热合成法合成的 Fe-TiO2/ZSM-5在解决上述问题上已经取得了很大的进步,已经在降解染料和有毒气体、液体方面取得了一定的成果,相信随着研究者们的不断探索,不断优化制备条件和创新工艺设备,纳米 TiO2/ZSM-5为主体的光催化剂将在化工催化和水质、土壤大气等环境治理等方面有着更为广泛的应用。
[1]Kansal S K,Singh M,Sud D. Studies on photodegradation of two commercial dyes in aqueous phase using different photocatalysts[J]. J.Hazard Mater.,2007,141:582-586.
[2]Di Paola A,Cufalo G,Addamo M,et al. Photocatalytic activity of nanocrystalline TiO2(brookite,rutile and brookite-based) powders prepared by thermohydrolysis of TiCl4in aqueous chloride solutions[J]. Colloids Surf. A,2008,317:366-376.
[3]Rao N N,Chaturvedi V. Photoactivity of TiO2-coated pebbles[J].Ind. Eng. Chem. Res.,2007,46:4406-4414.
[4]Ao Y H,Xu J J,Fu D G,et al. Low temperature preparation of anatase TiO2-coated activated carbon[J]. Colloids Surf. A,2008,312:125-130.
[5]Xu J J,Ao Y H,Fu D G,et al. Synthesis of Gd-doped TiO2nanoparticles under mild condition and their photocatalytic activity[J].Colloids Surf. A,2009,334:107-111.
[6]Ding X J,An T C,Li G Y,et al. Preparation and characterization of hydrophobic TiO2pillared clay:The effect of acid hydrolysis catalyst and doped Pt amount on photocatalytic activity[J]. J. Colloid Interface Sci.,2008,320:501-507.
[7]Kibanova D,Cervini-Silva J,Destaillats H. Nanocomposites on the photocatalytic elimination of a model hydrophobic air pollutant[J].Environ. Sci. Technol.,2009,43:1500-1506.
[8]Li F F,Sun S M,Jiang Y S,et al. Photodegradation of an azo dye using immobilized nanoparticles of TiO2supported by natural porous mineral[J]. J. Hazard Mater.,2008,152:1037-1044.
[9]Nam H J,Amemiya T,Murabayashi M,et al. Photocatalytic activity of Sol-Gel TiO2films on various kinds of glass substrates:The effects of Na+and primary particle size[J]. J. Phys. Chem. B,2004,108:8254-8259.
[10]Chen Y J,Dionysiou D D. Effect of calcination temperature on the photocatalytic activity and adhesion of TiO2films prepared by the P-25 powder-modified sol-gel method[J]. J. Mol. Catal. A:Chem.,2005,244(1-2):73-82.
[11]Sakthivel S,Shankar M V,Palanichamy M,et al. Photocatalytic decomposition of leather dye:Comparative study of TiO2supported on alumina and glass beads[J]. J. Photochem. Photobiol. A:Chem.,2002,148(1-3):153-159.
[12]Ao C H,Lee C S. Combination effect of activated carbon with TiO2for the photodegradation of binary pollutants at typical indoor air level[J]. J. Photochem. Photobiol. A:Chem.,2004,161(2-3):131-140.
[13]Liu B,Zeng H C. Carbon nanotubes supported mesoporous mesocrystals of anatase TiO2[J]. Chem. Mater.,2008,20(8):2711-2718.
[14]Sun B,Reddy E P,Smirniotis P G. TiO2-loaded Cr-modified molecular sieves for 4-chlorophenol photodegradation under visible light[J]. J. Catal.,2006,237(2):314-321.
[15]Tayade R J,Kulkarni R G,Jasra R V. Enhanced photocatalytic activity of TiO2-coated NaY and HY zeolites for the degradation of methylene blue in water[J]. Ind. Eng. Chem. Res.,2006,46(2):369-376.
[16]Shankar M V,Cheralathan K K,Arabindoo B M,et al. Enhanced photocatalytic activity for the destruction of monocrotophos pesticide by TiO2/Hβ[J]. J. Mol. Catal. A:Chem.,2004,223(1-2):195-200.
[17]Shankar M V,Anandan S,Venkatachalam N,et al. Fine route for an efficient removal of 2,4-dichlorophenoxyacetic acid (2,4-D) by zeolite-supported TiO2[J]. Chemosphere,2006,63(6):1014-1021.
[18]Takeuchi M,Kimura T,Hidaka M ,et al. Photocatalytic oxidation of acetaldehyde with oxygen on TiO2/ZSM-5 photocatalysis:Effect of hydrophobicity of zeolite[J]. J. Catal.,2007,246(2):235-240.
[19]Li F F,Jiang Y S,Yu L X,Zheng W Y,et al. Surface effect of natural zeolite (clinoptilolite) on the photocatalytic activity of TiO2[J]. Appl.Surf. Sci.,2005,252(5):1410-1416.
[20]Dubey N,Rayalu S S,Labhsetwar N K,et al. Photocatalytic properties of zeolite-based materials for the photoreduction of methyl orange[J]. Appl.Catal. A,2006,303(2):152-157.
[21]Yahiro H,Miyamoto T,Watanabe N,et al. Photocatalytic partial oxidation of α-methylstyrene over TiO2supported on zeolites[J].Catal. Today,2007,120(2):158-162.
[22]Zhang J,Xu Q,Feng Z C. Importance of the relationship between surface phases and photocatalytic activity of TiO2[J]. Angew. Chem.Int. Ed.,2008,120:1766-1769.
[23]Yoneyama H,Torimoto T. Titanium dioxide/adsorbent hybrid photocatalysts for photodestruction of organic substances of dilute concentrations[J]. Catal. Today,2000,58:133-140.
[24]Sakthivel S,Hidalgo M C,Bahnemann D W,et al.A fine route to tune the photocatalytic activity of TiO2[J]. Appl. Catal. B,2005,63:31-40.
[25]Panpa W,Sujaridworakun P,Jinawath S. Photocatalytic activity of TiO2/ZSM-5 composites in the presence of SO42−ion[J]. Appl. Catal.B,2008,80:271-276.
[26]Zainudin Nor Fauziah,Abdullah Ahmad Zuhairi,Mohamed Abdul Rahman. Characteristics of supported nano-TiO2/ZSM-5/silica gel(SNTZS):Photocatalytic degradation of phenol[J]. J. Hazard Mater.,2010,174:299-306.
[27]Gennequin C,Lamallem M,Cousin R,et al.Catalytic oxidation of VOCs on Au/Ce-Ti-O[J]. Catal. Today,2007,122:301-306.
[28]Boujday S,Wunsch F,Portes P,et al. Photocatalytic and electronic properties of TiO2powders elaborated by sol-gel route and supercritical drying[J]. Energy Mater. Sol. Cells,2004,83:421-433.
[29]Mohamed R M,Ismail A A,Othman I,et al. Preparation of TiO2-ZSM-5 zeolite for photodegradation of EDTA[J]. J. Mol. Catal.A:Chem.,2005,238:151-157.
[30]Reda M M,Hisham A M,Mohamed E F,et al. Effect of the silica sources on the crystallinity of nanosized ZSM-5 zeolite[J]. Micro.Meso. Mater.,2005,79:7-12.
[31]Huang Xin,Yuan Jian,Shi Jianwei,et al.Ozone-assisted photocatalytic oxidation of gaseous acetaldehyde on TiO2/H-ZSM-5 catalysts[J]. J. Hazard Mater.,2009,171:827-832.
[32]Mahadwad O K,Parikh,R V,Jasra P A ,et al. Photocatalytic degradation of reactive black-5 dye using TiO2impregnated ZSM-5[J]. Bull. Mater. Sci.,2011,34:551-556.
[33]Khatamian M,Hashemian S,Sabaee S. Preparation and photo-catalytic activity of nano-TiO2-ZSM-5 composite[J]. Mater. Sci.Semicond. Process,2010,13:156-161.
[34]王学琴,王祥生,郭新闻. 超细颗粒五元环沸石的制备方法:中国,99102700.0[P]. 1999-04-21.
[35]Guo Peng,Wang Xiangsheng,Guo Hongchen. TiO2/Na-HZSM-5 nano-composite photocatalyst:Reversible adsorption by acid sites promotes photocatalytic decomposition of methyl orange[J]. Appl.Catal. B,2009,90:677-687.
[36]Yuan Jian,Huang Xin,Chen Mingxia,et al. TiO2/Na-HZSM-5 nano-composite photocatalyst:Reversible adsorption by acid sites promotes photocatalytic decomposition of methyl orange[J]. Catal.Today,2012,201:182-188.
[37]Wang Lei,Cai Haijun,Li Shuzhen,et al. Ultra-deep removal of thiophene compounds in diesel oil over catalyst TiO2/Ni-ZSM-5 assisted by ultraviolet irradiating[J]. Fuel,2012,105:752-756.
[38]杨海明,柳丽芬,张兴文,等. Pt/TiO2/ZSM-5在日光下氧化氨氮的研究[J]. 环境科学与技术,2006,29(10):1-3.
[39]Ökte A Neren,YiImaz Özge. Photodecolorization of methyl orange by yttrium incorporated TiO2supported ZSM-5[J]. Appl. Catal. B,2008,85:92-102.
[40]Kitayama Y,Kodama T,Abe M,et al. Synthesis of titania pillared saponite in aqueous solution of acetic acid[J]. J. Porous Mater.,1998,5:121-126.
[41]Kaneko T,Fuji M,Kodama T,et al. Synthesis of titania pillared mica in aqueous solution of acetic acid[J]. J. Porous Mater.,2001,8:99-109.
[42]Yang R T,Tharappiwattananon N,Long R Q. Ion-exchanged pillared clays for selective catalytic reduction of NO by ethylene in the presence of oxygen[J]. Appl. Catal. B,1998,19:289-304.
[43]Ökte A Neren,Yilmaz Özge. Characteristics of lanthanum loaded TiO2-ZSM-5 photocatalysts:Decolorization and degradation processes of methyl orange[J]. Appl. Catal. A,2009,354:132-142.
[44]Ökte A Neren,Yilmaz Özge. La and Ce loaded TiO2-ZSM-5 catalysts:Comparative characterization and photocatalytic activity investigations[J]. Micro. Meso. Mater.,2009,126:245-252.
[45]夏凤丽,孙涛. 钐掺杂TiO2负载型催化剂降解甲基橙的影响因素[J]. 安徽农业科学,2010,38(11):5825-5826.
[46]李慧泉,李越湘,周新木,等. Sm2O3掺杂 TiO2光催化剂的制备和性能[J]. 催化学报,2004,5(10):814-818.
[47]Xu A W,Gao Y,Liu H Q. The preparation,characterization,and their photocatalytic activities of rare-earth-doped TiO2nanoparticles[J]. J.Catal.,2002,207:151-157.
[48]陈俊涛,李新军,杨莹,等. Sm掺杂对 TiO2薄膜光催化性能的影响[J]. 催化学报,2004,25(5):397-420.
[49]Zhu J,Zheng W,He B,et al.Characterization of Fe-TiO2photocatalysts synthesized by hydrothermal method and their photocatalytic reactivity for photodegradation of XRG dye diluted in water[J]. J. Mol. Catal. A:Chem.,2004,216:35-43.
[50]Khatamian M,Hashemian S,Yavari A,et al.Preparation of metal ion(Fe3+and Ni2+) doped TiO2nanoparticles supported on ZSM-5 zeolite and investigation of its photocatalytic activity[J]. Mater. Sci.and Eng. B,2012,177(18) :1623-1627.
[51]Ohno T,Murakami N,Tsubota T,et al. Development of metal cation compound-loaded S-doped TiO2photocatalysts having a rutile phase under visible light[J]. Appl. Catal. A,2008,349:70-75.

