2,2′-联萘酚及其衍生物的合成研究进展
张 丽 郑土才* 牟忠岳 潘劲松
(1.衢州学院化学与材料工程学院,浙江 衢州 324000;2.浙江山峪染料化工有限公司,浙江 椒江 318000)
1,1′-联-2,2′-萘酚,简称联萘酚,英文缩写 BINOL,为白色结晶固体,溶于多种有机溶剂,结构式
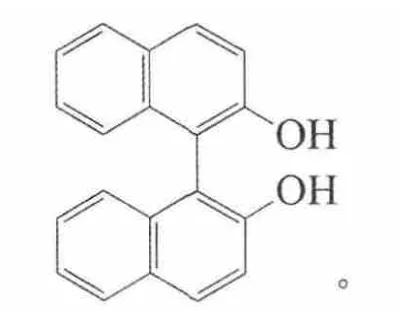
由于BINOL的2个对映异构体是含有2个相同联萘环的C2对称体,

因此其刚性结构和C2对称性在手性诱导中起到重要的作用,是一种优异的手性配体和手性辅助试剂,是目前手性合成特别是手性催化中出现最多的结构之一[1-3]。人们已经使用联萘酚合成出许多手性催化剂或金属催化剂的配体,并用于Diels-Alder反应、Aldol缩合、羰基化合物的烷基化、潜手性酮的还原、Michael加成和不对称环氧化等反应,展示了良好的催化活性和对映选择性,显示了广阔的应用前景[2-3]。
黄科林等曾对联萘酚的性质、联萘酚及其衍生物在不对称催化中的应用,及合成研究进展进行过综述[4-5]。刘焕梅等、陈丽等也对联萘酚类化合物的基本性能、应用以及国内外的合成方法进行了详细的综述[6-7]。
沙耀武等对联萘酚的合成方法,包括外消旋体的合成以及手性合成进行了详细的综述[8]。本文就近年来国内外在消旋联萘酚和手性联萘酚合成方面(但不包括消旋体的拆分[9]),以及在合成衍生物方面的研究作一综述。
1 消旋联萘酚的合成
金美红等研究了球磨机机械力化学作用下,2-萘酚经CuCl2·2H2O氧化偶联,无溶剂固态直接合成2,2′-联萘酚:
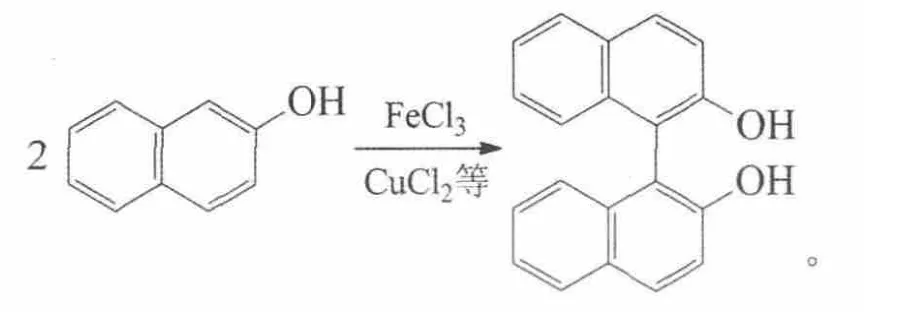
收率91%。优化反应条件为:球磨机转速350 r/min,CuCl2·2H2O与2-萘酚摩尔比2:1,碾磨时间2 h。还考察了其他Cu(II)/Fe(III)金属盐氧化剂作用下2-萘酚的氧化偶联[10]。
杜娟等研究了FeCl3催化和微波辐射下2-萘酚的氧化偶联反应,制得外消旋BINOL,反应时间为3 min,收率 39.8%[11]。
吕早生等研究了三氯化铁催化氧化偶联合成联萘酚,并分别采用了常规加热方法和微波诱导的方法,结果表明微波辐射法的反应时间缩短了一半,而收率却提高了10%[12]。
林敏等研究了以FeCl3·6H2O为氧化剂,水为溶剂,微波辐射合成BINOL,优化反应条件为:微波功率 495 W,辐射时间 40 s,n(β-萘酚):n(FeCl3)=1:2,收率91%。与常规加热方法相比,微波辐射法具有产率高、反应时间短、产物易分离和反应条件温和等优点[13]。
丁盈红等研究了FeCl3催化和微波辐射下,在水溶液中由2-萘酚制得外消旋BINOL,反应优化条件为:微波功率330 W,时间2 min,产率90%[14]。
翁文等使用CuCl-四甲基乙二胺络合物催化2-萘酚的氧化偶联,联萘酚收率达80%以上,并考察了金属盐种类、配体用量等对联萘酚产率的影响[15]。
王连增等以3-羟基-2-萘甲酸为原料,经微波(MW) 辐射和 FeCl3·6H2O 的氧化偶联制得 3,3′-二羧基-1,1′-联萘酚(收率 74.0%)[16]:

杨会来等以2-萘酚、2-萘胺为原料,CuCl2为催化剂,在苄胺(BzNH2)存在下偶联生成联萘酚胺(收率 65%)[17]。

2 手性联萘酚的合成
周超等制备了5种手性氨基酸与β-萘酚醛或水杨醛的氨基酸席夫碱及其手性席夫碱-Cu2+配合物,及D-氨基葡萄糖与β-萘酚醛或水杨醛的氨基葡萄糖手性席夫碱-VO2+配合物,并探索了这些配合物对联萘酚不对称合成反应的催化作用[18]。结果表明,L-氨基酸萘酚醛

(R=CHMe2、CH2CHMe2、CHMeC2H5、CH2Ph、CH2-3-吲哚,Me为甲基,Ph为苯基)的Cu(Ⅱ)配合物作催化剂,可得到最高收率81.7%,对映体过量 (ee)为28.4%。氨基葡萄糖-β-萘酚醛席夫碱-钒氧(Ⅱ)配合物
作催化剂时,得到的联萘酚的收率为87.5%,ee为60.3%。配合物中心离子(原子)的配位结构对产物的ee有较大影响。
秦川等报道以3个手性膦酰胺(Et为乙基)

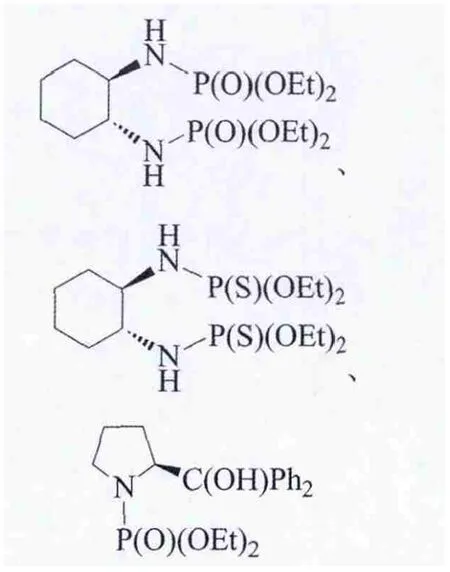
和CuCl组成的手性络合物为催化剂,通过2-萘酚直接氧化偶联得到(S)-BINOL:
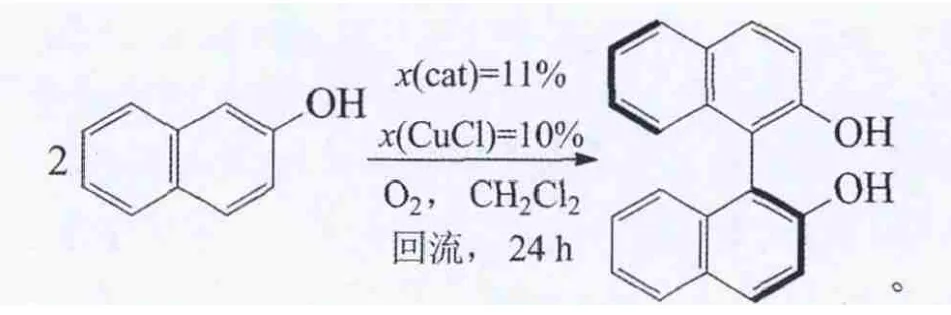
收率最高达59.0%,ee中等[19]。
翁文等研究了以D-葡萄糖缩二丙酮、D-甘露醇缩二丙酮和胆固醇3种含羟基的手性化合物构筑不对称环境,FeCl3作氧化剂,固相不对称合成联萘酚,产率最高91.5%,ee最高14.6%[20]。
王秀珍等以(+)-苯丙胺和CuCl2·2H2O形成的配合物为手性催化剂,3-羟基-2-萘甲酸甲酯和2,7-萘二酚进行偶联得到对映体过量的联萘酚衍生物2,2′,7′-三羟基-1,1′-联萘-3-甲酸甲酯:

收率21.6%,ee77.8%[21]。
3 由联萘酚制备联萘酚衍生物
安众福等详细综述了联萘酚衍生物的光电功能及其应用[22]。
3.1 联萘酚衍生的磷酸、磷酰胺、亚磷酸酯等类配体
Terada综述了手性联萘酚衍生的手性单磷酸

(R=H、C6H5、4-PhC6H4、4-MeC6H4、4-CF3C6H4、4-t-BuC6H4、4-(2-萘)C6H4、9-蒽、2-萘、3,5-双(2,4,6-三甲基苯基)苯基、3,5-二苯、苯基、2,4,6-i-Pr3C6H2、3,5-t-Bu2C6H3、2,4,6-Me3C6H2,t-Bu 为叔丁 基 ,i-Pr为异丙基)作为手性布朗斯特酸催化剂在有机反应,特别是对映选择性C—C键形成反应中的应用[23]。
杨磊等以手性联萘酚为原料,合成了一系列手性磷酸催化剂
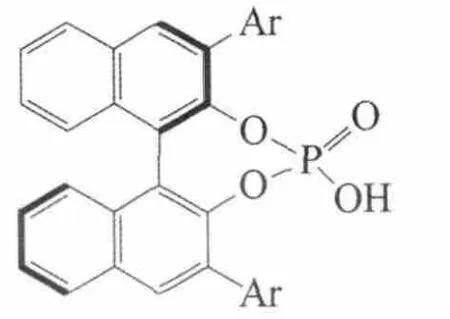
(Ar=C6H5、2,4,6-i-Pr3C6H2、3,5-(CF3)2C6H3、SiPh3、4-(2-萘)C6H4、9-蒽、9-菲基、1-萘、2-萘)并将其应用于催化芳香胺和硝基烯烃的不对称氮杂Michael加成反应中,产物β-硝基胺的产率和对映选择性分别达 65%~95%和 16%~70%[24]。
Momiyama等报道了由3,3′-二(2-羟基-3-芳基苯基)联萘酚衍生的手性双磷酸催化剂
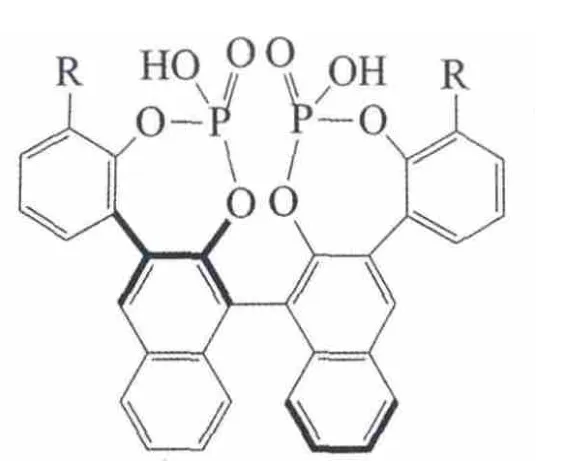
(R=C6H5、4-MeC6H4、2,4,6-i-Pr3C6H2、3,5-Me2C6H3、2,6-Me2C6H3), 及其在 α,β-不饱和醛与酰胺基丁二烯对映选择性Diels-Alder反应中的应用。通过优化催化剂的取代基,及丁二烯的酰胺取代基,获得了优异的对映选择性(ee=95%~99%)和广泛的底物适用性,效果明显优于单磷酸[25]。
He等报道了基于联萘酚的另一种结构的手性双磷酸催化剂
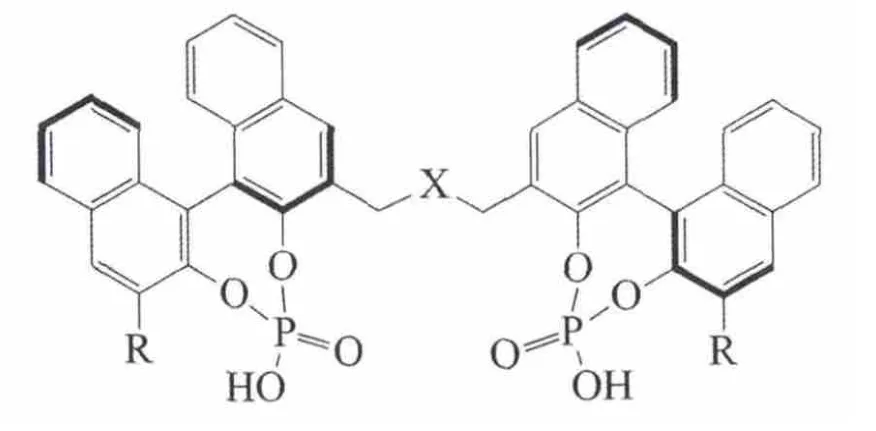
(R=H、X=O、S、SO2、CH2、NAc、R=Ph),并研究了其在甲亚胺叶立德与缺电子烯烃的对映选择性1,3-偶极环加成反应中的应用。结果显示了广泛的底物适用性,甲亚胺可由各种醛与α-氨基酯组成[26]。
苟绍华等在α-紫罗兰酮的催化合成中,以消旋联萘酚为原料,经与三氯氧磷、三乙胺(N3Et)、二氯甲烷等反应制得联萘酚磷酸催化剂(消旋,收率94%)[27]:

Lee等报道了基于联萘酚的手性N-三氟甲磺酰基磷酰胺
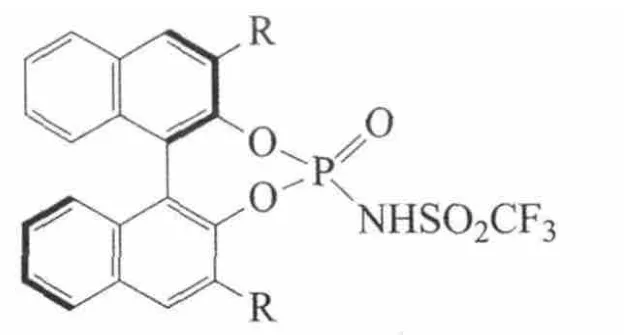
(R=4-PhC6H4、SiPh3、9-蒽,、2-萘 、2,4,6-i-Pr3C6H2、3,5-(CF3)2C6H3),并研究了在自由基与亚胺的对映选择性加成中的应用。产物具有较好的对映选择性(ee=73%~84%),而且不受亚胺苯基或自由基前体电子性质的影响[28]。
Pignataro等报道联萘酚衍生的亚磷酸酯

(R′=H,R=C6H5、CHMe2、C6H11;R′=Me,R=CHMe2)与C1对称亚膦胺组合产生混合配体Rh和Pd催化剂,并试用于Rh催化的加氢和Pd催化的烯丙位取代反应[29]。
万博等以联萘酚和大位阻的金刚烷酰氯为原料,经2步反应合成了系列新型手性单齿亚磷酸酯配体(DMAP为4-二甲氨基吡啶):
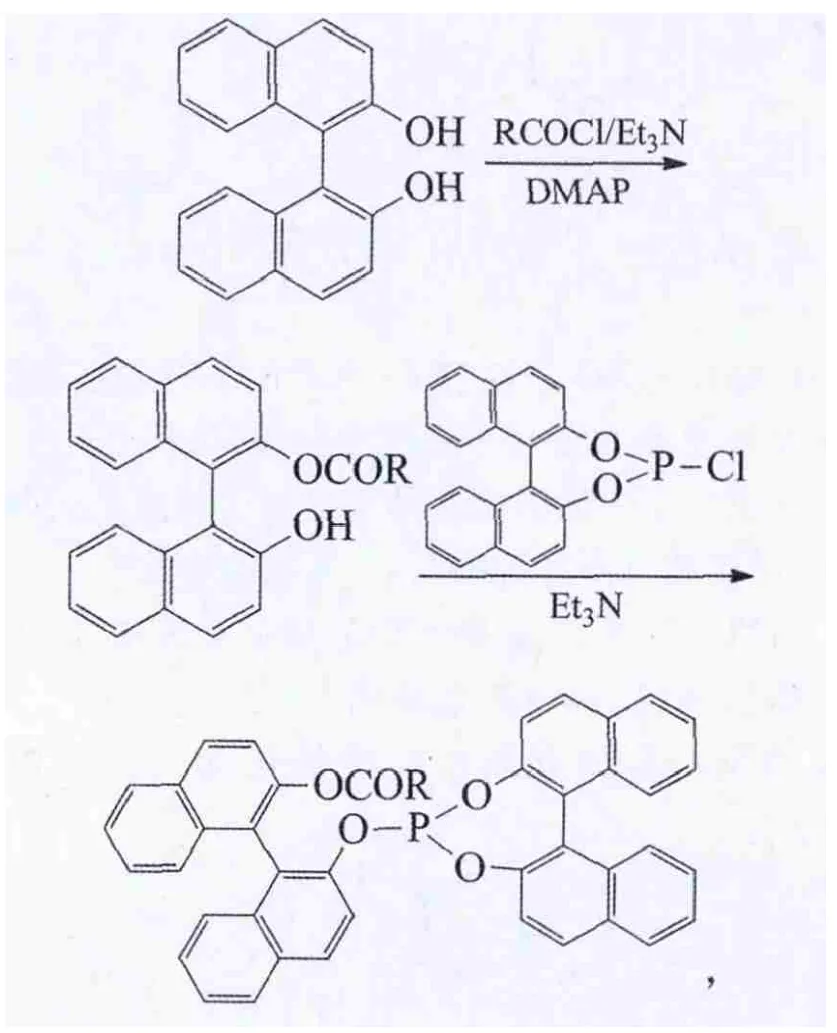
Wilting等报道了基于联萘酚的手性双亚磷酸酯配体

3.2 联萘酚衍生的醚及其OH被取代的化合物
Saad等将手性联萘酚引入到四硫富瓦烯(TCNQF4)中,制备了具有轴手性的四硫富瓦烯衍生物

并制备了与TCNQF4形成的电荷转移盐[32]。
Liu等将手性联萘酚经醚化连接到氨基糖上(DEAD为二硫代氨基甲酸二乙胺,TMSOTf为三氟甲磺酸三甲基硅酯,DMF为N,N-二甲基甲酰胺,PPh3为三苯基膦,Fmoc为9-芴甲氧羰基,Ac为乙酰基):并发现它们具有DNA凸出(bulge)部分结构成键选择性及中等的亲合力[33]。
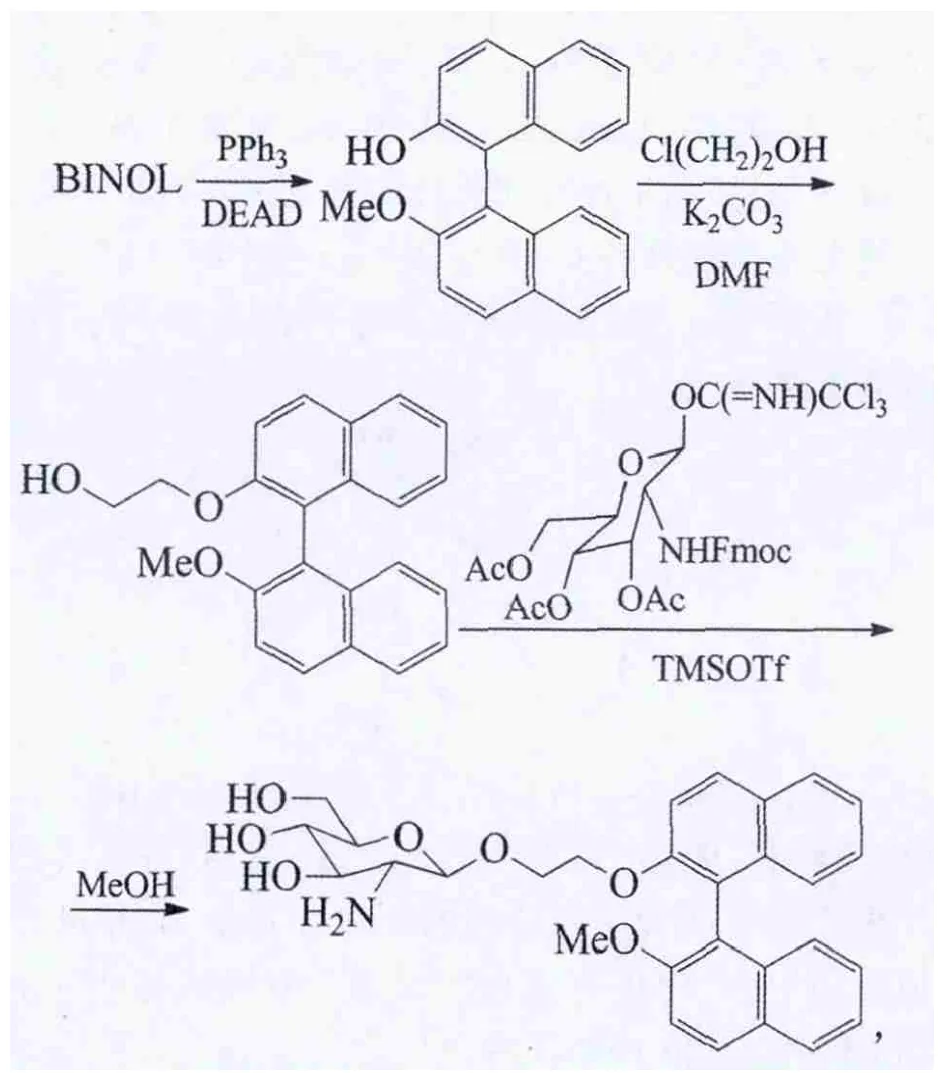
焦书燕等以(R)-联萘酚(或(S)-联萘酚)、2,2′-联苯酚、间苯二酚、三聚氯氰为原料合成了6个手性冠醚[34]:

(R)-原料所得产物收率分别为33%、28%和27%,(S)-原料分别为38%、25%和24%。
刘国庆等通过硅烷偶联剂将手性联萘酚键合到球形硅胶上制得手性固定相[35]:
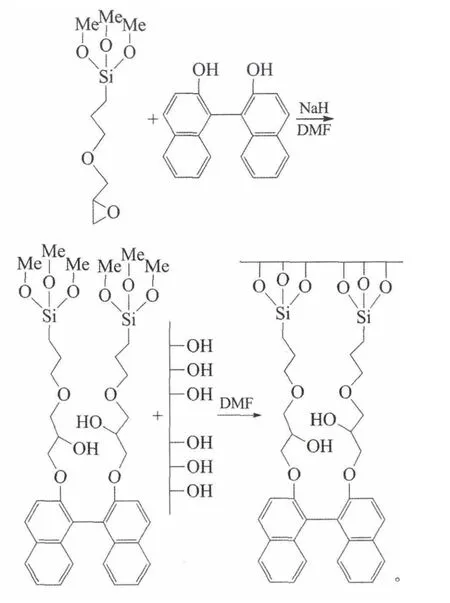
填装后考察其在7个联萘化合物手性拆分中的应用,表明对联萘酚和溴代联萘酚具有较好的手性识别能力。
尹丽华等报道手性联萘酚通过3步反应合成了手性联萘二甲酸(Tf2O为三氟甲磺酸酐,DPPP为1,3-二(二苯基膦基)丙烷):

总收率62%,产品ee大于99%[36]。
封科军等以外消旋联萘酚为原料,通过酚羟基的酯化、磺酸酐与格氏试剂的偶联、甲基的溴化、二溴甲基的水解和Wittig反应等步骤合成了2,2′-二乙炔基-1,1′-联萘 (Py为吡啶,NBS为N-溴代丁二酰亚胺,BPO为过氧化苯甲酰):

收率分别为99%、96%、83%、98%和69%[37]。
魏青等以手性联萘酚为原料,合成了手性加氢催化剂 BINAP的 Ru(Ⅱ)配合物(Merck路线:Ph2PH,质量分数 10%的 NiCl2-dppe,DMF,DABCO;2:Monsanto 路 线 ,Ph2PCl,NiCl2-dppe,Zn,DMF。 dppe 为1,2-二(二苯基膦基)乙烷,DABCO为三亚乙基二胺):

并比较了2条路线[38]。
3.3 联萘酚3-甲酰化和3,3′-双甲酰化产物及其衍生物
Xiong等以手性联萘酚为原料,经单醚化、甲氧甲基(MOM)保护、正丁基锂/DMF甲酰化、脱MOM保护、与环己二胺缩合、还原得到salan配体(R为甲基或苄基),或按文献方法得到salalen配体(R为甲基):


并将其与Ti(IV)的配合物用于烯烃与质量分数50%过氧化氢的不对称环氧化[39]。
Jiang等以3-甲酰基联萘酚为原料,经还原胺化制得仲胺配体
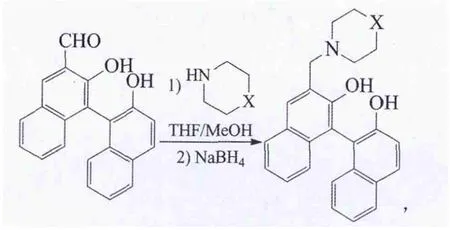
收率分别为 96%(X为 O)和 92%(X为 CH2),或与盐酸羟胺或2-氨基吡啶缩合制得肟或席夫碱配体
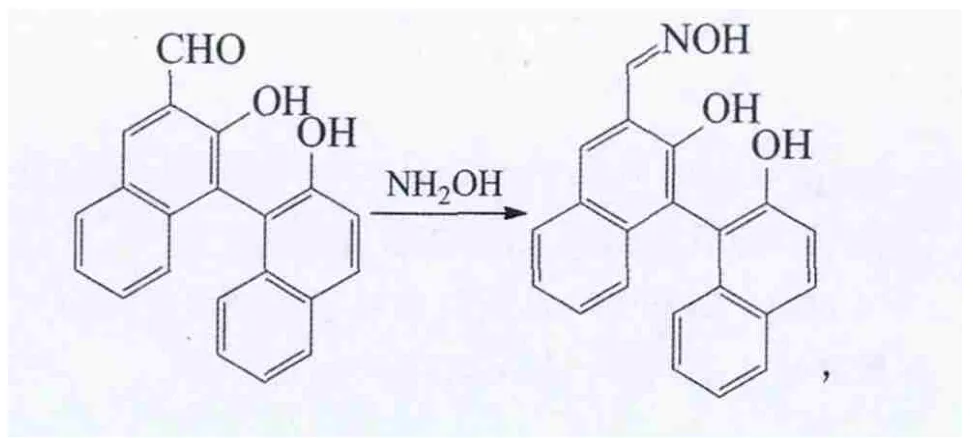

收率分别为85%(肟)和70%(席夫碱),并用于催化二乙基锌与醛的不对称加成[40]。
Tang等以3-甲酰基联萘酚为原料,经还原、保护、醚化、脱保护、氧化制得手性配体(p-TsOH为对甲苯磺酸,PCC为氯铬酸吡啶鎓盐):
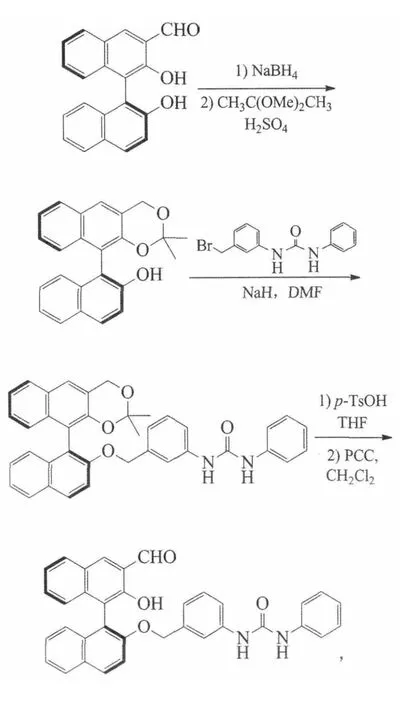
收率分别为97%、83%、95%、91%和91%,产物能够荧光识别L-色氨酸[41]。
Jung等报道了八氢化联萘酚衍生的配体(Boc为叔丁氧羰基):

及其对邻氨基醇的对映选择性识别和L-氨基酸向D-氨基酸的手性转化[42]。
王世高等从手性联萘酚出发,经MOM保护、甲酰化、脱保护及选择性酯化4步反应合成了水杨醛类结构的中间体,再与(1S,2R)-(+)-2-氨基-1,2-二苯基乙醇反应合成了1种新型手性席夫碱,最后经NaBH4还原制得其类似物:


收率分别为 91.5%、40%、41%、43%、80%和 82%[43]。
刘冰等合成了化合物rac-3-[(1H-1,2,4-三唑-1-基)甲基]-1,1′-联萘酚三唑:
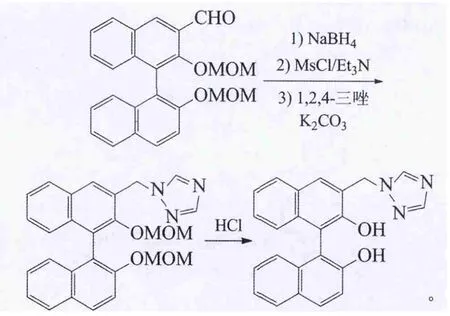
还原、甲磺酰化和三唑化反应的总收率57%,脱保护收率90%[44]。
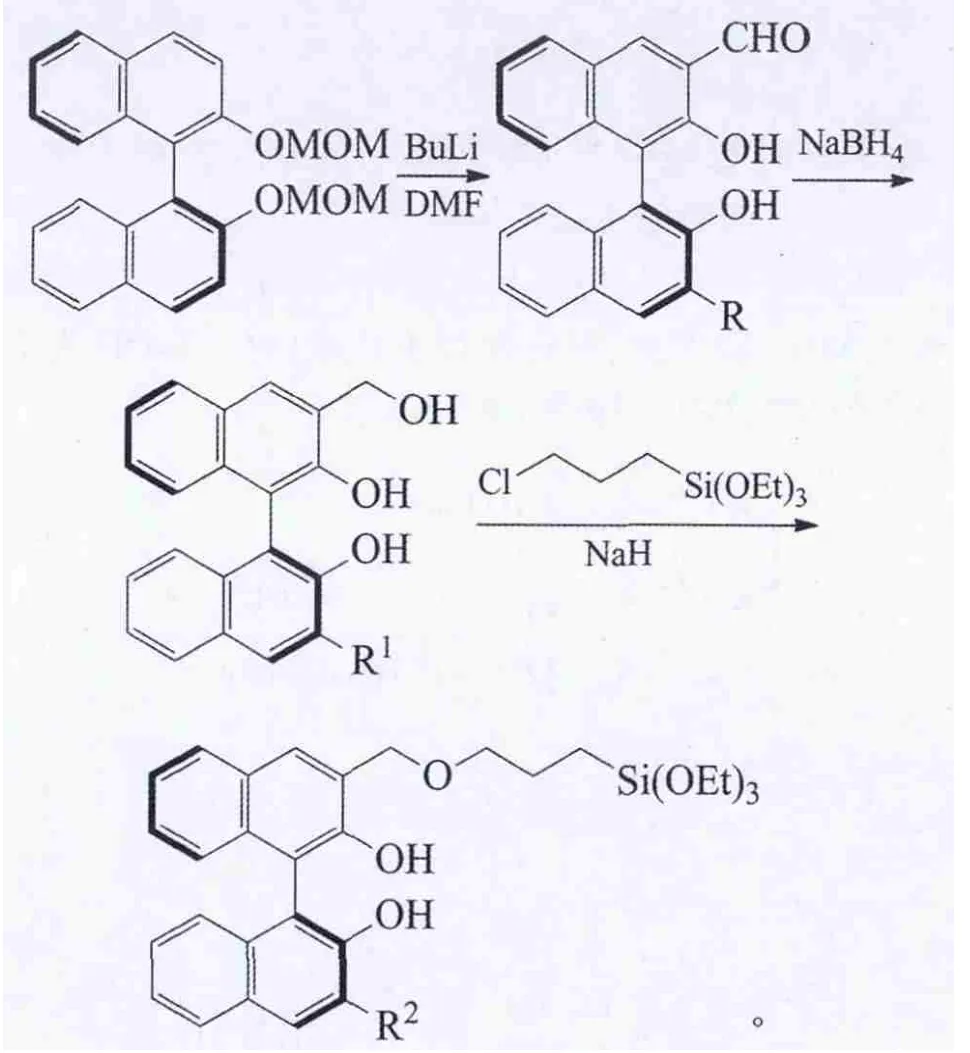
王晓梅等报道(S)-2,2′-二甲氧基甲氧基-1,1′-联萘经3位和3,3′位的甲酰化、硼氢化钠还原以及与氯丙基三乙氧基硅烷发生Williamson成醚反应,得到 3位、3,3′位的单取代(R=R1=R2=H)和双取代(R=CHO,R1=CH2OH,R2=CH2O(CH2)3Si(OEt)3)硅氧烷衍生物[45]:
Tang等以MOM保护的3,3′-二甲酰基联萘酚为原料,与氨基硫脲缩合得到相应的缩氨硫脲配体:
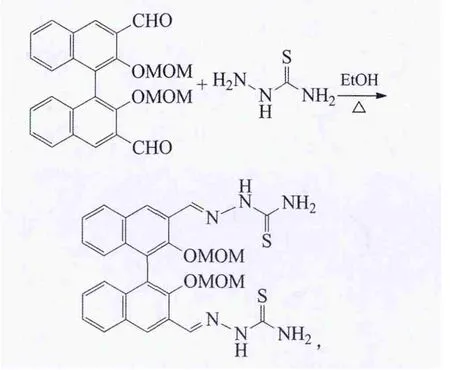
收率80%。产物能通过吸收光谱和荧光变化识别氟离子[46]。
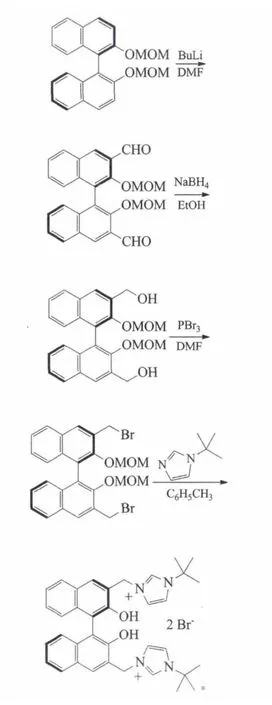
陈景超等以R-联萘酚为原料,经手性卤代烃中间体合成了手性咪唑鎓盐:
在碱性条件下这种盐可转化为咪唑卡宾配体[47]。
焦书燕等以N1-氨基丁基-N1,N4-二叔丁氧羰基-1,4-丁二胺和手性甲酰基联萘酚为原料,经NaBH4还原胺化、脱保护制得手性联萘酚的多胺缀合物[48]:


其中手性联萘酚经MOM保护、甲酰化、脱保护3步反应制备3,3′-双甲酰联萘酚的收率分别为98%、75%和60.4%。
3.4 联萘酚烃基化及羧化产物
Zou等以手性联萘酚等为原料,分别经多步反应合成了3种手性单体,二溴代物、二硼酸物和二端基炔,最后合成了2种含联萘酚和联萘基的可溶性聚合物[49]:
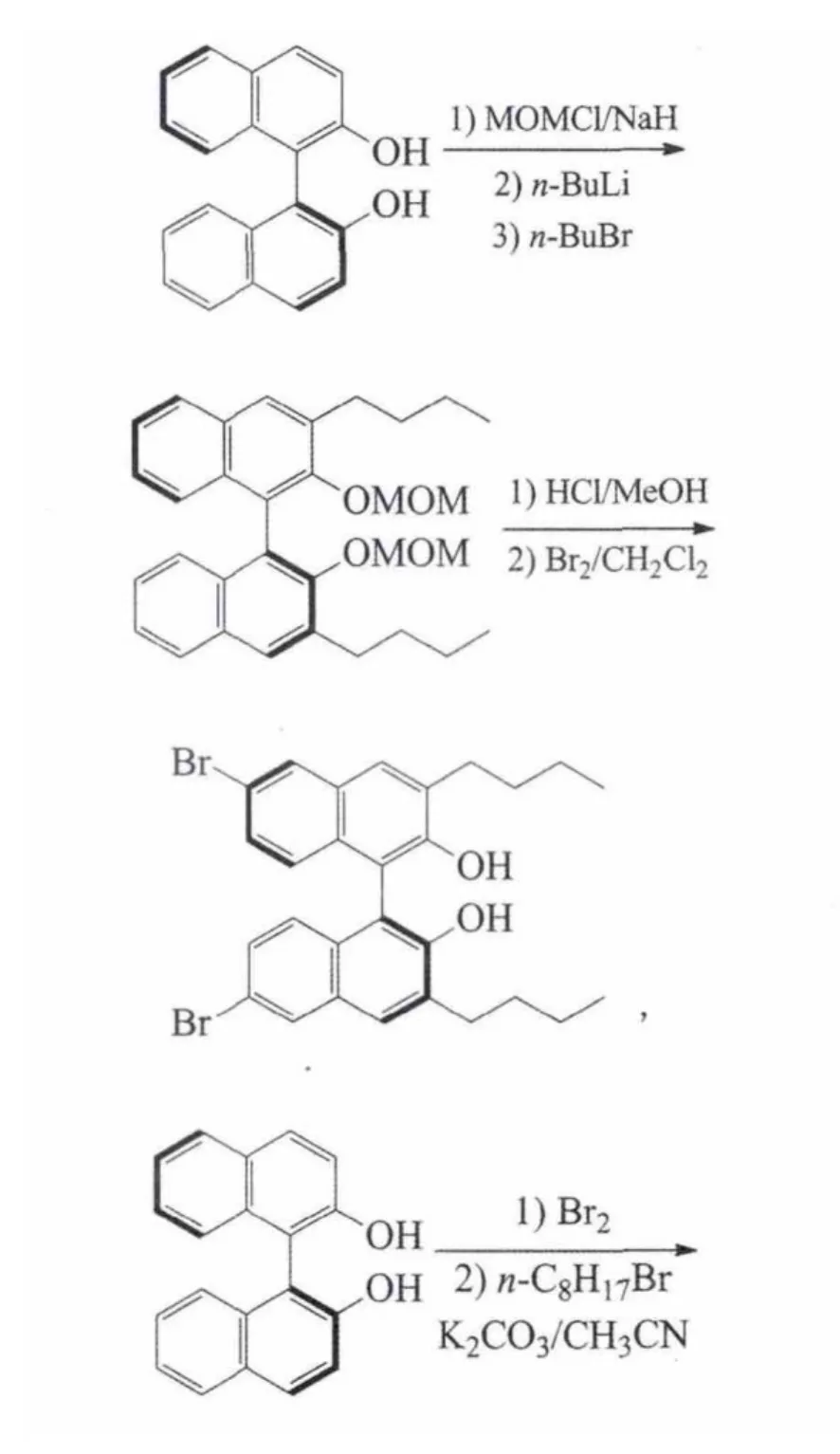
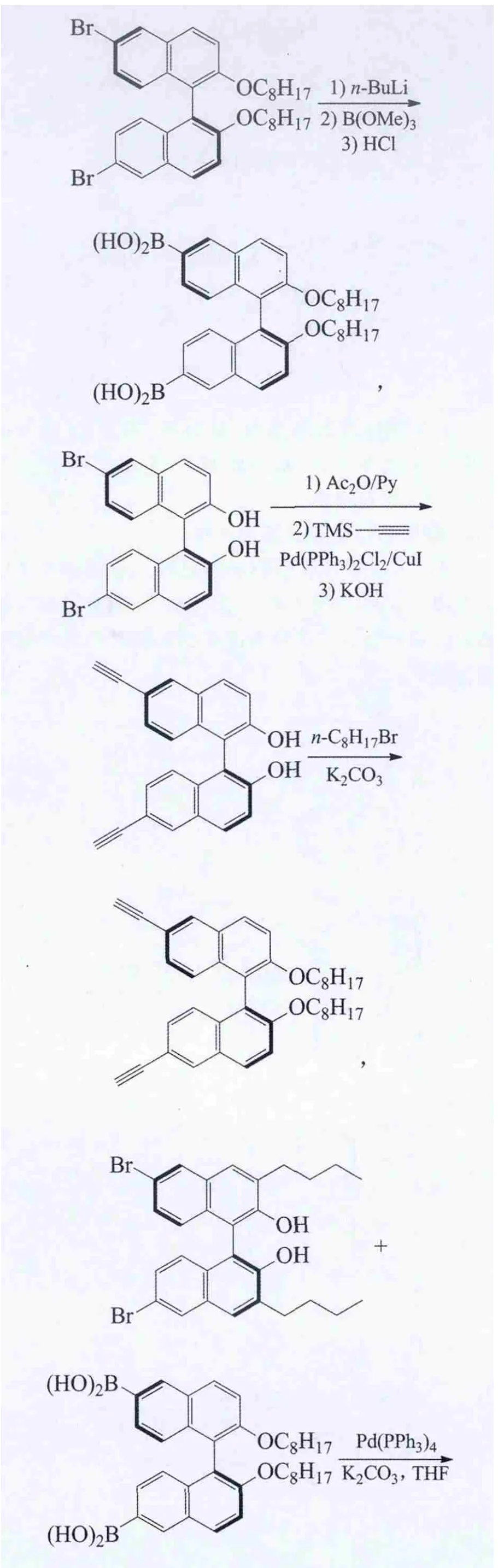

Belokon等以手性联萘酚为原料,按文献方法合成了3,3′-双(二苯基羟基甲基)联萘酚:

并研究了其锂盐作为多功能配体在不对称Michael加成中的应用[50]。
蒋胜前等以手性联萘酚为原料,经MOM保护、丁基锂(BuLi)处理后羧化、脱保护3步反应合成了(R)-3,3′-二羧酸联萘酚(i-PrOH为异丙醇):
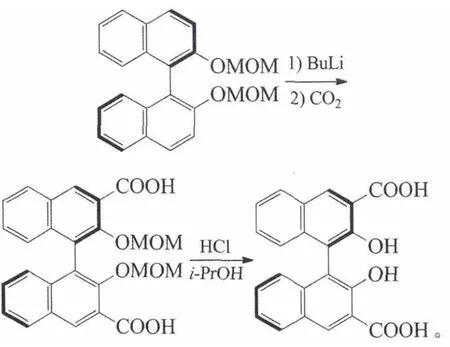
保护收率90%,后2步总收率75.7%[51]。
3.5 联萘酚卤代等产物及其衍生物
王俊等报道联萘酚经溴化、醚化合成了6,6′-二溴-2,2′-二己氧基联萘(收率 94.7%)[52]:

成义祥等以(R)-6,6′-二溴-2,2′-二甲氧甲氧基联萘与乙烯基三乙氧基硅烷经钯催化的Heck偶联反应制得前体分子:


再通过溶胶-凝胶法制得杂化硅干凝胶[53]。
蔡万玲等报道(R)-3,3′-二乙炔基-6,6′-二正丁基联萘酚与对苯二叠氮通过点击化学制得能有效识别Hg2+的荧光化学传感器的手性联萘酚高分子[54]:
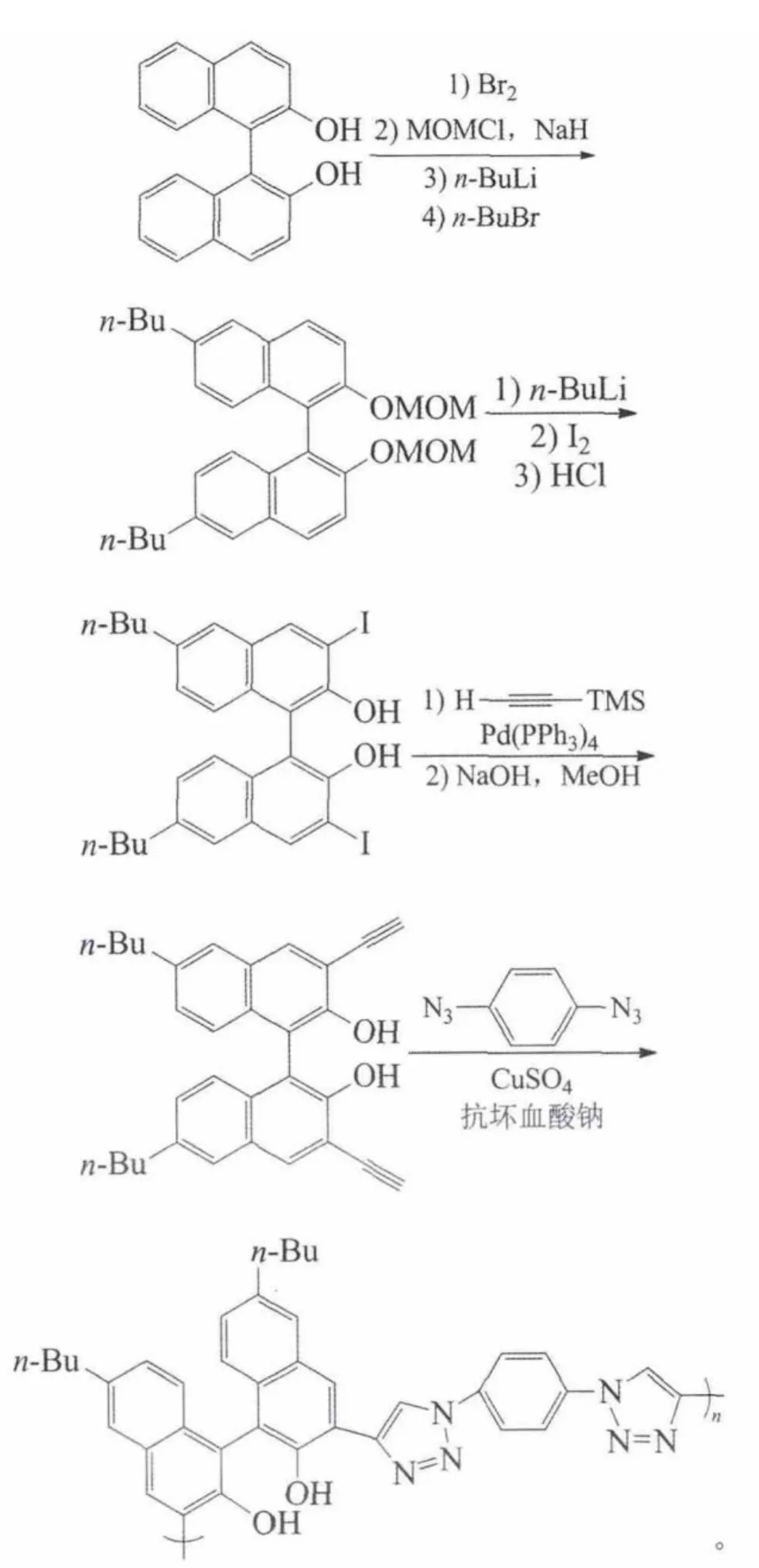
其中,手性联萘酚经溴素溴化、MOM保护和正丁基锂作用下的丁基化制得(R)-6,6′-二正丁基联萘酚二甲氧基甲醚,3步收率分别为97%、95%和76%;再经正丁基锂/THF处理后碘化、水解得到3,3′-二碘衍生物,收率51%;在钯催化剂和碘化亚铜作用下与三甲基硅基乙炔偶联得到3,3′-二乙炔基衍生物,收率80%。最后与对苯二叠氮的聚合在抗坏血酸钠和硫酸铜存在下进行,收率82%。
王晓梅等以双MOM保护的手性联萘酚为原料,经6位和6,6'位的单溴代和双溴代反应,再经正丁基锂/DMF的甲酰化、硼氢化钠还原以及与3-氯丙基三乙氧基硅烷的醚化反应,得到6位单取代和6,6′位双取代硅氧烷衍生物[45]。其中双醚化产物的合成如下:

余虹等报道联萘酚经6,6′位溴化、酚的甲基化、正丁基锂作用下的6,6′位硼酸化、氯化亚铜催化下的咪唑化得到咪唑化衍生物。其中单咪唑化产物再与对二溴苄反应形成联二萘酚咪唑鎓盐二聚体(X=Br-、I-、BF4-):

其中,碳酸钾、碘甲烷、丙酮中甲基化收率92%;正丁基锂/THF中与硼酸三甲酯作用,然后盐酸水解制得单和双硼酸,咪唑化3步总收率43%;与对二溴苄反应及离子交换收率20%[55]。
4 结束语
联萘酚具有良好的刚性结构和C2对称性,其合成较为容易,还可通过醚化、羟基取代、酯化、甲酰化、羧化、烃化、卤化、硝化等反应合成多种衍生物。这些化合物可能作为手性催化剂、手性配体、手性辅助试剂、手性分子识别受体、手性高分子材料单体、手性固定相等,具有广阔的应用前景。
联萘酚及其衍生物是目前研究报道最多的手性结构之一,作为催化剂、配体、辅助剂等已应用于多种不对称有机反应中,并取得了良好的催化活性和对映选择性。国内研究尚较多集中在消旋联萘酚的合成中,对联萘酚及其衍生物的应用也有所报道,但与国外研究相比,有关手性联萘酚及其衍生物的合成,以及在手性催化剂、手性配体、手性分子识别、手性固定相等方面的应用研究明显欠缺。希望通过对手性联萘酚及其丰富衍生化学的了解,推动国内相关研究,推进联萘酚及其衍生物的工业化。
[1]胡跃飞.现代有机合成试剂4:配体和手性辅助试剂[M].北京:化学工业出版社,2011:97-102.
[2]林国强,李月明,陈耀全,等.手性合成:不对称反应及其应用[M].4版.北京:科学出版社,2010.
[3]Leo A Paquette.不对称合成中的手性试剂[M].侯雪龙,吴喆,译.上海:华东理工大学出版社,2006:86-97.
[4]黄科林,黄春林,吴睿,等.β,β′-联萘酚的性质及应用[J].企业科技与发展,2010(4):16-20.
[5]黄科林,黄春林,彭小玉,等.β,β′-联萘酚的合成研究进展[J].企业科技与发展,2010(2):1-6.
[6]刘焕梅,王红,尚晓娴,等.1,1′-联二萘酚化合物的合成研究新进展[J].化学工程师,2009,23(9):33-36.
[7]陈丽,辛莹,陈风雷,等.1,1′-联-2-萘酚的合成新进展[J].广州化学,2007,32(3):59-64.
[8]沙耀武,陈瑞.2,2′-二羟基-1,1′-联萘合成方法综述[J].精细化工,2001,18(6):360-363.
[9]戴日强,黄春林.1,1′-联-2-萘酚的拆分进展[J].化工技术与开发,2007,36(6):24-29.
[10]金美红,宋国伟,王亮,等.球磨机中无溶剂高效合成1,1′-联二萘酚[J].现代化工,2011,31(6):35-37.
[11]杜娟,宋丽娜.微波辐射固相合成外消旋β,β′-联萘酚的研究[J].吉林师范大学学报:自然科学版,2005,26(1):52-53.
[12]吕早生,王俊,王晴东.β,β′-联萘酚的合成与拆分[J].化学与生物工程,2005,22(11):26-28.
[13]林敏,周金梅,杨瑞锋,等.微波水相法合成外消旋1,1′-联-2-萘酚[J].厦门大学学报:自然科学版,2005,44(1):139-141.
[14]丁盈红,廖九忠,张广文,等.微波辐射应用于 β,β′-联萘酚的合成与拆分[J].化学世界,2004(8):430-432,406.
[15]翁文,朱津,李赛清,等.过渡金属络合物催化合成联萘酚[J].应用化工,2004,33(5):19-20.
[16]王连增,李立军,王艳蕊,等.3,3′-二羧基-1,1′-联萘酚的合成、拆分及其配合物的合成[J].广东化工,2012,39(4):279-280.
[17]杨会来.联萘酚胺的合成及拆分研究[J].杭州化工,2006,36(4):12-14.
[18]周超,陆维敏,夏云超.手性席夫碱-铜(Ⅱ)与-钒氧(Ⅱ)配合物的合成及其在不对称氧化反应中的应用[J].应用化学,2005,22(2):142-147.
[19]秦川,刘敏,宋兰坤,等.新的手性配体促进的二芳基二酸和联萘酚的不对称合成[J].有机化学,2002,22(12):1013-1017.
[20]翁文,姚碧霞,陈武安,等.手性醇诱导下联萘酚的固相不对称合成[J].应用化工,2003,32(6):12-13,16.
[21]王秀珍,许遵乐.手性联萘酚衍生物的不对称合成及其对映体含量测定[J].化学研究,2007,18(3):21-23.
[22]安众福,陈润锋,史慧芳,等.联萘酚衍生物的光电功能及其应用[J].化学进展,2010,22(10):1973-1982.
[23]Terada M.Binaphthol-derived phosphoric acid as a versatile catalyst for enantioselective carbon-carbon bond forming reactions[J].Chem Commun,2008,44:4097-4112.
[24]杨磊,夏春谷,黄汉民.手性磷酸催化芳香胺与硝基烯烃的不对称加成反应[J].催化学报,2011,32(10):1573-1576.
[25]Momiyama N,Konno T,Furiya,Y,et al.Design of chiral bis-phosphoric acid catalyst derived from(R)-3,3′-di(2-hydroxy-3-arylphenyl)binaphthol:catalytic enantioselective Diels-Alder reaction of α,β -unsaturated aldehydes with amidodienes[J].J Am Chem Soc,2011,133:19294-19297.
[26]He L,Chen X-H,Wang D-N,et al.Binaphthol-derived bisphospho-ric acids serve as efficient organocatalysts for highly enantio-selective 1,3-dipolar cycloaddition of azomethine ylides to electron-deficient olefins[J].J Am Chem Soc,2011,133:13504-13518.
[27]苟绍华,彭汝芳.基于联萘酚的有机Bronsted酸高选择性催化合成α-紫罗兰酮[J].化学研究与应用,2008,20(9):1150-1153.
[28]Lee S,Kim S.Enantioselective radical addition reactions to imines using binaphthol-derived chiral N-triflyl phosphoramides[J].Tetrahedron Lett,2009,50:3345-3348.
[29]Pignataro L,Lynikaite B,Colombo R,et al.Combination of a binaphthol-derived phosphite and a C1-symmetric phosphinamine generates heteroleptic catalysts in Rh-and Pd-mediated reactions[J].Chem Commun.2009,45:3539-3541.
[30]万博,赵庆鲁,王来来.新型手性膦配体的合成及其在1,4-共轭加成反应中的应用[J].催化学报,2010,31(5):514-517.
[31]Wilting J,Janssen M,Muller C,et al.Binaphthol-based diphosphite ligands in asymmetric nickel-catalyzed hydrocyanation of styrene and 1,3-cyclohexadiene:influence of steric properties[J].Adv Synth Catal,2007,349:350-356.
[32]Saad A,Jeannin O,Fourmigue M.A binaphthol-substituted tetrathiafulvalene with axial chirality and its enantiopure TCNQF4charge-transfer salts[J].New J Chem,2011,35:1004-1010.
[33]Liu L,Yi L,Yang X,et al.Synthesis and spectroscopic characterization of binaphthol aminosugars for stimulation of DNA strand slippage synthesis[J].Tetrahedron,2008,64:5885-5890.
[34]Xiong D,Wu M,Wang S,et al.Synthesis of salan(salalen)ligands derived from binaphthol for titanium-catalyzed asymmetric epoxidation of olefins with aqueous H2O2[J].Tetrahedron:Asymmetry,2010,21:374-378.
[35]Jiang F-Y,Liu B,Dong Z-B,et al.Titanium(IV)as an essential promoter in the asymmetric addition of diethylzinc to aldehydes catalyzed by aminonaphthol and imme ligands based on 3-substituted binaphthol[J].J Organomet Chem,2007,692:4377-4380.
[36]Tang L,Wang N,Guo J.Colorimetric and Fluorescent RecognitionofFluoridebyaBinaphtholThioureidoDerivative[J].Bull Korean Chem Soc,2012,33:2145-2148.
[37]Tang L,Wei G,Nandhakumar R,et al.Facile Synthesis of the Uryl Pendant Binaphthol Aldehyde and Its Selective Fluorescent Recognition of Tryptophan[J].Bull Korean Chem Soc,2011,32:3367-3371.
[38]Belokon Y N,Gugkaeva Z T,Maleev V I,et al.Four hydroxyls are better than two.the use of a chiral lithium salt of 3,3′-bis-methanol-2,2′-binaphthol as a multifunctional catalyst of enantioselective Michael addition reactions[J].Tetrahedron:Asymmetry,2011,22:167-172.
[39]Jung H,Nandhakumar R,Yoon H-J,et al.Synthesis of novel H8-binaphthol-based chiral receptors and their applications in enantio-selective recognition of 1,2-amino alcohols and chirality conversion of L-amino acids to D-amino acids[J].Bull Korean Chem Soc,2010,31:1289-1294.
[40]Zou X,Zhang S,Cheng Y,et al.Synthesis and enantioselectivities of soluble polymers incorporating optically active binaphthyl and binaphthol[J].J Appl Polym Sci,2007,106:821-827.
[41]尹丽华,钟石,陈林,等.制备手性联萘二甲酸的工艺改进[J].化学试剂,2012,34(3):277-279.
[42]封科军,邵光.2,2′-二乙炔基-1,1′-联萘分子的合成[J].惠州学院学报:自然科学版,2012,32(3):47-49.
[43]魏青,陈波,刘秋香,等.BINAP-Ruthenium(II)催化剂的合成研究[J].浙江冶金,2010(1):39-41.
[44]焦书燕,姚文涌,谢恩,等.基于联萘酚的手性冠醚的合成及其晶体结构[J].化学研究,2011,22(6):1-4.
[45]刘国庆,詹峰萍,林爱清,等.联萘酚键合手性固定相的合成与应用[J].应用化工,2011,40(3):402-403,407.
[46]王世高,郭培江,孙晓菲,等.新型手性Schiff碱的合成[J].合成化学,2011,19(1):56-58.
[47]刘冰.3-[(1H-1,2,4-三唑-1-基)甲基]-1,1′-联萘酚的合成及晶体结构[J].化学研究,2010,21(1):52-55.
[48]王晓梅,韩鹏,邱雪鹏,等.新型手性联萘酚硅氧烷衍生物的合成与表征[J].应用化学,2009,26(1):42-46.
[49]陈景超,任周阳,刘颖玲,等.2个手性咪唑配体的合成[J].云南大学学报:自然科学版,2012,34(1):66-71.
[50]焦书燕,马金飞,杨丽,等.手性联萘酚的多胺缀合物的合成与表征[J].化学研究,2010,21(4):52-54,57.
[51]蒋胜前,王周玉,蒋珍菊,等.(R)-3,3′-二羧酸-1,1′联萘酚的合成[J].西华大学学报:自然科学版,2011,30(2):99-101.
[52]王俊,李俊,秦金贵.简法合成 6,6′-二溴-2,2′-二烷氧基-1,1′-联萘[J].化学试剂,2004,26(4):245.
[53]余虹,赵元聪,余孝其.联二萘酚咪唑鎓盐二聚体的合成[J].化学研究与应用,2006,18(10):1235-1237.
[54]陈泳,王秀珍,庞冀燕,等.6-硝基-1,1′-联-2-萘酚的合成及仿生氧化反应[J].中山大学学报:自然科学版,2007,46(2):45-48.
[55]蔡万玲,库肯·比哈利,刘晓虎,等.基于手性联萘酚高分子对汞离子的荧光传感器[J].无机化学学报,2010,26(7):1147-1152.

