两种气氛预氧化后裂解炉管合金的结焦和碳化行为
王申祥,王国清,王红霞,郏景省,崔立山
(1. 中国石油大学(北京) 理学院,北京 102249;2. 中国石化 北京化工研究院,北京 100013)
两种气氛预氧化后裂解炉管合金的结焦和碳化行为
王申祥1,2,王国清2,王红霞2,郏景省2,崔立山1
(1. 中国石油大学(北京) 理学院,北京 102249;2. 中国石化 北京化工研究院,北京 100013)
研究了裂解炉管用HP40合金在H2-H2O及空气-H2O气氛中预氧化后的表面形貌、元素分布及相组成,并在98%(φ)N2-2%(φ)C2H6和98%(φ)H2-2%(φ)CH4气氛中研究了预氧化合金的结焦和碳化行为。实验结果表明,HP40合金在H2-H2O中形成的氧化膜由致密的笼型球团状MnCr2O4尖晶石组成;而在空气-H2O中形成的氧化膜发生剥落,且Fe和Ni元素在剥落处富集,未剥落的氧化膜由八面体MnCr2O4尖晶石及Cr1.3Fe0.7O3氧化物组成。经H2-H2O预氧化的合金结焦后表面存在少量不连续的絮状焦炭,而经空气-H2O预氧化的合金结焦后表面覆盖了大量丝状焦炭,前者的结焦量占后者的17%。经H2-H2O预氧化的合金的氧化膜碳化后仍为致密的MnCr2O4尖晶石;而经空气-H2O预氧化的合金的氧化膜转化成由(Cr,Fe)7C3和Fe3C组成的碳化物膜。
裂解炉管;乙烯;HP40合金;预氧化;结焦;碳化
石油烃高温裂解生产低碳烯烃时,焦炭会在管式裂解炉辐射段炉管的内表面沉积,增大炉管传热阻力,升高炉管外表面温度,同时减小炉管内径,增大炉管内流体压降,甚至造成炉管堵塞,影响裂解装置的正常运行。烃类热裂解结焦的机理分为3种:催化结焦、缩合结焦及自由基结焦[1-3]。催化结焦由裂解炉管合金中的Fe和Ni等催化活性元素造成,主要发生在裂解炉运行初期,对缩合结焦和自由基结焦起桥梁作用;而后两种结焦主要与裂解原料本身有关,与炉管合金材质无关[4]。由此可见,催化结焦是烃类热裂解结焦的基础,而降低炉管表面Fe和Ni元素的含量是抑制结焦的关键。自20世纪80年代,人们开始研究采用表面涂层技术抑制结焦[5]。但在高温、高碳势、强冲刷的裂解工况下,涂层的寿命仍达不到长期使用的要求。对裂解炉管内表面进行预氧化是一种成本低、操作简单的抑制催化结焦的方法,其原理是在一定的氧化气氛下,在炉管Fe-Cr-Ni合金表面生成一层氧化物薄膜,该薄膜的阳离子均来自炉管基体,与基体的结合力高,具备相当的防结焦、抗渗碳能力。该方法现已得到广泛应用,在工业生产中,新裂解炉管在服役前均需经过空气-H2O混和气预氧化。近年来,Nova公司发明了一种新的预氧化方法[6-8],能大幅延长裂解炉的生产周期,该方法是在H2-H2O混合气中进行预氧化。尽管预氧化技术已在工业裂解炉管中得到应用,但对预氧化后合金的结焦和碳化行为并没有进行深入研究。
本工作以常用的裂解炉管合金HP40为材料,分别利用H2-H2O低氧分压气氛及工业上常用的空气-H2O气氛进行预氧化,对预氧化后合金的表面形貌、元素分布及相组成进行了分析;利用N2-C2H6和H2-CH4气氛研究了预氧化后HP40合金的结焦和碳化行为。
1 实验部分
1.1 试样的制备与氧化
HP40合金的元素组成见表1。用数控线切割机床切取尺寸为5 mm×5 mm×3 mm的正方形试样,控制线切割的走丝速度,使每个试样的表面粗糙度基本一致。切割后的试样在超声波清洗机中依次用丙酮和去离子水清洗,晾干待用。
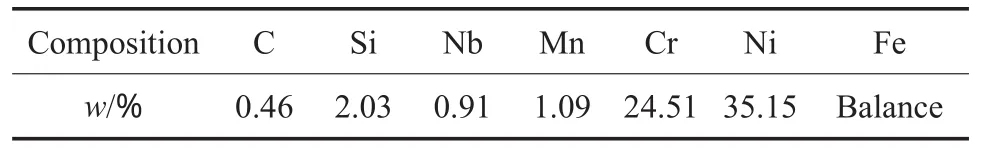
表1 HP40合金的元素组成Table 1 Composition of the HP40 alloy
试样的氧化实验在图1所示装置中进行,试样悬挂于电加热炉的恒温区域。氧化气体为一定比例的H2-H2O或空气-H2O混合气,流量为200 mL/ min。氧化过程中的升温速率为10 ℃/min,升至一定温度后恒温一段时间,降温速率约为2 ℃/min,整个氧化过程中一直通入氧化气体。当氧化气体为H2-H2O混合气时,需在常温状态下用真空泵将反应器中的空气排除干净。H2-H2O及空气-H2O混合气预氧化的试样分别称为H2-H2O预氧化试样和空气-H2O预氧化试样。
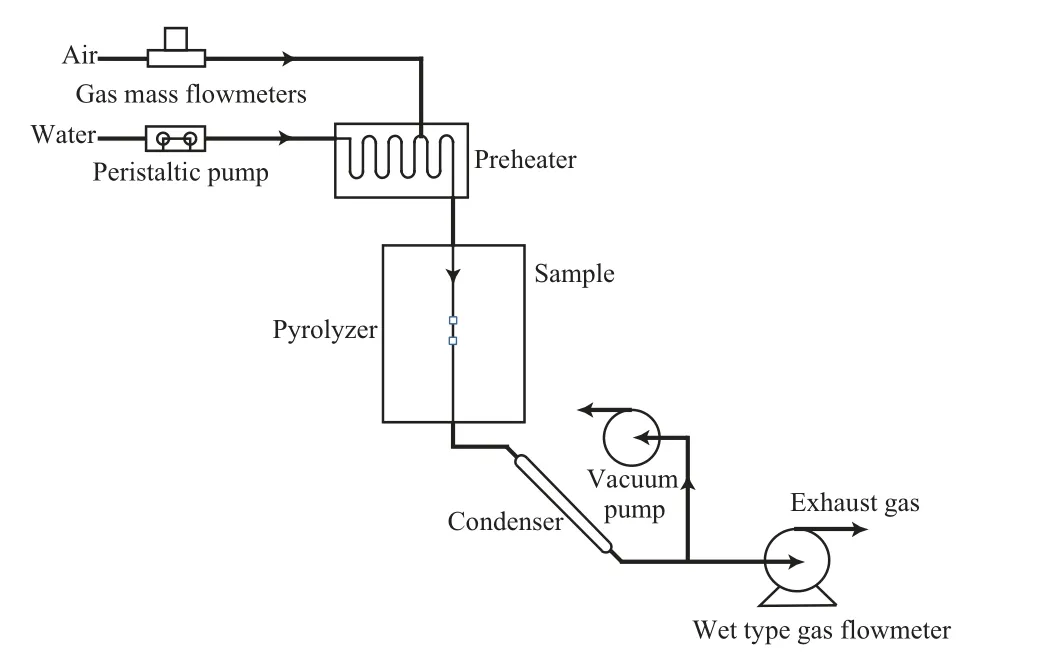
图1 实验装置的示意图Fig.1 Schematic diagram of test unit.
1.2 试样的结焦和碳化
试样的结焦、清焦和碳化实验也在图1所示装置中进行,试样悬挂于电加热炉的恒温区域。进行结焦实验时,结焦气体为98%(φ)N2-2%(φ)C2H6混合气,升温速率为10 ℃/min,升至900 ℃后恒温一段时间,降温速率约为2 ℃/min,升温和恒温过程中一直通入结焦气体,气体流量为200 mL/min。每个试样结焦 3 次,前两次结焦3 h,第三次结焦4 h,共10 h。每次结焦实验前后,称取试样的质量,结焦10 h后进行分析表征。
进行清焦实验时,清焦气体为空气,升温速率为10 ℃/min,升至900 ℃后恒温2 h,降温速率约为2 ℃/min,整个过程中一直通入空气,空气流量为200 mL/min。
进行碳化实验时,碳化气体为98%(φ)H2-2%(φ)CH4混合气,升温速率为10 ℃/min,升至1 000℃后恒温10 h,降温速率约为2 ℃/min,升温和恒温过程中一直通入碳化气体,气体流量为200 mL/ min。每个试样碳化4次,每次碳化10 h,共40 h。每次碳化实验前后,称取试样的质量,碳化40 h后进行分析表征。
结焦和碳化实验前,需在常温下用真空泵将反应器中的空气排除干净。
1.3 分析与表征
采用FEI公司的XL-30型场发射环境扫描电子显微镜观察试样的表面形貌,加速电压15 kV。采用EDAX公司的Apollo XP型 X射线能量色散谱仪(EDS)分析试样的元素含量。采用Bruker公司的D8 Advace型X射线衍射仪分析试样的相组成,CuKα射线,管电压40 kV,管电流30 mA,扫描范围2θ=5°~90°,扫描速率8 (°)/min。采用Denver公司的AA-200型电子分析天平称量每次结焦和碳化实验前后试样的质量,精度为0.1 mg。
2 结果与讨论
2.1 表面形貌和相组成
不同气氛预氧化试样的表面形貌见图2,图2中不同位置的元素含量见表2。
由图2和表2可知,在H2-H2O气氛中形成的氧化膜非常完整(见图2a和2b),表面完全被致密的笼型球团氧化物所覆盖(见图2c点1);在空气-H2O气氛中形成的氧化膜有剥落(见图2d区域Ⅳ),且剥落处Fe和Ni元素富集,未剥落的区域被八面体块状氧化物(见图2e点3)及晶粒团氧化物(见图2e点4)所覆盖。
不同气氛预氧化试样的XRD谱图见图3,图3中的Fe-Ni衍射峰来源于基体合金。由图3可见,H2-H2O预氧化试样的氧化膜含有MnCr2O4尖晶石和Cr2O3;而空气-H2O预氧化试样的氧化膜含有MnCr2O4尖晶石和Cr1.3Fe0.7O3。结合EDS分析可知,笼型球团氧化物及八面体块状氧化物均为MnCr2O4尖晶石,晶粒团氧化物为Cr1.3Fe0.7O3。H2-H2O预氧化试样的氧化膜中,笼型球团氧化物MnCr2O4尖晶石非常致密,以至于用电子显微镜几乎观察不到其下方的Cr2O3氧化物层;而空气-H2O预氧化试样的氧化膜中,八面体块状MnCr2O4尖晶石间有很多间隙,间隙被Cr1.3Fe0.7O3氧化物填充。

图2 不同气氛预氧化试样的表面形貌Fig.2 Surface morphology of samples pre-oxidized in different atmosphere.
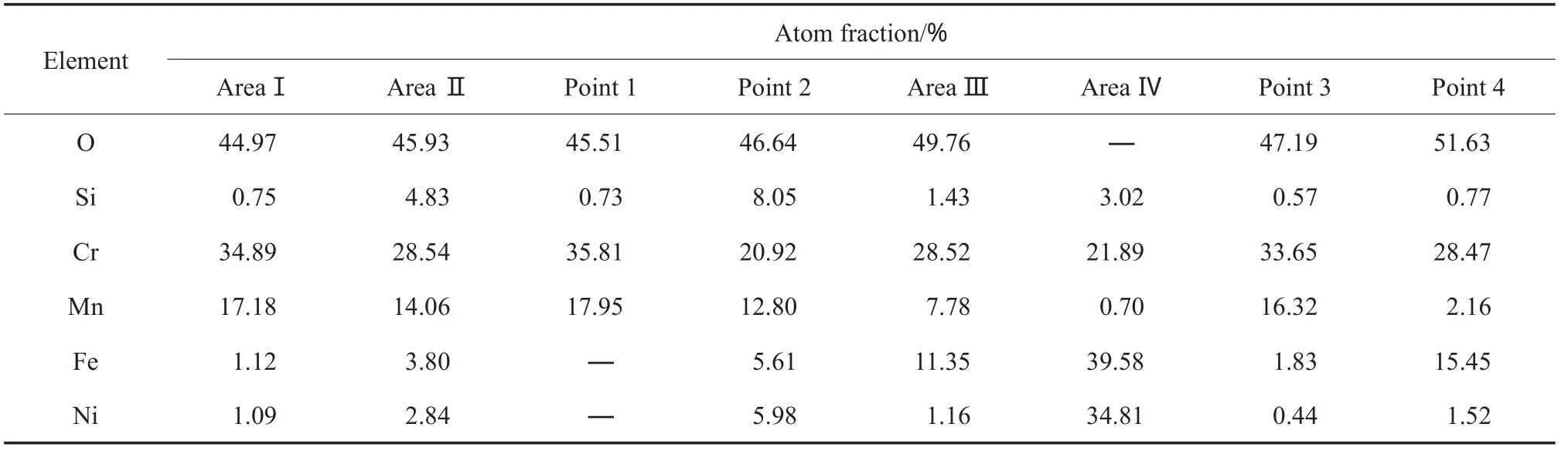
表2 图2中不同位置的元素含量Table 2 Contents of elements in different positions in Fig.2
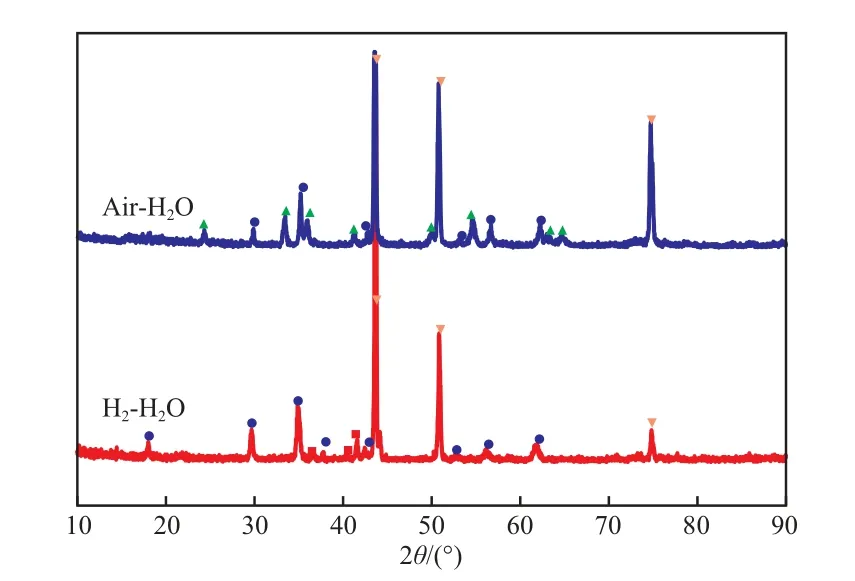
图3 不同气氛预氧化试样的XRD谱图Fig.3 XRD patterns of the samples pre-oxidized in different atmosphere.
HP40合金试样的氧化主要是Cr,Mn,Fe,Ni的氧化,每种元素与O2的反应式及相应的标准吉布斯自由能(ΔGΘ)为[9]:
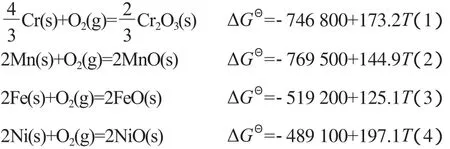
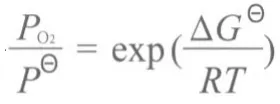
对于本实验所采用的H2-H2O及空气-H2O混合气,不同温度下的氧分压可由相关公式计算得到,计算结果见图4。
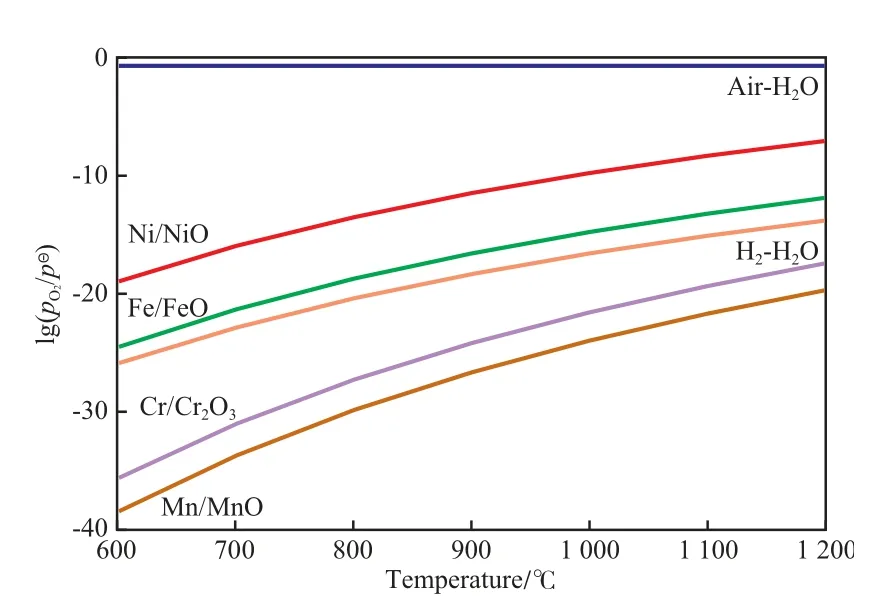
图4 金属/氧化物的平衡氧分压与H2-H2O、空气-H2O的氧分压Fig.4 Equilibrium oxygen pressures of metal/oxide and H2-H2O,air-H2O gas mixtures.
由图4可知,H2-H2O混合气可将HP40合金中的Cr和Mn元素氧化成Cr2O3和MnO,同时Fe和Ni元素不被氧化;而空气-H2O混合气可将HP40合金中的Mn,Cr,Fe,Ni元素全部氧化,分别形成MnO,Cr2O3,Fe2O3,NiO。另一方面,Mn元素通过初始氧化膜向外扩散的能力比Cr元素快两个数量级[10],因此尽管Mn元素在合金中的含量只有约1%(w),但它仍能扩散至氧化膜的表层,形成MnO后与Cr2O3反应生成MnCr2O4尖晶石[11]。所以,H2-H2O预氧化试样的氧化膜含有MnCr2O4尖晶石和Cr2O3,几乎没有Fe和Ni元素;而空气-H2O预氧化试样的氧化膜含有MnCr2O4尖晶石和Cr1.3Fe0.7O3(Cr2O3与Fe2O3的混合物)。
空气-H2O预氧化试样的氧化膜易剥落可从生长应力释放的角度解释。当新的氧化物(如Cr2O3,Fe2O3,MnO)不断形成时,生长应力在氧化膜内部聚集。H2-H2O预氧化试样的氧化膜的晶粒尺寸小于空气-H2O预氧化试样的氧化膜,所以前者通过蠕变的方式释放应力,后者通过裂纹的方式释放应力[12],裂纹导致空气-H2O预氧化试样的氧化膜更易剥落。
在H2-H2O和空气-H2O气氛中形成的MnCr2O4尖晶石的形貌差异可从生长机理角度解释。H2-H2O气氛中,笼型球团状MnCr2O4尖晶石主要在氧化膜的晶界处形成[13],因为Mn离子和Cr离子在晶界处的扩散速率更快,所以大量的MnO 和Cr2O3在晶界处形成,它们形成了具有快速扩散通道的凸起。在H2-H2O气氛中,氧化介质是H2O,而H2O能被这些凸起催化分解成氧原子[14],大量的氧原子吸附在凸起处,使得凸起持续长大,最终晶界处的凸起转变成了直立的片状氧化物[13]。在片状氧化物上方,MnO与Cr2O3反应生成MnCr2O4,这导致片状氧化物上方相互连接,最终形成了笼型球团状尖晶石,与其下方过量的Cr2O3形成了双层MnCr2O4/ Cr2O3氧化膜[15]。在空气-H2O气氛中,氧化介质是O2而不是H2O[16],从O2分解出的氧原子不仅仅吸附在晶界处的凸起上,而是吸附在整个表面,因此MnCr2O4尖晶石的形貌不是直立的片状物,而是普通的八面体形貌。空气-H2O气氛中,过量的Cr2O3与Fe2O3反应形成了Cr1.3Fe0.7O3氧化物。
2.2 结焦行为
不同气氛预氧化试样的结焦增重曲线见图5,将试样清焦后再次结焦,得到的二次结焦增重曲线见图5。
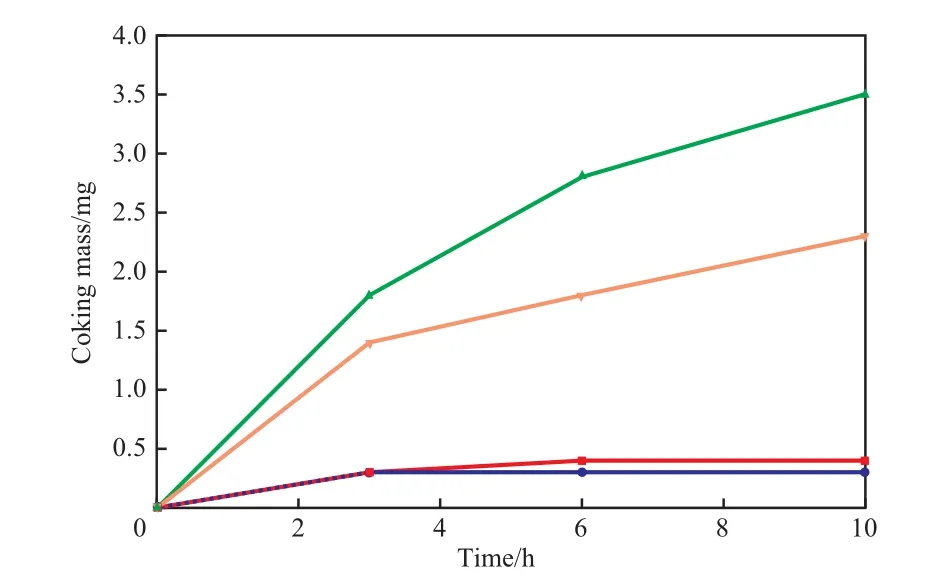
图5 不同气氛预氧化试样的结焦增重曲线及清焦后的二次结焦增重曲线Fig.5 Coking mass of the samples pre-oxidized in different atmosphere before and after decoking.
由图5可知,H2-H2O预氧化试样结焦10 h后的结焦量为0.4 mg,而空气-H2O预氧化试样结焦10 h后的结焦量为2.3 mg,前者约为后者的17%;清焦后二次结焦时,H2-H2O预氧化试样结焦10 h后的结焦量为0.3 mg,而空气-H2O预氧化试样结焦10 h后的结焦量为3.5 mg。清焦前后H2-H2O预氧化试样的结焦量变化很小,而空气-H2O预氧化试样清焦后的二次结焦量比清焦前增加约50%。
不同气氛预氧化试样结焦10 h后的形貌见图6,图6中不同位置的元素含量见表3。由图6和表3可知:1)H2-H2O预氧化试样结焦后表面只有少量不连续的絮状焦炭团聚,没有丝状焦炭;2)空气-H2O预氧化试样的表面被大量的丝状焦炭覆盖,剥落处丝状焦炭更多,直径更大。

图6 不同气氛预氧化试样结焦10 h后的形貌Fig.6 Surface morphology of the samples pre-oxidized in different atmosphere after coking 10 h.
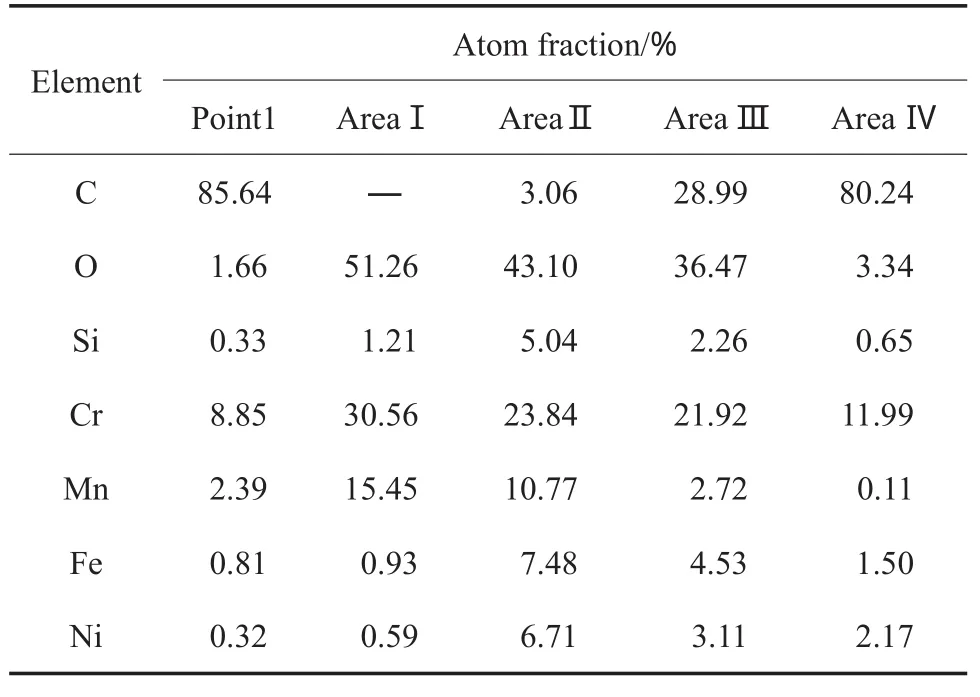
表3 图6中不同位置的元素含量Table 3 Contents of elements in different positions in Fig.6
MnCr2O4尖晶石具有良好的热稳定性,试样表面致密的MnCr2O4尖晶石氧化膜能隔离基体中具有催化结焦活性的Fe和Ni元素,同时MnCr2O4尖晶石可能会对沉积于其上的焦炭起到催化气化的作用[17-18]。H2-H2O预氧化试样的表面为致密的笼型球团MnCr2O4尖晶石,有效抑制了催化结焦,因此结焦量很少;空气-H2O预氧化试样表面形成的八面体MnCr2O4尖晶石不致密,其间隙被具有催化结焦活性的Cr1.3Fe0.7O3填充,且氧化膜较厚,易剥落,剥落处富集大量Fe和Ni元素,所以结焦量远高于H2-H2O预氧化试样。在N2-C2H6裂解过程中,大量的C2H6和C2H4吸附在空气-H2O预氧化试样的Cr1.3Fe0.7O3氧化物及剥落处的Fe和Ni单质的表面,并在这些金属粒子的高能面分解成碳原子,碳原子再在金属粒子的低能面析出[19-20],该过程不断进行,析出的碳原子长成了丝状焦炭,这就是空气-H2O预氧化试样的表面被大量的丝状焦炭覆盖的原因。
不同气氛预氧化试样结焦10 h再清焦2 h后的表面形貌见图7,图7中不同位置的元素含量见表4。由图5可知,清焦对H2-H2O预氧化试样的抗结焦能力的影响不明显,但减弱了空气-H2O预氧化试样的抗结焦能力。由图7和表4可知,清焦后的H2-H2O预氧化试样表面致密的笼型球团尖晶石转化成了致密的八面体块状尖晶石(见图7b),这是由于在清焦过程中,H2-H2O预氧化试样的表面被O2氧化,导致尖晶石形貌改变,但八面体块状尖晶石的致密性仍然很好,而清焦后空气-H2O预氧化试样表面的氧化膜剥落更加严重(见图7c)。这就是清焦前后H2-H2O预氧化试样的结焦量几乎不变,而空气-H2O预氧化试样在清焦后结焦量大幅增加的原因。

图7 不同气氛预氧化试样结焦再清焦后的形貌Fig.7 Surface morphology of the samples pre-oxidized in different atmosphere after coking and decoking. Coking time 10 h,decoking time 2 h.
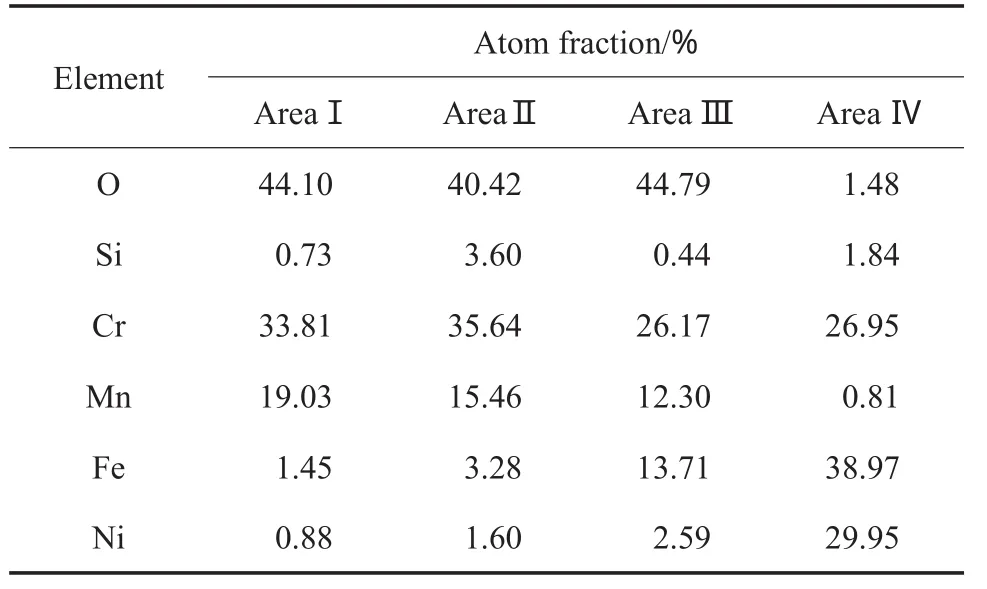
表4 图7中不同位置的元素含量Table 4 Contents of elements in different positions in Fig.7
本实验采用以催化结焦为主的结焦气氛98%(φ)N2-2%(φ)C2H6(其中,N2为稀释气体,C2H6为结焦气体),主要是为了能清晰地观察到两种试样结焦后的表面形貌。这种组分单一的结焦氛围与工业裂解气氛围差别较大,工业裂解气含有碳氢化合物、H2和H2O,也是一种低氧分压氛围,故H2-H2O气氛中形成的氧化膜在裂解过程中可以修复和再生。由此可以推测,在真实的裂解环境中H2-H2O预氧化后得到的氧化膜具有相当长的寿命。但长期处于高温裂解工况下的氧化膜,避免不了大量的开裂和剥落,剥落和开裂区域的Cr和Mn含量很低,该区域的MnCr2O4尖晶石很难再生。这种不可再生性可能是H2-H2O预氧化技术的主要缺陷。
2.3 碳化行为
不同气氛预氧化试样在1 000 ℃下的碳化增重曲线见图8。由图8可知,H2-H2O预氧化试样在碳化过程中几乎没有增重,而空气-H2O预氧化试样碳化增重明显。
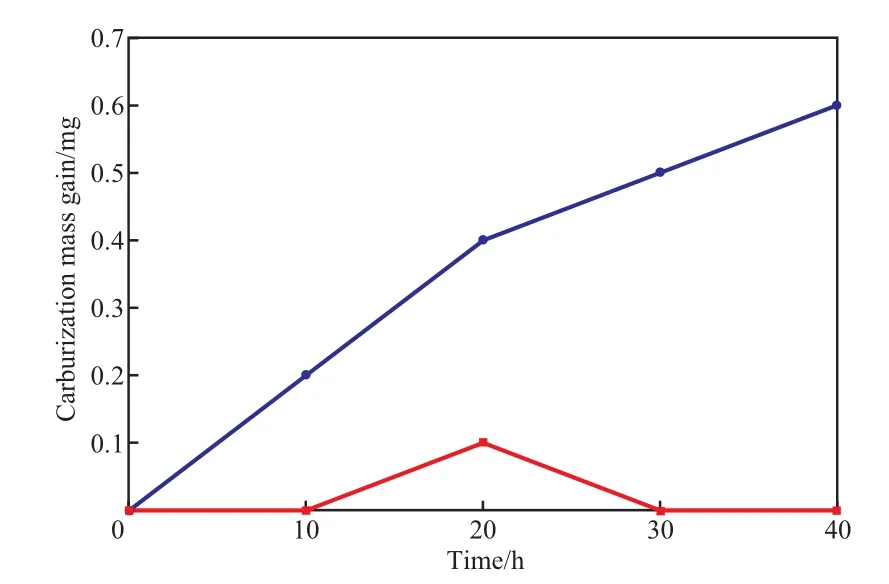
图8 不同气氛预氧化试样在1 000 ℃下的碳化增重曲线Fig.8 Carburization mass gain at 1 000 ℃ of the samples pre-oxidized in different atmosphere.
不同气氛预氧化试样碳化40 h后的表面形貌和XRD谱图分别见图9和图10,图9中不同位置的元素含量见表5。图10中的Fe-Ni衍射峰来源于基体合金。由图9和表5可知,空气-H2O预氧化试样碳化后,表面的氧化膜几乎转化成了碳化膜,增重是由于八面体块状尖晶石MnCr2O4和晶粒团氧化物Cr1.3Fe0.7O3碳化成了(Cr,Fe)7C3(见图9b区域Ⅱ和Ⅳ),且氧化膜剥落处Fe和Cr单质被碳化成了Fe3C和Cr7C3(见图9b区域Ⅲ)。空气-H2O预氧化试样形成的MnCr2O4尖晶石疏松、不致密,CH4气体易穿过,且氧化膜剥落处裸露的基体合金也易被碳原子入侵,这些都大大促进了碳化过程,因此空气-H2O预氧化试样的氧化膜在高温碳化气体氛围中不具有良好的保护作用。H2-H2O预氧化试样碳化后,表面依然覆盖着致密的笼型球团状MnCr2O4尖晶石(见图9a区域Ⅰ)。这说明致密的MnCr2O4尖晶石具有良好的热稳定性和抗碳化能力[21],对碳化气体传质或碳原子的扩散有着良好的阻隔作用,H2-H2O预氧化试样的氧化膜对基体合金有显著的保护作用。

图9 不同气氛预氧化试样碳化40 h后的表面形貌Fig.9 Surface morphology of the samples pre-oxidized in different atmosphere after carburization for 40 h.
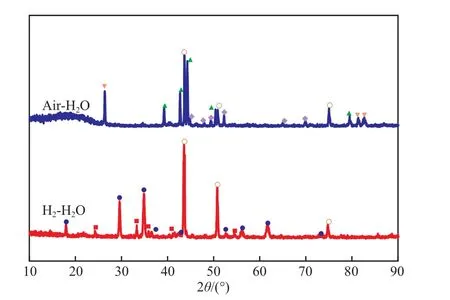
图10 不同气氛预氧化试样碳化40 h后的XRD谱图Fig.10 XRD patterns of the samples pre-oxidized in different atmosphere after carburization for 40 h.
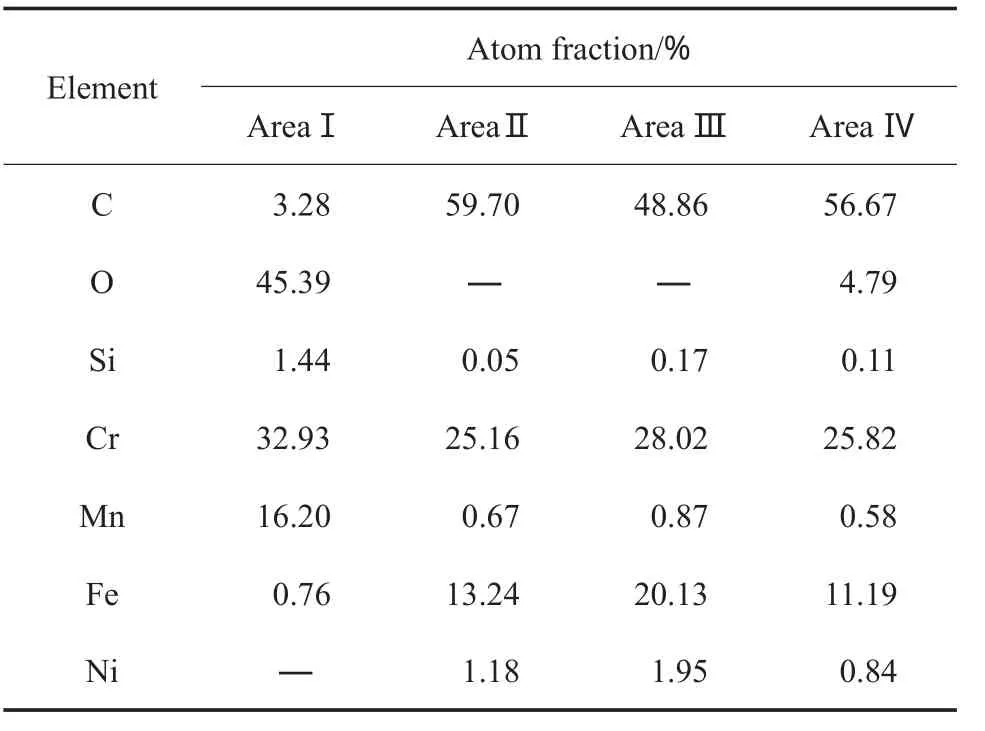
表5 图9中不同位置的元素含量Table 5 Contents of elements in different positions in Fig.9
3 结论
1)HP40合金在H2-H2O气氛中形成的氧化膜非常完整,表面完全被致密的笼型球团状MnCr2O4尖晶石覆盖;HP40合金在空气-H2O气氛中形成的氧化膜存在剥落,且剥落处Fe和Ni元素富集,未剥落的区域被八面体形状的MnCr2O4尖晶石及Cr1.3Fe0.7O3氧化物覆盖。
2)H2-H2O预氧化试样具有更好的抗结焦能力,其结焦量只占空气-H2O预氧化试样的17%,结焦后空气-H2O预氧化试样被大量的丝状焦炭覆盖,而H2-H2O预氧化试样表面只有少量不连续的絮状焦炭团聚。清焦后H2-H2O预氧化试样表面致密的笼型球团状MnCr2O4尖晶石转化成致密的八面体块状MnCr2O4尖晶石,清焦前后结焦量几乎一致;而空气-H2O预氧化试样的氧化膜剥落严重,清焦后的结焦量比清焦前增加50%。
3)H2-H2O预氧化试样具有更好的抗碳化能力,在碳化过程中几乎没有增重;而空气-H2O预氧化试样碳化增重明显。经40 h碳化后,H2-H2O预氧化试样的表面依然保持致密的MnCr2O4尖晶石,而空气-H2O预氧化试样表面的氧化膜几乎转化成了碳化膜,表面形成了(Cr,Fe)7C3和Fe3C等碳化物。
[1] Albright G W,Fisher G,Schillmoller C M. A Combination of Metallurgy and Surface-Coating Materials Mitigate Coke Formation on Furnace Tubes[J].Hydrocarbon Process,1999,78(1):97 - 104.
[2] Figueiredo J L. Carbon Deposition Leading to Filament Growth on Metals[J].Mater Corros,1998,49(5):373 - 377.
[3] Albright L F,Marek J C. Analysis of Coke Produce in Ethylene Furnace:Insights on Process Improvements[J].Ind Eng Chem Res,1988,27(5):751 - 785.
[4] Cai Haiyong,Krzywicki A,Oballa M C. Coke Formation in Steam Cracker for Ethylene Production[J].Chem Eng Process:Process Int,2002,41(3):199 - 214.
[5] 周建新,徐宏,刘京雷,等. 乙烯裂解炉管抑制结焦涂层技术的研究进展[J]. 石油化工,2007,36(3):310 - 314.
[6] Nova Chemicals(International) S.A.(CH). Process of Treating a Stainless Steel Matrix:US,6436202[P]. 2002-08-20.
[7] Nova Chemicals(International) S.A.(CH). Surface on a Stainless Steel Matrix:US,6824883[P]. 2004-11-30.
[8] Nova Chemicals(International) S.A.(CH). Surface on a Stainless Steel Matrix:US,7488392[P]. 2009-02-10.
[9] Povoden E,Grundy A N,Gauckler L J. Thermodynamic Assessment of the Mn-Cr-O System for Solid Oxide Fuel Cell(SOFC)Materials[J].Int J Mater Res,2006,97:569 - 578.
[10] Lobnig R E,Hennesen K,Grabke H J,et al. Diffusion of Cations in Chromia Layers Grown on Iron-Base Alloys[J].Oxidat Metal,1992,37(1/2):81 - 93.
[11] Hammer J,Laney S,Jackson R,et al. The Oxidation of Ferritic Stainless Steels in Simulated Solid-Oxide Fuel-Cell Atmospheres[J].Oxidat Metal,2007,67(1):1 - 38.
[12] Zurek J,Young D J,Essuman E,et al. Growth and Adherence of Chromia Based Surface Scales on Ni-Base Alloys in Highand Low-pO2Gases[J].Mater Sci Eng,A,2008,477(1/2):259 - 270.
[13] Raynaud G M,Rapp R A. In Situ Observation of Whiskers,Pyramids and Pits During the High-Temperature Oxidation of Metals[J].Oxidat Metal,1984,21(1):89 - 102.
[14] Polman E A,Fransen T,Gellings P J. Oxidation Kinetics of Chromium and Morphological Phenomena[J].Oxidat Metal,1989,32(5/6):433 - 447.
[15] Susan D,van den Avyle J,Monroe S,et al. The Effects of Pre-Oxidation and Alloy Chemistry of Austenitic Stainless Steels on Glass/Metal Sealing[J].Oxidat Metal,2009,73(1):311 - 335.
[16] Hänsel M,Quadakkers W J,Young D J. Role of Water Vapor in Chromia-Scale Growth at Low Oxygen Partial Pressure[J].Oxidat Metal,2003,59(3/4):285 - 301.
[17] Holcomb G R,Alman D E. The Effect of Manganese Additions on the Reactive Evaporation of Chromium in Ni-Cr Alloys[J].Scripta Mater,2006,54(10):1821 - 1825.
[18] Mckimpson M G,Albright L F. Future Coils for Ethylene Furnaces Reduced of No Coking and Increased Coil Longevity[J].Am Chem Soc Diν Fuel Chem,2004,49(2):776 -777.
[19] Baker R T K,Gadsby G R,Thomas R B,et al. The Production and Properties of Filamentous Carbon[J].Carbon,1975,13(3):211 - 214.
[20] Baker R T K. Catalytic Growth of Carbon Filaments[J].Carbon,1989,27(3):315 - 323.
[21] Li Hao,Zheng Yanjun,Benum L W,et al. Carburization Behaviour of Mn-Cr-O Spinel in High Temperature Hydrocarbon Pyrolysis Environment[J].Corros Sci,2009,51(10):2336 - 2341.
(编辑 王 萍)
Coking and Carburization Behaviors of Radiant Coils in Pyrolyzer Alloy Pre-Oxidized in Two Atmospheres
Wang Shenxiang1,2,Wang Guoqing2,Wang Hongxia2,Jia Jingsheng2,Cui Lishan1
(1. College of Science,China University of Petroleum-Beijing,Beijing 102249,China;2. SINOPEC Beijing Research Institute of Chemical Industry,Beijing 100013,China)
HP40 alloy was usually used in radiant coils in pyrolyzers. The surface morphology,phase structure and element distribution of the HP40 alloy samples pre-oxidized in H2-H2O and air-H2O atmospheres were investigated. The coking and carburization behaviors of the pre-oxidized samples were studied in 98%(φ)N2-2%(φ)C2H6and 98%(φ)H2-2%(φ)CH4atmospheres. The results showed that the oxide f lm grown in H2-H2O was composed of cage-shaped pelletizing MnCr2O4spinel,while the exfoliation of the oxide f lm grown in air-H2O occurred and the elements Fe,Ni were enriched there,and the un-exfoliated oxide f lm was composed of octahedral-shaped MnCr2O4spinel and Cr1.3Fe0.7O3oxide clusters. The sample pre-oxided in H2-H2O was covered with a small amount of discontinuous f oc coking,while the sample pre-oxided in air-H2O was covered with a lot of f lamentous coking. The coking mass of the former was about 17% of that of the latter. The oxide f lm grown in H2-H2O remained unchanged after carburization test,but the oxide f lm grown in air-H2O was converted into the carbide f lm consisting of (Cr,Fe)7C3and Fe3C.
radiant coil;ethylene;HP40 alloy;pre-oxidation;coking;carburization
1000 - 8144(2014)09 - 1000 - 08
TQ 221.21
A
2014 - 03 - 10;[修改稿日期] 2014 - 05 - 28。
王申祥(1979—),男,湖北省浠水县人,博士生,高级工程师,电话 010 - 59202252,电邮 wangsx.bjhy@sinopec.com。联系人:崔立山,电话 010 - 89733200,电邮 lishancui63@126.com。

