有机化合物的氢化学位移和酸度关系探讨
乐传俊 壮亚峰 朱少萍 叶文玲
(常州工学院理学院化工系 江苏常州213022)
酸是化学中的重要概念。在现有的有机化学教材中,往往把酸放在序言中概述。实际上,酸概念在烯烃加成、醇脱水和缩合等有机反应中有着广泛的应用,但由于有机化合物在结构上与无机化合物有着显著的差别,从而导致学习者对该概念在有机化合物上的理解和应用产生了困难。如用pH能方便地区分各类无机化合物的酸性大小,但却不能用pH对所有有机化合物进行酸度量。常见的酸滴定、电位测定法等也只能测量少量一定浓度范围的有机化合物的pH。因此,目前主要采用酸离解常数(pKa)来表征有机化合物的酸强度。但从一些无机物的pH和pKa来看,两者是存在差异的,故从理论上说,虽然目前广泛采用pKa来度量有机化合物的酸度,但用其表达有机化合物的酸值是不准确的。
核磁共振波谱技术是解析有机化合物结构的强大工具,在有机化学教学中,我们往往会归纳各类化合物的氢化学位移值范围,以便记忆和应用。然而,当我们带着酸概念比较不同结构有机化合物中的一些氢化学位移值时,发现化学位移值大小也能在一定程度上反映出该有机化合物在相应溶剂中的酸性强弱(表1)。
事实上,在一般情况下,有机酸的酸性比醇大,而醇的酸性比烷烃大,相对应的化合物部分的氢化学位移由大变小;因此,有机化合物的氢化学位移和酸性就可能存在着某种关系。
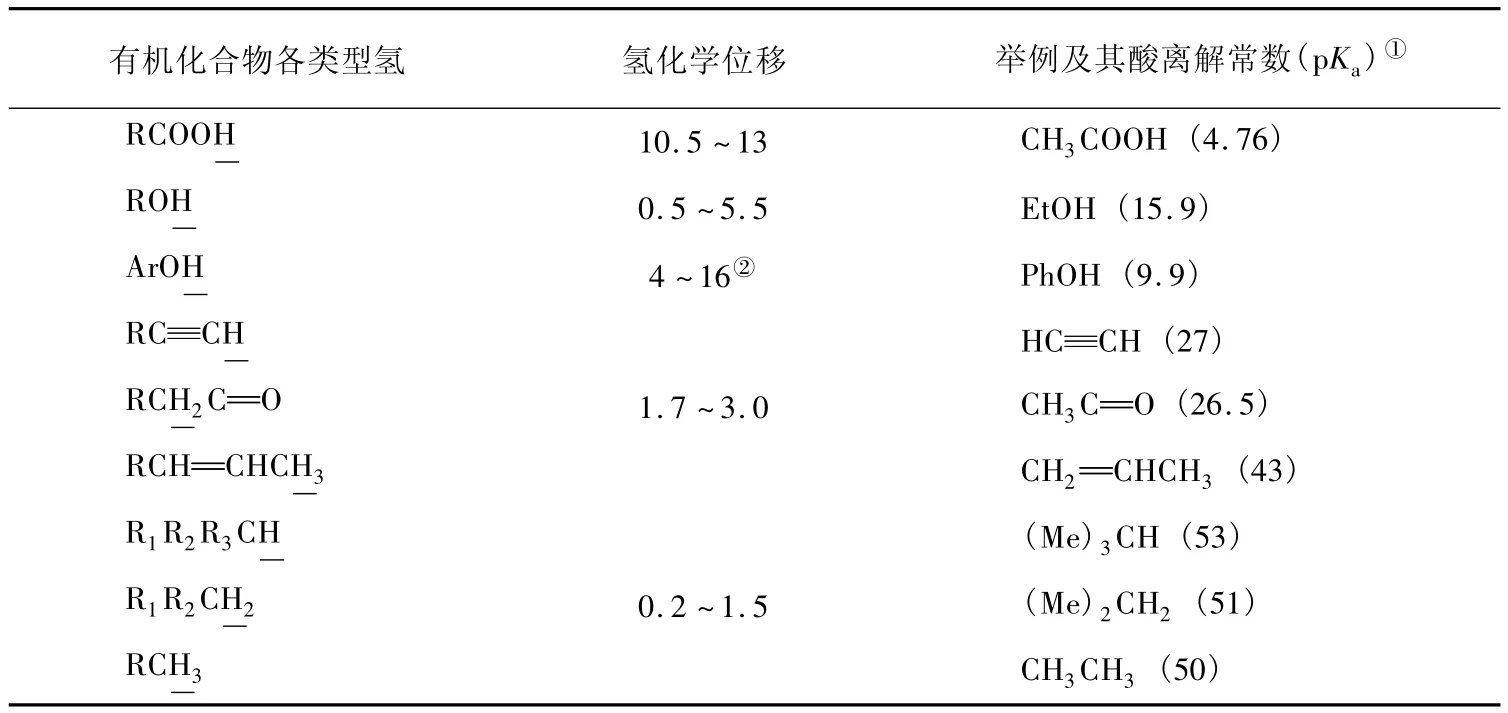
表1 不同类型有机化合物氢的化学位移和酸离解常数
1 理论基础
为了更好地理解有机化合物中的氢化学位移与其酸性的关系,有必要在这里对相关的知识进行概括。
核磁共振是基于特定原子核在外加磁场作用下发生的共振,即发生能级跃迁,也就是原子核磁矩与外加磁场的夹角会发生变化。这种能级跃迁可以获取核磁共振信号。在给定的外加磁场中,某种特定的原子核只吸收某一特定频率射频场提供的能量,这样就形成了核磁共振信号。如果仅考虑某一个孤立的原子核如氢核,则该氢核即使在有机分子中分布于不同位置,也只会在核磁共振波谱图的同一频率处出现共振信号,这样就不能区别不同结构环境中的氢核;但外加磁场会受核外电子的影响,不同环境中的核外电子情况不同,使不同环境的核在不同磁场强度处出现信号,即屏蔽效应。为了表示由于屏蔽效应引起的不同环境下的核在各磁场强度处的共振信号,引入了化学位移概念。化学位移是借磁场强度来表达的相对值概念,反映的是共振原子核所处环境的核外电子密度状况,即屏蔽效应的程度,揭示的是原子所处环境的结构信息。
酸碱理论(如酸碱电离理论和酸碱质子理论)是属于热力学范畴的理论。质子理论认为,凡是能给出质子的分子或离子称为酸,反之为碱;酸碱是成对的,属共轭关系。对于弱酸,存在着电离平衡,平衡常数表示处于平衡状态的几种物质的浓度关系(更确切地说,是活度关系),可以应用化学平衡原理找到衡量酸碱强弱的定量量度(如pH)。而能涵盖酸碱电离和质子理论的酸碱电子理论能从物质的化学结构组成上揭示其本质,接受电子对的是酸,相反为碱。这样,化学位移δ和酸碱pH均反映着物质的化学结构信息。因此,可以用化学位移来研究有机化合物的酸碱平衡、酸性等热力学问题。
2 氢化学位移与酸性关系的探讨
下面从基本知识出发推导有机化合物的酸性和特定氢化学位移的定量关系。现假设一个有机化合物HA,其在一定温度和溶剂下存在以下电离平衡:
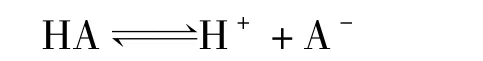
该有机物的电离平衡常数可表达为:
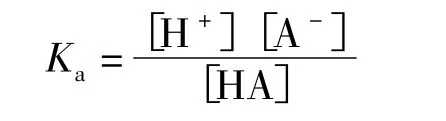
酸离解常数为:
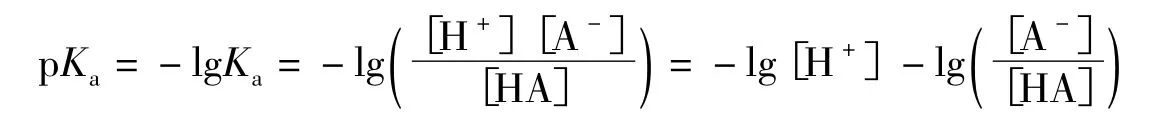
即:

再回到化合物HA在溶液中的氢化学位移上。事实上,在溶液(包括非水溶剂)中测定有机物中某一个氢在核磁共振波谱图上只显示一个信号(偶合裂峰只是一个峰的分裂,整体上仍是来源于一个峰),这说明化合物HA的去质子化和A-质子化的交换反应速率是非常快的,以至于核磁共振仪对此测量的响应时间都无法把交换中是否含质子的物质区分开。因此,核磁共振的响应信号峰是在溶剂中与质子作用的各物种在快速质子交换时特定氢的平均响应信号,这个平均响应信号是和溶液中的各质子作用物种浓度相关的,可以用下式来表达:
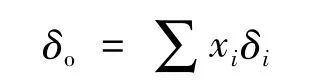
式中,δo是溶液中在核磁共振波谱上显示的特定氢化学位移,xi和δi分别为溶液中的i物种的质量分数和某一特定氢的化学位移。
对于物质HA来说,有:
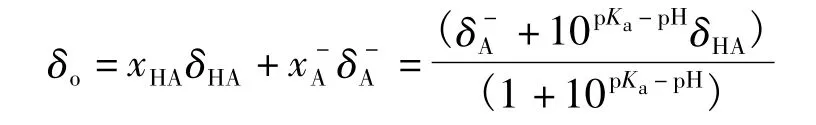
变化上式可得:

从式(1)可以看出,通过核磁共振仪测得HA在溶液中各相关物种中某个特定氢的化学位移值,就可以从pH或pKa计算出其中的另一个值,理论上可以测算出有机化合物中任何氢原子的酸值。由于高分辨率核磁共振仪的使用,使得用该法测定溶液酸值的精度越来越高。如二氯乙酸pKa的测定,首先,在pH分别为0.16和4.28的溶液(H2O/D2O)中可分别测得纯HA和A-中非羧基氢的化学位移δHA和;接着用酸度计测得一定条件下的二氯乙酸的pH(也可通过核磁共振滴定获得,参看文献[4]);最后根据式(1)可精确求得二氯乙酸在特定条件下的pKa。这种方法可以用来测定超强酸的pKa(参看文献[5]),从而扩大了该法的适用范围。式(1)的使用条件和热力学上的电离平衡常数一样,受温度、溶剂和压力等的影响。
另外,pH和pKa并不是总保持正相关关系的。从式(1)可知δo值处于和间。当时,一定温度、浓度和溶剂中所测得的pH随所测得的δo增加而增加;当时则正好相反。因此,用pKa表达有机化合物的酸度是不准确的,存在着差值但由于有机物的电离常数往往很小,所以一定溶液中含量低,这样就可以近似用pKa代替pH来度量酸度。但从有机反应复杂性来看,细小的酸值差可能会导致反应的进度和选择性改变,甚至会改变反应的途径。因此,精确度量酸值或酸离解常数是有意义的,因为热力学参数pH和pKa从一定意义上说和化学位移δ一样也能反映物质的结构信息。最后需要说明的是关系式中的特定氢化学位移往往不是对外表现酸性的氢化学位移,但两者通过化学键联系着;而对外表现酸性的氢的化学位移和其酸性的关系可通过酸碱电子理论和核磁共振原理得到定性解释,因为酸值pH和化学位移δ属于不同范畴的概念。
3 结论
有机化合物的pH和pKa是反映物质酸性等理化性质的重要热力学参数。这两个参数从严格意义上说是有差异的,不能用pKa完全代替pH来判断有机化合物的酸值。对于指定物质,前者只与温度有关,后者还与溶液浓度有关,且两者之间可以通过核磁共振技术分别测量出有机化合物在溶剂中质子化和非质子化物种的特定氢化学位移后,用定量关系式进行转化。这提供了沟通有机化合物的pH和pKa间关系的一个方法,对理解热力学的pH或pKa及其内在联系和表征有机化合物结构参数的化学位移都是很有意义的。这样有利于学生理解和掌握与有机化学内容相关的知识,培养学生知识迁移和综合创新能力。
[1]邢其毅,裴伟伟,徐瑞秋,等.基础有机化学.第2版.北京:高等教育出版社,1993
[2]大连理工大学无机化学教研室.无机化学.第5版.北京:高等教育出版社,2006
[3]GiraltE,ViladrichR,PedrosoE.OrgMagnReson,1983,21(3):208
[4]SzakácsZ,HägeleG.Talanta,2004,62(4):819
[5]SommerJ,RimmelinP,DrakenbergT.JACS,1976,98(9):2671

