2个十钒酸盐类化合物的合成及晶体结构
张桂玲, 冉 靓, 罗绪强
(1.贵阳学院 化学与材料工程学院, 贵阳 550005;2.贵州师范学院 资源环境与灾害研究所, 贵阳 550018)
2个十钒酸盐类化合物的合成及晶体结构
张桂玲1*, 冉 靓1, 罗绪强2
(1.贵阳学院 化学与材料工程学院, 贵阳 550005;2.贵州师范学院 资源环境与灾害研究所, 贵阳 550018)
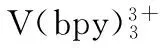
多金属氧酸盐; 十钒酸盐; 合成; 晶体结构
多金属氧酸盐是无机化学中的一个重要研究领域,发展至今已有100多年的历史.因其不寻常的功能特性和反应特性,在光、电、磁、催化、药物等领域引起了人们的广泛兴趣,合成和表征含有机分子的多金属氧酸盐自组装化合物已成为多金属氧酸盐合成化学的热点之一[1-5].钒有三价、四价、五价等化合态,通常以钒氧键的形式存在,与氮和硫也容易形成较强的配位键,并且具有多变的立体化学配位结构,从四面体和八面体到三角双锥、五角双锥等.可组装成如带形,半球形,笼型等各种形状的孤立的多阴离子簇,还可以形成一维(1D)链状,二维(2D)层状和三维(3D)网状等结构复杂多样的金属氧簇合物[6-9].在众多的含钒化合物中,十钒酸盐因其结构独特有趣,组成多变,极具潜在应用价值越来越吸引人们的关注和兴趣.将有机或有机金属基团引入多酸化合物以修饰多阴离子的部分外部骨架结构,对于多酸化合物结构及性质的改变,获得新的功能材料以及开发新的应用领域都具有积极的意义[10-11].
目前,基于十钒酸阴离子和过渡、碱金属水合阳离子的化合物已有很多报道,但鲜有含低价钒配合物的报道.文献报道的十钒酸盐类化合物都是由五价钒本身在酸性条件下聚合所得[12-14],本文尝试在弱碱性条件下,VO2+和空气中的氧发生氧化还原反应,辅以其它有机配体,获得了2个新型十钒酸盐化合物,其中一个外界阳离子为质子化的三乙胺、咪唑和溶剂分子水和甲醇,另一个的阳离子为三价钒配合物.
1实验部分
1.1仪器与试剂
Vario EL 型元素分析仪,德国Elementar公司;Bruker Smart-1000 CCD型X-射线单晶衍射仪;Nicolet Nexus 470型FT-IR,KBr压片,在400 ~ 4000 cm-1范围内摄谱;咪唑、甲醇、乙醇、三乙胺、VOSO4·3H2O、2,2’-联吡啶(bpy)、六氢吡啶均为市售分析纯.
1.22个化合物的合成1.2.1十钒酸盐化合物(C2H5N3)4[HN(C2H5)3]2V10O28·MeOH·3H2O (1)的合成 搅拌下,将5 mL含有0.025 6 g (0.4 mmol) 的咪唑甲醇溶液缓慢滴加进含有VOSO4·3H2O (0.065 1 g, 0.3 mmol) 的10 mL水/乙醇(V∶V=1∶5)溶液,再以适量三乙胺调节pH值至7.3,333 K加热回流6 h.抽滤,滤液室温缓慢蒸发,7 d后得到适于X-ray单晶衍射的橙色晶体.红外光谱(KBr, cm-1): 3 460(s), 3 137(w), 2 976 (w), 2 678(w), 2 358(s),1 700(w), 1 187(w), 975(s), 819(s), 733(s), 829(w).元素分析,Calculated(%): C, 19.78; H, 1.45; N, 8.65;Found(%): C, 19.69; H, 1.40; N, 8.59.
1.2.2十钒酸盐化合物[V(bpy)3]2V10O28(2)的合成 搅拌下,将5 mL (0.033 6 g, 0.2 mmol) bpy甲醇溶液缓慢滴加进(0.065 1 g, 0.3 mmol)VOSO4·3H2O的10 mL水/乙醇(V∶V=1∶5)溶液,再以适量六氢吡啶调节pH值至7.3,333 K加热回流4 h.抽滤,滤液室温缓慢蒸发,10 d后得到适于X-ray单晶衍射的红色晶体.红外光谱(KBr, cm-1): 3 405(s), 3 070(w), 1 636(w), 1 596(m), 1 576(s), 1 474(w), 1 442(m), 1 316(w), 1 162(w), 1 010(m), 958(s), 837(s), 774(s),737(m), 597(w). 元素分析,Calculated(%): C, 35.88; H, 3.01; N, 8.37; Found(%): C, 35.81; H, 2.98; N, 8.31.
1.3晶体数据收集和结构解析
选取大小合适的晶体用于单晶X-射线衍射结构测定.将选好的单晶置于Bruker Smart-1000 CCD型X射线面探器上,衍射测定的温度为293 K,采用经过石墨单色器单色化的Mo Kα射线(λ=0.71073 Å)收取,以面探扫描方式进行数据收集.结构分析由Shelxl-97软件包完成,配合物的结构由直接法解出,非氢原子的坐标是在以后的数轮差值Fourier合成中陆续确定的.通过全矩阵最小二乘法对F2进行修正收敛得到全部非氢原子的坐标及各向异性参数.
单晶(1)、单晶(2)的主要衍射数据见表1,单晶(1)部分键长值列于表2,单晶 (2)部分键长值列于表3.晶体学数据已经存放在剑桥晶体数据库中心(Cambridge Crystallographic Data Center, CCDC),单晶(1) CCDC number:995757,单晶(2) CCDC number:995758.
2结果与讨论
2.1十钒酸盐化合物(1)和(2)的合成反应和一般性质
化合物(1)的氧化还原反应离子方程式为:
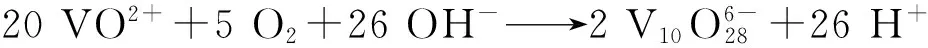

表1 配合物的主要晶体衍射数据Tab.1 Crystal data and structure for two compounds
化合物(2)在氧化还原反应的同时三价钒离子发生配位反应,生成产物.其氧化还原反应离子方程式为:
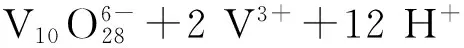
化合物(1),化合物(2)在非极性溶剂乙醚、四氯化碳、苯中难溶,在极性溶剂水、甲醇、乙醇、DMSO和DMF中易溶.元素分析的结果和下文红外表征、单晶X-ray衍射所确定的化合物的结构一致.

表2 配合物(1)的部分键长数值Tab.2 Selected bond lengths of compound (1) Å
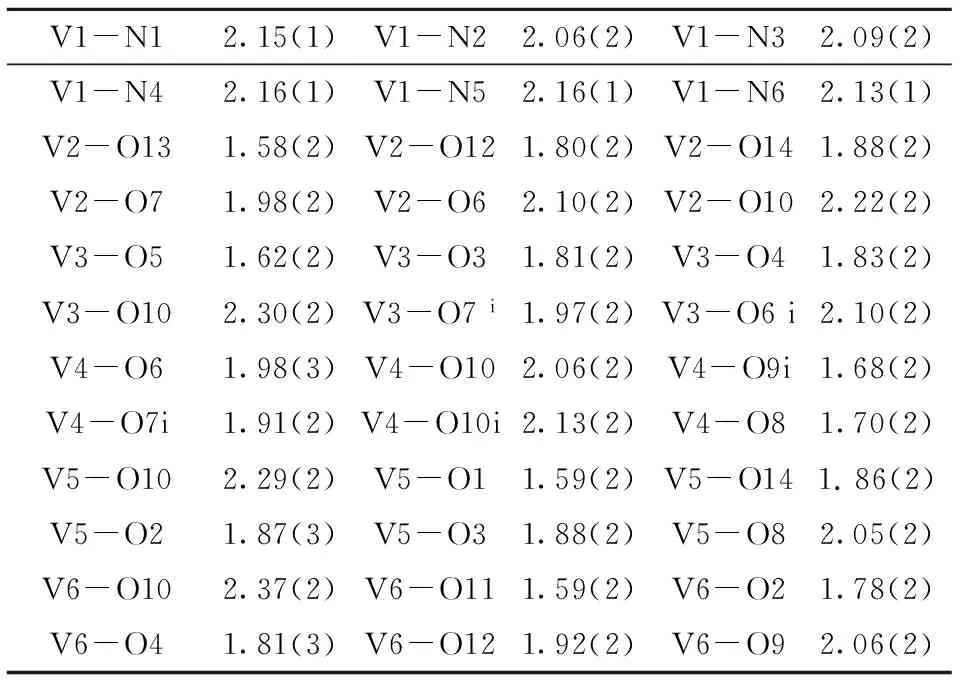
表3 配合物(2)的部分键长数值Tab.3 Selected bond lengths of compound (2) Å
Symmetry code:i=-x+1,-y,-z+1.
2.2十钒酸盐化合物的红外光谱
2.2.1十钒酸盐化合物(1)的红外光谱 结晶水的O—H伸缩振动出现在3 460 cm-1,3 137 cm-1处为咪唑的N—H伸缩振动,2 979~2 358 cm-1为三乙胺的C—H 伸缩振动,钒氧键的振动吸收峰在1 000 cm-1以下,975 和649 cm-1归属为端基V—O伸缩振动,819、733 cm-1为桥联V—O—V 非对称伸缩振动.2.2.2十钒酸盐化合物(2)的红外光谱 配体bpy的骨架振动ν(C=N)和ν(C=C)分别为1 457 cm-1和1 419 cm-1,在配合物中位移到了1 473 cm-1和1 442 cm-1,C—H面外弯曲振动频率δ(C—H)也由758 cm-1,619 cm-1位移到774 cm-1和737 cm-1,说明bpy参与配位.钒氧键的振动吸收峰在1 000 cm-1以下,958、837、774 和 597 cm-1是端基V—O和桥联 V—O—V 伸缩振动.
2.3十钒酸盐化合物 (1)和(2)的晶体结构
十钒酸盐化合物(1)和(2)的晶体结构如图1、图2和图3所示.化合物(1)包含1个[V10O28]6-
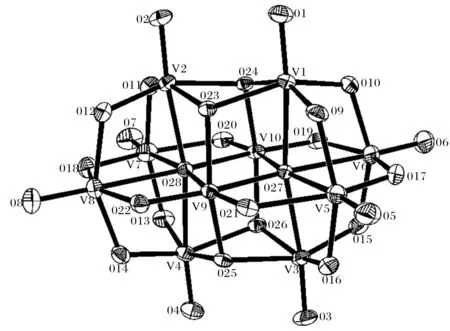
(30%椭球度,为清晰可见,其它阳离子、溶剂分子省略)图1 化合物(1)的十钒酸根阴离子部分ORTEP图Fig.1 ORTEP drawing of compound (1) decavanadate, with 30% thermal ellipsoid probability
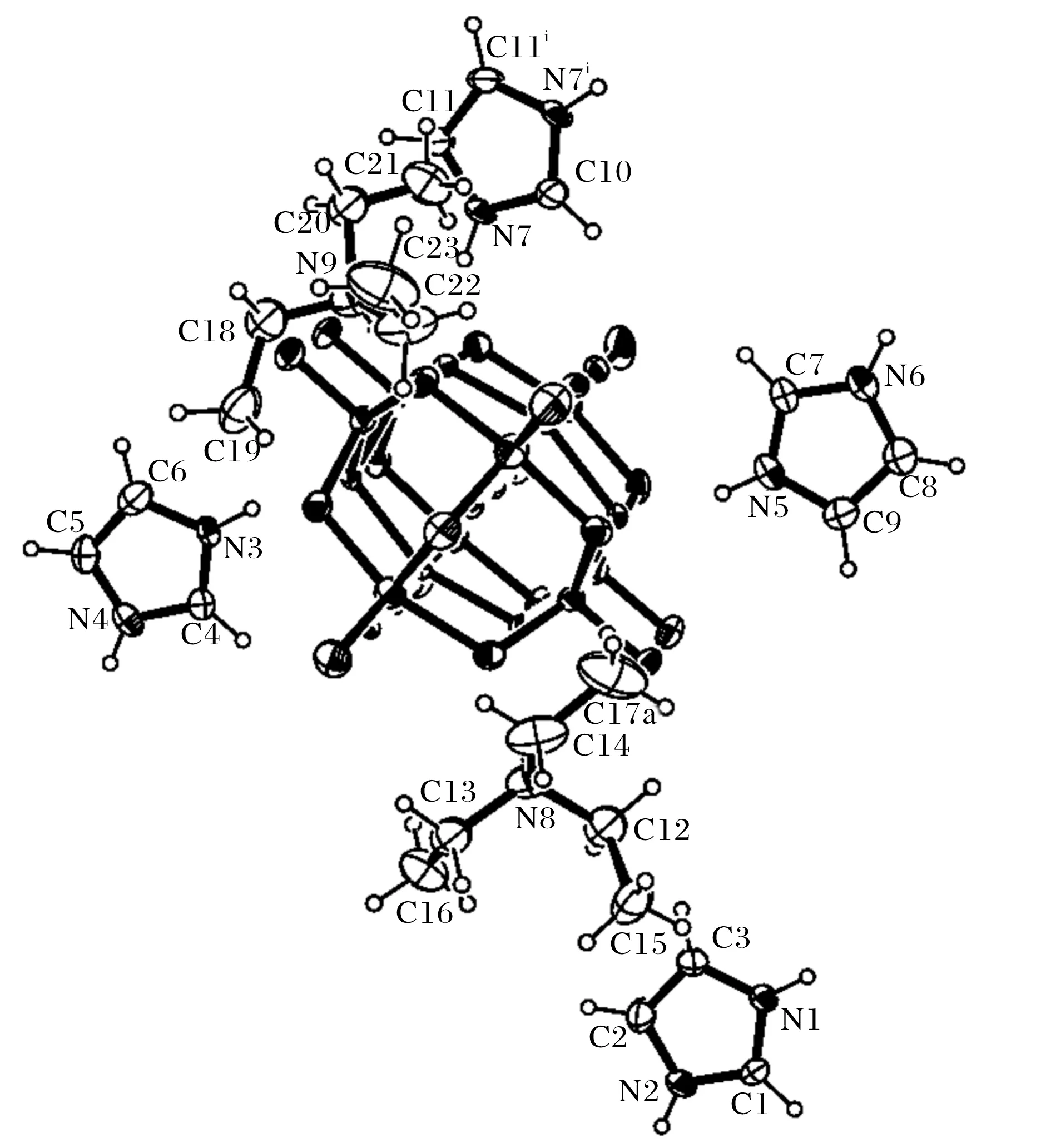
(30%椭球度.为清晰可见,溶剂分子氢原子省略)图2 化合物(1)的ORTEP图 [对称操作码:i=-x,y,-z+1/2]Fig.2 ORTEP drawing of compound (1) with 30% thermal ellipsoid probability

(30%椭球度.为清晰可见,氢原子省略) [对称操作码:i=-x+1,-y,-z+1.]图3 化合物(2)的ORTEP图 Fig.3 ORTEP drawing of compound (2) with 30% thermal ellipsoid probability

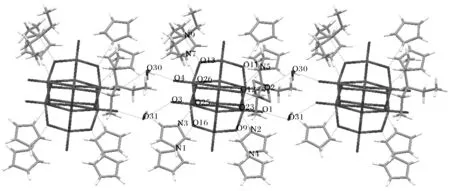
图4 化合物(1)分子间氢键作用示意图Fig.4 A view of hydrogen bonds among the complexes of the compound (1)
化合物(2)中三价钒阳离子和来自3个联吡啶的6个氮原子配位,形成八面体构型.N1/N3/N5/N6 和钒离子在同一平面上,定义为赤道平面,N2/N4为轴向配位,部分键长键角列于表3.同时,如图4所示,化合物(1)中的结晶水与钒酸根中的氧原子、三乙胺与钒酸根中的氧原子、咪唑和钒酸根中的氧原子形成大量的氢键,从而使化合物(1)形成二维超分子结构,氢键数据见表4.
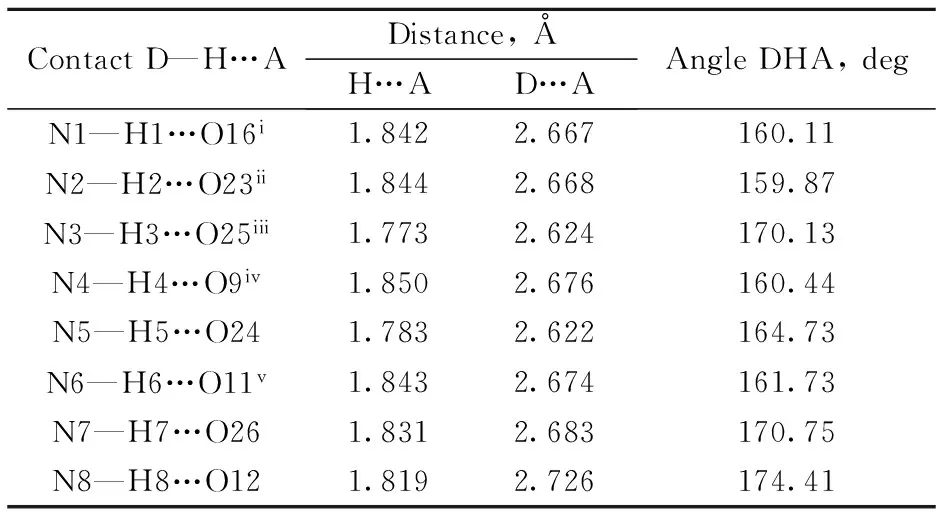
表4 配合物(1)的部分氢键数据Tab.4 Geometric parameters of hydrogen bonds for structure(1)
Symmetry codes: i)x,y-1,z; ii)-x+1/2,-y+1/2,-z+1;iii)x,y-1,z; iv)-x+1/2,-y+1/2,-z+1; v)-x,y,-z+1/2
[1] Izarova N V, Sokolov M N, Samsonenko D G, et al. Synthesis and structures of two new coordination polymers formed by large polyoxometalate fragments and lanthanide cations [J]. Russ Chem Bull, 2008, 57(1): 78-82.
[2] Popem T, Muler A. Polyoxometalate chemistry: An old field with new dimensions in several disciplines [J]. Angew Chem Int Ed, 1991, 30: 34-48.
[3] Yamase T. Polyoxometalates for molecular devices: Antitumor activity and luminescence [J]. Mol Eng, 1993, 3: 241-262.
[4] Debbie C C, Carmen M S, Richard C H, et al. Interaction of porcine uterine fluid purple acid phosphatase with vanadateand vanadyl cation[J]. Biochemistry, 1992, 31: 11731-11739.
[5] Jeffrey T R, Craig L H, Debarah A J. Polyoxometalates in medicine [J]. Chem Rev, 1998, 98: 327-357.
[6] Hamilton E E, Fanwick P E, Wilker J J. The elusive vanadate (V3O9)3-: Isolation, crystal structure, and nonaqueous solution behavior [J]. J Am Chem Soc, 2002, 124 (1): 78-81.
[7] Jouanneau S, Verbaere A, Guyomard D. On a new calcium vanadate: synthesis, structure and Li insertion behavior [J]. Journal of Solid State Chem, 2003, 172: 116-120.
[8] Bangbo Y, Paul A M. M(bipyridine)V4O10(M=Cu, Ag): Hybrid analogues of low-dimensional reduced vanadates [J]. Inorg Chem, 2007, 46(16): 6640-6646.
[9] Le C, Esther A L, Mark H, et al. Reactive sputtering of bismuth vanadate photoanodes for solar water splitting [J]. J Phys Chem C, 2013, 117(42): 21635-21642.
[10] Zhang Y,Warren C J,Haushalter R C,et a1.Comparative study of the structural,electronic,and magnetic properties of the layered ternary vanadium oxides [J]. Chem Mater, 1998, 10(4): 1059-1063.
[11] Khan M I,Haushalter R C,O’Connor C, et a1.An octahedral-tetrahedral vanadiun phosphate-D chain with incorporation 1-aminoethane-2-ammonium cation as ligands [J].China Mater, 1995, 7(4): 593-596.
[12] Zhang X M, Chen X M. Three-dimensional supramolecular arrays supported by decavanadate clusters: Syntheses and crystal structures of (NH4)2[M(dod)(H2O)4]2V10O28·6H2O, (M=Zn; Mn) [J]. Inorg Chem Commun, 2003, 6: 206-209.
[13] Erasmo C, Dainis D, Andrew D, et al. Synthesis and characterization of (NH4)4[H4V10O28][NTPH2]2·4H2O [NTPH3=N(CH2CH2COOH)3)] [J]. Inorg Chim Acta, 2000, 298: 172-177.
[14] Dametto A C, de Arauju A S, de Souza C R, et al. Synthesis, infrared spectroscopy and crystal structure determination of a new decavanadate [J]. J Chem Crystallogr, 2010, 40: 897-901.
Synthesis and crystal structure of two decavanadates
ZHANG Guiling1, RAN Liang1, LUO Xuqiang2
(1.College of Chemistry and Materials Engineering, Guiyang University, Guiyang 550005;2.Institute of Resources Environment and Disaster, Guizhou Normal College, Guiyang 550018)
polyoxometalate; decavanadate; synthesis; crystal structure
2013-11-30.
国家自然科学基金项目(31100187); 贵州省教育厅自然科学基金项目[KY字(2012)059]; 贵州省科技厅自然科学基金项目[J字LKG(2013)14].
1000-1190(2014)04-0544-05
O614.51
A
*E-mail: glzhang996@163.com.

