碱金属改性对Pd-Au/Al2O3催化剂上异戊二烯选择性加氢性能的影响
王宗波,张孔远,杨 康,刘晨光
(中国石油大学重质油国家重点实验室,CNPC催化重点实验室,山东 青岛 266555)
碱金属改性对Pd-Au/Al2O3催化剂上异戊二烯选择性加氢性能的影响
王宗波,张孔远,杨 康,刘晨光
(中国石油大学重质油国家重点实验室,CNPC催化重点实验室,山东 青岛 266555)
采用等体积浸渍法制备了不同K2O、Li2O含量的Pd-AuAl2O3催化剂,采用低温氮吸附法、吡啶吸附红外光谱、程序升温还原(H2-TPR)等方法进行了表征研究。吡啶吸附红外光谱表征结果表明,催化剂表面只有L酸,无B酸,K2O改性比Li2O改性催化剂的表面酸性弱。H2-TPR表征结果表明,催化剂表面形成了Pd-Au二元合金,加入碱金属改性后,催化剂的还原峰向高温方向移动。以异戊二烯的模型化合物为原料评价了自制的改性Pd-AuAl2O3催化剂的选择加氢性能,结果表明:催化剂经过Li2O改性后,异戊二烯的转化率和单烯烃选择性提高,而用K2O改性时,异戊二烯的转化率降低,单烯烃选择性提高;采用K2O质量分数为1.2%的催化剂,在反应温度为70 ℃时异戊二烯的转化率为90.0%,单烯烃的选择性为86.0%。
碱金属 Pd-AuAl2O3L酸 Pd-Au二元合金 异戊二烯
石脑油裂解制乙烯生产过程中副产大量的C5馏分,裂解C5馏分的开发及化工利用得到了非常广泛的关注[1]。对C5资源进行合理、高效地利用,已经成为石油化工科研工作者的研究重点。近年来全球丙烯的需求量不断增加,价格持续走高,开发C5烯烃转化增产丙烯的课题已成为研究热点。但是,需要将裂解C5馏分中的双烯烃通过加氢除去才能作为烯烃转化的原料[2-3]。汽油的升级换代限制了C5馏分全加氢后作为汽油调合组分的使用,C5烯烃醚化和烷基化可以提高品质,但要求脱除C5馏分中的二烯烃,以防止醚化催化剂的快速失活[4]。
Fagal等[5]发现用KNO3、LiNO3改性的Al2O3载体在700 ℃下焙烧后,随着改性剂含量的增加,孔体积基本不变但载体的比表面积增加,且KNO3、LiNO3在高温情况下焙烧放出NOx,对Al2O3来说K2O、Li2O可认为是一种结构性助剂;K2O、Li2O还能和活性位发生作用,这不仅可以提高活性组分的分散度,还可以起到稳定活性相的作用。谢慧[6]研究了碱金属Na+、K+改性的负载型Pd催化剂对二苯并噻吩加氢脱硫性能的影响,结果表明,碱金属离子的添加影响二苯并噻吩在活性位上的吸附方式并改变了二苯并噻吩加氢脱硫的反应路径,从而降低了总的加氢脱硫的活性。
本课题主要研究不同含量KNO3和LiNO3改性的Pd-Au/Al2O3催化剂对异戊二烯选择性加氢的活性和单烯烃选择性的影响,并就表征和评价结果进行讨论。
1 实 验
1.1 试 剂
AuCl3·HCl·4H2O、PdCl2:分析纯,国药集团化学试剂有限公司生产;KNO3、LiNO3:优级纯,国药集团化学试剂有限公司生产;浓硝酸(65%~68%):国药集团化学试剂有限公司生产;盐酸:分析纯,西陇化工股份有限公司生产;正辛烷:化学纯,国药集团化学试剂有限公司生产;异戊二烯:纯度99%,东京化成工业株式会社生产。
1.2 载体及催化剂的制备
取100 g氢氧化铝干胶粉与适量田菁粉均匀混合,将适量的硝酸(65%~68%)和一定量的改性剂加入到80 g去离子水配成均匀溶液,将配好的溶液逐滴加入混好的干胶和田菁粉中混匀,在挤条机上混捏成型,然后于120 ℃下烘干,于空气气氛中500 ℃下焙烧3 h,再于空气气氛中升温至1 000 ℃焙烧,最终得到改性Al2O3载体。根据KNO3、LiNO3添加量的不同,制得几种载体,分别为Al2O3,Li2O-Al2O3,K2O-Al2O3载体。
浸渍液以Pd和Au为活性组分,分别以PdCl2和AuCl3·HCl·4H2O为该活性组分的前躯物,溶解于去离子水中得到相应浸渍液。采用等体积浸渍法浸渍,于120 ℃下烘干,再于500 ℃下焙烧,得到相应的碱金属改性Pd-Au/Al2O3催化剂。所制得的未改性催化剂标记为Al2O3;所制得的碱金属改性的催化剂标记为M2O-1,M2O-2,M2O-3(M为Li,K),氧化锂质量分数依次为0.2%,0.4%,0.6%,氧化钾质量分数依次为0.6%,1.2%,1.8%;二者的质量摩尔浓度接近,分别约为0.065,0.130,0.195 mol/kg。其中Pd和Au的质量分数分别为0.2%和0.1%。
1.3 催化剂的表征
采用Mocromeritics公司生产的ASAP3020型自动吸附仪,用低温氮吸附法测定试样的孔结构。以高纯氮为吸附介质,液氮为冷阱,吸附温度-196 ℃,脱附温度573 K。采用BET法计算比表面积,BJH法计算孔体积和孔径。
采用热电尼高力公司生产的Nexus型傅里叶变换红外光谱仪,用吡啶吸附红外光谱(FT-IR)方法分析催化剂表面的酸类型。样品在300 ℃下焙烧3 h后,在抽真空的条件下吸附吡啶18 h,再在120 ℃的真空干燥箱中进行吡啶的物理脱附2 h;空白样只在300 ℃下焙烧,不进行吡啶吸附。
程序升温还原(H2-TPR)实验在Quanta Chrome公司生产的CHEMBE-3000型NH3-TPD-TPR联合实验装置上进行。将0.10 g试样置入U形石英反应管中,在He(100 mL/min)气氛中于30 ℃下预处理30 min,切换为H2-Ar混合气吹扫,至热导池检测器基线平稳,以10 ℃/min的速率升温至350 ℃,得到H2-TPR曲线。
1.4 催化剂的活性评价
原料采用含异戊二烯2%(φ)的正辛烷溶液,选择加氢反应在10 mL固定床微型反应器(内径15 mm、高800 mm)中进行,催化剂装填量3 mL,用同体积的石英砂稀释。反应压力1.5 MPa,氢油体积比90,反应温度60 ℃。催化剂在相应条件下稳定24 h后取样,当连续2个试样的分析误差在允许范围内后切换评价条件。
采用Agilent-7890N型气相色谱仪对原料和产物进行分析,100 m PONA色谱柱,FID检测。
2 结果与讨论
2.1 催化剂的表征结果
2.1.1 低温氮吸附表征结果 碱金属改性Pd-Au/Al2O3催化剂的物理性质见表1。从表1结果看出:加入碱金属改性与未改性的催化剂比较,催化剂的比表面积、孔体积比较接近;500 ℃下焙烧NO2气体已经完全放出,起到了造孔作用,再于1 000 ℃焙烧过程中,小孔发生的坍塌非常严重,NO2的造孔作用因为高温焙烧消失;用混捏法加入硝酸锂对载体改性,随着锂含量的增加,催化剂比表面积略有降低,孔体积变化不大,平均孔径和最可几孔径均变大;混捏法加入硝酸钾对载体改性,随着钾含量的增加,催化剂的比表面积和孔体积略有增加,催化剂的平均孔径和最可几孔径均变大;在载体成型过程中加入LiNO3和KNO3进行改性,所测催化剂的孔径分布明显向大孔方向移动,最可几孔径由10.3 nm增加到12.7 nm;对比不同类型相同质量摩尔浓度碱金属的改性效果可以发现,对最可几孔径的影响几乎相同,且孔径分布均很集中。
表1 碱金属改性Pd-AuAl2O3催化剂的物理性质
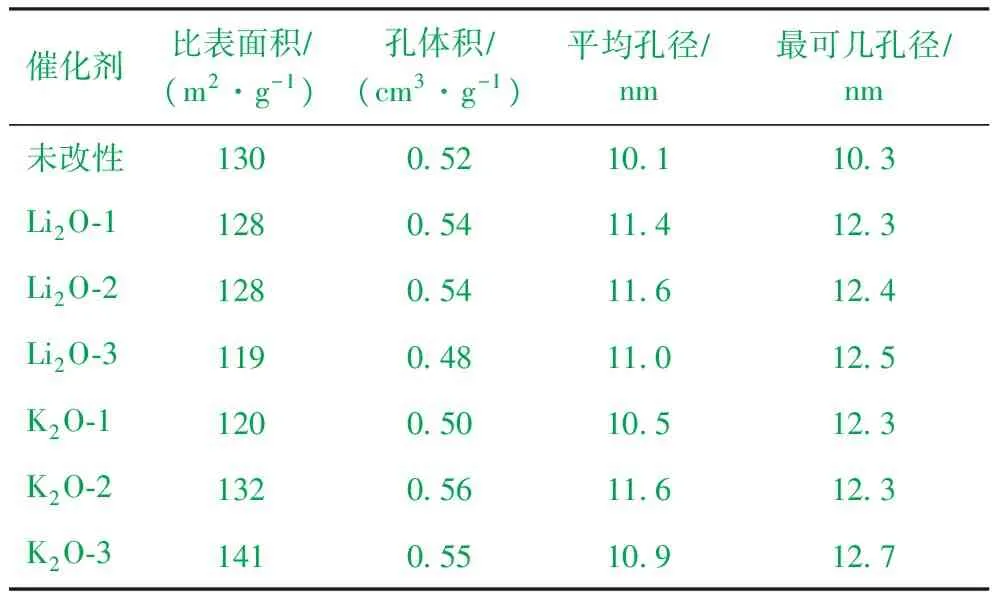
表1 碱金属改性Pd-AuAl2O3催化剂的物理性质
催化剂比表面积∕(m2·g-1)孔体积∕(cm3·g-1)平均孔径∕nm最可几孔径∕nm未改性130052101103Li2O⁃1128054114123Li2O⁃2128054116124Li2O⁃3119048110125K2O⁃1120050105123K2O⁃2132056116123K2O⁃3141055109127
2.1.2 FT-IR表征结果 采用吡啶吸附FT-IR对碱金属改性前后催化剂的酸类型进行定性分析及对酸量进行半定量分析,其FT-IR谱图见图1。催化剂中L酸的峰位置主要出现在1 443,1 577,1 592,1 616 cm-1处,B酸的峰位置主要出现在1 540 cm-1处,L酸、B酸均会出现的峰位置是1 490 cm-1。从图1可以看出,随着碱金属加入量增大,在1 443,1 490,1 577,1 592,1 616 cm-1等峰位的峰面积均逐渐减小,酸量(L酸)逐渐减小,碱金属氧化物毒化酸性中心的作用越来越强。根据Johnson模型[7],氧化铝在高温焙烧的过程中,其表面颗粒的羟基会逐渐缩合,促进氧化铝的生长。在1 540 cm-1处未出现探针分子吡啶(Py)与质子酸结合的PyH+的C—C(N)键伸缩振动峰,则催化剂不含质子酸(B酸),一是因为高的焙烧温度使表面羟基缩合形成Al—O—Al键,质子酸几乎消失;二是因为碱性金属的加入,调变酸性中心,所起作用为毒化作用,对强酸中心的毒化作用最为明显。Sun等[8]制备了碱金属钾改性的介孔氧化铝,CO2-TPD表征结果表明,K的改性使氧化铝表面产生了强碱中心,相对应的是介孔氧化铝的酸性减弱。
通过对比可知,在Li2O与K2O的质量摩尔浓度相同时,使用K2O改性的催化剂比使用Li2O改性的催化剂的各峰的峰面积略小,相对应的酸性较弱。
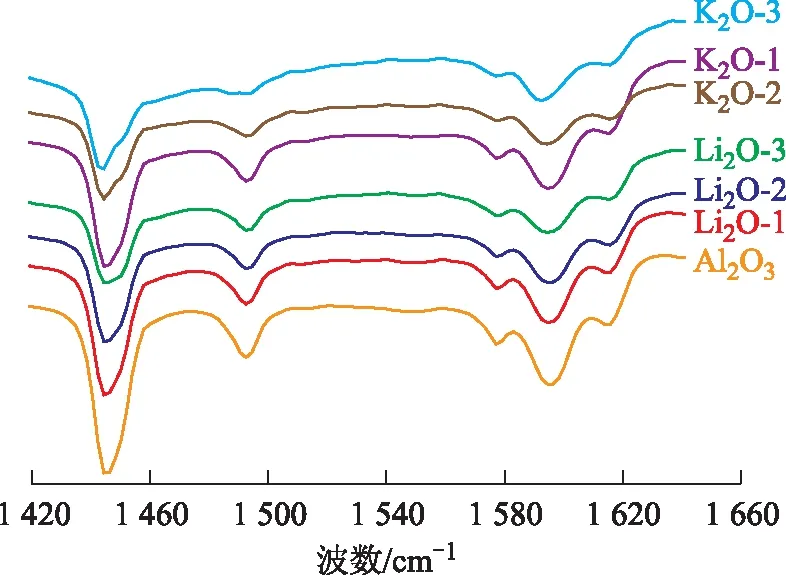
图1 碱金属改性Pd-Au/Al2O3催化剂的FT-IR图谱
2.1.3 H2-TPR表征结果 烃类选择加氢反应过程中,贵金属催化剂表面活性组分一般处于还原状态,考察催化剂的还原性能是评价催化剂催化性能的一个重要指标。Li2O和K2O改性催化剂的H2-TPR曲线分别见图2和图3。由图2和图3可以看出,加入碱金属改性与未改性催化剂在80~300 ℃内均只出现一个耗氢峰,且信号较强。因此可推测,加入碱金属改性前后,在所制备的催化剂表面上均只形成了一种复合氧化物,该复合氧化物经还原后,形成了Pd-Au二元合金。由图2和图3可知,未加入碱金属改性,催化剂的还原峰在133.0 ℃,不同含量Li2O改性催化剂的还原峰的峰位在155.0,157.4,156.4 ℃,不同含量K2O改性催化剂的还原峰的峰位在156.4,164.7,160.3 ℃,很明显地看出,加入碱金属Li和K改性后还原峰的峰位向高温方向移动。这是因为碱金属K、Li改性后,碱金属进入体相氧化铝中的晶格而造成晶格缺陷,其所结合的化学键力强,使得催化剂表面氧向体相迁移,表面晶格氧的浓度降低,Pd基合金的还原温度向高温方向移动。一般认为,还原温度对贵金属催化剂的催化性能影响很大,由于金属与载体的相互作用,造成还原温度和分散度提高[9]。

图2 Li2O改性Pd-Au/Al2O3催化剂的H2-TPR曲线
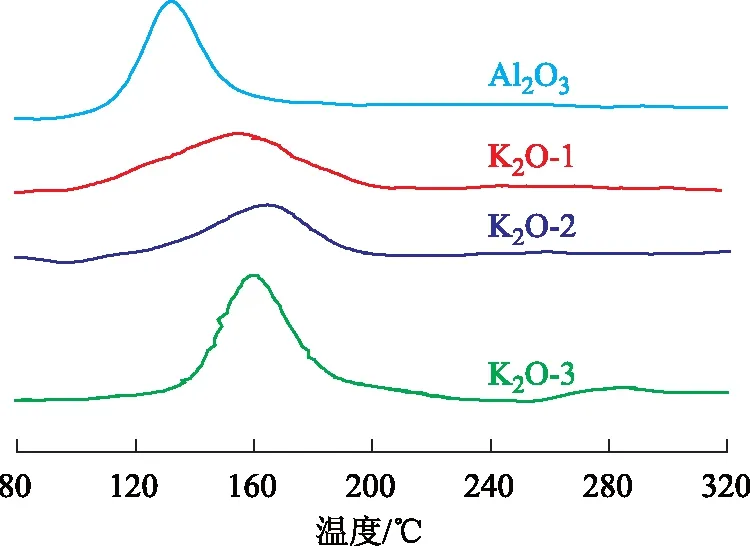
图3 K2O改性Pd-Au/Al2O3催化剂的H2-TPR曲线
Li2O改性的一系列催化剂在100 ℃左右出现了一个倒峰,而K2O改性催化剂并没有发现。因为Li2O改性催化剂表面有氢溢流的发生,而未改性及K2O改性催化剂没有发生。Li2O、K2O改性后,催化剂的还原峰由尖锐变宽泛,金属与载体的相互作用同未改性催化剂相比发生了变化,表面物种(Pd-Au二元合金)更加多样化,其还原性能发生变化。
2.2 催化剂的选择性加氢活性评价
不同碱金属改性Pd-Au/Al2O3催化剂上异戊二烯加氢转化率如图4所示。由图4可以看出:加入碱金属Li改性后,异戊二烯的转化率增大,当Li的质量摩尔浓度为0.065 mol/kg时,异戊二烯的转化率最高(96.1%);加入碱金属K改性后,异戊二烯的转化率明显降低,当K的质量摩尔浓度为0.195 mol/kg时,异戊二烯的转化率最低(58.0%)。各碱金属改性催化剂上单烯烃(异戊烯同分异构体的总称)的选择性如图5所示。由图5可以看出:加入碱金属改性的催化剂与未改性的相比,单烯烃的选择性明显提高,且随着碱金属加入量的增加,对单烯烃的选择性不断提高;不同的碱金属改性的催化剂对单烯烃的选择性影响不同,加入碱金属K改性的催化剂对异戊烯的选择性提高程度明显好于加入碱金属Li改性的催化剂。
异戊二烯选择性加氢与单烯烃的加氢在催化剂的表面是竞争反应,当未加入碱金属改性时,单烯烃的选择性仅为19.2%,异戊二烯的选择性加氢是连串反应,此时,大部分异戊二烯选择性加氢后,未及时从催化剂活性中心上脱附下来,而是继续加氢生成异戊烷。对K改性催化剂进行试验,K2O-2催化剂上单烯烃的选择性最高,大部分异戊二烯选择性加氢生成单烯烃后,单烯烃从催化剂的活性中心上脱附下来,异戊二烯吸附上去继续反应。当反应温度为70 ℃时,K2O-2催化剂上异戊二烯的转化率达到了90.0%,单烯烃的选择性为86.0%;而K2O-1催化剂和K2O-3催化剂上异戊二烯的转化率分别为91.6%和73.1%,单烯烃的选择性分别为30.2%和86.7%。
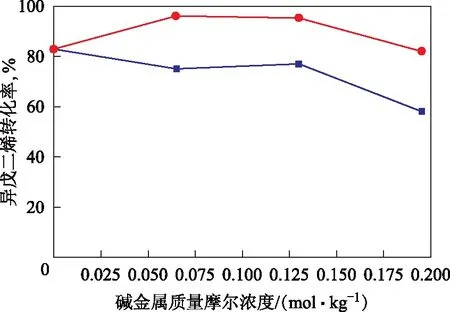
图4 碱金属改性催化剂上异戊二烯转化率●—Li改性; ■—K改性。 图5同

图5 碱金属改性催化剂上单烯烃的选择性
对产物进行分析后,没有检测到高沸点的化合物,说明在反应过程中,异戊二烯与异戊烯在加氢反应过程中均未发生聚合反应,因为反应温度比较低,且红外光谱分析结果表明,催化剂表面并没有强酸中心,即不存在聚合反应发生的活性位。异戊二烯转化成几种异戊烯形式,包括3-甲基-1-丁烯(3M1B)、2-甲基-1-丁烯(2M1B)和2-甲基-2-丁烯(2M2B)。碱金属Li与碱金属K改性催化剂上各种单烯烃的选择性分别见图6、图7。由图6和图7可以看出:异戊二烯选择加氢生成的异戊烯中2M2B是主要产物,其次是2M1B,含量最低的是3M1B;在Li改性的催化剂上,2M2B,2M1B,3M1B的选择性随Li的添加量的增加而升高,分别由18.5%,1.0%,0.1%升高到58.3%,13.6%,4.4%;在K改性的催化剂上,各单烯烃选择性的变化不是单一的规律,K2O-2催化剂上单烯烃的选择性最高,2M2B,2M1B,3M1B分别为72.2%,15.9%,4.1%。这种差别主要是由异戊二烯在钯基催化剂上吸附时与双键相邻的甲基位阻效应[10]、异戊二烯在催化剂表面化学吸附后加成一个氢原子生成的两种烯丙基自由基中间体进一步加氢的难易程度不同[11]引起的。
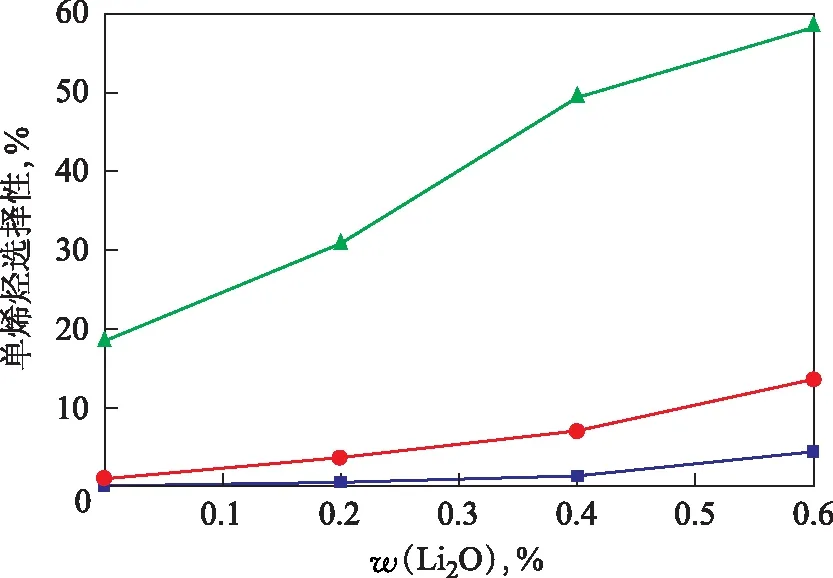
图6 Li2O含量对催化剂上单烯烃选择性的影响●—2M1B; ▲—2M2B; ■—3M1B。 图7同
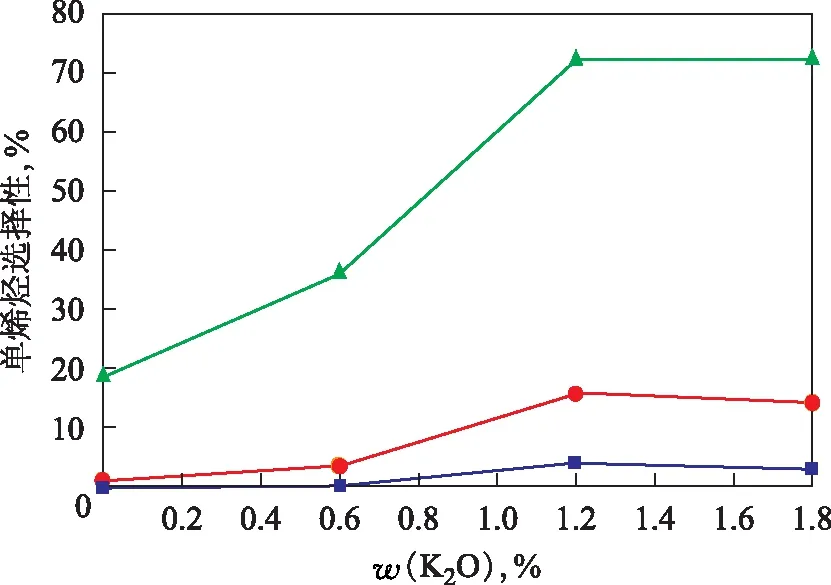
图7 K2O含量对催化剂上单烯烃选择性的影响
3 结 论
(1) 碱金属改性后,催化剂的平均孔径变大,K2O改性比Li2O改性时表面酸性弱。
(2) 在所制备的Pd-Au/Al2O3催化剂的表面上形成了Pd-Au二元合金,加入碱金属改性后,催化剂的H2-TPR还原峰向高温方向移动,活性组分的分散度提高。
(3) 催化剂经Li2O改性后,异戊二烯的转化率明显提高,而用K2O改性时,异戊二烯的转化率明显降低;异戊烯的选择性随碱金属的加入量增加而逐渐增加。当K2O质量分数为1.2%时,催化剂的催化性能最好,当反应温度为70 ℃时,异戊二烯的转化率达到90.0%,异戊烯的选择性为86.0%。
[1] 李东风,马立国.裂解碳五馏分分离技术研究进展[J].石油化工,2007,36(8):755-761
[2] 田保亮,戴伟,杨志钢,等.裂解碳五双烯烃选择加氢[J].化工进展,2009,28(11):1932-1935
[3] 马鸣,田保亮,杨志钢,等.裂解碳五馏分选择加氢催化剂的研究[J].石油化工,2009,38(10):1044-1047
[4] 张志华.C5烯烃的醚化及烷基化[J].石油炼制与化工,1996,27(5):20-25
[5] Fagal G A,El-Shobaky G A.Surface and catalytic properties of Fe2O3-Cr2O3Al2O3solids as being influenced by Li2O and K2O-doping[J].Colloids and Surfaces A:Physicochemical and Engineering Aspects,2001,178(123):287-296
[6] 谢慧.哌啶及碱金属粒子对Pt和Pd催化剂加氢脱硫性能的影响[D].大连:大连理工大学,2012
[7] Johnson M F L.Surface-area stability of aluminas[J].Journal of Catalysis,1990,123 (1):245-259
[8] Sun Linbing,Yang Jing,Zhu Jiahui,et al.One-pot synthesis of potassium-functionalized mesoporous-alumia:A solid superbase[J].Angewandte Chemie:Inernational Edition,2008,47 (18):3418-3421
[9] Cai Jindi,Huang Yiyin,Guo Yonglang.Bi-modified PdC catalyst via irreversible adsorption and its catalytic activity for ethanol oxidation in alkaline medium[J].Electrochimica Acta,2013,99(1):22-29
[10]郑彦彬,黄兴亮.镍基催化剂催化模型化合物中异戊二烯加氢性能[J].石油化工,2003,32(12):1024-1027
[11]Bond G C.Product selectivities in isoprene hydrogenation:Diagnosis of π-allylic intermediates[J].Journal of Molecular Catalysis A:Chemical,1997,18(3):333-339
EFFECT OF ALKALI METAL MODIFICATION ON SELECTIVE HYDROGENATION OF ISOPRENE ON Pd-AuAl2O3CATALYSTS
Wang Zongbo, Zhang Kongyuan, Yang Kang, Liu Chenguang
(StateKeyLaboratoryofHeavyOilProcessing,CNPC,KeyLaboratoryofCatalysis,ChinaUniversityofPetroleum,Qingdao,Shandong266555)
A series of Pd-Au/Al2O3catalysts modified by different amount of alkali metal K or Li were prepared by incipient wetness impregnation and characterized by low temperature nitrogen adsorption, FT-IR and H2-TPR techniques. The isoprene was used to evaluate the selective hydrogenation performance of the modified catalysts. The FT-IR results show that only Lewis acid sites exist on the catalysts, no Bronsted acid is found. The acid strength of K-modified catalyst is weaker than Li-modified catalyst. The H2-TPR results indicate that Pd-Au binary alloy is formed, the reduction peaks of catalysts shift to higher temperature after modified by alkali metals. The reaction results of isoprene selective hydrogenation on the modified Pd-Au/Al2O3catalysts show that the isoprene conversion and isopentenes selectivity increase when addition of K2O. The LiO modification reduces the conversion of isoprene but isopentenes selectivity increases. At 70 ℃, isoprene conversion reaches 90.0%, isopentenes selectivity is 86.0% on the catalyst Pd-Au/Al2O3with 1.2% K2O.
alkali metal; Pd-Au/Al2O3; Lewis acid; Pd-Au binary alloy; isoprene
2014-05-04; 修改稿收到日期: 2014-08-21。
王宗波,硕士,石油与天然气加工专业。
张孔远,E-mail:zkyuana@126.com。
国家重点基础研究发展计划项目(2010CB226905);国家自然科学基金项目(21176258,U1162203)。

