持续输注小剂量右美托咪定对瑞芬太尼全凭静脉麻醉后痛觉过敏的影响
杨静远,刘继鑫,王东昕
(吉林省肿瘤医院 麻醉科,吉林 长春130012)
瑞芬太尼以其优良药代动力学特性,已成为临床上常用的麻醉性镇痛药。但大剂量使用后,会出现痛觉过敏的现象[1,2]。表现为难以控制的疼痛、寒颤、躁动等不良反应,还可能诱发心脑血管意外,危及围麻醉期安全。盐酸右美托咪定(dexmedetomidine,Dex) 是高选择性α2肾上腺素受体激动药,具有抗交感神经活性并能产生一定的镇静、镇痛作用。本研究观察在创伤较大的开胸肺叶切除术中持续输注小剂量的右美托咪定,对大剂量使用瑞芬太尼麻醉苏醒期痛觉过敏的影响,为右美托咪定在临床应用提供一定的理论依据。
1 资料与方法
1.1研究对象
选择开胸肺叶切除术患者60例,(ASA Ⅰ-Ⅱ级),年龄30-60岁,体重46-75 kg。随机均分法分成观察组(D组)和对照组(C组),每组30例。排除有心脑血管系统疾病史、精神神经系统疾病史或听觉障碍者,镇痛药物乱用或酒精成瘾者,肝肾功能不全和右美托咪啶过敏者。
1.2麻醉方法手术前30 min肌注阿托品0.5 mg。入室开放静脉通路,给予晶胶(按1∶1)予扩容治疗,麻醉前约注入250 ml。监测ECG、SBP、SpO2,行挠动脉穿刺置管有创血压监测 (SBP/DBP、MAP),麻醉后监测呼气末二氧化碳分压(PETCO2)。D组患者于麻醉诱导前10 min开始静脉泵注右美托咪定0.2 μg·kg-1·h-1,至手术结束前30分钟停药,C组只给生理盐水。麻醉诱导:静脉注射咪达唑仑0.05 mg/kg、丙泊酚效应室3 μg/ml、瑞芬太尼效应室4 ng/ml、顺式阿曲库铵0.15 mg/kg诱导,气管插双腔管,机械通气,维持PETCO2于35-40 mmHg。麻醉维持:丙泊酚效应室1.5-4 μg/ml、瑞芬太尼效应室1.5-4 ng/ml、间断每30 min静注顺式阿曲库铵0.05 mg/kg维持肌松。所有患者均在手术结束前30-45 min停用肌松剂,结束前10 min 停止输注丙泊酚和瑞芬太尼,静注芬太尼2 μg/kg作为术后镇痛负荷量,出室前接镇痛泵。两组患者拔除气管导管指标为自主呼吸恢复,潮气量不低于6 ml/kg,PETCO2<45 mmHg时,不吸氧条件下脉搏氧饱和度不低于95%,吞咽、咳嗽反射恢复,呼之睁眼。拔除气管插管后观察 15-30 min,待生命体征平稳后再送回胸科苏醒室。
1.3观察指标(1)记录术前(T0)、术后5 min(T1)、拔管时 (T2) 、拔管后5 min (T3)、拔管后10 min (T4)、拔管后30 min (T5)时 MAP、HR和 SpO2值。(2)记录两组患者自主呼吸恢复时间(停止瑞芬太尼至自主呼吸恢复)、苏醒时间(停止瑞芬太尼至呼之睁眼)、拔管时间(停止瑞芬太尼至拔除气管导管)、定向力恢复时间(停止瑞芬太尼至定向力恢复)。(3)观察组患者拔管后5 min (T3)、拔管后10 min (T4)、拔管后30 min (T5)时静息疼痛评分VAS和镇静评分Ramsay。(4)记录术后30分钟内不良反应,包括术后躁动、寒颤、恶心呕吐、呼吸抑制。

2 结果
2.1 D组术后各时点(T1-T5)MAP、HR均低于C组(P<0.05),各时点(T1-T5)MAP与T0比较无统计学意义(P>0.05),HR均低于T0(P<0.05)。C组术后各时点(T1-T5)MAP、HR均高于T0(P<0.05)。SpO2组间及组内比较均无统计学意义(表1)。
2.2两组患者自主呼吸恢复时间、苏醒时间、拔管时间、定向力恢复时间组间比较无统计学意义(P>0.05)(表2)。

表1 两组患者各时点MAP、HR、SpO2比较
注:组间比较,aP<0.05;组内与T0比较,bP<0.05

表2 两组患者自主呼吸恢复时间、苏醒时间、拔管时间、定向力恢复时间
注:组间比较,P>0.05
2.3 两组拔管后5 min,10 min,30 min疼痛评分和镇静评分D组均优于C组(P<0.05)(表3)。
2.4 术后不良反应比较D组优于C组(P<0.05)。术后躁动、寒颤发生率C组高于D组(P<0.05) (表4)。

表3 两组患者拔管后VRS疼痛评分和Ramsay镇静评分
注:组间比较,aP<0.05
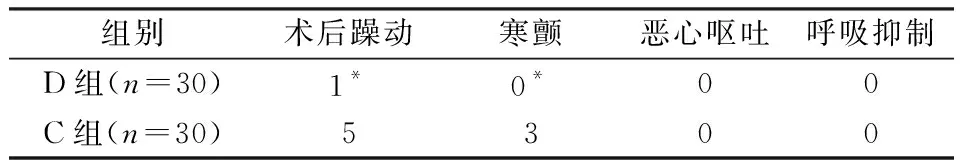
表4 两组患者不良反应发生情况(例 n=30)
注:组间比较,*P<0.05
3 讨论
阿片类镇痛药使用后还能激活体内的促伤害机制,导致机体对疼痛的敏感性增高,使术后镇痛药物的需要量增加,即阿片诱导的痛觉过敏 (opioid-induced hyperalgesia,OIH)[2]。这一现象在使用超短效阿片类药物瑞芬太尼时更容易发生[3],这种痛觉过敏是全身性的,表现为难以控制的疼痛、寒颤、躁动等不良反应,还可能诱发心脑血管意外,危及围麻醉期安全,影响术后康复。
瑞芬太尼诱发痛觉过敏的机制较复杂,其主要原因是瑞芬太尼停药后出现阿片受体的失活产生急性阿片耐受和中枢NMDA受体的激活,脊髓背角神经元的敏感化,中枢敏感化是主要原因[4]。同时脊髓强啡肽的释放、细胞内cAMP水平的上调等形成了痛觉过敏的发生机制。JOLYV认为在疼痛过敏出现前应早做防范[5],而目前防范瑞芬太尼术后痛觉过敏还没有特别有效的方法,常用措施有术毕使用小剂量长效阿片类药物如芬太尼、苏芬太尼、曲马多等和NMDA受体拮抗剂氯胺酮、硫酸镁等。其中长效阿片类药物同样会激活中枢NMDA受体,只是通过镇痛作用掩盖了痛觉过敏的症状,氯胺酮、硫酸镁等又会产生新的不良反应。
盐酸右美托咪定是高选择性的а2肾上腺素能受体激动剂,α2肾上腺素能受体广泛存在于中枢神经系统、外周神经和自主神经节中,а2受体分为四个亚型,即α2A、α2B、α2C和α2D受体亚型,右美托咪定能激动所有а2受体亚型产生临床效应。右美托咪定通过兴奋蓝斑和延髓α2A/D受体发挥中枢性镇静、抗交感活性等效应,通过作用于脊髓后角的突触后膜上的α2A受体发挥镇痛效应。而在初级感觉神经元中也含有α2A和α2C亚型,兴奋后还能减弱外周疼痛信号向中枢的传递。目前研究认为,α2A/D受体亚型介导了右美托咪定的麻醉和镇痛作用[6,7]。有研究表明,右美托咪定还能抑制NMDA受体介导的突触后电位的作用,从而抑制初级传入神经元的突触传递产生抗伤害性刺激作用[8]。α2A受体激动时还可抑制腺苷酸环化酶活性,使细胞内cAMP降低,从而减低了神经元的兴奋性。这些均可能是右美托咪定对抗痛觉过敏的机制。
开胸肺叶切除手术,涉及到皮肤、肌肉、肋骨、甚至胸膜和肋间神经的损伤,创伤较大,手术时间多在两个小时以上,瑞芬太尼用量较大,停药后更易发生痛觉过敏现象,局部的疼痛和全身性的痛觉敏化会诱发和加重术后躁动[9]、寒颤等不良反应的发生率。本研究中D组术后镇痛、镇静评分均好于C组,因此,对痛觉过敏的预防也减少了术后躁动、寒颤等不良反应的发生。
右美托咪啶对血流动力学的影响,受剂量和给药速度的影响,快速给予负荷量可直接激活血管平滑肌内的α2B受体产生的血管收缩作用,引起短暂的血压升高,反射性降低心率。缓慢注射(超过10 min)或肌注可减弱这种高血压反应,产生的效果几乎完全是抗交感神经的作用仅表现为降压效应[10]。持续输注可产生稳定的中枢性抗交感和增加迷走活性的作用,血压和心率可发生中度下降。本研究实验组以0.2 μg·kg-1·h-1静脉泵注只表现出稳定血压和心率的作用没有出现严重的低血压和心动过缓,两组患者自主呼吸恢复时间、苏醒时间、拔管时间、定向力恢复时间均无统计学差异。
本研究表明,术中持续静脉泵注小剂量右美托咪定能减轻瑞芬太尼麻醉术后的痛觉过敏,稳定血流动力学,并能减轻不良反应的发生,不影响苏醒时间,提高术后病人质量,有利于患者的恢复。
参考文献:
[1] Angst M S,Koppert W,Pahl I,et al.Short-term infusion of the mu-opioid agonist remifentanil in humans causes hyperalgesia during withdrawal [J].Pain,2003,106:49.
[2]Silverman SM.Opioid induced hyperalgesia:clinical implications for the pain practitioner [J].Pain Physician,2009,12(3):679.
[3]Derrode N,I ebrun F,Levron JC,et al.Influence of preoperative Opioid on postoperative pain after major abdominal surgery:sufentanil TCI versus remifentanil TCI. A ran-domized,controlled study[J].Br J Anaesth,2003,91(6):842.
[4]Dirks J,Miniche S,Hilsted KL,et al.Mechanisms of postoperative pain:clinical indications for a contribution of central neuronal sensitization[J].Anesthesiology,2002,97:1591.
[5]Joly V,Richebe P,Guignard B,et al.Remifentanil- induced postoperative Hyperalgesia and its prevention with small-dose ketamine[J].Anesthesiology,2005,103(1):147.
[6]Aantaa R,Marjamaki A,Scheinin M.Molecular pharmacology of α2-adrenoceptor subtypes[J].Ann Med,1995,27(4):439.
[7]宋 威.右美托咪定的药理和临床研究[J].国外医学合成药生化药制剂分册,2001,22(2):106.
[8]Faber ES,Chambers JP,Evans RH,et al.Depression of NMDA receptor-mediated synaptic transmission by four a2 adrenoceptor agonists on the in vitro rat spinal cord Preparation[J].Br J Clin Pharmacol,1998,124:507.
[9]邓立琴,丁凤兰,刘 红.全麻术后躁动225例分析[J].实用医学杂志,2006,22(2):165.
[10]Sagen J,Proudfit HK.Evidence for pain modulation by pre- and postsynaptic noradrenergic receptors in the medulla oblongata[J].Brain Res,1985,331:285.

