胰管支架向内移位的原因分析及启示
张亚萍 潘小平
(内蒙古科技大学包头医学院第二附属医院,包头市 014030)
·个案报告·
胰管支架向内移位的原因分析及启示
张亚萍 潘小平*
(内蒙古科技大学包头医学院第二附属医院,包头市 014030)
目的通过分析胰管支架向近端移位的原因,探讨如何预防其发生。方法追踪观察1例胰管支架向内移位特殊病例的治疗全过程。结果胰管支架置入术后可以向内移位,使用十二指肠活检钳能取出移位支架。结论置入胰腺支架的技术水平要求较高,如何选择合适的支架是本技术的关键。活检钳可以作为移除胰管支架的工具。
胰管支架;逆行性胰胆管造影;胰腺炎;并发症
胰管支架置入术(pancreatic duct stenting)是预防逆行性胰胆管造影(endoscopic retrograde cholangio-pancreatography,ERCP)术后胰腺炎的有效方法[1]。大量临床研究表明[2],胰管支架置入可以降低具有高危因素患者ERCP术后胰腺炎的发生率,并可以减少患者住院费用和住院时间。但此项技术具有高风险和高难度,甚至可以发生严重的并发症,其中包括重度胰腺炎、早期支架移位、穿孔、出血和感染等[3]。我们在此项技术实施过程中,发生1例术后4个月胰管支架向内移位(胰尾方向)的病例,现报告如下。
1 临床资料
1.1 病例简介 患者女性,74岁,因“无诱因出现右上腹部持续性胀痛,向背部放散1月”就诊。超声波检查提示:胆囊切除术后,胆总管扩张,胆总管下段结石。以“胆总管结石”收入院。查体:生命体征平稳,巩膜及全身无黄染,心肺未闻及杂音。腹部平软,未见静脉曲张,右上腹压痛明显、无反跳痛及肌紧张。肝肋下未触及。辅助检查:核磁共振水成像(MRCP)示胆囊切除术后改变,胆总管下段多发结石伴低位不全胆道梗阻。实验室检查血常规正常,肝肾功能及血尿淀粉酶未见异常,心电图及肺功能正常。
1.2 手术方法 入院3 d后行ERCP术。因为胆总管多发结石,故同时行十二指肠乳头切开术(EST)、胆总管网篮取石术和鼻胆管引流术(ENBD)。考虑到十二指肠乳头憩室和术中导丝和造影剂反复进入到胰管内,为预防术后胰腺炎的发生,故行胰管支架置入术(见图1)。胰管支架型号为美国COOK公司生产的GPSO-5-5塑料支架。
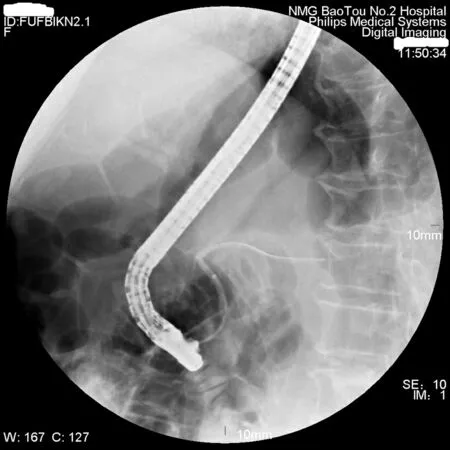
图1 置入胰管支架
1.3 术后情况 术后患者生命体征平稳,临床症状反应轻微。实验室检查血尿淀粉酶明显增高,脂肪酶正常,故采取禁食水,使用抑制腺体分泌药物等处理措施,3 d后血尿淀粉酶恢复正常,拔除鼻胆管,防止拔除胰管支架在短时间内对胰腺造成二次损伤,建议出院观察,3个月再行胰管拔除术。
1.4 再次手术 4个月后患者因“胰管支架拔除”入院。腹部平片示胰管支架向内移位(胰尾方向)。超声提示:胰头后方条状强回声,胰腺大小形态正常,回声均匀,胰管无扩张。实验室检查未见异常。术前讨论考虑为胰管支架长时间放置导致支架移位,并准备了球囊、圈套器、活检钳等取支架器材。术中首先用Olympus TJF 260型电子十二指肠镜做ERCP,通过胰管造影显示支架在胰管内位置;胰管轻度扩张,可以将活检钳插入到胰管内,所以在X射线监视下,将十二指肠活检钳插入到胰管内夹住支架头端(见图2);缓慢拉出支架(见图3)。
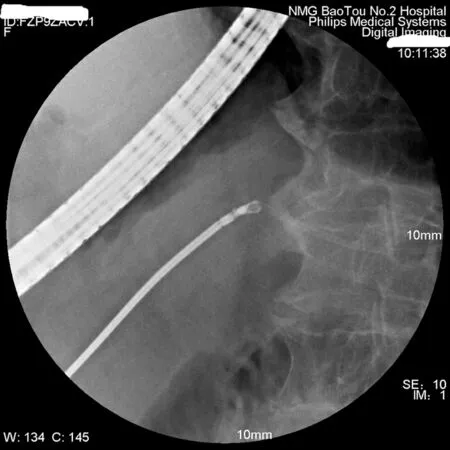
图2 活检钳夹取胰管支架

图3 取出后的胰管支架
1.5 结果 术后患者再次出现急性胰腺炎症状。腹痛明显,血淀粉酶增高至785 u/L,尿淀粉酶增高至12 866 u/L,脂肪酶增高至2 910 u/L。给予禁食水、抑制胰液分泌、抗感染等对症治疗,1周后血尿淀粉酶及脂肪酶恢复正常,CT检查胰腺未见异常,痊愈出院。
2 讨 论
虽然胰管支架置入术预防ERCP术后胰腺炎的效果肯定,但此项技术操作难度大,术后容易产生严重并发症,而且术后需再次行内镜操作取出胰管支架,可能增加组织损伤的机会,故所有学者都认为应该谨慎地对待[4]。
2.1 支架向内移位的原因 胰管支架置入术后并发胰管支架移位,绝大多数是在置入早期支架向外(胰头方向)移位,支架脱出后无法起到引流胰液的作用,胰腺炎症状明显。置入后期胰管支架向内移位(胰尾方向)仅见到个案报道,且原因各不相同。根据本病例实际情况分析,我们认为胰管支架向内移位的主要原因有:①胰管支架置入过深,外侧端支架倒刺置入过程中未张开,无法阻止支架向内移位;②胰管支架靠近胰尾侧倒刺随着胰液向外流动反而向内使力,如同虾向前使力而身体向后移动的原理;③此患者胰管在胰头部成角,使支架的大部分位于成角内侧,根据杠杆原理,利于支架向内移位。
2.2 操作要点
2.2.1 支架的选择 从理论上讲,胰管支架置入可以降低ERCP术后胰腺炎的发生率。但由于胰管狭小、曲折而使导丝或支架置入失败,则反而容易提高胰腺炎的发生率。所以选择合适的支架是此项技术的重要环节。采用3F短小支架可明显提高困难的胰管支架置入成功率,从而避免了因支架置入失败造成的风险。但支架在置入过程中不易掌控,而且还要大大增加患者的经济负担。而5F胰管支架将有效改善操控方面的问题,对未见扩张的胰管插入相对困难。如何选择要参考操作者的习惯手法。
2.2.2 造影剂的使用 在使用造影剂方面,不同类型造影剂引发胰腺炎的研究还未完全定论,但造影剂会诱发胰腺炎是不争的事实。造影剂的渗透压及离子浓度被认为是引起造影后不良反应的主要因素。所以推荐使用低渗透压的造影剂,最好是非离子型的,可减少ERCP术后并发症的发生。
2.2.3 术后护理 胰管支架置入术后的护理非常重要,可以有效降低胰腺炎发生率。行ERCP常规护理、一级护理、胃肠减压。常规规范使用抗感染、保肝、保护胃黏膜等药物。根据血清淀粉酶的指标及临床症状决定使用减少胰液分泌的药物时间。因胆道系统疾病行ERCP术的患者常规使用鼻胆管引流,一周后作鼻胆管造影,行鼻胆管拔出术和胰管支架取出术。
2.3 启示
2.3.1 胰管支架置入术的技术水平要求高,任何小的操作失误都可能产生严重后果。本病例因支架置入时外侧端支架倒刺未张开,给支架向内移位创造了条件。因此,我们建议准备开展此项技术的机构,必须到培训基地进行系统化训练,熟练掌握ERCP的操作技巧,并规范医疗措施,操作力求准确。
2.3.2 术前讨论中,我们认为圈套器、球囊及活检钳等都可以作为胰管支架取出的器械。实践证明,如果胰管支架扩张,十二指肠活检钳可以取出已深入到胰管内的支架。
2.3.3 病人在胰管支架取出后出现急性胰腺炎症状,考虑为支架取出过程中损伤了胰腺组织。同时我们认为胰管支架长时间置入(4个月)也是发生胰腺炎的原因之一。因此胰管支架不宜长时间放置,当病情稳定后须尽快拔除。
2.3.4 有关胰管支架的选择。Freeman等[5]采用短小支架(2~3 cm,3F~5F),可明显提高困难的胰管支架置入成功率,从而避免了因支架置入失败造成的风险。Rashdan等[6]回顾性的研究认为3F~4F胰管支架与传统使用的5F~6F的胰管支架相比,预防ERCP术后胰腺炎更为有效。我们在实际操作过程中发现,3F胰管支架在置入过程中不易掌控,而且还大大增加患者的经济负担。而5F胰管支架可有效改善操控方面的问题,有利于手术顺利完成,这可能与操作者的习惯手法有关。如果采用COOK公司生产的胰管支架,我们多数将插入胰腺端的倒刺切除,以减少拔出过程中倒刺对胰管的损失和防止再次发生向内移位的并发症。
综上所述,虽然胰管支架置入术可以预防ERCP术后胰腺炎的发生,同时其手术风险不可回避,所以要谨慎对待此项技术的开展。
[1] Pan XP,Dang T,Meng XM,et al.Clinical study on the prevention of post-ERCP pancreatitis by pancreatic duct stenting[J].Cell Biochemistry and Biophysics,2011,61(3):473-479.
[2] Fazel A,Quadri A,Catalano MF,et al.Does a pancreatic duct stent prevent post-ERCP pancreatitis? A prospective randomized study[J].Gastrointest Endosc,2003,57(3):291-294.
[3] Andriulli A,Forlano R,Napolitano G,et al.Pancreatic duct stents in the prophylaxis of pancreatic damage after endoscopic retrograde cholangiopancreatography:a systematic analysis of benefits and associated risks[J].Digestion,2007,75(2-3):156-163.
[4] Freeman ML.Pancreatic stents for prevention of post-endoscopic retrograde cholangiopancreatography pancreatitis[J].Clin Gastroenterol Hepatol,2007,5(11):1354-1365.
[5] Freeman ML,Overby C,Qi D.Pancreatic stent insertion:consequences of failure and results of a modified technique to maximize success[J].Gastrointest Endosc,2004,59(1):8-14.
[6] Rashdan A,Fogel EL.Improved stent characteristics for prophylaxis of post-ERCP pancreatitis[J].Clin Gastroenterol Hepatol,2004,2(4):322-329.
Analysisofthecauseofproximalmigrationofpancreaticstentafterendoscopicretrogradecholangiopancreatographyanditsimplication
ZHANGYaping,PANXiaoping
(TheSecondAffiliatedHospitalofBaotouMedicalCollege,InnerMongoliaUniversityOfScienceandTechnology,Baotou014030,P.R.China)
ObjectivesTo analyze the cause of proximal migration of pancreatic stent after endoscopic retrograde cholangiopancreatography (ERCP ), aiming at exploring its prevention methods.MethodsThe whole treatment period of one rare case of proximal migration of pancreatic stent after ERCP was reviewed.ResultsPancreatic stent migrated proximally after ERCP, and the migrated stent could be removed by using duodenal biopsy forceps.ConclusionsPancreatic stenting requires high technical skills, and choosing the right stent is crucial to the success of ERCP. Biopsy forceps can be used to remove the migrated pancreatic stent.
Pancreatic stent; Endoscopic retrograde cholangiopancreatography; Pancreatitis; Complications
张亚萍(1971~),女,大专,主管护师,研究方向:高级护理。
R 657.5
B
1673-6575(2014)01-0099-03
10.11864/j.issn.1673.2014.01.32
2013-12-07
2014-01-21)
*通讯作者

