硫化温度对NiW/Al2O3催化剂加氢脱硫性能的影响
倪雪华,龙湘云,聂 红,陈文斌,刘清河
(中国石化 石油化工科学研究院,北京100083)
硫化温度是决定加氢催化剂硫化效率的关键因素之一,有关硫化温度对加氢催化剂硫化行为和催化性能的研究时见报道。Okamato等[1-3]以 H2S为硫化剂研究了硫化温度对CoMo/SiO2和CoW/SiO2催化剂催化性能的影响,发现这2种催化剂均存在最佳硫化温度。他们认为,一方面,高温能够阻碍Co9S8的形成,有利于活性中心由TypeⅠ变为TypeⅡ,从而提高HDS活性;另一方面,高温硫化会减少边缘活性位数量,不利于催化活性的提高,两方面的作用导致了最佳硫化温度的出现。对于NiW 催 化 剂,Van der Vlies等[4-5]的 研 究 表 明,W—O键的强度强于Mo—O键,使得W氧化物需要更高的硫化温度才能转变为W硫化物,而W硫化度是影响催化剂活性的关键因素[6-8]。与CoMo系催化剂相似,NiW系催化剂同样存在最佳硫化温度[9-10]。笔者认为,NiW系催化剂上Ni的存在物种有在催化剂表面高度分散的NiO物种、Ni-W混合氧化物和载体内部具有尖晶石结构的NiAl2O43种。随着硫化温度的提高,一方面,Ni物种的硫化度以及WS2的结晶度提高,均有利于催化活性的提高;另一方面,WS2晶粒在873K时[9]开始出现少量烧结,表面的Ni物种进入载体Al2O3中的四面体空隙内部,形成NiAl2O4尖晶石,使其活性降低。因此NiW系催化剂的硫化温度应控制在适宜的范围。
尽管有关硫化温度对催化剂性能的影响有较多报道,但这些研究主要以不含有机络合剂的加氢催化剂为考察对象,而对于含有络合剂的加氢催化剂,尤其是高压硫化条件下的研究报道则较为少见。对于硫化温度对络合类催化剂性能的影响,此前曾报道了柠檬酸对NiW/Al2O3催化剂硫化行为的影响[11],但考察的硫化温度局限于473~633K范围,而对更高硫化温度下催化剂的硫化行为还未进行研究,因而难以确定最佳硫化温度。本研究中,笔者考察了含柠檬酸的NiW/Al2O3催化剂在4.0MPa氢分压下、523~723K硫化温度范围内的硫化行为和加氢脱硫活性,旨在从更宽的温度范围和一定的硫化压力下,揭示硫化温度影响含柠檬酸NiW/Al2O3催化剂催化活性的作用本质,同时确定获得最佳脱硫性能的硫化温度。
1 实验部分
1.1 原料和试剂
硝酸镍、环己烷,分析纯,北京益利精细化学品有限公司产品;偏钨酸铵,工业级,株洲钻石钨制品有限公司产品;柠檬酸,食品级,齐茂催化剂有限公司产品;正癸烷,分析纯,天津科密欧化学试剂有限公司产品;4,6-二甲基二苯并噻吩,分析纯,J&K Chemical产品;十氢萘,分析纯,北京化工厂产品。
1.2 催化剂的制备
采用孔饱和浸渍法,以Ni-W-柠檬酸溶液(偏钨酸铵、硝酸镍和柠檬酸以一定比例混合的水溶液)浸渍工业氧化铝载体,393K干燥,制得含柠檬酸的NiW/Al2O3催化剂,以NiWCA表示,其中,柠檬酸与Ni的摩尔比为1。同样,以Ni-W溶液(偏钨酸铵和硝酸镍以一定比例混合的水溶液)浸渍工业氧化铝载体,393K干燥后再于723K活化,制得NiW/Al2O3催化剂,以NiW表示。所制备的催化剂中,NiO和WO3的负载量均分别为3.1%和20.1%。
1.3 催化剂的硫化和催化4,6-DMDBT脱硫反应
在高压微型反应器加氢试验装置中进行催化剂的硫化和评价其对4,6-DMDBT的催化脱硫活性。在反应管恒温区内装填1g 40~60目的催化剂,其余部分装填40~60目处理过的石英砂,催化剂与石英砂中间用耐高温的玻璃布隔开。以含5%质量分数CS2的环己烷作为硫化油,流速0.4mL/min,在4.0MPa分压、流速400mL/min的氢气流下原位硫化4h,硫化温度分别为523、573、623、673和723K。硫化结束,在N2保护下,将硫化态催化剂倒入环己烷中封存。
将40~60目的催化剂样品约0.15g和处理过的40~60目的石英砂1g均匀混合,置于反应器恒温段内,其余部分装填石英砂。采用上述相同方法进行硫化,硫化结束,保持同样氢气流速和压力,切换反应油,流速保持0.2mL/min。反应油为质量分数为0.45%4,6-DMDBT和等量十氢萘的正癸烷溶液。反应在553K下稳定3h后取样分析,然后将温度分别降至533和523K稳定1h后取样分析。从反应器流出的反应产物经水冷却,在高压分离器中定期收集液体产物,采用Agilent 7860系列气相色谱仪分析其组成。
在测定原料和产物中4,6-DMDBT的含量时,以十氢萘为内标物,计算4,6-DMDBT的转化率(x)、反应产物中组分i的选择性(si)、脱硫反应总活性(AT)、直接脱硫活性(ADDS)和加氢脱硫活性(AHYD)[11]。4,6-DMDBT 加氢脱硫反应有直接脱硫(DDS)和加氢脱硫(HYD)2条主要路径。DDS路径中,含硫化合物分子中的C—S键直接断裂而使S脱除,产物为二甲基联苯(DMBiPh);HYD路径中,含硫化合物分子中与S相邻的苯环先被加氢,之后再发生C—S键断裂,产物为二甲基环己基苯(DMCHB)和二甲基联环己烷(DMBCH);加氢未脱硫(HN)的产物为六氢-4,6-二甲基二苯并噻吩[11]。
4,6-DMDBT加氢脱硫反应为拟一级动力学反应,由此可以据实验数据计算4,6-DMDBT加氢脱硫反应的反应速率常数和反应的表观活化能,见式(1)~(3)。
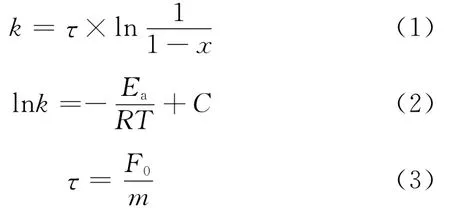
式(1)~(3)中,τ为空速,mol/(kg·s);x为转化率,%;k为4,6-DMDBT加氢脱硫反应速率常数,mol/(kg·s);Ea为4,6-DMDBT加氢脱硫反应活化能,kJ/mol;R为气体常数;T为反应温度,K;C为常数;m为催化剂的质量,kg;F0为单位时间内原料的流速,mol/s。
1.4 催化剂的表征
采用Thermo Scientific公司ESCALab 250型X射线光电子能谱仪对催化剂样品进行XPS表征。激发源为单色化的AlKαX射线,功率约300W,分析室的基础真空约为3×10-7Pa,以C1s峰(284.6eV)进行能量校正。
采用FEI公司Tecnai G2F20S-TWIN高分辨透射电镜对催化剂样品进行HRTEM表征。加速电压200kV。统计计算500个以上层状晶粒的长度和层数,得到晶粒的尺寸分布。根据公式(4)和(5)计算WS2晶粒的平均长度)和平均堆叠层数()。
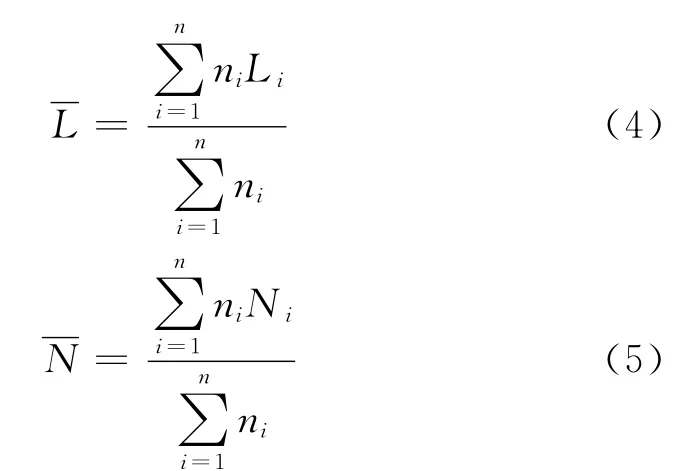
式(4)、(5)中,i为照片数;n为每张照片上的WS2晶粒数量;L为每张照片上WS2晶粒的平均长度;N为每张照片上WS2晶粒的平均堆叠层数。
2 结果与讨论
2.1 硫化温度对NiWCA和NiW催化剂催化4,6-DMDBT加氢脱硫反应性能的影响
2.1.1 对催化活性的影响
图1为 NiWCA 和 NiW 催 化 剂 催 化4,6-DMDBT加氢脱硫反应总活性(AT)随其硫化温度(T′)的变化,加氢脱硫反应温度553K。由图1可知,2种催化剂催化4,6-DMDBT加氢脱硫反应的AT随其T′的变化规律相同。随着T′的升高,2种催化剂的AT均提高;623K以后,AT的增速减缓,673K时出现峰值;继续升高至723K时,AT出现不同程度的回落,与高晓东[12]对于NiW催化剂的研究结果一致。由图1还可看到,在所有T′下,络合方法制备的NiWCA催化剂的AT均高于常规方法制备的NiW催化剂,表明柠檬酸的存在有利于提高催化剂的反应活性,与聂红等[11]和Rinaldi等[13]的研究结果一致。

图1 NiWCA和NiW催化剂催化4,6-DMDBT的加氢脱硫总活性(AT)随硫化温度(T′)的变化Fig.1 Hydrodesulfurization activity(AT)of NiWCA and NiW catalysts for 4,6-DMDBT vs their sulfuration temperature(T′)
2.1.2 对反应产物选择性的影响
表1给出了NiWCA和NiW催化剂催化4,6-DMDBT加氢脱硫反应产物选择性(sHYD)和直接脱硫产物选择性(sDDS)随其硫化温度(T′)的变化。从表1可知,对于NiWCA催化剂,随着T′的升高,sHYD不断增加,而sDDS和加氢未脱硫产物HN选择性(sHN)不断降低;当T′由623K升至673K时,sHYD、sDDS和sHN均变化不大;当T′进一步升高至723K时,sHYD降低,而sDDS和sHN相应增加;sDDS和sHN与sHYD基本呈现相反的变化趋势,而sHYD的变化趋势则与AT的变化趋势相一致。对于NiW催化剂,随其T′的升高,sHYD和sDDS的变化趋势与NiWA一致。在所有T′下含柠檬酸催化剂的sHYD均略高于不含柠檬酸催化剂的sHYD,表明柠檬酸的存在不影响4,6-DMDBT产物选择性的变化规律,但可以略提高sHYD。

表1 不同硫化温度(T′)下NiWCA和NiW催化剂催化4,6-DMDBT加氢脱硫、直接脱硫和加氢未脱硫产物的选择性(sHYD、sDDS和sHN)Table 1 sHYD,sDDSand sHNof 4,6-DMDBT over NiWCA and NiW catalysts sulfided at various sulfuration temperatures(T′)
2.1.3 对反应活化能的影响
根据Arrhenius方程,以温度的倒数1/T为横坐标,反应速率常数k的对数lnk为纵坐标作图,求得不同T′下4,6-DMDBT加氢脱硫反应的活化能Ea和指前因子A。在4.0MPa氢分压下,523~723K硫化的NiWCA和NiW催化剂催化4,6-DMDBT加氢脱硫反应的活化能数据列于表2。由表2可以看出,对于NiWCA催化剂,623K是一个关键性的硫化温度。采用该温度硫化NiWCA催化剂时4,6-DMDBT加氢脱硫反应的活化能Ea显著高于采用523和573K硫化时的Ea,硫化温度超过623K后,Ea的变化明显趋缓。上述Ea随催化剂硫化温度的变化规律显示,与523和573K硫化的催化剂相比,623K的硫化更完全,催化剂上活性中心种类的主要存在形式发生了改变。低于623K硫化时,催化剂中形成的主要是活性较低的TypeⅠ类活性中心,623K及更高温度下硫化,则主要形成本征活性更高的TypeⅡ类活性中心[14]。NiW催化剂催化4,6-DMDBT加氢脱硫反应的Ea变化规律与采用NiWCA催化剂时的Ea较为一致,但在623~723K硫化温度范围内,NiW 催化剂的Ea在85~88kJ/mol范围,小于 NiWCA 催化剂的Ea(90~96kJ/mol)。
由表2还可看到,采用较低硫化温度(<623K)的催化剂,4,6-DMDBT加氢脱硫反应的HYD途径反应活化能低于DDS;而采用较高硫化温度(≥623K)的催化剂,HYD的反应活化能则高于DDS。前者与Kim等[15]在NiMo和CoMo体系低4,6-DMDBT转化率下(<50%)得到的结果一致,后者则与李丁建一[16]在NiMoP体系高4,6-DMDBT转化率(>50%)下得到的结果一致。这种HYD和DDS途径反应活化能的相对变化也在一定程度上反映了硫化温度对催化剂活性相的影响,即低温硫化时生成的Type I类活性中心与高温硫化时生成的Type II类活性中心对HYD途径和DDS途径的促进作用程度可能存在差异。
在Arrhenius方程中,指前因子A与催化剂的活性中心数相关,指前因子A值越大,则活性中心数量越多[17]。表2数据显示,对于NiWCA催化剂,随着硫化温度的升高,指前因子A增大,623K时A出现突跃,之后小幅上升,在673K时达到最大值;硫化温度进一步升高至723K时,指前因子数值变小。指前因子的变化与催化剂的活性变化趋势高度一致(见图1)。以上结果表明,催化剂活性中心的大量形成主要发生在573~623K的硫化温度区间,硫化温度高于623K之后,活性中心数量增长明显趋缓,在673K时活性中心数量达到顶峰。723K硫化时催化剂的活性、加氢脱硫反应活化能和指前因子均同步降低,可能是过高的硫化温度导致金属硫化物聚集所致。值得注意的是,在高于573K下硫化的NiWCA的A值均高于相同硫化温度NiW催化剂的A值,表明柠檬酸的加入有利于增加催化剂上的活性中心数量。
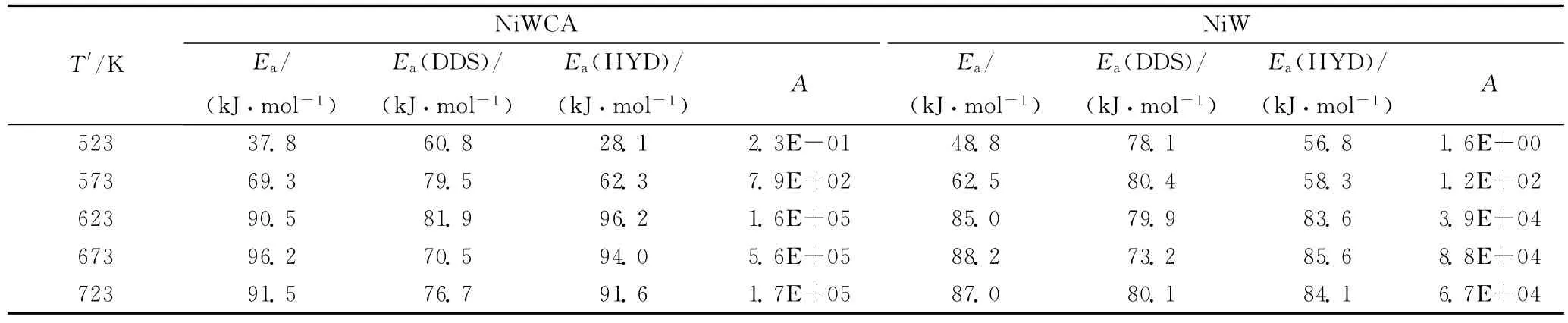
表2 不同硫化温度(T′)下NiWCA和NiW催化剂催化4,6-DMDBT加氢脱硫反应的表观活化能(Ea)和指前因子(A)Table 2 Active energies(Ea)and pre-exponential factors(A)of 4,6-DMDBT hydrodesulfurization reactions over NiWCA and NiW catalysts sulfided at various sulfuration temperatures(T′)
2.2 NiWCA和NiW催化剂的物性
2.2.1 XPS分析
对不同硫化温度下2种催化剂的W4fXPS谱进行拟合[18],结果示于图2。采用文献[18]的方法对W4f进行分峰拟合。523K硫化的硫化态NiWCA催化剂在结合能为35.7和37.9eV出现明显的双峰,归属于氧化态的 W6+物种[19-20];在32.3和34.4eV处的双峰对应于硫化态的 W4+物种[21];随着硫化温度的升高,W4+物种的特征峰不断增强,而W6+物种的特征峰逐渐减弱,表明更多的WO3被硫化为WS2物种。NiW催化剂W4f谱变化规律与NiWCA一致,即随着硫化温度的升高WS2物种的特征峰不断增强,而WO3的特征峰逐渐减弱。

图2 不同硫化温度(T′)下NiWCA和NiW催化剂的W4fXPS谱Fig.2 W4fXPS profiles of NiWCA and NiW catalysts sulfided at various sulfuration temperatures(T′)
为了定量表征催化剂上活性金属的硫化度随温度的变化规律和柠檬酸对金属硫化度的影响,在分峰拟合中统计了 W4+在所有 W物种中所占的百分数,以其表示W物种的硫化度,结果绘于图3。由图3可知,对于2种催化剂,活性金属W硫化度随硫化温度的变化规律与催化活性和W硫化度均随硫化温度的变化规律基本一致。在523~623K硫化温度范围内,催化剂脱硫催化活性和W硫化度均随硫化温度的升高快速上升,高于623K之后,活性和W硫化度增长速率均明显放缓。硫化过程中,Ni原子占据WS2边角位置形成的Ni-W-S相结构是加氢脱硫的主要活性相[11,22]。硫化度越高,意味着生成的WS2微晶数量越多,相应地生成Ni-W-S活性相的概率也越高。图3结果表明,含柠檬酸的催化剂W物种的硫化度明显高于不含柠檬酸的催化剂,与前述评价结果一致。柠檬酸能削弱载体与活性金属之间的相互作用,改善活性组分在载体上的分散状态,从而促进活性金属的硫化[23]。这是柠檬酸能提高催化剂催化活性的重要原因。

图3 不同硫化温度(T′)下NiWCA和NiW催化剂上W物种的硫化度Fig.3 W sulfuration degree of NiWCA and NiW catalysts sulfided at various sulfuration temperatures(T′)(1)NiWCA;(2)NiW
2.2.2 HRTEM 分析
不同温度硫化的NiWCA和NiW催化剂的HRTEM照片如图4所示。
从图4可以看出,随着硫化温度的升高,NiWCA和NiW催化剂中 WS2微晶[23]的数量不断增加,与前述XPS分析结果相一致。523K硫化的2种催化剂中均存在纳米尺寸的斑点状颗粒相,被认为是未结晶的W硫化物或硫氧化物颗粒[1,8];随着硫化温度的升高,斑点状颗粒相消失,条纹相增多,显示W物种的晶化程度提高。对于723K硫化的催化剂,可以观察到WS2微晶堆叠层数明显增加,尺寸明显增大。由图4还发现,在相同硫化温度下,NiWCA催化剂的WS2微晶数量均多于NiW,表明柠檬酸的存在有利于促进W金属的硫化,也与XPS得到的结果一致。

图4 不同温度硫化(T′)的NiWCA和NiW催化剂高分辨透射电镜照片Fig.4 HRTEM images of NiWCA and NiW catalysts sulfided at various sulfuration temperatures(T′)
为了定量比较不同硫化温度下WS2片晶的形貌特征,随机选取催化剂上的不同部位,拍摄高分辨透射电镜照片20张,对这20张HRTEM照片的条纹长度和堆叠层数进行了统计,并计算其平均长度和平均堆叠层数,结果列于表3。
从表3可以看出,随着硫化温度的升高,NiWCA和NiW催化剂中WS2微晶的和总体上均呈现增加趋势。Van der Meer等[10]和Okamoto等[1]在其研究中也发现了高温硫化时催化剂中金属硫化物长大的类似现象。NiWCA催化剂的WS2平均堆叠层数高于NiW,同时WS2晶粒平均长度也略大,是由于柠檬酸存在下金属-载体之间的相互作用减弱,在促进W金属硫化的同时,也导致倾向于形成尺寸和堆叠层数较高的WS2微晶。WS2晶粒变长会导致其边角位置减少,而堆叠层数增加又有利于TypeⅡ类活性相的形成,两个因素在对催化剂活性的影响方面在一定程度上具有抵消效应。
表3 不同硫化温度(T′)下硫化态NiWCA和NiW催化剂中WS2晶粒的平均长度)和平均堆叠层数Table 3 Average slab length)and average stacking number)of WS2particles in sulfided NiWCA and NiW catalysts at various sulfuration temperatures(T′)
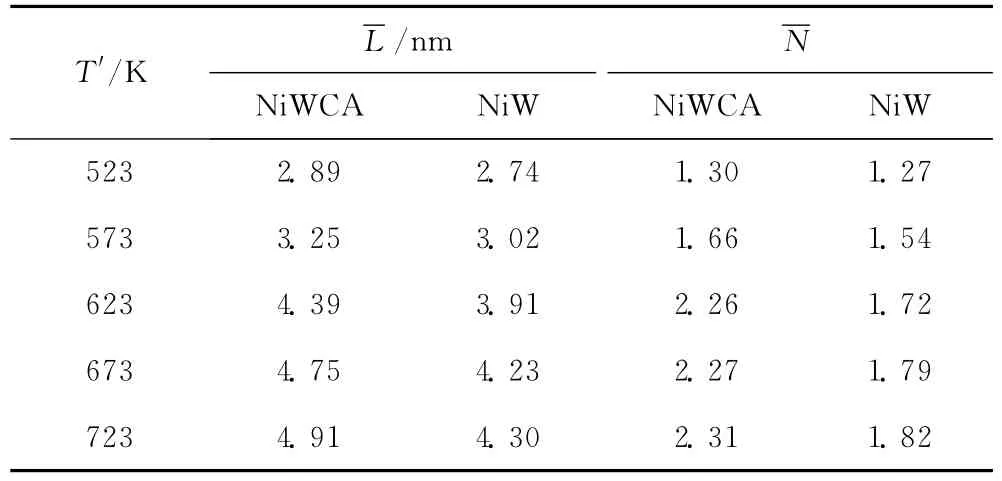
表3 不同硫化温度(T′)下硫化态NiWCA和NiW催化剂中WS2晶粒的平均长度)和平均堆叠层数Table 3 Average slab length)and average stacking number)of WS2particles in sulfided NiWCA and NiW catalysts at various sulfuration temperatures(T′)
T′/K L/nm N NiWCA NiW NiWCA NiW 523 2.89 2.74 1.30 1.27 573 3.25 3.02 1.66 1.54 623 4.39 3.91 2.26 1.72 673 4.75 4.23 2.27 1.79 723 4.91 4.30 2.31 1.82
3 结 论
(1)在所考察的实验条件下,含柠檬酸的NiWCA催化剂和无柠檬酸的NiW催化剂最佳硫化温度均出现在673K左右。硫化温度对于2类催化剂的影响表现出基本相似的规律。硫化温度升高,一方面导致W物种硫化度增加,生成的WS2微晶数量增多,另一方面使WS2晶粒尺寸变大。在相对较低的温度范围(523~623K)内,硫化温度升高,W物种硫化度和催化剂活性均快速提高,二者的变化具有一致性,W物种硫化度是影响催化剂活性的主导因素;在相对较高的温度范围内(623~723K),硫化温度升高,W物种硫化度缓慢增长,WS2晶粒尺寸增大带来的负面因素逐渐显著,催化剂活性同时受到上述两方面因素的双重影响。
(2)含柠檬酸的NiWCA催化剂的加氢脱硫活性明显高于无柠檬酸的NiW催化剂。柠檬酸的存在一方面提高了W物种的硫化度,有利于生成更多的活性中心;另一方面也导致生成较大的WS2微晶,不利于活性相的形成。前者对于催化剂活性的提高具有关键性的意义。
[1]OKAMOTO Y,KATO A,USMAN,et al.Effect of sulfidation temperature on the intrinsic activity of Co-MoS2and Co-WS2hydrodesulfurization catalysts[J].J Catal,2009,265(2):216-228.
[2]OKAMOTO Y,KATO A,USMAN,et al.Intrinsic catalytic activity of SiO2-supported Co-Mo and Co-W sulfide catalysts for the hydrodesulfurization of thiophene[J].J Catal,2005,233(1):16-25.
[3]DINTER N,RUSANEN M,RAYBAUD P,et al.Temperature-programmed reduction of unpromoted MoS2-based hydrodesulfurization catalysts: Firstprinciples kinetic Monte Carlo simulation sand comparison with experiments[J].J Catal,2010,275(1):117-128.
[4]VAN DER VLIES A J, KISHAN G,NIEMANTSVERDRIET J W,et al.Basic reaction steps in the sulfidation of crystalline tungsten oxides[J].J Phys Chem B,2002,106(13):3449-3457.
[5]VAN DER VLIES A J,PRINS R,WEBER T,et al.Chemical principles of the sulfidation of tungsten oxides[J].J Phys Chem B,2002,106(36):9277-9285.
[6]REINHOUDT H R,TROOST R,VAN LANGEVELD A D,et al.The nature of active phase in sulfide NiW/γ-Al2O3in relation to its catalytic performance in hydrodesulfurization reactions[J].J Catal,2001,203(2):509-515.
[7]VISSENBERG M J,VAN DER MEER Y,HENSEN E J M,et al.The effect of support interaction on the sulfidability of Al2O3-and TiO2-supported CoW and NiW hydrodesulfurization catalysts[J].J Catal,2001,198(2):151-163.
[8]REINHOUDT H R, VAN LANGEVELD A D,KOOYMAN P J,et al.The evolution of surface species in NiW/Al2O3catalysts in various stages of sulfidation:A quasi in-situ high resolution transmission electron microscopic investigation[J].J Catal,1998,179(2):443-450.
[9]HYON C H,YOON W L,LEE I C,et al.The effect of Ni loading and the sulfidation temperature on the structure and catalytic activity of Ni-W hydrodesulfurization catalysts[J].Appl Catal A,1996,144(1-2):159-175.
[10]VAN DER MEER Y,HENSEN E J M,VAN VEEN J A R, et al. Characterization and thiophene hydrodesulfurization activity of amorphous-silicaalumina-supported NiW catalysts[J].J Catal,2004,228(2):433-446.
[11]聂红,龙湘云,刘清河,等.柠檬酸对NiW/Al2O3加氢脱硫催化剂硫化行为的影响[J].石油学报(石油加工),2010,26(3):329-335.(NIE Hong,LONG Xiangyun,LIU Qinghe,et al.Effect of citric acid on sulfidation behavior of NiW/Al2O3hydrodesulfurization catalyst[J].Acta Petrolei Sinica(Petroleum Processing Section),2010,26(3):329-335.)
[12]高晓东.NiO-WO3/γ-Al2O3加氢精制催化剂硫化工艺研究[D].北京:石油化工科学研究院,1992.
[13]RINALDI N,KUBOTA T,OKAMOTO Y.Effect of citric acid addition on the hydrodesulfurization activity of MoO3/Al2O3catalysts[J].Appl Catal A,2010,374(1-2):228-236.
[14]TOPSØE H,CLAUSEN B S.Active sites and support effects in hydrodesulfurization catalysts[J].Appl Catal,1986,25(1-2):273-293.
[15]KIM J H,MA X,SONG C,et al.Kinetics of two pathways for 4, 6-dimethyldibenzothiophene hydrodesulfurization over NiMo,CoMo sulfide,and nickel phosphide catalysts[J].Energy &Fuel,2005,19(2):353-364.
[16]李丁健一.NiMo/拟薄水铝石加氢处理催化剂制备技术探索[D].北京:石油化工科学研究院,2011.
[17]XIE Xiaowei,LI Yong,LIU Zhiquan,et al.Lowtemperature oxidation of CO catalysed by Co3O4nanorods[J].Nature,2009,458(9):746-749.
[18]QIU L,XU G.Peak overlaps and corresponding solutions in the X-ray photoelectron spectroscopic study of hydrodesulfurization catalysts[J].Appl Surf Sci,2010,256(11):3413-3417.
[19]SUN M,BÜRGI T,CATTANEO R,et al.TPS,XPS,QEXAFS,and XANES investigation of the sulfidation of NiW/Al2O3-F catalysts[J].J Catal,2001,201(2):258-269.
[20]聂红,龙湘云,刘清河,等.活化温度对NiW/Al2O3催化剂中金属-载体相互作用的影响[J].石油炼制与化工,2010,41(7):1-5.(NIE Hong,LONG Xiangyun,LIU Qinghe,et al.Influence of activation temperature on metal-support interaction in NiW/Al2O3catalyst[J].Petroleum Processing and Petrochemicals,2010,41(7):1-5.)
[21]KIM C-H,YOON W L,LEE I C,et al.The effect of Ni loading and the sulfidation temperature on the structure and catalytic activity of NiW hydrodesulfurization catalysts[J].Appl Catal A,1996,144(1-2):159-175.
[22]左东华,聂红,Michel Vrinat,等.硫化态NiW/Al2O3催化剂加氢脱硫活性相的研究ⅠXPS和HREM表征[J]. 催 化 学 报,2004,25(4):309-314.(ZUO Donghua,NIE Hong,MICHEL Vrinat,et al.Study on the hydrodesulfurization active phase in sulfided NiW/Al2O3catalystⅠXPS and HRTEM characterizations[J].Chinese Journal of catalysis,2004,25(4):309-314.)
[23]聂红.柴油超深度加氢脱硫催化剂活性影响因素研究[D].北京:石油化工科学研究院,2010.

