培美曲塞或紫杉醇联合卡铂一线治疗老年晚期肺腺癌疗效比较
胡兴胜,杜永良,马玉洁,郭 燕,王 彬,石远凯
培美曲塞或紫杉醇联合卡铂一线治疗老年晚期肺腺癌疗效比较
胡兴胜1,杜永良2,马玉洁2,郭 燕2,王 彬1,石远凯1
目的探讨培美曲塞(pemetrexed,PEM)或紫杉醇(taxol,TAL)联合卡铂(carboplatin,CBP)一线治疗老年晚期肺腺癌的临床疗效、毒副反应及生存期。方法109例年龄≥65岁的老年晚期肺腺癌患者分别应用PC(培美曲塞联合卡铂)方案及TC(紫杉醇联合卡铂)方案化疗。PC组53例,第1天静脉滴注培美曲塞 500 mg/m2;TC组56例,第1天静脉滴注紫杉醇135~175 mg/m2;第2天两组均联合卡铂AUC=4~5,静脉滴注,21 d为一疗程。每例至少完成2个疗程后评价疗效及毒副反应。结果两组总有效率分别为33.9%、26.8%;疾病控制率分别为75.4%、69.7%,两组比较差异无统计学意义。两组中位无进展生存期分别为6.5、4.7个月,差异无统计学意义。两组中位生存期分别为16.8、11.8个月,PC组明显高于TC组,差异有统计学意义(P=0.032)。两组1年生存率分别为58.2%及42.3%,差异亦有统计学意义(P=0.013)。两组2年及3年生存率分别为27.3%及24.3%、14.2%及12.5%;两组比较无统计学意义。毒副反应主要为骨髓抑制,TC组在白细胞减少、中性粒细胞减少、脱发等方面发生率明显高于PC组(P<0.05)。结论PC方案及TC方案均安全有效,适用于老年晚期肺腺癌化疗,但PC方案生存率高、毒副反应轻,值得进一步研究。
培美曲塞;紫杉醇;老年;肺腺癌
近年来,肺癌的发病率和死亡率呈现逐年上升的趋势,成为危害人类健康的重大疾病之一,死亡率亦高居第1位。肺癌患者中非小细胞肺癌约占80%[1],化疗是主要治疗手段。一线化疗方案往往采取第3代化疗药物联合铂类的两药方案,可改善生存质量,提高生存率。但是,老年人晚期肺癌患者由于生理功能退化,对于化疗耐受性下降,不良反应增多,因此,对老年患者是否值得进行化疗争议不断。培美曲塞(pemetrexed,PEM)是一种新型的多靶点抗叶酸制剂,具有抑制肿瘤细胞增殖、毒副反应小的优点[2],与铂类药物联合应用疗效较好[3,4]。笔者采用PC方案(培美曲塞联合卡铂)及TC方案(紫杉醇联合卡铂)治疗≥65岁老年晚期肺腺癌,并比较两组的近期疗效、毒副反应及生存期。
1 对象与方法
1.1 对象 选取我院2006-01至2011-12资料完整的老年晚期肺腺癌患者109例,年龄65~76岁,纳入标准:(1)经病理学/细胞学确诊的初治局部晚期或转移性(ⅢA、ⅢB期或Ⅳ期)的不能手术或不愿意手术的肺腺癌患者,或既往手术、术后辅助化疗结束6个月后复发,且未经培美曲塞、紫杉醇治疗者;(2)至少有一个可测量的肿瘤病灶;(3)ECOG评分≤1分,预计生存时间≥3个月;(4)治疗前血、尿常规,电解质,肝肾功能,心电图基本正常;(5)没有症状的脑转移或脑转移放疗结束后1个月。采用PC方案(53例)及TC方案(56例)化疗。两组一般情况比较,差异无统计学意义(表1)。
1.2 治疗方法 PC方案,第1天培美曲塞500 mg/m2,静脉滴注;TC方案,第1天紫杉醇135~175 mg/2,静脉滴注;第2天,两药均联合卡铂,卡铂剂量AUC=4~5,静脉滴注。21 d为一疗程,至少2个疗程。培美曲塞用药前给予叶酸、维生素B12和地塞米松;紫杉醇用药前给予地塞米松、西咪替丁、苯海拉明。密切监测血压、心率和呼吸。
1.3 疗效及毒副反应评价标准 治疗2个疗程后,采用RECIST1.1标准评价疗效,分为完全缓解(CR)、部分缓解(PR)、稳定(SD)、进展(PD),计算总有效率(CR加PR的和占总例数的百分率)和疾病控制率(CR、PR加SD的和占总例数的百分率)。毒副反应按NCI-CTC3.0常见毒性分级标准评价。每周复查血常规,每周期复查肝、肾功能,心电图。


表1 培美曲塞或紫杉醇联合卡铂一线治疗老年晚期肺腺癌两组一般情况比较 (n;%)
2 结 果
2.1 临床疗效 全部患者均可评价临床疗效。PC组共完成253周期,平均4.8周期,其中完成2周期4例,3周期5例,4周期10例,5周期14例,6周期或6周期以上单药培美曲塞维持20例。TC组共完成209周期,平均3.7周期,其中完成2周期7例,3周期15例,4周期13例,5周期18例,6周期3例。PC组平均周期数明显高于TC组平均周期数(P=0.012)。疗效方面:PC组CR 1例 (1.8%),PR 17例(32.1%),SD 22例(41.5%),PD 13例(24.6%);TC组无CR病例,PR 15例(26.8%),SD 24例(42.9%),PD 17例(30.4%)。PC组及TC组总有效率分别为33.9%和26.8%;病病控制率分别为75.4%和69.7%,两组比较无统计学意义(P=0.678)。
2.2 生存情况 全组病例均随访至2013-06,PC组及TC组中位无进展生存期(PFS)分别为6.5个月及4.9个月,差异无统计学意义(P=0.057)。两组中位生存期(OS)分别为16.8个月及11.8个月,PC组明显高于TC组,差异有统计学意义(P=0.032)。PC组及TC组1年生存率分别为58.2%及42.3%,差异亦有统计学意义(P=0.013)。两组2年生存率分别为27.3%及24.3%;3年生存率分别为14.2%及12.5%;两组比较无统计学意义。
2.3 毒副反应 两组均出现血液学毒性,以及恶心、呕吐、便秘、脱发、肝肾功能损害等不良反应。PC组及TC组Ⅲ-IV度白细胞减少发生率分别为13.2%及48.2%,Ⅲ-IV度中性粒细胞减少发生率分别为16.9%及32.1%,Ⅲ-IV度脱发发生率分别为0及17.8%,以上三方面TC组均明显高于PC组,差异比较有统计学意义(P<0.05,表2)。
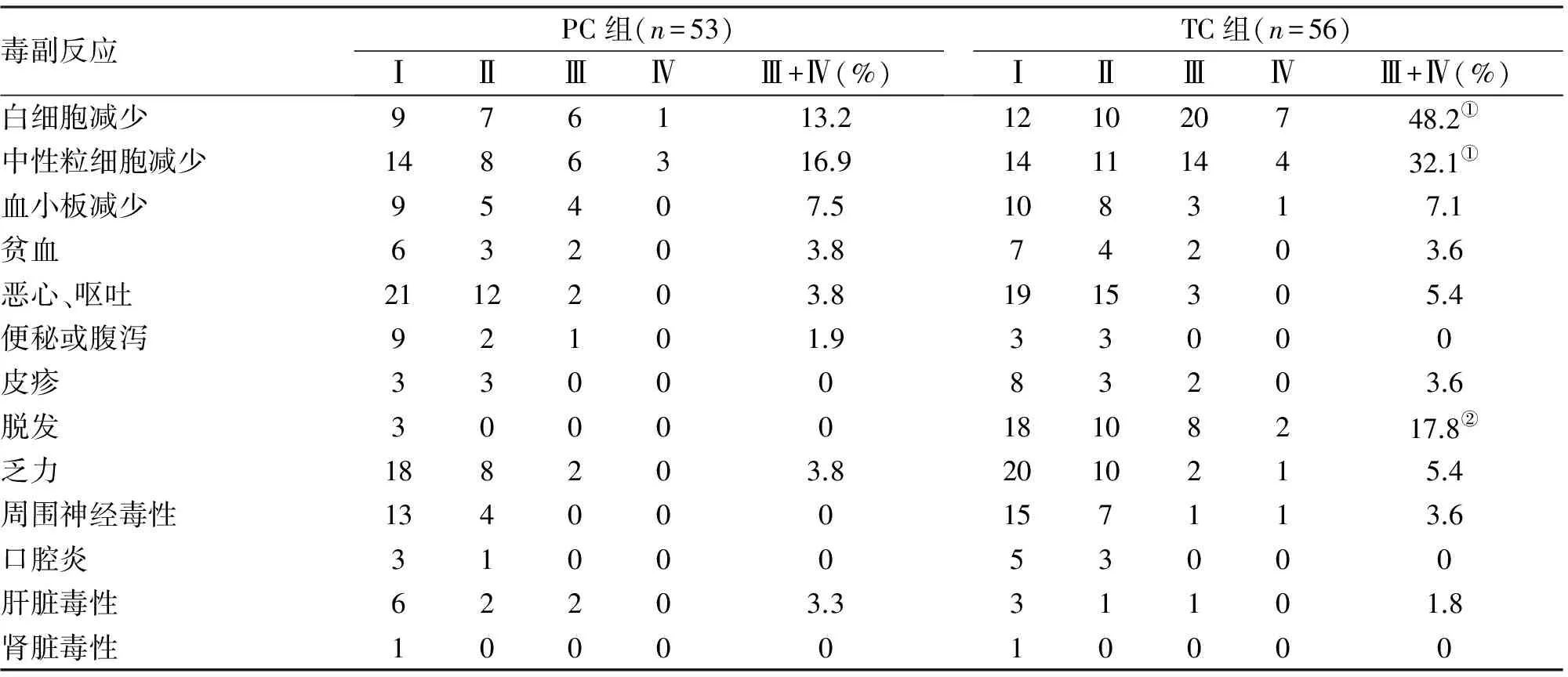
表2 培美曲塞或紫杉醇联合卡铂一线治疗老年晚期肺腺癌毒副反应比较
注:与PC组比较,①P<0.05,②P<0.01
3 讨 论
肺癌是最常见的恶性肿瘤,发病年龄40岁以后开始升高,70岁左右达高峰,≥70岁肺癌患者约占40%,大多数诊断时已是局部晚期或出现远处转移,化、放疗成为治疗的主要方法[5]。老年肺腺癌人群的特殊性决定了其治疗的特殊性,因为他们对化疗耐受性差,风险大,所以,对老年人群是否要进行化疗需要谨慎,如何减少化疗的毒副反应,最大程度地提高生活质量,延长生存期是关注的焦点[6,7]。目前,对晚期肺腺癌患者首选方案是第3代化疗药物,如紫杉醇、吉西他滨、长春瑞滨、多西紫杉醇联合铂类(顺铂或卡铂),它们可明显延长中位生存期,但也存在诸多不良反应,对于老年患者更是如此,因此临床医师一直在努力寻找不良反应轻、疗效好的方案[8,9]。
培美曲塞是新一代多靶点的抗叶酸药物,作用于叶酸依赖性代谢途径的多个酶,导致嘌呤和嘧啶合成障碍,使肿瘤细胞的增殖停滞于S期从而控制其生长,尤其对胸膜间皮瘤有突出疗效[10],并率先明确该药在胸膜间皮瘤中的适应证。在肺癌二线治疗中,显示对腺癌的疗效好于多西他赛。国外临床研究观察了培美曲塞联合顺铂对比吉西他滨联合顺铂一线治疗NSCLC的疗效和毒副反应,亚组分析结果显示,培美曲塞组与吉西他滨组相比,在腺癌和大细胞癌中OS明显延长,腺癌分别为12.6个月和10.9个月,大细胞癌分别为10.4个月和6.7个月[11]。腺癌和大细胞癌OS比较,有统计学差异。吴标等[12]报道,培美曲塞联合卡铂一线治疗老年人晚期肺腺癌的结果显示客观有效率31.4%,疾病控制率80.0%,中位无进展生存期为3.5个月,中位生存期为10.5个月,1年生存率为31.4%。最常见毒副反应为Ⅰ、Ⅱ级骨髓抑制。本研究在有效率方面与其相似,但在生存期及生存率方面都高于其报道数据,主要原因可能是本组部分患者<70岁,且应用培美曲塞维持治疗。
紫杉醇主要作用机制为促进微管聚合,抑制解聚,从而阻断肿瘤细胞合成。ECOG1594研究显示,TC方案对70~80岁的NSCLC患者有效率24.5%,中位生存期8.25个月,1年生存率35.2%,2年生存率13.7%,疗效较好,毒副反应可耐受[13]。Thomas等[14]报道,紫杉醇联合卡铂治疗67例≥70岁的NSCLC患者,中位周期数4,总有效率27%,中位生存期7.8个月,1年生存率33%,2年生存率7%,毒副反应较轻,表明紫杉醇联合卡铂方案在老年NSCLC治疗中的优势,可作为合理的标准治疗方案。本组中TC方案治疗老年肺腺癌的总有效率为26.8%,中位生存期11.8个月,1年生存率42.3%,2年生存率24.3%,略优于同类研究。
本研究中PC组在中位OS及1年生存率方面均优于TC组,差异有统计学意义,可能原因是PC组后续单药培美曲塞维持治疗和2线应用络氨酸激酶抑制药(TKI)比例高。本研究中,PC组白细胞减少及中性粒细胞减少发生率、脱发发生率明均低于TC组(P<0.05),而在恶心、呕吐、乏力、ALT/AST升高、皮疹、便秘的发生率方面,两组差异均无统计学意义。本研究的不良反应发生率与国内外研究结果相当[12,14]。
上述结果表明,PC方案和TC方案一线治疗老年晚期肺腺癌疗效较好,毒副反应可以耐受。PC方案有较轻的毒副反应,较高的生存率,值得临床进一步研究。
[1] Song H P, Wang S P, Sun C P,etal. Randomized study of docetaxcel plus cisplatin versus gecitabine plus cisplatin in treatment of advanced non-small cell lung cancer [J]. Chin Oncol, 2008, 18(7): 531-534.
[2] Wolfgang W H S, Andreas G, Martin S,etal. A randomized Phase Ⅱ study of Pemetrexed in combination with cisplatin or carboplatin as first-line therapy for patients with locally advanced or metastatic non-small-cell lung cancer[J]. Clin Lung Cancer, 2013, 14(3): 215-223.
[3] 朱海生,严浩林,伍纶庆,等. 培美曲塞联合卡铂治疗老年晚期非小细胞肺癌36例疗效观察[J]. 中国现代医药杂志,2011, 13(4): 84-86.
[4] Koumarianou A, Fountzilas G, Kosmidis P,etal.Non small cell lung cancer in the elderly:clinico-pathologic,management and outcome characteristics in comparison to younger patients[J]. J Chemother, 2009, 21(5): 573-583.
[5] Socinski M A, Langer C J, Okamoto I,etal. Safety and efficacy of weekly nab-paclitaxel in combination with carboplatin as first-line therapy in elderly patients with advanced non-small-cell lung cancer [J]. Ann Oncol, 2013, 24: 314-321.
[6] Gronberg B H,Bremnes R M,Flotten O,etal.Phase III study by the Norwegian lung cancer study group:pemetrexed plus earboplatin compared with gemcitabine plus earboplatin as first-line chemothera-py in advanced non-small-cell lung cancer [J].J Clin Oncol,2009,27(19):32l7-3224.
[7] 胡兴胜,焦顺昌,张树才,等. 培美曲塞及吉西他滨分别联合顺铂治疗初治晚期非小细胞肺癌安全性和有效性的随机对照研究[J].中国肺癌杂志,2012,15(10) : 569-575.
[8] 钱嘉琳,沈 洁,白 皓,等. 不同剂量紫杉醇联合卡铂一线治疗晚期非小细胞肺癌的临床研究[J]. 中国肺癌杂志, 2011, 14(4): 323-327.
[9] Gandara D R, Kawaguchi T, Crowley J,etal.Japanese-US common-arm analysis of paclitaxel plus carboplatin in advanced non-smal-cell lung cancer:a model for assessing population-related pharmacogenomics [J]. J Clin Oncol,2009, 27(21): 3540-3546.
[10] VogeLzang N J, Rusthoven J J, Symanowski J,etal. Phase Ⅲ study of pemetrexed in combination with cisplatin versus cisplstin alone in patients with malignant pleural mesothelioma [J]. J Clin Oncol, 2003, 21(14): 2636-2644.
[11] Scagliotti G V, Parikh P, Pawel J V,etal. Phase Ⅲ study comparing cisplatin plus gemcitabine with cisplatin plus pemetrexed in chemotherapy-naïve patients with advanced-stage non-small-cell lung cancer [J]. J Clin Oncol, 2008, 26(21): 3543-3551.
[12] 吴 标,黄 诚,张 晶,等. 培美曲塞联合卡铂一线治疗老年晚期肺腺癌临床观察[J]. 中国肿瘤临床与康复,2013, 20(3): 207-210.
[13] Langer C J, Vangel M, Schiller J,etal. Age-specific sub-analysis of ECOG1594: fit elderly patients(70-80yrs) with NSCLC do as well as younger patients (<70yrs) [J]. Proc Am Soc Clin Oncol, 2003, 34: 2571-2578.
[14] Thomas H A, Peterman A H, Schell M J,etal. The impact of age on toxicity, response rate, quality of life, and survival in patients with advanced, stage ⅢB or IV nonsmall cell lung cancer triated with carboplatin and paclitaxel [J]. Cancer, 2013, 98(4): 788-799.
(2013-09-23收稿 2013-10-20修回)
(责任编辑 武建虎)
Clinicalanalysisofpemetrexedortaxolpluscarboplatinchemotherapyasfirst-linetreatmentforelderlyadvancedlungadenocarcinoma
HU Xingsheng1, DU Yongliang2, MA Yujie2, GUO Yan2, WANG Bin1, and SHI Yuankai1.
1. Department of Medical Oncology, Cancer Hospital &Institute, Chinese Academy of Medical Sciences,Beijing 100021,China;2.Department of Medical Oncology, Sanhuan Cancer Hospital, Chaoyang District of Beijing,Beijing 100122,China
ObjectiveTo evaluate the efficacy and toxicity of pemetrexed(PEM) or taxol (TAL) plus carboplatin chemotherapy as first-line treatment for elderly advanced lung adenocarcinoma.MethodsOne hundred and nine patients (≥65 years) with advanced lung adenocarcinoma were treated with pemetrexed plus carboplatin (PC) or taxol plus carboplatin (TC) regimen as first-line chemotherapy. Fifty-three patients
PC regimen: pemetrexed 500 mg/m2, intravenous drip day 1; Fifty-six patients received TC regimen: taxol 135-175 mg/m2, intravenous drip day 1; carboplatin in both groups: area under the curve 4-5 mg/(ml·min), day 2; every 3 weeks. Each patient was evaluated on efficacy and toxicity after at least 2 cycles. The general characteristics of patients in the two groups were comparable.ResultsThe response rates in PC group and TC group were 33.9% and 26.8%, whereas the disease control rates were 75.4% and 69.7%, respectively; there was no significant difference between the two groups. Median progression-free survival was 6.5 months in the PC group, and 4.7 months in the TC group, there was also no significant difference. The median overall survival rate in PC group was significantly higher than that in TC group with 16.8 months and 11.8 months, respectively; the difference was statistically significant (P=0.032).The 2-year and 3-year survival rates in the two groups were 27.3% and 24.3%, 14.2% and 12.5%, respectively; no significant difference was found between the two groups. The main toxicity was myelosuppression. Leucocytopenia, neutropenia and alopecia were more common in the TC group.ConclusionsBoth the PC regimen and TC regimen are moderately safe and effective for elderly advanced lung adenocarcinoma as first-line treatment. The PC regimen has higher survival rate and tolerated toxicity. It is worth further clinical study.
pemetrexed;taxol;the elderly, lung;adenocarcinoma
国家“重大新药创制”科技重大专项“十一五” 课题(2008ZX09312-020),北京市科技计划项目(Z111102071011001)
胡兴胜,硕士,副主任医师,E-mail:huxingsheng66@163.com
1.100021北京,中国医学科学院北京协和医学院肿瘤医院内科、抗肿瘤分子靶向药物临床研究北京市重点实验室;2. 100122,北京市朝阳区三环肿瘤医院内科
通迅作者:石远凯,E-mail: syuankaipumc@126.com
R734.2

