磷酸-重铬酸钾分光光度法测定氧化锌酸性浸出液中的锰量
周丽砂
(湖南株洲冶炼集团股份有限公司,湖南株洲 412004)
磷酸-重铬酸钾分光光度法测定氧化锌酸性浸出液中的锰量
周丽砂
(湖南株洲冶炼集团股份有限公司,湖南株洲 412004)
建立了分光光度法测定氧化锌酸性浸出液中锰量的新方法。试样在硫酸介质中用双氧水将二价铁离子氧化成三价铁离子,消除了亚铁离子的干扰,使重铬酸钾能在8~10 mol/L磷酸溶液中,室温下将Mn(Ⅱ)迅速定量地氧化为Mn(Ⅲ),形成紫红色的锰(Ⅲ)-磷酸络和物,于分光光度计波长550 nm处测量其吸光度。样品测定具有较好的精密度,相对标准偏差为2.52%~3.81%,加标回收率为96.5%~104.6%。适合测定的范围为1.00~12.00 mg/mL。
锰;氧化锌酸性浸出液;分光光度法
氧化锌酸性浸出液是锌浸出工艺过程中所生产出的中间物料,其成分复杂,主要含有锌、铁、铅、锰、铜、镉、铟等元素,其中锰含量在1.00~6.00 mg/mL。目前锌浸出液中锰量的测定主要采用的是《硫酸亚铁铵容量法测定锰量》,该方法虽然准确,但在操作过程中,对酸度的控制和用过硫酸铵氧化二价锰为七价锰时煮沸的时间要求很严格,控制不好,对结果影响较大,操作繁琐,需时较长,而采用原子吸收光谱仪测定锰,灵敏度高,误差大,且氧化锌酸性浸出液中锌基较高,容易污染仪器。本实验提出了将二价铁离子氧化成三价铁离子,以消除亚铁离子的干扰,在8~10 mol/L磷酸溶液中,重铬酸钾将Mn(Ⅱ)迅速定量地氧化为Mn(Ⅲ),形成紫红色的锰(Ⅲ)-磷酸络和物,于分光光度计波长550 nm处测量其吸光度。方法简便快速,结果准确。
1 实验部分
1.1 试剂
硫酸(5+95)、硫酸(1+1)、30%双氧水磷酸、重铬酸钾(5 g/L)。
磷酸-重铬酸钾混合液:磷酸与重铬酸钾(5 g/L)按3+1比例混匀。
硫酸亚铁溶液(30 mg/mL):称取149.35 g硫酸亚铁(FeSO4·7H2O)于300 mL烧杯中,加入100 mL硫酸(1+1)和100 mL水,溶解完全后移入1 000 mL容量瓶中,用水稀释至刻度,摇匀。
硫酸锌溶液(100 mg/mL):称取439.80 g硫酸锌(ZnSO4·7H2O)于1 000 mL烧杯中,加入100 mL硫酸(1+1)和800 mL水,溶解完全后移入1 000 mL容量瓶中,用水稀释至刻度,摇匀。
锰标准溶液A(1 mg/mL):称取3.107 g分析纯一水硫酸锰(99%以上MnSO4·H2O)于200 mL烧杯中,加入40 mL水和10 mL硫酸(1+1)溶解完全后,移入1 000 mL容量瓶中,用水稀释至刻度,摇匀。
锰标准溶液B(3 mg/mL):称取9.322 g分析纯一水硫酸锰(99%以上MnSO4·H2O)于200 mL烧杯中,加入40 mL水和10 mL硫酸(1+1)溶解完全后,移入1 000 mL容量瓶中,用水稀释至刻度,摇匀。
所有试剂均为分析纯,实验室用水为二级水。
1.2 仪器
UV-2000型紫外可见分光光度计(上海仪器有限公司生产)。
1.3 实验方法
1.3.1 试样
所送试样量在200 mL以上,试样中不含悬浮物。送达分析室后应立即过滤,确保溶液清亮。
1.3.2 测定
移取1.00 mL试液于100 mL烧杯中,加2 mL硫酸(5+95),2 mL双氧水,放置电热板上低温处蒸发体积至2 mL左右,取下,冷却。将试液移入25 mL比色管中,加20 mL磷酸-重铬酸钾混合液,水稀至刻度,摇匀,放置10~20 min。取部分试液于比色皿中,以试剂空白作参比,于分光光度计波长550 nm处,测量其吸光度A。
1.4 工作曲线的绘制
分别移取锰标准溶液A/mL:0.00、1.00、2.00和锰标准溶液B/mL:1.00、2.00、3.00、4.00,于一系列25 mL比色管中,加入20 mL磷酸-重铬酸钾混合液.水稀至刻度,摇匀。以随同试剂空白作参比,于分光光度计波长550 nm处,测量其吸光度。以锰标准含量为横坐标,吸光度为纵坐标,绘制工作曲线,如图1所示。
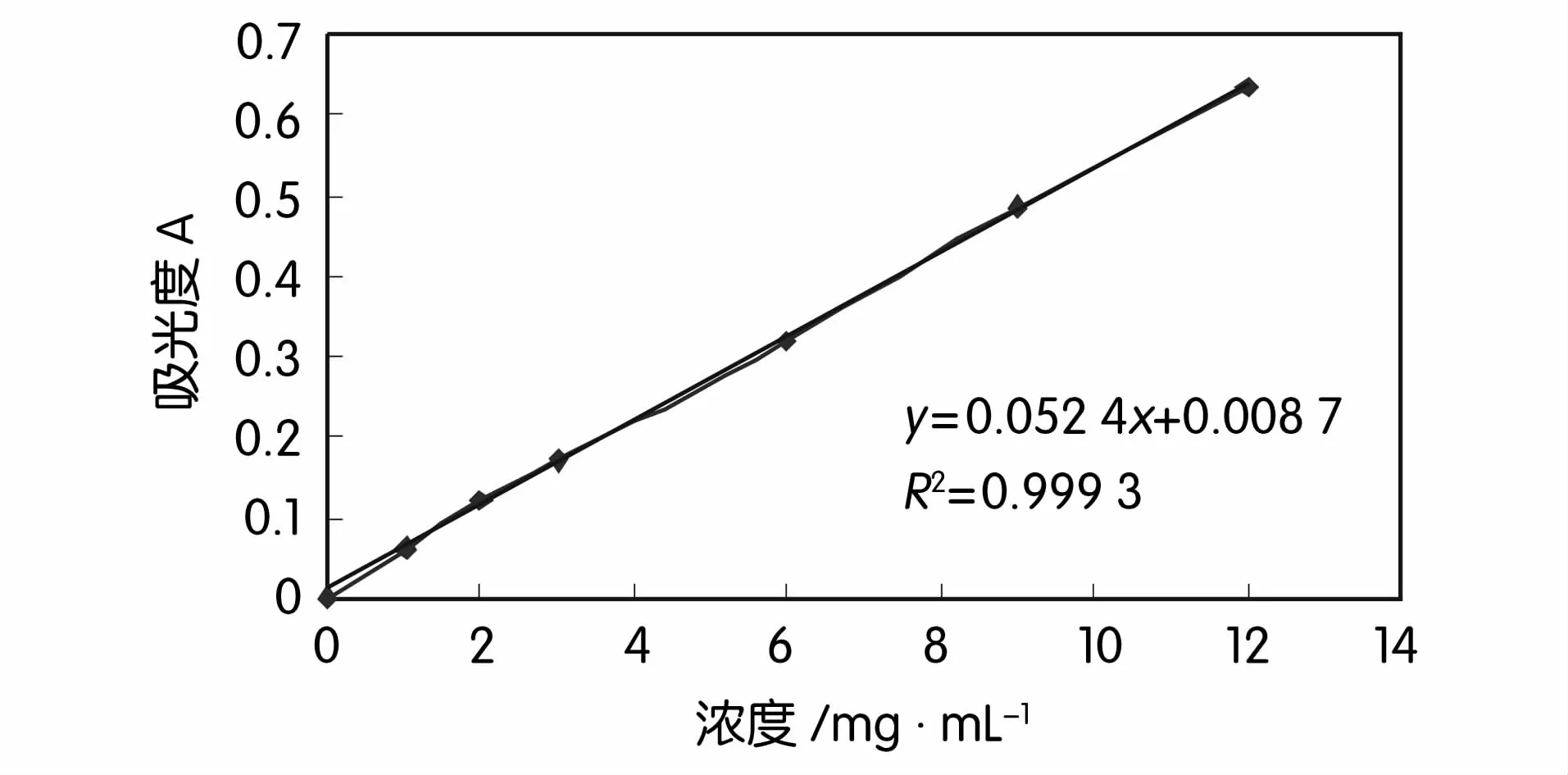
图1 工作曲线的绘制
2 结果与讨论
2.1 光谱吸收曲线
Mn(Ⅲ))-磷酸紫色络合物在550 nm波长处有最大的吸收峰,且干扰最小,本实验选择550 nm为测量波长。
2.2 磷酸-重铬酸钾混合液的用量
锰(Ⅲ)-磷酸紫色络合物在8~10 mol/L磷酸中有最大稳定的吸光度,本实验选择磷酸的用量为9 mol/L(即15 mL磷酸),重铬酸钾的用量直接关系到能否将Mn(Ⅱ)定量地氧化为Mn(Ⅲ)形成紫红色的锰(Ⅲ)-磷酸络和物。通过实验,5 mL重铬酸钾(5 g/L)足可以氧化12 mg以下的锰量。本实验选择磷酸-重铬酸钾混合液20 mL。
2.3 络合物的显色时间和稳定时间
将试液稀释至刻度,充分摇匀,放置10~20 min即可比色,稳定时间在24 h以上。
2.4 干扰元素的影响及消除
氧化锌酸性浸出液含有的共存元素有:锌(50~100 mg/mL),硫酸(80~120 mg/mL),全铁(10~40 mg/mL),亚铁离子(5.0~30 mg/mL),锰(1~6 mg/mL),镁(1~6 mg/mL),铜(0.5~3 mg/mL),镉(1~3 mg/mL),砷(0.5~2.5 mg/mL),锑(0.1~0.4 mg/mL),铅(0.01~0.50 mg/mL),锗(0.01~0.04 mg/mL),钴(0.01~0.04 mg/mL),镍(0.005~0.05 mg/mL),铟(0.4~1 mg/mL),二氧化硅(0.0 5~0.25 mg/mL)。依据文献[1]锌(100 mg/mL),镁(6 mg/mL),二氧化硅(0.25 mg/mL)不干扰锰的测定。
2.4.1 亚铁离子的影响及消除
氧化锌酸性浸出液中含亚铁离子较高,由于其还原能力强,严重阻扰了重铬酸钾定量氧化Mn(Ⅱ)为Mn(Ⅲ)。为了消除亚铁离子的干扰,实验采用了在硫酸介质中加双氧水,低温处加热,使亚铁离子氧化成三价铁离子,消除干扰。
试验方法:将100 mg锌,3.00mg锰,30mg亚铁离子(模拟氧化锌酸性浸出液),于一系列100 mL烧杯中,加入不同体积的硫酸(5+95)和双氧水(30%),按试验方法测定锰量,结果见表1。

表1 硫酸和双氧水加入量实验 mg
实验表明,加入0.50~4.00 mL的硫酸和1.00~4.00mL的双氧水能够完全消除亚铁离子的干扰,测定的锰结果稳定,因此,本实验选择硫酸加入量为2.00 mL,双氧水加入量为2.00 mL。
2.4.2 氧化干扰元素的时间和温度
将试液放在电热板低温处加热,待气泡消失,溶液平静后,保留体积2 mL左右,取下冷却,此时,亚铁离子已经被氧化成三价铁离子,过量的双氧水也被驱赶干净。在此过程中,一定要注意防止试液蒸干,使结果偏低。
2.4.3 其它共存元素干扰实验
从前面(2.4.1)实验可知,0.50~4 mL硫酸(5+95)(相当于45~360 mg)不干扰测定,而氧化锌酸性浸出液中的硫酸含量为80~120 mg,因此试液本身的硫酸含量不会影响测定。其它元素可能干扰测定,现考察干扰元素的最大影响量,实验方法:取3.00 mg锰,100 mg锌,30 mg亚铁离子(模拟氧化锌酸性浸出液),于一系列25 mL比色管中,分别加入其它共存元素,按试验方法测定锰,结果见表2。

表2 共存元素的干扰试验数据
表2数据表明,共存元素在上述浓度下对锰的测定没有干扰。
2.5 精密度实验
选取5个实验样品,按样品分析步骤,每个样品重复分析5次,结果见表3。
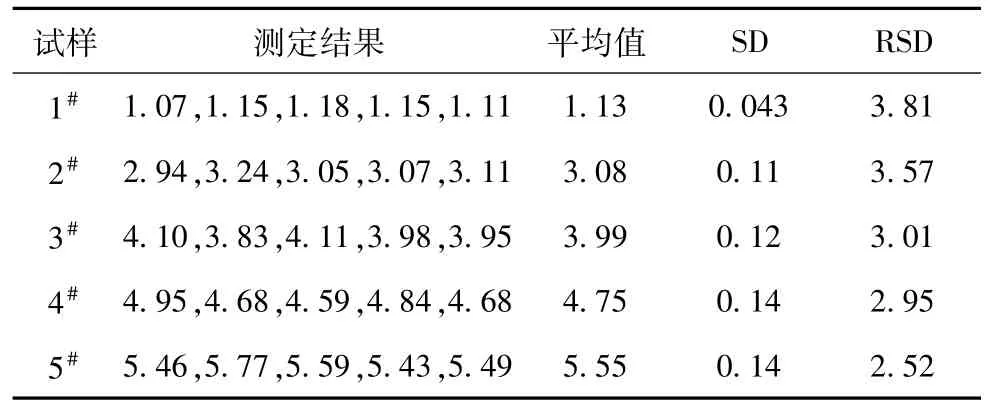
表3 方法的精密度考核 %
从表3数据可以看出,锰的测定相对标准偏差在2.52%~3.81%,满足分析要求。
2.6 方法加标回收率实验
为了考察方法的准确度,分别在5个实验样品中加入不同量的锰,按样品分析步骤进行测定,结果见表4。
通过实验测得锰的加标回收率达到96.5%~104.6%,完全能够满足氧化锌酸性浸出液中锰量的测定。
2.7 方法对比
用分光光度法与硫酸亚铁铵容量法分别测定1#、2#、3#、4#、5#氧化锌酸性浸出液中锰量测定结果见表5。

表4 加标回收率
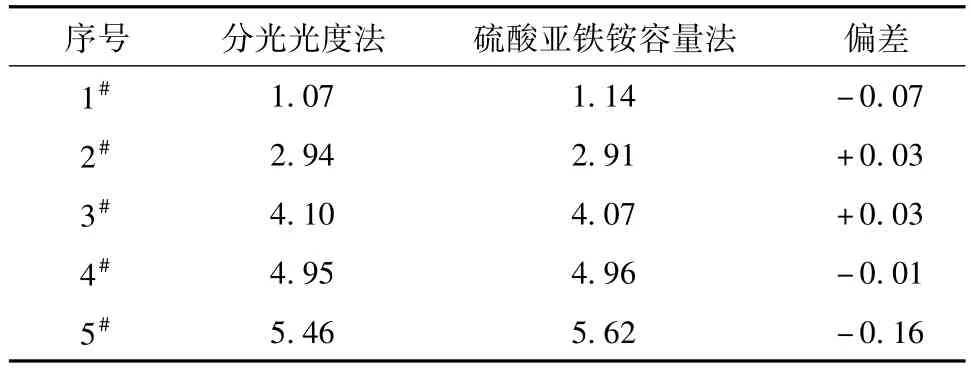
表5 分光光度法与硫酸亚铁铵容量法结果对比mg
表5结果表明,两种方法结果吻合。
3 结 语
实验通过条件选择,采用精密度、加标回收率和方法结果对比考察方法的重现性和准确性。锰的测定结果精密度相对标准偏差(n=5)在2.52%~3.81%,加标回收率在96.5%~104.6%,偏差在-0.16~+0.03,实验结果表明,采用磷酸-重铬酸钾分光光度法测定氧化锌酸性浸出液中锰量的方法,具有成本低、方法简捷易于掌握、准确度高等特点。
[1] Q/ZY09.02.47.25-2011.锌湿法冶炼溶液化学分析方法:磷酸-重铬酸钾分光光度法测定锰量[S].
[2] 李秀艳.锰(Ⅲ)—磷酸分光光度法测定电解液中锰量[J].有色矿冶,2010,26(2):60-61.
Determ ination of M anganese Content in Acid Leaching Solution of Zinc Oxide by Phosphate-potassium Dichromate Spectrophotometry
ZHOU Li-sha
(Zhuzhou Smelter Group Co.,Ltd,Zhuzhou 412004,China)
manganese;acid leaching solution of zinc oxide;spectrophotometry
O657.3
:A
:1003-5540(2014)05-0074-04
2014-08-06
周丽砂(1966-),女,技师,主要从事化学分析工作。
Abstract:The new method of confirm determination ofmanganese content in the acid leaching solution of zinc oxide by spectrophotometry is established.The sample in sulfuric acid solution is oxidized by hydrogen peroxide from ferrous ion to ferric ion.It can eliminate the ferrous ion interference andmake potassium dichromate quickly and quantitatively oxidize Mn(II)into Mn(III)in 8~10 mol/L phosphoric acid at room temperature,form prunosus Mn(III)-phosphoric acid complex,measure the absorbancy at the 550 nm wave length of spectrophotometer.This samplemeasurement is of good accuracy,the relative standard devitation is from 2.05%to 3.81%.The recovery rate is from 96.5%to 104.6%.The appropriate determination range is from 1.00 mg/mL to 12.00 mg/mL.

