类芬顿法降解环境内分泌干扰物双酚A的研究进展
宋丽红,李娟,宛中华,黄晓英
(深圳市环境科学研究院,深圳 518001)
类芬顿法降解环境内分泌干扰物双酚A的研究进展
宋丽红,李娟,宛中华,黄晓英
(深圳市环境科学研究院,深圳 518001)
作为环境内分泌干扰物代表之一的双酚A,由于具有生物难降解性及内分泌干扰性,国内外广泛开展了针对双酚A的高级氧化降解技术研究。高级氧化技术中的类芬顿法能有效降解双酚A并克服传统芬顿法的主要缺点。从双酚A的物理化学性质、降解双酚A的类芬顿类型、降解的效果等方面进行了分析,着重介绍了近年来国内外运用类芬顿法对双酚A进行降解处理的研究成果和现状,并对研究前景进行了展望。
类芬顿反应;双酚A;降解
环境内分泌干扰物[1](environmental endocrine disruptors,EEDs)是指由于人类的生活和生产而释放到环境中的、对人体和动物体内原本营造的正常激素功能(合成、分布、转运和代谢等过程)施加影响,从而引起内分泌系统众多生理生化功能改变的“外源性干扰内分泌的化学物质”。随着全球经济和社会的发展,这类物质对环境的污染日趋严重,被列为继臭氧层空洞和地球变暖之后迫切需要治理的“第三代环境污染物”。
其中,类雌激素物质双酚A(bisphenol A,BPA)作为聚碳酸酯和环氧树脂的原材料,被广泛运用在诸如塑料水瓶、医药用品、电子设备和食物包装等生活消费品生产中,是应用最广泛的化学工业品之一[2-4],它会在生产过程或者生命周期中得到释放[5]。随着生产和使用范围的进一步扩大,BPA已成为一种全球性污染物,其低浓度下即表现出明显的雌激素作用而对环境产生危害[6]。因此,BPA的污染越来越受到世界各国政府卫生部门和学术界的广泛关注,是具有代表性的环境内分泌干扰物[7]。
在常规好氧生物处理工艺中,BPA降解的半衰期达数天到数周[8-9],不完全降解的BPA可能会给生态带来更大的危害[10],所以有必要研发能彻底、快速降解BPA的技术。
近年来,高级氧化技术(advanced oxidation processes,AOPs)在有机污染物的降解处理方面得到广泛的关注。原因是高级氧化技术能产生羟基自由基(hydroxyl radicals,·OH),羟基自由基是水体系下氧化性仅次于氟的自由基[11]。此外,高级氧化反应过程中产生的羟基自由基具有高活性和无选择性,能够有效地降解生物难以降解的有机污染物[12-13]。
类芬顿反应(fenton-like reaction)是将氧化方法与传统芬顿方法结合的方法。本文从双酚A的基本物理化学性质,近几年类芬顿法处理双酚A研究的催化剂的制备、降解的效果、影响因素等方面进行研究进展综述,并对其发展前景进行了展望。
1 双酚A物理化学性质
BPA的化学结构及理化性质见表1[16-17]。它由刚性平面芳环和可塑的非线性脂肪侧链组成,该结构组成决定了其理化性质和进入环境后的行为。BPA属于难挥发、疏水性有机污染物,稍溶于氯化烷烃和苯类,易溶于醇、酮。在环境条件下为白色固体,市售的BPA为晶体、球状或片状。羟基的4个邻位氢很活跃,易进行卤化、硝化、磺化、烃化反应。
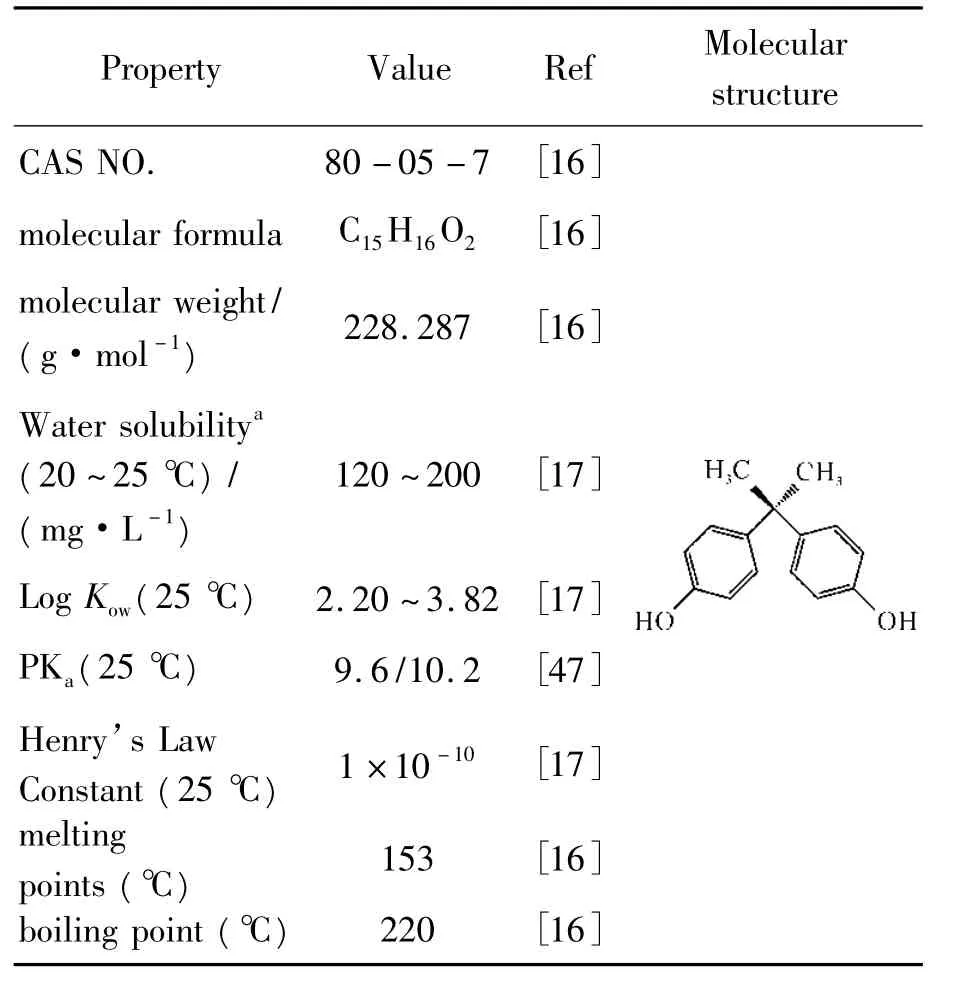
表1 双酚A的结构及理化性质
2 类芬顿法降解双酚A的研究
目前对于芬顿、类芬顿降解BPA的研究,主要是以模拟污水体系为主。而实际污水、自然水体、沉积物或污泥等更具实际意义的研究体系却鲜见报道。
在同样的条件下,对比传统类芬顿法,传统芬顿能明显提高BPA的去除率。部分报道证明:类芬顿法能有效解决传统芬顿在中性介质中失效等问题。
2.1 传统芬顿法降解BPA
传统芬顿法是在强酸性条件下投加一定比例的2价铁离子与双氧水。在2价铁离子的催化作用下,体系产生羟基自由基,从而将BPA降解。传统芬顿体系中羟基自由基产生的反应如下:
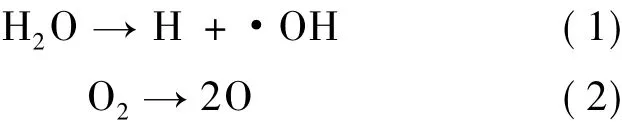
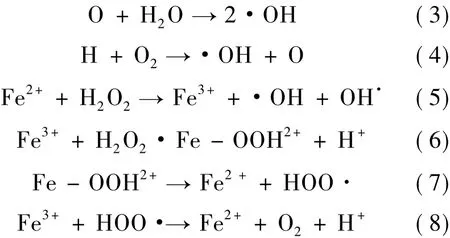
Ioan等[18]研究了pH值为4~6.5时传统芬顿法对BPA的降解效果。研究发现:在pH值为4,FeSO4·7H2O与双氧水投加量分别为2.5 mg/L 与7 mg/L时,BPA的初始浓度为25 mg/L,反应10 min去除率达86.36%,反应进行60 min能彻底去除BPA,各种物质最佳比例为H2O2/Fe(II)/ BPA=2.8∶1∶10,最佳条件下的BPA质量浓度随时间变化如图1所示[18]。

图1 传统芬顿反应中BPA浓度随时间变化
Torres等[19]进行了传统芬顿法在去离子水与自然水体2种体系下对BPA降解去除的对比研究。在去离子水体系中,当pH值为3时,FeSO4与双氧水投加量分别为100 μmol/L及35×10-3mol/L,BPA初始浓度为118 μmol/L时,反应进行90 min能彻底去除BPA。在自然水体中,当pH值为7.6,且在其他条件一致的情况下,传统芬顿试剂对BPA几乎不起降解作用。此外,该研究还进行了传统芬顿法降解BPA的最终产物的HPLC/ MS分析,结果表明传统芬顿法降解BPA的最终产物为7种:

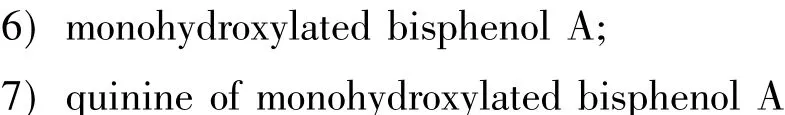
其中,除1)外,其他的降解产物在关于芬顿法降解BPA的产物研究中均有报道[20]。
以上研究结果表明:传统芬顿法能对BPA进行快速、彻底的去除。但在自然水体中,由于pH值较高,氢氧化铁溶解度低,同时,自然水体中各种阴离子(尤其是)能起到羟基自由基捕捉剂的效果,因此在不做任何pH调节的自然水体体系下,芬顿法对BPA基本不起降解作用。在研究克服传统芬顿法处理双酚A的缺点的过程中催生了多种类芬顿技术。
2.2 超声类芬顿降解双酚A
1927年数篇有关超声处理有机废水过程中声化学过程的研究报道[21]证明:超声能作为有机污染物的有效前处理方法。
超声处理有机污染物的原理如下:超声波在溶液体系中进行传播会产生大量的空穴微泡;空穴微泡进而膨胀并在微秒时间内破裂;这样,在空穴的核心形成数千度高温与高压[22],具有挥发性的有机污染物容易转移至空穴核心进行直接的热解[23]。另外,空穴微泡核心中的水分子与氧气分子受激发同时形成活性基团,如氢原子自由基、羟基自由基、过氧化自由基,反应如下[24-28]:

在该过程中产生的高活性强氧化性的自由基能对有机物进行降解。
但是,超声处理废水中有机污染物主要是针对诸如苯酚、卤代有机物等具有挥发性的有机污染物[23,26,28]。因挥发性有机物能在超声过程中产生的破裂空穴之中或附近进行直接的热分解(也能受羟基自由基的氧化作用而分解),对于如双酚A等不具挥发性或挥发性较低的有机污染物,其降解途径主要是羟基自由基的氧化作用,如式(14):

然而,在纯粹的超声环境下,用于降解难挥发有机污染物的羟基自由基及超氧自由基等具有强氧化性的自由基,对比降解有机污染物,更易形成过氧化氢[25,29-30],如下:

过氧化氢虽然对有机物有一定的降解作用,但反应活性较低。因此,纯粹的超声处理对有机物的降解往往是效率低下的。
为了克服传统芬顿法的缺点,提高超声对有机物的降解作用,近年来开发了超声类芬顿法。研究发现,在超声反应体系中加入铁离子或能均匀分散的铁氧化物,能大大提高有机污染物降解的速率[18,31]。
一些超声类芬顿的方法采取利用超声过程中产生的过氧化氢而非额外投加双氧水的方法[15,32-33],彻底解决了传统芬顿法中双氧水使用费用高的缺点。
Torres等[19]在进行传统芬顿降解BPA研究的同时,也进行了超声芬顿降解BPA的对比研究,研究采取持续投加双氧水的方式。在传统芬顿失效的自然水体介质中,采取与传统芬顿研究中同样的投加量与投加方式(详见表2),即反应体积为300 mL,反应温度为20±1℃,FeSO4投加量为100 μmol/L,H2O2投加采用持续投加方式,投加量为110 μmol/h。结果表明:它能在90 min中取出BPA接近100%,同时,取得较高的BPA,COD及TOC去除率。自然水体中传统芬顿及超声芬顿降解BPA效率对比如图2所示[19]。
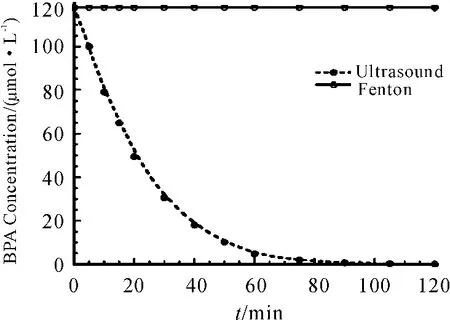
图2 自然水体中传统芬顿与超声类芬顿对BPA(118 μmol/L)的降解率对比图
Mohapatra等[34]分别采用超声(ultrasonication)、传统芬顿氧化(fenton’s oxidation)和2价铁离子超声类芬顿(ferro-sonication)处理3种方法进行了污水二沉池污泥(wastewater sludge,WWS)中BPA进行降解的实验研究。结果表明:对于超声与传统芬顿方法,采取2价铁离子类芬顿法对污泥进行针对BPA的处理能获取悬浮固体(suspended solids,SS)、挥发性悬浮固体颗粒(volatile suspended solids,VSS)、COD及溶解性有机碳(soluble organic carbon,SOC)等比污泥常规处理效率指标更高的去除率,同时实现了最高的BPA去除率(82.7%)。最后,采取LC-MS/MS分析,探究了BPA在过程中进行的高级氧化机理。
可见,超声协助传统芬顿而组成的超声芬顿系统,在同一条件下,能大幅提高BPA的去除率;同时,因超声独有的空化作用,能减少氧化剂双氧水的投加量甚至避免投加双氧水,大幅降低了方法的运行成本;此外,在传统芬顿法失效的自然水体或中性pH值下,超声类芬顿仍然对BPA保持优良的去除效果。
对于超声芬顿优于传统芬顿的原因分析,经Gogate[21]及Blume等[35]研究,归结为超声芬顿在提供超声空化作用及混合作用的同时,提高了反应式(5)的反应速率,从而提高了羟基自由基OH·的产率,最终提高BPA的去除效率。当反应体系处在中性甚至碱性的条件下,从传统芬顿的反应式可以看出:产碱的反应式(5)是整个芬顿反应的控制步骤,而增加超声的空化作用,能提高反应式(5)的速率,也使得超声芬顿法在pH值较高的范围仍对BPA具有良好的去除效果,克服了传统芬顿只能在酸性条件下保持良好去除效果的弊端。此外,超声的空化作用能使得体系中持续保持氧化剂双氧水的生成,可大幅度降低双氧水的投加量甚至完全避免双氧水的投加,同时也克服了传统芬顿法中双氧水投加耗费的缺点。
总体而言,我国各地未成年人公共文化服务发展不均衡,很多未成年人并没有形成到图书馆学习的意识。部分图书馆开展的未成年人阅读推广活动,由于缺乏连续性或趣味性,难以长久地吸引读者[6]。究其原因,与我国图书馆未成年人服务尚未制度化,缺乏与之对应的法律、行业标准等有关。国家应该尽快出台政策与法规,保障未成年人公共文化服务的规范、科学化。同时政府部门要完善版权保护制度,明确公共文化治理主体的权责,营造良好的公共文化服务环境,加大对文化服务市场的监管,为图书馆未成年人服务提供支持。图书馆也有必要根据服务实际,制定合理的规章制度,以为未成年人提供有益的阅读引导。
2.3 光催化类芬顿降解双酚A
传统芬顿法与紫外光照射联合称为光芬顿法(photo-fenton process),光芬顿法能显著提高有机污染物的分解速率[36]。
光芬顿法包含2个反应[37-38]:
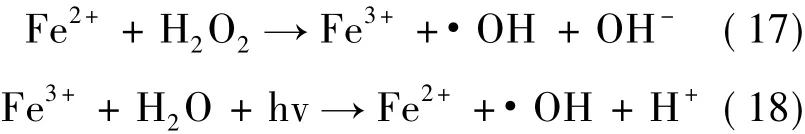
在光芬顿反应中,羟基自由基来源于2价铁离子催化过氧化氢及3价铁离子在光照的条件下与水反应。以上2个反应在光芬顿的进程上反复进行,将有机污染物彻底降解为二氧化碳和水。
Katsumata等[36]研究了双酚A在光芬顿体系下的高级氧化。最佳条件下反应进行10 min,BPA去除率达100%,经过36 h紫外光照,90%以上的双酚A彻底氧化为CO2,远高于在避光状态下的去除率。研究探讨了双酚A在光芬顿过程中双酚A矿化的机理。
然而,单纯的传统芬顿法与紫外光照联合,仍存在铁离子损耗与污水处理后铁离子后续处理的传统芬顿缺点[39-40]。所以国内外进行了大量的负载型非均相光芬顿催化剂的研究,载体有如沸石[40-41]、膜状或球状尼龙[42-43]、硅石织物[39,44]等,开展广泛的非均相类芬顿法研究以解决其缺陷。
2.4 其他类芬顿法降解双酚A
Ricardo[45]等投加2价铁离子与二氧化钛,在光照与超声的环境下研究了新型类芬顿方法降解双酚A的实验,经4 h的反应去除了93%的可溶性有机污染物,并用两种方法实现了协同作用。
Wanpeng Liu[46]等将具有强氧化作用的零价金属铝-酸性系统(zero valent aluminum(ZVAl)-acid system)结合2价铁离子组成类芬顿系统对BPA进行降解。零价金属铝-酸性系统产生一定浓度的H2O2并与2价铁离子组成芬顿系统,增强了系统的氧化能力,见图3。该体系反应温度为25±1℃,pH值为1.5,BPA初始浓度为2.0 mg/L,零价金属铝(ZVAl)投加量为4.0 g/L。实验8 h内BPA去除率大于99%。同时,该团队探究了该系统下BPA的降解机理,得出结论:此体系下,低pH值、高ZVAl及Fe2+投加量、高温有助于提高BPA的降解速率。
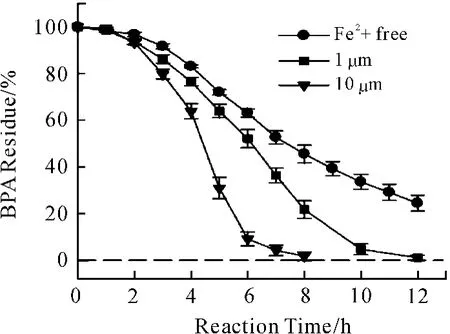
图3 零价金属铝-酸性系统中Fe2+浓度影响BPA去除率曲线图[46]
3 结束语
综上所述,与传统芬顿法相比,采用类芬顿方法在处理BPA时不仅能达到传统芬顿的处理效率,而且也可解决传统芬顿法存在的问题,在BPA的处理方面具有较大的发展前景。
目前存在的主要问题和发展方向如下:
1)目前类芬顿法运用在含BPA的废水处理中较大的障碍是运行成本高,其主要来源之一是催化剂失效后更换而产生的成本。因此研发催化活性高、成本低、稳定性强且可回收利用的负载型或者修饰型非均相类芬顿催化剂以处理BPA废水已成为当前的研究趋势。此外,具有选择性吸附性能的分子印记技术与类芬顿结合能有效提高类芬顿催化剂对BPA的选择性吸附与催化降解。
2)关于类芬顿降解BPA的机理研究鲜有报道。因此,在尝试各种辅助手段与传统芬顿结合以解决传统芬顿法问题的同时,有必要对其协同作用机理进行研究,以彻底弥补传统芬顿在处理BPA时的缺陷。
3)BPA的污染已出现在环境中的多个介质中,而目前类芬顿法处理BPA主要集中在模拟污水介质体系的研究。因此,应开展在如实际水体、沉积物、土壤等介质体系中的降解研究。
[1]Hutchinson T H,Matthiessen P.Endocrine disruption in wildlife:identification andecological relevance[J].Sci Total Environ,1999,233(1/2/3):1-3.
[2]Chang S M,Hou C Y,Lo P H,et al.Preparation of phosphated Zr-doped TiO2exhibiting high photocatalytic activity through calcination of ligand-capped nanocrystals [J].Appl Catal B:Environ,2009,90(1/2):233-241.
[3]Kang J H,Kito K,Fusao K.Factors influencing the migration of bisphenol A from cans[J].Food Prot,2003,66 (8):1444-1447.
[4]Naik P.Vijayalaxmi K K.Cytogenetic evaluation for genotoxicity of Bisphenol-A in bone marrow cells of Swiss albino mice[J].Mutat Res,2009,676:106-112.
[5]Kang J H,Asai D,Katayama Y.Bisphenol A in the aquatic environment and its endorinedisruptive effects on aquatic organisms[J].Crit Rev Toxicol,2007,37(7):607 -625.
[6]Welshons W V,Nagel S C,vom Saal F S.Large effects from small exposures.III.Endocrine mechanisms mediating effects of bisphenol A at levels of human exposure [J].Endocrinology,2006,147(6):56-69.
[7]Sliva D,Labarrere C,Slivova V,et al.Ganoderma lucidum suppresses motility of highly invasive breast and prostate cancer cells[J].Biochem Bioph Res Co,2002,298 (4):603-6l2.
[8]Chin Y P,Miller P L,Zeng L,et al.Photosensitized Degradation of Bisphenol A by Dissolved Organic Matter[J]. Environ Sci Technol,2004,38(22):5888-5894.
[9]Hu J Y,Chen X,Tao G,et al.Fate of Endocrine Disrupting Compounds in Membrane Bioreactor Systems[J]. Environ Sci Technol,2007,41(11):4097-4102.
[10]Hu J Y,Aizawa T,Ookubo S.Products of Aqueous Chlorination of Bisphenol A and Their Estrogenic Activity [J].Environ Sci Technol,2002,36(9):1980-1987.
[11]Liu H,Wang C,Li X Z,Xuan X L,et al.A Novel Electro-Fenton Process for Water Treatment:Reaction-controlled pH Adjustment and Performance Assessment[J]. Environ Sci Technol,2007,41(8):2937-2942.
[12]Pignatello J J.Dark and photoassisted iron(3+)-catalyzed degradation of chlorophenoxy herbicides by hydrogen peroxide[J].Environ Sci Technol,1992,26(5):944 -951.
[13]Sun Y F,Pignatello J J.Photochemical reactions involved in the total mineralization of 2,4-D by iron(3+)/hydrogen peroxide/UV[J].Environ Sci Technol,1993,27(2): 304-310.
[14]Ventura A,Jacquet G,Bermond A,et al.Electrochemical generation of the Fenton’s reagent:application to atrazine degradation[J].Water Res,2002,36(14):3517-3522.
[15]Ai Z H,Lu L R,Li J P,et al.Fe@Fe2O3core-shell nanowires as iron reagent.2.An efficient and reusable sono-Fenton system working at neutral pH[J].Phys. Chem.C,2007,111(20):7430-7436.
[16]Lide D R.CRC Handbook of Chemistry and Physics.87th ed[M].Boca Raton,FL:CRC Press,2007.
[17]Staples C A,Dorn P B,Klecka G M,et al.A review of the environmental fate,effects,and exposures of bisphenol A [J].Chemosphere,1998,36(10):2149-2173.
[18]Ioan I,Wilson S,Lundanes E,et al.Comparison of Fenton and sono-Fenton bisphenol A degradation[J].J Hazard Mater,2007,142(1/2):559-563.
[19]Torres R A,Abdelmalek F,Combet E,et al.A comparative study of ultrasonic cavitation and Fenton’s reagent for bisphenol A degradation in deionised and natural waters[J].J Hazard Mater,2007,146(3):546-551.
[20]Gozmen B,Oturan M A,Oturan N,et al.Environ.Indirect electrochemical treatment of bisphenol A in water via electrochemically generated Fenton’s reagent[J].Sci Technol,2003,37(16):3716-3723.
[21]Gogate P R,Pandit A B.A review of imperative technologies for wastewater treatment II:hybrid methods[J].Adv Environ Res,2004,8(3/4):553-597.
[22]Henglein A.historical deveopments and modern aspects [J].Ultrasonics,1987,25(1):6-16.
[23]Hua I,Hoffmann M R.Kinetics and mechanism of the sonolytic degradation of CCl4:intermediates and byproducts[J].Environ Sci Technol,1996,30(3):864-871.
[24]Makino K,Mossoba M M,Riesz P.Chemical effects of ultrasound on aqueous solutions.Formation of hydroxyl radicals and hydrogen atoms[J].J Phys Chem,1983,87 (8):1369-1377.
[25]Riesz P,Berdahl D,Christman C L.Free radical generation by ultrasound in aqueous and nonaqueous solutions [J].Environ Health Persp,1985,64:233-252.
[26]Petrier C,Casadonte D,Mason T J,et al.Advances in Sonochemistry,Ultrasound in Environmental Protection [M].Stamford:JAI Press Inc.,2001:91-109.
[27]Makino K,Mossoba M M,Riesz P.Chemical effects of ultrasound on aqueous solutions.Evidence for hydroxyl and hydrogen free radicals(·OH and·H)by spin trapping[J].J Am Chem Soc,1982,104(12):3537-3539.
[28]Joseph C G,Puma G L,Bono A,et al.Sonophotocatalysis in advanced oxidation process:a short review[J].Ultrason Sonochem,2009,16(5):583-589.
[29]Weissler A.Formation of hydrogen peroxide by ultrasonicwaves:free radicals[J].J Am Chem Soc,1959,81(5): 1077-1081.
[30]Hart E J,Henglein A.Free radical and free atom reactions in the sonolysis of aqueous iodide and formate solutions[J].J Phys Chem,1985,89(20):4342-4347.
[31]Muruganandham M,Yang J S,Wu J J.Effect of ultrasonic irradiation on the catalytic activity and stability of goethite catalyst in the presence of H2O2at acidic medium [J].Ind Eng Chem Res,2007,46(3):691-698.
[32]Torres R A,Pétrier C,Combet E,et al.Bisphenol A mineral-ization by integrated ultrasound-UV-iron(II)treatment[J].Environ Sci Technol,2007,41(1):297-302.
[33]Ai Z H,Lu L R,Li J P,et al.Fe@Fe2O3core-shell nanowires as iron reagent.1.Efficient degradation of rhodamine B by a novel sono-Fenton process[J].J Phys Chem C,2007,111(11):4087-4093.
[34]Mohapatra D P,Brar S K,Tyagi R D,et al.Concomitant degradation of bisphenol A during ultrasonication and Fenton oxidation and production of biofertilizer from wastewater sludge[J].Ultrason Sonochem,2011,18 (15):1018-1027.
[35]Blume T,Neis U.Improved wastewater disinfection by ultrasonic pre-treatment[J].Ultrason Sonochem,2004,11 (5):333-336.
[36]Hideyuki K,Shinsuke K,Satoshi K,et al.Degradation of bisphenol A in water by the photo-Fenton reaction[J].J photoch photobio A,2004,162(2-3):297-305.
[37]Will I B S,Moraes J E F,Teixeira A C S C,et al.Photo-Fenton degradation of wastewater containing organic compounds in solar reactors[J].Sep Purif Technol,2004,34 (1/3):51-57.
[38]Wu D,Liu M,Dong D,et al.Effects of some factors during electrochemical degradation of phenol by hydroxyl radicals.Microchem[J].Microchem,2007,85(2):250 -256.
[39]Li D,Yuranova T,Albers P,et al.Accelerated photobleaching of Orange II on novel(H5FeW12O4010H2O)/silica structured fabrics[J].Water Res,2004,38(16):3541 -3550.
[40]Rios-Enriquez M,Shahin N,Durán-de-Bazúa C,et al. Optimization of the heterogeneous Fenton-oxidation of the model pollutant 2,4-xylidine using the optimal experimental design methodology[J].Solar Energy,2004,77 (5):491-501.
[41]Bossmann S H,Oliveros E,Göb S,et al.Degradation of polyvinyl alcohol(PVA)by homogeneous and heterogeneous photo catalysis applied to the photochemicaly enhanced Fenton reactions[J].Water Sci Technol,2001,44 (5):257-262.
[42]Fernandez J,Bandara J,Lopez A,et al.Photoassisted Fenton degradation of nonbiodegradable azo dye(Orange II)in Fe-free solutions mediated by cation transfer membranes[J].Langmuir,1999,15(1):185-192.
[43]Fernandez J,Bandara J,Lopez A,et al.Efficient photoassisted Fenton catalysis mediated by Fe ions on Na?on membranes active in the abatement of nonbiodegradable azo-dye[J].Chem Commun,1998:1493-1494.
[44]Bozz A,Yuranova T,Mielzcarski E,Mielzcarski J,Buffat P A,Lais P,Kiwi J.Superior biodegradability mediated by immobilized Fe-fabrics of waste waters compared to Fenton homogeneous reactions[J].Appl Catal B:Environ,2003,42(3):289-303.
[45]Torres-Palma R A,Nieto J I,Combet E,et al.An innovative ultrasound,Fe2+and TiO2photoassisted process for bisphenol a mineralization[J].Water Res,2010,44(7): 2245-2252.
[46]Liu W P,Zhang H,Cao B P,et al.Oxidative removal of bisphenol A using zero valent aluminum-acid system[J]. Water Res,2011,45(4):1872-1878.
[47]Li C,Li X Z,Graham N,et al.The aqueous degradation of bisphenol A and steroid estrogens by ferrate[J].Water Res,2008,42(1/2):109-120.
(责任编辑 何杰玲)
Degradation of Environmental Endocrine Disruptors Bisphenol A by Fenton-like Method
SONG Li-hong,LI Juan,WAN Zhong-hua,HUANG Xiao-ying
(Shenzhen Academy of Environmental Science,Shenzhen 518001,China)
Bisphenol A(BPA)has
a great deal of attention from regulatory agencies and scientists,for it has estrogenic activity and serves as an environmental endocrine disruptor.For the properties of endocrine disrupt activity and poor biodegradability,there are many researches on developing rapid,ef?cient,economic AOPs for the degradation of BPA in wastewater both at home and abroad. As one of the most efficient method of AOPs,Fenton-like method can overcome the disadvantage of traditional Fenton method and degrade BPA rapidly.In this paper,the physical and chemical properties of Bisphenol A are introduced.The types of Fenton-like methods for degradation of BPA and the effect as well as influencing factors are also discussed.The progress in degradation of BPA by Fentonlike method is illuminated emphatically.At last,the promising future of this technology is prospected.
Fenton-like reaction;bisphenol A;degradation
X506
A
1674-8425(2014)08-0064-07
10.3969/j.issn.1674-8425(z).2014.08.014
2014-02-16
宋丽红(1980—),女(蒙古族),内蒙古开鲁县人,主要从事环境影响评价及污染控制、环境管理研究。
宋丽红,李娟,宛中华,等.类芬顿法降解环境内分泌干扰物双酚A的研究进展[J].重庆理工大学学报:自然科学版,2014(8):64-70.
format:SONG Li-hong,LI Juan,WAN Zhong-hua,et al.Degradation of Environmental Endocrine Disruptors Bisphenol A by Fenton-like Method[J].Journal of Chongqing University of Technology:Natural Science,2014 (8):64-70.

