HPLC法测定肠虫清胶囊中阿苯达唑的含量
游国叶,樊轻亚,熊大伟
(信阳职业技术学院药学院,河南信阳464000)
肠虫清胶囊的主药成分为阿苯达唑(Albendazole,ABZ),又名丙硫咪唑,化学名为5-丙硫基-1H-苯并咪唑-2-氨基甲酸甲酯,为一广谱高效低毒的驱虫药,该药现已被列入医保产品,成为临床上用于治疗各种蠕虫感染性疾病的首选药物[1]。在阿苯哒唑原料的现行标准中,其含量测定在美国药典29 版[2]、欧洲药典 5.0 版[3]和中国药典 2010 年版中均为滴定法,其胶囊剂含量测定在中国药典2010年版规定的方法为分光光度法,利用295 nm处的吸收系数计算含量[4]。HPLC法测定阿苯达唑的含量的报道较为少见[5],笔者通过建立高效液相色谱法(high performance liquid chromatography,HPLC)测定肠虫清胶囊中阿苯达唑的含量,方法快速、准确,重现性好。
1 仪器与试剂药品
1.1 仪器 Waters 2695高效液相色谱仪;Waters 2996紫外检测器 (美国Waters公司);BP 211D型半微量电子天平;PHS—2CA数字式酸度计(上海理达仪器厂)。
1.2 试剂与药品 肠虫清胶囊(新乡市同心药业,批号20080110,20080113,20080117,规格0.2 g);阿苯达唑对照品 (中国药品生物制品检验所,批号100373—200301);纯化水(新乡市平安药业有限公司);甲醇为色谱纯(江苏国达,200704),其他试剂均为分析纯。
2 方法与结果
2.1 色谱条件与系统适用性试验 阿苯达唑为碱性化合物,与硅胶柱的硅醇基有较强的相互作用,会造成强保留,因此应选择硅醇相互作用弱的色谱柱,Luna C18的硅醇相互作用约为 0.2[5],能够获得理想的分析结果。
流动相之一应该选择缓冲液,以获得稳定的保留时间,同时为了解决阿苯达唑的溶解性问题,选取0.1 mol·L-1醋酸铵缓冲液(用醋酸调节 PH至3.1)。当缓冲液和甲醇的比例调整到40∶60时,阿苯达唑的保留时间稳定在9.8 min左右。流量为1 mL/min,柱温20℃。
取阿苯哒唑对照品用醋酸溶解,流动相稀释成1 mg·mL-1,在200~400 nm的波长范围内扫描,阿苯哒唑在288 nm处有最大吸收,故紫外检测器的波长为288 nm。
所以色谱条件为:色谱柱:Luna C18(5 μm,250×4.6 mm);流动相:甲醇 -0.1 mol·L-1醋酸铵缓冲液(用醋酸调节PH至3.1)(60∶40);检测波长:288 nm;流量:1 mL/min;进样量:20 μl;柱温:20 ℃。
在上述色谱条件下,阿苯达唑的色谱图见图1,和杂质峰的分离度大于1.5,拖尾因子1.03,理论塔板数按阿苯达唑计算大于3 500。
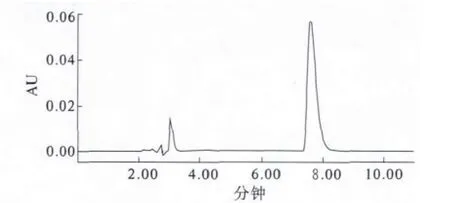
图1 阿苯达唑的色谱图
2.2 溶液制备
2.2.1 对照品溶液的制备 精密称取阿苯达唑对照品50 mg,置50 mL量瓶中,加醋酸10 mL,振摇使溶解,加甲醇稀释至刻度,摇匀,准确量取5.0 mL置10 mL量瓶中,加流动相定容,摇匀,稀释成0.5 mg·mL-1对照品液。
2.2.2 供试品溶液的制备 取本品内容物,研细,精密称取适量(约相当于阿苯达唑50 mg),置50 mL量瓶中,加醋酸10 mL,振摇使溶解,加甲醇稀释至刻度,摇匀,滤过,取续滤液5.0 mL置10 mL量瓶中,加流动相定容,摇匀,即得。
2.3 线性关系考察 精密称取干燥至恒重的阿苯达唑对照品50 mg,置50 mL量瓶中,加醋酸10 mL,振摇使溶解,加甲醇稀释至刻度,摇匀,即得阿苯达唑对照品储备液。分别准确量取 1.0,2.0,4.0,5.0,6.0,8.0 和 10.0 mL 阿苯达唑对照品储备液置10 mL 量瓶中,加流动相定容,摇匀,即成 0.1,0.2,0.4,0.5,0.6,0.8,1.0 mg·mL-1系列溶液,按 2.1项下色谱条件测定峰面积,以峰面积对浓度作线性回归,结果见图2。结果表明,阿苯达唑在0.1~1.0 mg·mL-1浓度范围内 A=2.85 ×106C+6.5 ×104,r=0.999 5,线性关系良好。

图2 阿苯达唑的线性关系
2.4 精密度试验 取0.5 mg·mL-1阿苯达唑对照品溶液,按2.1项下色谱条件进样6次,测定峰面积,结果见表2,可见精密度试验RSD为0.40%,精密度良好。

表2 精密度实验结果
2.5 重复性试验 取同一批号20080113样品,按2.3项下方法制备6份供试液,按2.1项下色谱条件进样,测定峰面积,计算含量,结果见表3,重复性试验RSD为0.66%,重复性良好。
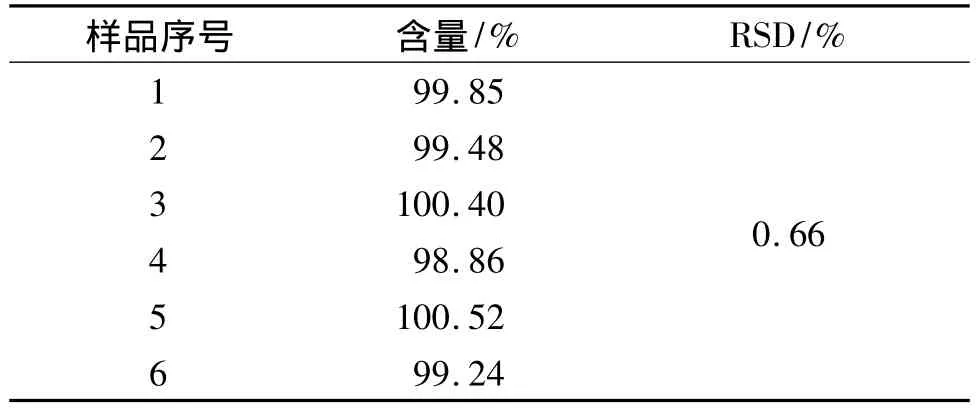
表3 重复性试验结果
2.6 加样回收率试验 称取已知含量的样品(20080113)细粉 50 mg,分别加入高、中、低(20 mg、40 mg、60 mg)不同量干燥至恒重的阿苯达唑对照品,各3份,按含量测定方法进行测定,计算回收率,结果见表4。
2.7 稳定性试验 取同一供试品溶液在放置时间为0、2、4、6、10 h 时进样,测定峰面积,结果见表 5,稳定性试验RSD为0.52%,稳定性良好。
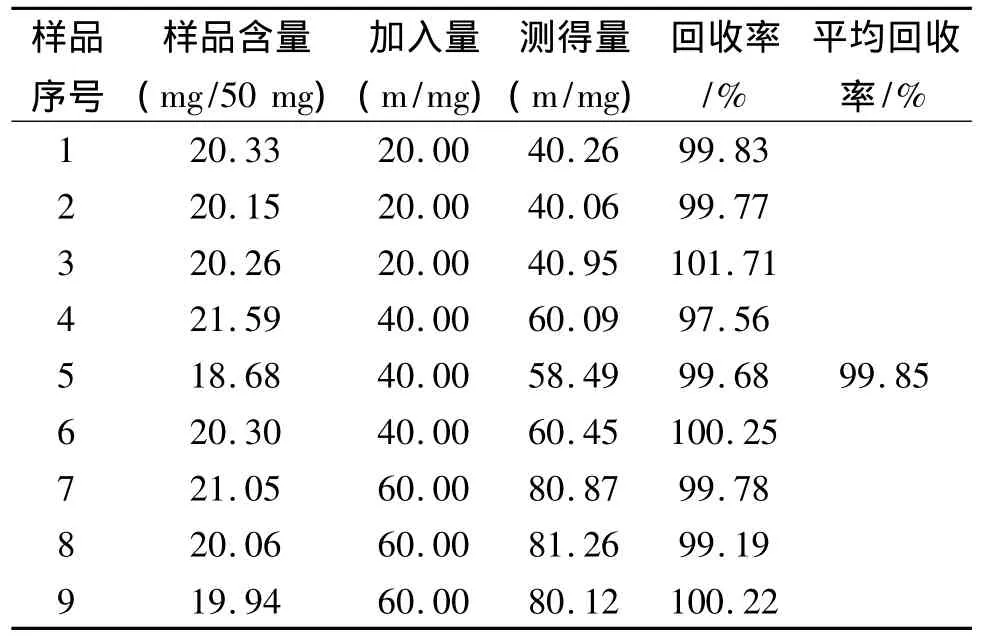
表4 加样回收率试验结果
2.8 定量限 按信噪比为3(S/N=3)对最低检测限进行测定,结果表明,当进样浓度为 0.25 μg·mL-1时,阿苯哒唑峰信号约为基线噪音的3倍,即最低检测浓度为 0.25 μg·mL-1。
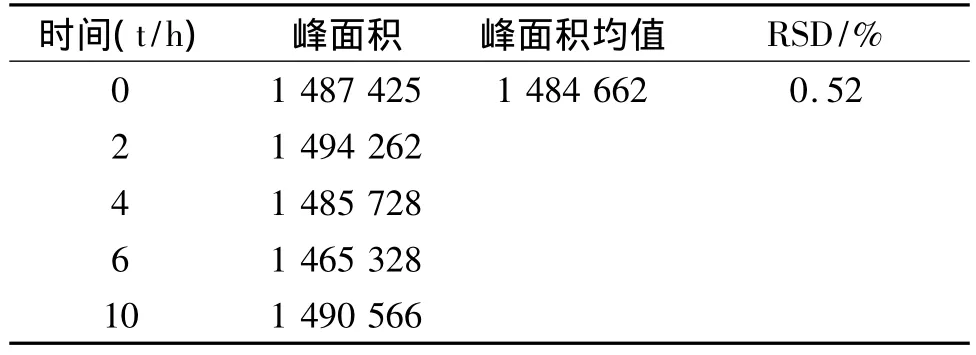
表5 稳定性试验结果
2.9 样品含量测定 取3批样品各20粒胶囊,倾出内容物,囊壳用小刷拭净,精密称定,精密称取适量(约相当于阿苯达唑50 mg),按2.2.2项下方法制备供品溶液。分别取供试液和2.2.1项下对照品液,在2.1项下色谱条件进样,用峰面积外标法计算含量;并与中国药典[6]规定的紫外分光光度法(UV法)测定的结果比较,结果见表6。
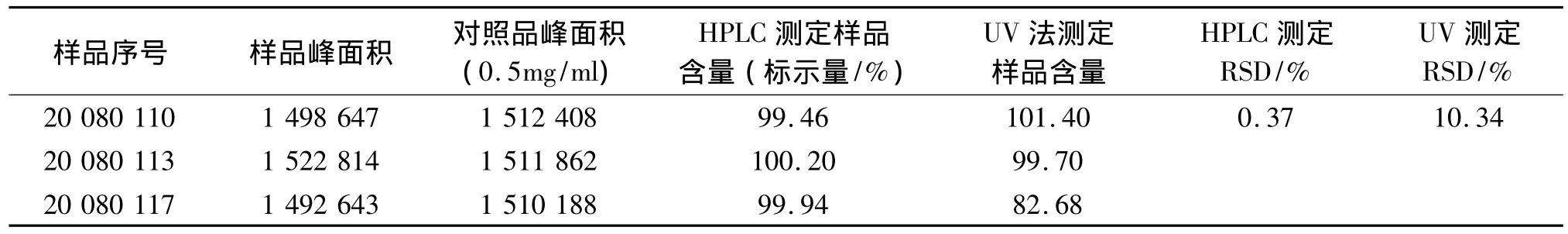
表6 样品含量测定结果
3 讨论
阿苯达唑微溶于丙酮、乙酸,不溶于乙醇、水[3],制约了流动相的选择,采用甲醇-醋酸铵缓冲液为流动相,通过调整流动相比例和PH值,既解决了溶解性问题,也获得了较好的系统适用性。
虽然药典规定的分光光度法在295 nm波长处测定吸收值,但在本实验的色谱条件下,阿苯达唑的最大吸收在288 nm处,这是因为在pH 3.1时,阿苯达唑以离子状态存在,共轭结构减少,最大吸收向短波方向移动。
与中国药典规定的分光光度法相比(当时没做其他比较,单从分光光度法和HPLC两种方法的测定同批产品的含量,根据RSD来判断后精密度、准确度高于前者,故得出结论。)本法能够排除杂质干扰,准确度高,HPLC法重复性、稳定性好。
[1]万启惠.广谱驱蠕虫新药—— 丙硫咪唑[J],遵义医学院学报,1988,l1(1):73-74.
[2]美国药典委员会.美国药典/国家处方集[M].29版.美国:美国药典委员会,2006:2505.
[3]欧洲药品质量委员会.欧洲药典5.0.(EDQM)[M].编辑出版.法国:中外药品质量管理局:2004,1 122-1 123.
[4]国家药典委员会.中华人民共和国药典(二部)[M].北京:化学工业出版社,2010:290.
[5]邵 超.HPLC法测定阿苯达唑颗粒的含量[J].黑龙江医药,2011,03(5):341-342.
[6]国家药典委员会.中国药典[M].二部.北京:中国医药科技出版社,2010:395.

