尿素乳膏护理干预索拉非尼相关手足皮肤反应随机对照研究
安林静,张昕,张丽娜,李因茵,陆荫英,杨永平
(1.解放军302医院肝脏肿瘤诊疗与研究中心一科,北京,100039;2.解放军第302医院护理部,北京,100039)
尿素乳膏护理干预索拉非尼相关手足皮肤反应随机对照研究
安林静1,张昕2,张丽娜1,李因茵1,陆荫英1,杨永平1
(1.解放军302医院肝脏肿瘤诊疗与研究中心一科,北京,100039;2.解放军第302医院护理部,北京,100039)
目的评价尿素乳膏(UBC)护理干预索拉非尼治疗肝细胞癌(HCC)所诱导手足皮肤反应(HFSR)的效果。方法202例进展HCC患者,随机分为2组各101例,尿素乳膏组采取10%尿素乳膏涂抹手脚一日3次加基础护理,对照组采取单纯基础护理。护理干预12周,每2周观察HFSR发生情况,一旦发生HFSR患者允许应用任何乳膏包括尿素乳膏。结果
护理干预结束时,尿素乳膏组48.5%(49/101)的患者发生HFSR,显著低于基础护理组的69.3%;2级以上HFSR发生者占19.8%(20/101),明显低于基础护理组35.6%(36/101)。尿素乳膏组患者首次发生HFSR的中位时间是基础护理组的1.63倍,尿素乳膏不影响索拉非尼治疗剂量调整、临床反应和疾病控制。结论尿素乳膏护理干预可降低HCC患者接受索拉非尼治疗时HFSR发生,减轻HFSR发生程度,延长首次HFSR发生时间,改善服用索拉非尼治疗患者的生活质量。
护理干预;尿素乳膏;索拉非尼;手足皮肤反应;进展期肝细胞癌
肝细胞癌(HCC)列中国第二位肿瘤相关死亡疾病,70%以上的HCC 患者确诊时已是进展期,缺少有效治疗,预后差[1]。索拉非尼经临床试验证明是治疗进展期HCC的有效治疗药物,成为进展期HCC的标准一线治疗。接受索拉非尼治疗的HCC患者常发生皮肤相关药物副作用,譬如手足皮肤反应(HFSR)和脱发等。HFSR发生率为46%~63.6%,Ⅲ级HFSR发生率为12.2%~15.5%[2-3]。虽然HFSR不危及生命,但影响患者的生活质量。因此,给予科学护理干预降低或减轻HFSR,确保HCC患者能耐受索拉非尼治疗剂量,提高生活质量,延长生存期是临床护理亟须解决的问题。尿素乳膏(UBC)广泛应用治疗皮肤过度角化[4],本文通过前瞻性随机对照研究尿素乳膏联合基础护理干预对进展期HCC患者接受索拉非尼治疗发生HFSR的效果,现报道如下。
1 资料与方法
1.1 一般资料
依据HCC巴塞罗那分期[5-6],2010年1月—2012年12月,718例连续收住本中心进展期HCC患者。127例为Child-Pugh C;93例Child -Pugh B,但血胆红素>51.3μmol/L;76例人体性能指数>2;64例预计生存期小于3个月;156例因经济条件放弃服用索拉非尼治疗。516例进展期HCC患者被排除。202例HCC患者进入该研究,其中男性162例,女性40例,年龄35~67岁,平均51.9岁,有乙肝家族史128例,有肝癌家族史66例;Child-Pugh A5(60/202,29.7%),A6(79/202,39.1%),B7(46/202,22.8%)和B8(17/202,8.4%)。按1∶1比例随机分成尿素乳膏加基础护理组(UBC+BSC)和基础护理组(BSC)各101例,2组间患者基本临床特点没有显著差异。入选标准:根据实体瘤疗效评价标准(RECIST)[7]至少有1个能测量的靶病灶的进展期HCC患者接受索拉非尼治疗;人体性能指数≤2;Child-Pugh A或B,且血胆红素<51.3μmol/L,ALT及AST水平为5倍正常值以内;血小板>50×109/L,血红蛋白>89 g/L;预计生存时间至少12周以上。所有入选患者均签署知情同意书。
1.2 试验设计
所有患者接受索拉非尼标准剂量(0.4,口服,1日2次)治疗满12周,按1:1随机分入尿素乳膏加基础护理组(10%尿素乳膏涂抹手脚一日3次)和基础护理组。HFSR和其他药物相关不良反应的评价参照NCI-CTCAE version 3.0标准[5]。患者一旦出现HFSR可应用其他软膏。12周内每2周检查一次,随访14周。每4周复查血常规和血生化,每8周复查腹部增强CT扫描或MRI。主要终点服用索拉非尼治疗12周内任何级别HFSR的发生例数;次要终点包括Ⅱ级以上HFSR发生例数,首次出现HFSR时间,HFSR持续时间和索拉非尼剂量调整例数。
1.3 样本量
据前期观察HFSR累计发生率65.5%[2];设想尿素乳膏护理干预后HFSR累计发生率为45.5%,采用单侧检验,检测水准0.05,功效0.80,应用Pass 2002统计软件,按1∶1完成样本量估算,大约需要202个患者包括5%的脱失率。
1.4 索拉非尼剂量调整
根据药物相关毒性级别而调整索拉非尼剂量。Ⅰ级药物相关毒性反应索拉非尼剂量不调整;Ⅱ级毒性反应索拉非尼改为0.2 g,1日2次,待毒性反应恢复到0-Ⅰ级恢复索拉非尼改为0.4 g,1日2次;Ⅲ级毒性反应停用索拉非尼,待毒性反应恢复到0-Ⅰ级恢复索拉非尼改为0.2 g,1日2次。
1.5 疗效和不良反应评价
治疗后每4周CT或MRI检查1次,根据RECIST评价治疗效果[7]。不良反应分级采用美国国立癌症研究所常见毒性分级标准3.0版(NCICTC 3.0)共分1~4级[5]。
1.6 统计学方法
采用SPSS 13.0软件进行分析。采用Kaplan -Meier法进行生存分析,率的比较采用x2检验,P<0.05为差异有统计学意义。
2 结果
2.1 尿素乳膏护理干预对手足综合征发生情况的影响
进展期肝癌患者服用索拉非尼治疗期间,给予尿素乳膏加基础护理干预12周结束时,尿素乳膏护理干预组累计发生HFSR患者(49/101)显著低于基础护理组(70/101);且2/3级HFSR发生患者在尿素乳膏护理干预组(20/101)显著低于基础护理组(29/101)。尿素乳膏护理干预组首次发生HFSR的中位时间是基础护理组的1.63倍,明显滞后于基础护理组。2组比较差异均有统计学意义(P<0.05),见表1。
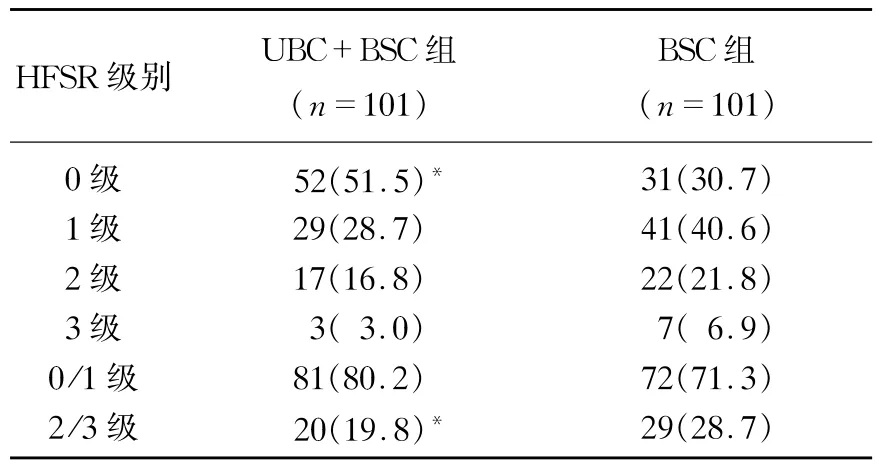
表1 尿素乳膏护理干预对肝癌患者索拉非尼相关HFSR发生情况的影响[n(%)]
2.2 尿素乳膏护理干预对手足综合征发生时间的影响
尿素乳膏护理干预组与基础护理组对HFSR发生时间分布显示,服用索拉非尼治疗2周以内尿素乳膏加基础护理干预组发生HFSR患者占30.6%(15/49),明显低于基础护理组39.5%(28/70);而服用索拉非尼治疗6周以后,尿素乳膏加基础护理干预组中发生HFSR的患者占到了44.9%(22/49),明显高于基础护理组的33.7%(24/71),2组比较差异均有统计学意义(P<0.05),见表2。
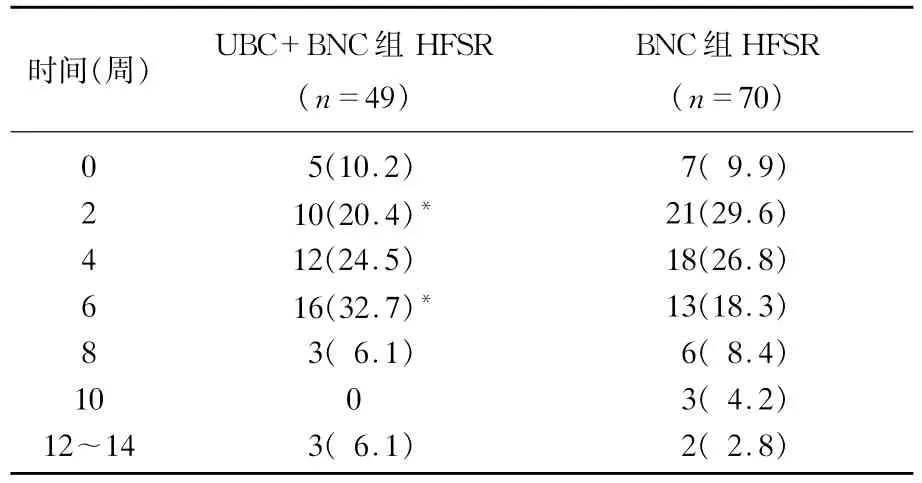
表2 尿素乳膏护理干预对肝癌患者索拉非尼相关HFSR发生时间分布的影响[n(%)]
2.3 尿素乳膏护理干预对索拉非尼相关不良反应的影响
结果显示,尿素乳膏加基础护理干预对其他索拉非尼相关不良反应没有明显的影响作用,进一步分析尿素乳膏加基础护理干预不影响HCC患者的索拉非尼治疗剂量调整、临床反应和疾病控制。见表3。
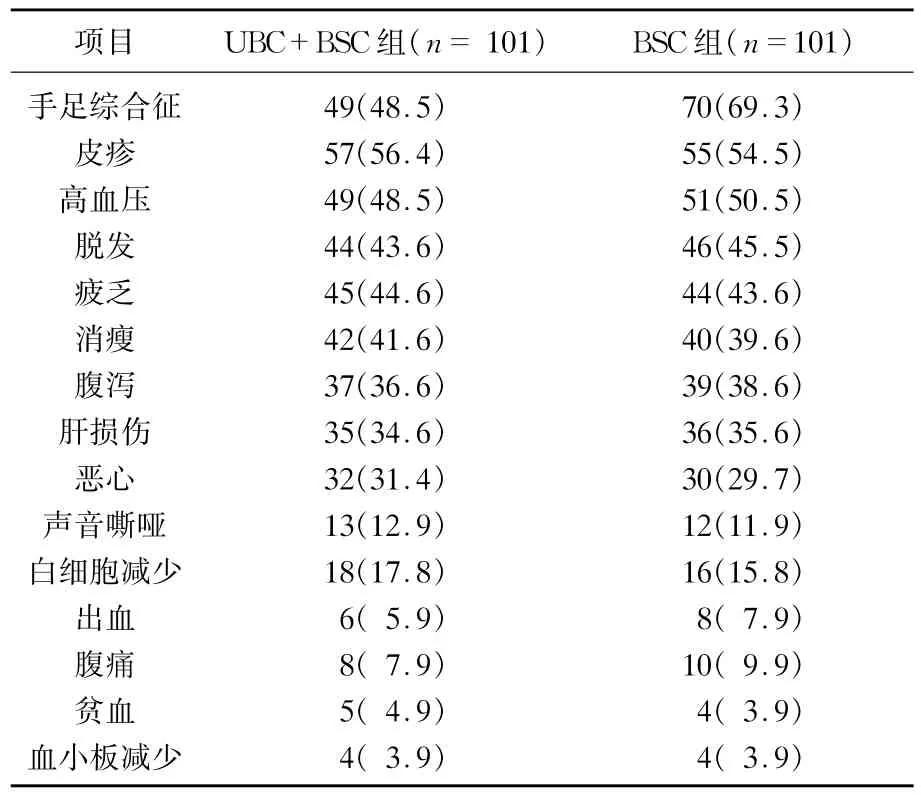
表3 尿素乳膏护理干预索拉非尼治疗肝细胞癌相关不良反应发生情况[n(%)]
3 讨论
酪氨酸激酶抑制剂包括索拉非尼应用2~4周患者常出现HFSR,5周达到高峰,随后逐渐减低。重度HFSR需要减少酪氨酸激酶抑制剂剂量甚至停用[8-9],严重影响患者的生活质量和接受酪氨酸激酶抑制剂的依从性[10]。尽管HFSR具有较高的发生率,但缺乏有效的护理干预措施。报道[4]称无对照观察应用含40%尿素,0.1%他佐罗汀和5%氟尿嘧啶的乳膏局部处理HFSR患者临床获益较好。因此,本研究前瞻性随机对照观察了尿素乳膏护理干预对索拉非尼相关HFSR的影响和临床获益。本研究按照意向性全部分析了纳入研究的202例接受索拉非尼治疗的HCC患者,系统分析了尿素乳膏护理干预对接受索拉非尼治疗的HCC患者发生HFSR的影响。本研究结果表明接受索拉非尼治疗的HCC患者发生HFSR率为69.3%,与其他研究观察到的结果相似[2,6,11-14]。但尿素乳膏护理干预不仅降低了HFSR总体发生率,即由69.3%降为48.5%,而且2/3级HFSR发生率也由28.7%降为19.8%,提高了HCC患者接受索拉非尼治疗的耐受性。更为重要的是,发现尿素乳膏护理干预明显延长了首次发生HFSR的中位时间,这样使进展期HCC患者因HFSR而不能完成12周索拉非尼治疗的风险明显降低。与维甘乳膏联合维生素B6治疗卡培他滨相关手足综合征可以提高患者对化疗的耐受性结果相一致[15]。由于索拉非尼诱导HFSR发生的机理还不清楚[8],尽管尿素乳膏护理干预可降低HFSR总体发生率和减轻HFSR发生程度,但进一步分析发现尿素乳膏护理干预并不能影响HCC患者的索拉非尼治疗剂量调整,临床反应和疾病控制。这可能因单中心研究的局限性掩盖了尿素乳膏护理干预对HCC患者索拉非尼治疗剂量调整,临床反应和疾病控制的影响作用,需多中心随机对照研究加以进一步证实。
[1]Yuen M F,Hou J L,Chutaputti A.Hepatocellular carcinoma in the Asia Pacific region[J].Gastroenterol Hepatol,2009,24:346.
[2]安林静,郝莉燕,张昕,等.索拉非尼治疗进展期肝细胞癌患者的不良反应及其对预后的影响[J].解放军护理杂志,2010,28(9A):8.
[3]Chunping Wang,Yinting Lu,Hong Wang,et al.Cryotherapy is associated with improved clinical outcomes of sorafenib for the treatment of advanced hepatocellular carcinoma[J]. Experimental and Therapeutic Medicine,2012,4(10):188.
[4]Hagemann I,Proksch E.Topical treatment by urea reduces epidermal hyperproliferation and induces differentiation in psoriasis[J].Acta Derm Venereo,1996,176:353.
[5]Trotti A,Colevas A D,Setser A,et al.CTCAE v3.0:development of a comprehensive grading system for the adverse effects of cancer treatment[J].Semin Radiat Oncol,2003,13:176.
[6]Bruix J,Sherman M.Management of hepatocellular carcinoma Practice Guidelines Committee,American Association for the Study of Liver Diseases[J].Hepatology,2005,42:1208.
[7]Therasse P,Arbuck SG,Eisenhauer E A,et al.New guidelines to evaluate the response to treatment in solid tumors. European Organization for Research and Treatment of Cancer,National Cancer Institute of the United States,National Cancer Institute of Canada[J].J Natl Cancer Inst,2000,92:205.
[8]Dranitsaris G,Vincent M D,Yu J,et al.Development and validation of a prediction index for hand-foot skin reaction in cancer patients receiving sorafenib[J].Ann Oncol,2012,23:2103.
[9]周胜涟,陈州华,龚辉.化疗后手足综合征的中西医治疗研究进展[J].中西医结合研究,2013,5(10):38.
[10]Manchen E,Robert C,Porta C.Management of tyrosine kinase inhibitor-induced handfoot skin reaction:viewpoints from the medical oncologist,dermatologist,and oncology nurse[J].JSupport Oncol,2011,9:13.
[11]Cheng A L,Kang Y K,Chen Z,et al.Efficacy and safety of sorafenib in patients in the Asia-Pacific region with advanced hepatocellular carcinoma:a phaseⅢrandomised,double-blind,placebo-controlled trial[J].Lancet Oncol,2009,10:25.
[12]杨笑梅,廖鑫,聂新,等.卡培他滨致患者腹泻和手足综合征的防护[J].护理学杂志,2014,29(9):37.
[13]张永红,邵春燕.抗肿瘤治疗致手足综合征26例护理体会[J].吉林医学,2014,35(7):1568.
[14]李莹.使用卡培他滨维持化疗引起的手足综合征发病特点的观察[J].临床医学工程,2014,21(1):66
[15]连文,张通,杨平,等.维甘乳膏联合维生素B6治疗卡培他滨相关手足综合征的临床观察[J].中国药房,2013,24(48):4529.
Randomized controlled trial of nurse intervention of urea-based cream on sorafenib-associated hand-foot skin reactions of patients
AN Linjing1,ZHANG Xin2,ZHANG Lina1,LI Yinyin1,LU Yinying1,YANG Yongping1
(Center of Therapeutic Research for Hepatocellular Carcinoma,Beijing 302nd Hospital of PLA,Beijing,100039)
Objective To assess the effect of nurse intervention of urea-based cream(UBC)on sorafenib-induced hand-foot skin reaction(HFSR)in patients with advanced hepatocellular carcinoma(HCC).Methods 202 advanced HCC patients were randomly divided into 2 groups.101 patients in the urea-based cream group were applied with 10%UBC three times daily and best nursing while 110 patients in the control group were applied basic nursing alone.The treatment lasted for 12 weeks.HFSR was assessed every 2 weeks.Once HFSR occurred,patients were allowed any cream,including UBC.Results After the nursing,the incident rate of HFSR and incidence of grade≥2 HFSR in the UBC group were lower that than in the BNC group.The Median time to first occurrence of HFSR was 1.63 times of UBC group.UBC did not affect the adjustment of sorafenib dose,response or disease control.Conclusion UBC nurse intervention of advanced HCC patients could reduce HFSR rate,extend the time of first occurrence of HFSR and improve the quality of life of patients.
nurse intervention;UBC;sorafinib;hand-foot skin reaction;advanced hepatocellular carcinoma
R 472.9
A
1672-2353(2014)22-045-03
10.7619/jcmp.201422014
2014-05-25
解放军“十二五”重点项目资助课题(BWS11J074)
杨永平,E-mail:yongpingyang@hotmail.com

