改良空肠间置术在近端胃癌根治术中应用的临床研究
蔡联明 卢致洋 刘振华 肖幼华
胃癌是临床中常见的恶性肿瘤,近年来胃底贲门癌在胃癌发病中有逐步增多的趋势[1-2]。手术治疗仍是最理想的治疗方式,根治性近端胃切除术与根治性全胃切除术均适用于近端胃癌[3]。而近端胃癌根治术后,无论是全胃切除还是次全胃切除,患者的生活质量均受到严重影响[4-5]。因此,选用1 种合理的消化道重建方法,对于减少近端胃癌患者术后并发症的发生,改善患者术后的生活质量显得尤为重要。本研究在近端胃癌根治术中,近端胃次全切后,分别采用改良空肠间置术和传统残胃-食管吻合进行消化道重建,比较二者术后并发症及生活质量等情况,现报道如下。
1 资料与方法
1.1 一般资料 选取江西省赣州市肿瘤医院2011年7月~2013年6月期间明确诊断为近端胃癌30 例患者作为研究对象(30 例患者术前均经CT、胃镜及活检病理检查明确诊断,均为近端胃癌,术前分期为T1-3N0-2M0),其中男18 例,女12 例,男女比例为3∶2,年龄42~78岁,中位年龄为57 岁。根据近端胃癌根治术后重建方式不同均分为改良空肠间置术组(观察组)和传统胃-食管吻合组(对照组)(n=15)。2 组患者间一般资料无明显差异,具有可比性。
1.2 治疗方法 观察组和对照组患者均于全身麻醉后经腹完成。观察组患者处理方式:按照近端胃癌根治术常规行含肿瘤组织在内的食管、胃组织切除和淋巴清扫(D 2 或D 2+)。并注意保留胃网膜右血管弓及胃右血管1~2 分支。缝合关闭胃断端,在结肠前提起空肠,将距Treitz 韧带25~30 cm 的空肠段与食管用管状吻合器行侧端吻合,注意保证吻合口无张力,在空肠输出袢距此吻合口15~20 cm 处作空肠与残胃后壁侧侧吻合,距空肠残胃吻合口远段10~15 cm,作输入、输出袢空肠侧侧吻合,分别距食管空肠吻合口5 cm 输入袢空肠和残胃输出袢吻合口下方(注意不要形成空肠盲袋)行肠管缩窄闭锁术(用7#丝线在拟闭锁处系膜侧紧贴肠壁缝过,结扎肠管后,在结扎线两侧行浆肌层缝合1 圈)。其它治疗同常规胃癌手术。对照组按传统胃-食管吻合术式进行。
1.3 观察指标 比较2 组患者术中出血情况、手术时间;术后胃排空情况及返流性食管炎发生情况;术后6 个月的体质量及营养指标变化情况。
1.4 统计学方法 对本组研究的数据采用SPSS 17.0 统计软件进行分析。正态计量资料采用“±s”表示,组间比较采用t检验。计数资料用例数(n)表示,计数资料组间率(%)的比较采用χ2检验;以P<0.05 为差异有统计学意义。
2 结果
所有病例均无围手术期死亡及吻合口漏、中度以上贫血及倾倒综合征病例发生。中位随访时间8 个月(6~10 个月)。观察组和对照组手术出血量无显著差异;观察组手术时间略长于对照组手术时间,2 组差异有统计学意义(P<0.05)。见表1。核素餐胃半排空时间(T1/2)和胃内核素残留率(RR 1)比较差异有统计学意义(P<0.05)。见表2。
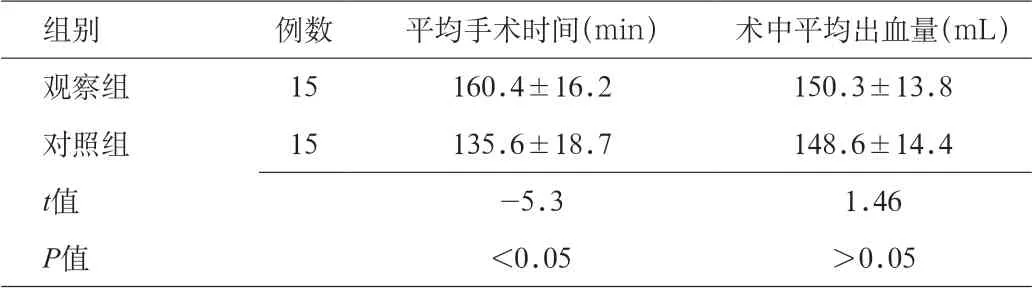
表1 2 组患者的手术时间和术中出血量比较
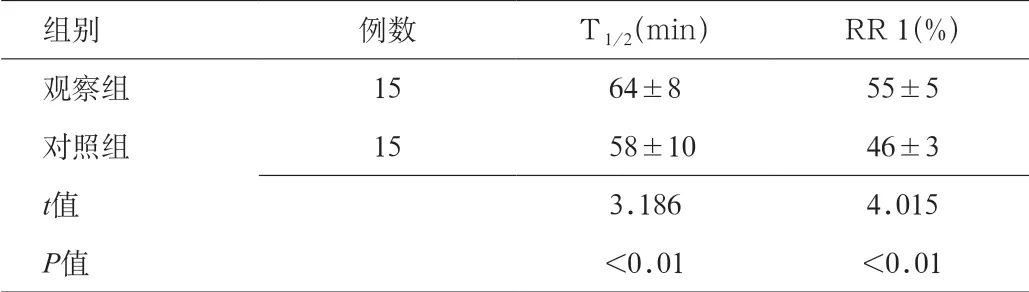
表2 2 组患者术后1 个月时的核数餐胃排空结果比较
术后6 个月对观察组和对照组所有患者进行随访,行胃镜检查,统计2 组患者反流性食管炎发生率分别为25%和60%,差异有统计学意义(χ2=5.153,P<0.05)。术后6 个月时,观察组和对照组患者体质量增加值、各项营养评价指标比较,差异均有统计学意义(P<0.05)。见表3。
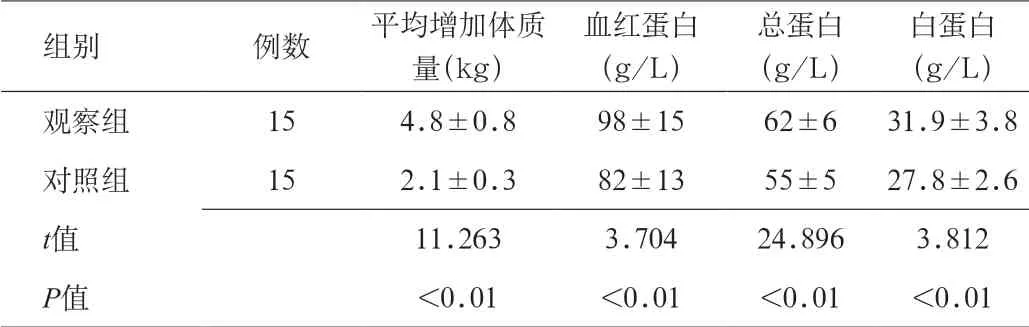
表3 2 组患者营养评价指标比较
3 讨论
近端胃癌具有组织学分化程度低、恶性程度高、进展快、起病隐匿等特点,就诊时多处于进展期和No.5、No.6 淋巴结可能已经出现转移[6-7]。因此,许多学者主张对于近端胃癌的治疗宜行全胃切除。但是,全胃切除与次全胃切除对比的回顾性分析显示,长期生存差异并无统计学意义[8]。Ogoshi 等[9]的回顾性研究显示,次全胃切除的预后优于全胃切除、十二指肠途径重建优于非十二指肠途径,认为宜在保证残胃无癌残留的情况下行最小化的胃切除和保留十二指肠的食物流经途径。
近端次全胃切除术后的反流性食管炎是影响患者术后生活质量的严重并发症,间置空肠(袋)被推荐应用于改善近端胃次全(全胃)切除术后的生活质量[10]。空肠间置术手术时间较长,吻合口较多,与胃食管吻合术相比,术后并发症应相对增加,吻合口漏几率应增加。本研究中,患者均采用吻合器吻合,手工加固缝合,吻合口漏的几率大大降低。2 组患者均未发生吻合口瘘并发症。近侧胃切除食管胃吻合术后由于贲门被切除,患者几乎均有胃酸返流入食管,出现返流性食管炎临床表现者约占79%左右[11]。本研究中,通过比较2 组患者术后胃排空情况可以看出,对患者采用改良空肠间置术大大降低了患者发生返流性食管炎的发生率。改良空肠间置术保留了传统空肠间置术的抗返流优势,而且对于移植段肠攀及系膜不必游离切断,这样不会影响吻合处的血供,可以降低吻合口漏的几率。
根治性近端胃切除术、改良空肠间术操作相对复杂,手术时间延长,围手术期潜在风险增加,但是,大大降低了返流性食管炎的发生率,明显改善了患者术后的生活质量,具有较大的临床应用价值,由于本研究病例数相对较少,随访研究时间较短,对于远期效果有待观察,值得临床进一步研究。
[1]Krejs GJ.Gastric cancer:epidemiology and risk factors[J].Dig Dis,2010,28(4-5):600-603.
[2]Kim DY,Joo JK,Park YK,et a 1.Predictors of long-term survivgl in node•positive gastric carcinoma patients with curative resection[J].Langenbecks Arch Surg,2007,392(2):131-134.
[3]Namikawa T,Oki T,Kitagawa H,et al.Impact ofjejImal pouch interposition reconstruction after proximal gastrectomy for early gastric cancer on quality of life:short-and long-term consequences[J].Am J Surg,2012,20(4):203-209.
[4]Paimela H,Ketola S,Iivonen M,et al.Long-term results after surgery for gastdc cancer with or without jejunal reservoir:resuits of surgery for gastric cancer in Kanta-Hilme central hospital in two consecutive periods without or with jejunal pouch reconstruction in 1985-1998[J].Int J Gastrointest Cancer,2005,36(3):147.
[5]Chadha MK,Kuvshinoff BW,Javle MM.Neoadjuvant therapy for gastric cancer[J].Oncology(Williston Park),2005,19(9):11-19.
[6]Varadhachary G,Ajani JA.Preoperative and adjuvant therapies for upper gastrointestinal cancers[J].Expert Rev Anticaneer Ther,2005,5(4):719.
[7]陈志新,胡建昆,于永扬,等.近、远端胃癌临床病理特点分析(附428例报告)[J].中国普外基础与临床杂志,2002,9(3):151.
[8]粱寒,郝希山.胃癌术式对患者术后营养的影响[J].中国肿瘤临床,2007,34(12):716.
[9]Ogoshi K,Okamoto Y,Nabeshima K.et al.Focus on the onnditions of resection and reconstruction in gastric cancer.What extent of resection and what kind of reconstruction provide the best outcomes for gastric cancer patients?[J].Digestion,2005,71(4):213.
[10]wata T,Kurita N,Ikemoto T,et al.Evaluation of reconstruction after proximal gastrectomy:prospective comparative study of jejunal interposition and jejunal pouch interposition[J].Hepatogastroenterolo gy,2006,53(68):301.
[11]张霜.贲门癌切除空肠间置移植术[J].中国肿瘤临床,1988,15(6): 363.

