用主成分回归法同时测定Zn2+、Cd2+、Pb2+和Cu2+的研究
李 展 王洪前 蒋 燕 王 斌
(四川大学建筑与环境学院,四川 成都,610065)
水体中重金属污染问题[1]是目前较为突出的环境问题之一,国家环保部明确逐步实现对总量控制指标的在线监测,因此对废水中的多种重金属离子同时测定[2,3]将是今后的研究重点。分光光度法结合化学计量学方法可实现对混合体系中的多种组分同时测定[4]。根据测量分析结果可对水环境水质现状进行合理预测,从而加强对水环境区域的保护。
研究了Zn2+、Cd2+、Pb2+、Cu2+与双硫腙形成稳定的络合物的最佳显色条件,利用多元分析方法中的聚类分析结合光谱分析可以定量化确定最佳缓冲体系。在pH值=6.0的条件下,不经萃取,利用主成分回归法结合分光光度法直接测定含有干扰离子存在下的待测水样中 Zn2+、Cd2+、Pb2+、Cu2+的浓度,并计算其回收率和相对标准偏差,结果较为有意义。
1 计算方法基本原理
主成分回归(PCR)是以主成分分析为依据的多参数拟合和多组分分析方法[5]。其化学测量模型:
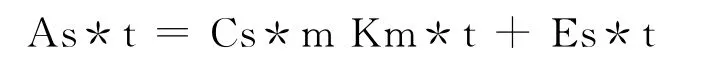
式中:As*t为测得的吸光度数据矩阵,Cs*m为浓度矩阵,Km*t为吸光系数矩阵,Es*t为残差阵。
对A进行主成分分析,得出:
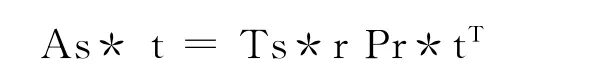
Tp*r为得分矩阵,为混合物浓度组成矩阵;PT为载荷矩阵,为混合物的吸光度矩阵。用一个系数矩阵G取回归矩阵T和C,C则为真实浓度组成矩阵:
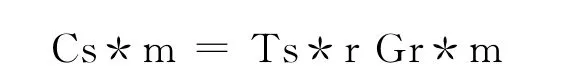
主成分回归的校正步骤:配制已知浓度的多组分混合标准溶液,构成浓度矩阵,测定吸光度,构成吸光度矩阵。根据最小二乘原理,得到系数矩阵G:
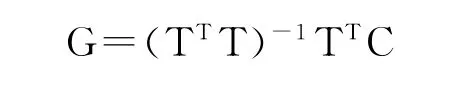
然后需要求未知多组分混合溶液的吸光度数据A未知来计算对应各组分的浓度向量矩阵C模拟:

2 实验部分
2.1 试剂
1.000 g/L重金属离子标准储备液(GB 602-77方法配制),稀释至10.0mg/L标准使用液;双硫腙使用液(0.02%);丙酮;36%乙酸;氨水;Triton X-100;无水乙酸钠;β-环糊精,以上均为分析纯。
pH标准缓冲剂:四硼酸钠(pH 值=9.18)、混合磷酸氢钾盐(pH值=6.86)、邻苯二甲酸氢钾(pH值=4.00)。
2.2 实验仪器
USB4000型光谱仪,电子分析天平(BS124S);电热 恒 温鼓 风 干 燥 箱 (DHG-06-100B);酸 度 计(PHS-25A 型);优 普 超 纯 水 制 造 系 统 (ULUPURE);容量瓶;移液管;石英比色皿;擦镜纸,滴管,称量纸。
2.3 实验过程
准确移取2.0ml的Zn2+、Cd2+、Pb2+、Cu2+的标准使用液于25ml的容量瓶中,依次加入3.0ml的双硫腙显色剂,5.0ml、pH值=6.0的缓冲溶液,2.0ml的1%的β-环糊精,5.0ml的triton X-100非离子表面活性剂,用去离子水定容,放置10分钟。用1.0cm石英比色皿,以试剂空白作为参比,用USB4000光谱仪测定四种离子的吸光度。在450~650nm波长范围内,对所测得的吸光度值在确定的最佳条件下进行主成分回归法计算。
3 结果与讨论
3.1 最佳缓冲体系的确定
本实验应用聚类分析法[6]对测定的 Zn2+、Cd2+、Pb2+、Cu2+吸光度光谱进行聚类分析,使用MATLAB软件中的欧式距离(Euclidian)的类平均(average linkage)对不同缓冲体系下四种离子的吸光度光谱值进行聚类。结果表明,pH值=6.0时类平均距离最大为0.9246,因此本实验确定最佳的缓冲体系为pH值=6.0的缓冲体系。图1为使用ORIGIN 8.0绘制pH值=6.0时的吸收光谱图。

表1 Zn2+ 、Cd2+ 、Pb2+ 、Cu2+聚类分析结果
3.2 最佳显色条件用量的确定
在25ml溶液体积中加入2.0ml重金属离子的标准使用液(10mg/L)的实验条件下,pH 值=6.0的缓冲溶液、双硫腙显色剂和β-环糊精溶液的最佳用量分别为5.0ml、3.0ml、2.0ml。显色剂和重金属离子的络合反应[15]在室温下迅速完成,其吸光度在定容10min后达到最大值且较稳定,因此实验选定在定容10min后进行测定。
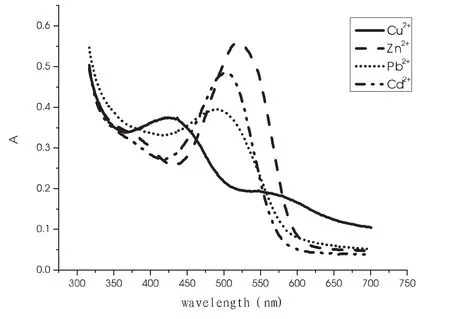
图1 pH值=6.0时Zn2+、Cd2+、Pb2+、Cu2+吸收光谱图
3.3 四种离子的线性关系
图2为不同离子在pH值=6.0时吸光度与浓度关系曲线。结果表明:Zn2+回归方程y=0.5783x-0.0137,相关系数 R为0.9936;Cd2+回归方程y=0.1973x+0.0165,相关系数为0.9981;Pb2+回归方程y=0.1464x-0.0009,相关系数为0.9989;Cu2+回归方程y=0.1504x-0.0042,相关系数为0.9995。四种离子在0~0.080mg/L浓度内均具有良好的线性关系,且在线性范围内有良好的线性加和性。
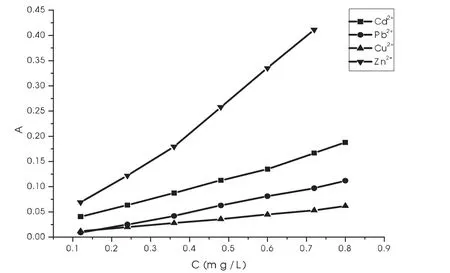
图2 吸光度与浓度的关系曲线
3.4 分析波长的选取
在最佳显色条件下,Zn2+、Cd2+、Pb2+、Cu2+与双硫腙显色剂络合后的配合物最大吸收波长分别为535nm、530nm、528nm、573nm。本实验通过对6组不同波段的模拟样测定结果进行回收率和相对标准偏差(RSD)计算,以平均回收率和相对标准偏差的计算结果为判断依据,确定在300~700nm时校正结果计算值最接近真实值。测定校正水样中Zn2+、Cd2+、Pb2+、Cu2+浓度时,宜选择的波段为300~700nm。
3.5 标准溶液的配制
实际水样不仅存在 Zn2+、Cd2+、Pb2+、Cu2+四种离子,同时还有其他离子,因此在标准溶液中加入Ni2+、Fe2+、Co2+、Mn2+干扰离子。本文用主成分回归方法计算样品中多个组分浓度,通过多波长校正分析分析样品的一个吸收光谱来获得多个组分的含量,实验过程中对标准样品配制要求较高。均匀设计方法[7]是一种在试验范围内均匀散布的方法,其目标就是要用最少的试验获得系统的充分信息。为了使标准样品更好的反应实际水样,多组分溶液浓度采用均匀设计表来配制,配制10个标准溶液和6个模拟水样。

图3 加和性实验光谱图
3.6 样品分析
通过使用MATLAB软件中主成分回归法计算程序,对已知的标准样品浓度和待测样品的吸光度进行计算,计算6个待测样品中 Zn2+、Cd2+、Pb2+、Cu2+的浓度、回收率和相对标准偏差,结果如表5和6。
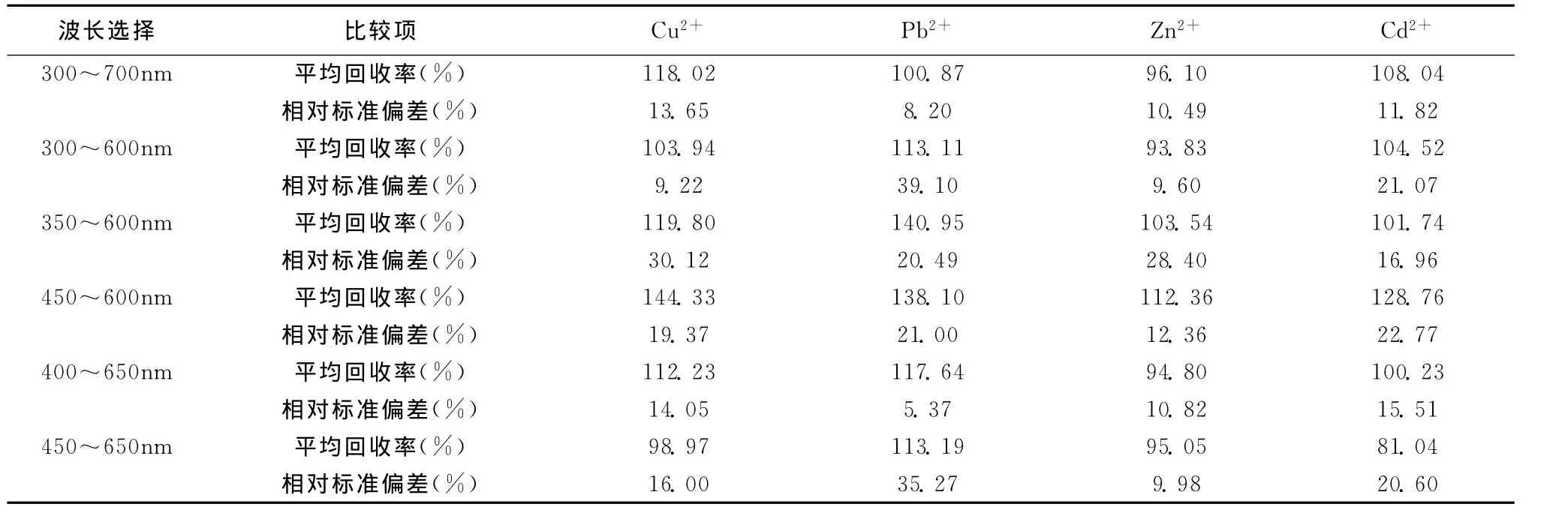
表2 不同波段四种离子回收率和相对标准偏差比较
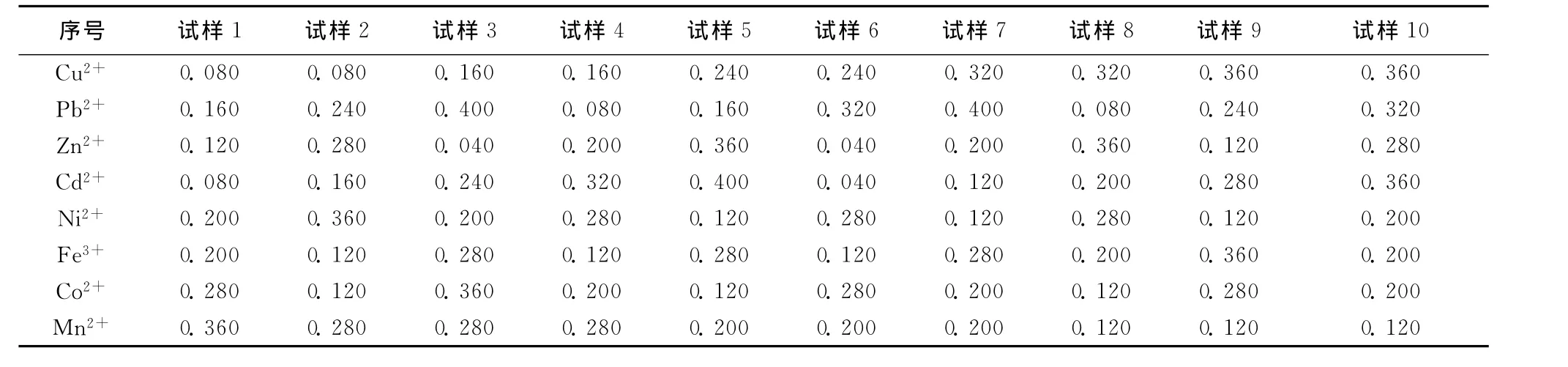
表3 10个混合标准水样组分浓度表(mg/L)
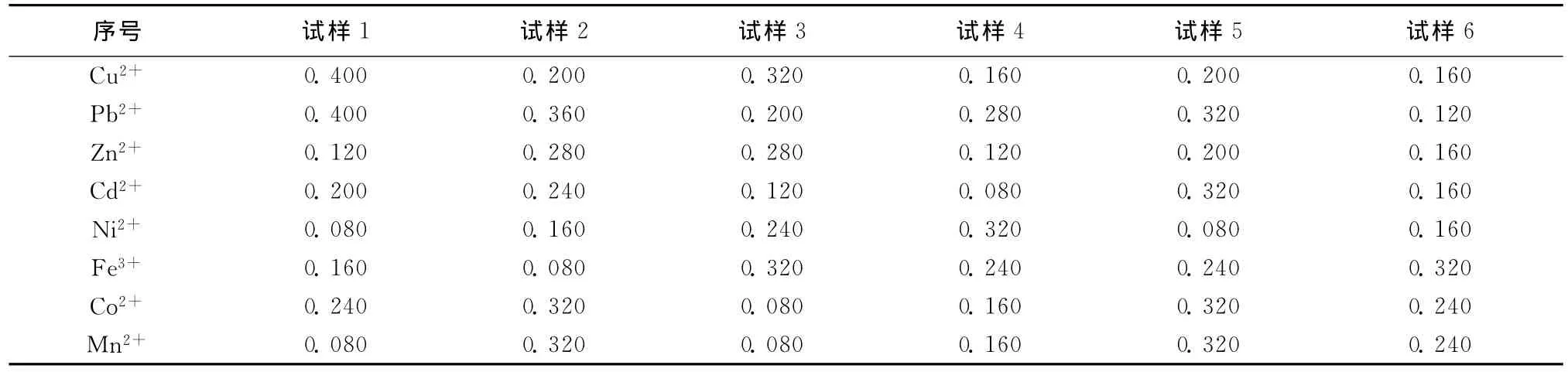
表4 6个混合模拟水样各组分浓度表(mg/L)

表5 波长范围为300~700nm波段模拟水样分析结果
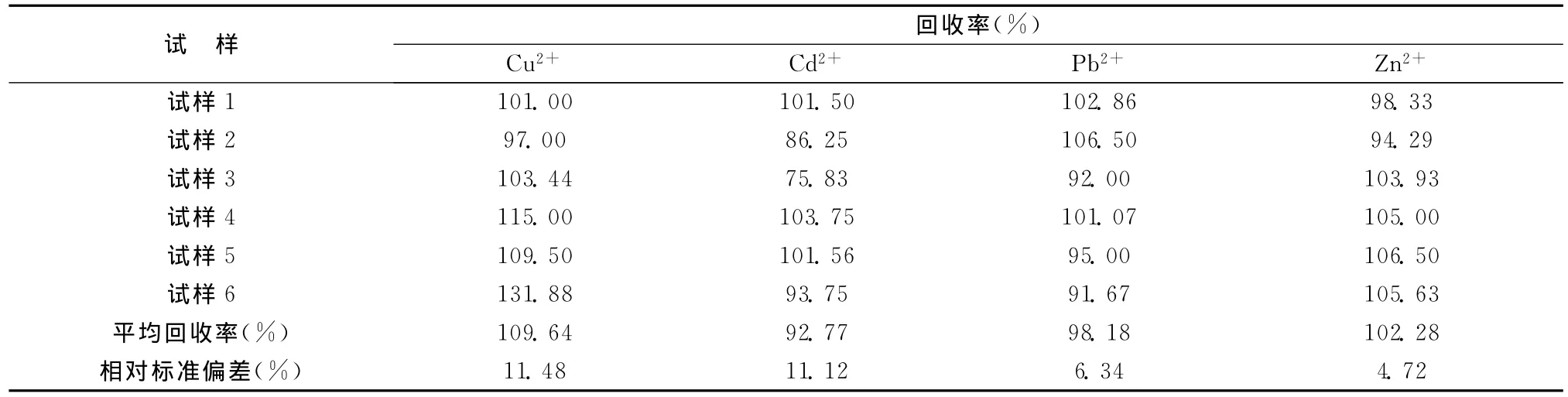
表6 6个模拟水样中Zn2+、Cd2+、Pb2+、Cu2+的回收率和相对标准偏差比较
利用主成分回归法对含有 Mn2+、Co2+、Fe3+、Ni2+干扰离子存在的情况下对多组分同时测定,测得 Cu2+、Cd2+、Pb2+、Zn2+的 平 均 回 收 率 为109.64%、92.77%、98.18%、102.28%,相对标准偏差分别为11.48%、11.12%、6.34%、4.72%,Pb2+和Zn2+的回收率很接近100%,且相对标准偏差较小,结果较为满意。经过对实验的优化和更深入准确的研究,从而实现对实际水样中多组分的同时测定分析。
4 结论与建议
通过对不同缓冲体系下的金属离子的光谱数据进行聚类分析,定量确定最佳pH值以及最佳显色条件下各溶液的用量。利用主成分回归法计算校正水样中各组分的浓度,通过比较回收率和相对标准偏差指标来选择最佳波长范围。同时主成分回归法结合分光光度法对含有干扰离子存在的水样中Cu2+、Pb2+、Zn2+、Cd2+的同时测定经实验结果证明是可行的,对同时测定实际水样中的重金属离子有一定实际意义。
分光光度法结合主成分回归法对混合体系中的多组分同时测定仍需进一步研究,实际废水监测过程中要求方法尽可能的简单、经济、快速、准确。结合化学计量学中的其他方法校正讨论,使测定结果更加的准确,为实现废水中多种重金属离子在线监测提供依据和技术方法。
[1]韩玲玲,曹惠昌,代淑娟,等.重金属污染现状及治理技术研究进展[J].有色矿冶,2011,27(3):94-97.
[2]于庆凯,李丹.阳极溶出伏安法同时测定海水中铜、铅、镉、锌[J].化学工程师,2009,169(10):25-27.
[3]储海虹,储长群,夏红.络合吸附伏安法同时测定多种重金属离子[J].分析实验室,2004,23(4):58-59.
[4]Wold S.,Trygg J.,Berlund A.,et al.Chemometrics and Intelligengt.Laboratory Systems,2001,58:131.
[5]Ying Ouyang.Evaluation of River Water Quality Monitoring Stations by PCA.Water Research,2005,26:21-2635.
[6]Cheng Yongqian.,Song Qianwu.,Ma Hongme.Research on Optimization of Water Quality Monitoring Sites Using Principal Component Analysis and Cluster Analysis.International Conference on Computer Distributed Control and Intelligent Environmental Monitoring,2011,570-573.
[7]杨启霞,韩吉衢,常显波,等.均匀设计在优化原子荧光法测砷条件中的应用[J].光谱学与光谱分析,2009,29(2):526-529.

