抗HIV药物的研发现状及发展趋势分析
(中国医学科学院·北京协和医学院·医学信息研究所/图书馆,北京 100020)
艾滋病又称获得性免疫缺陷综合征(AIDS),是由人类免疫缺陷病毒(HIV)感染人体淋巴细胞所致的传染性疾病[1]。近年来,AIDS感染人数急剧增加,呈逐年上升趋势,形势严峻,故抗HIV药物的研究投入了大量的资金和人力。本研究基于Thom-son Reuters Integrity[2]数据库收录的抗HIV药物数据,分析其研究现状和发展趋势,为抗HIV药物的研发方向提供信息支撑。
1 数据来源
通过检索Thomson Reuters Integrity数据库,对所收录抗HIV药物的研究数据进行统计和分析。Thomson Reuters Integrity是医药信息数据库,收录了最新的在研药物信息,能为药物研发一线人员提供可靠、及时、持续和深度的前沿科研信息,加速“药物发现”向“临床应用”阶段的转化,并最终降低研发风险。本研究中对数据库收录的抗HIV药物进行检索和分析,以了解最新研发动态。从 Thomson Reuters Integrity 数据库的“Knowledge Areas”入口,选择“Drugs&Biologics”进入检索中心,共有405210条记录。设置检索条件“condition”为“Infection,HIV”,共检索到11298条记录。检索时间为2013年7月5日。
2 结果与分析
2.1 临床研究及上市情况
检索结果见表1。可见,数据库中的抗HIV药物研究大多处于“Biological Testing”(生物测定)阶段,有9 516项;其次是临床前研究阶段,有1 201项。此外,处于临床研究共424项,已上市的抗HIV药物研究有76项,说明抗HIV药物的研发十分活跃。同时,也再次印证了进行临床前试验的上千种化合物中只有几种能进入到后续的临床试验,而最终得到上市批准的化合物可能只有1种。

表1 抗HIV药物发展阶段及各阶段数量分布
“生物测定”是生物学、医学、特别是毒理学的重要内容和基础。“临床前研究”是为确定一个新的化合物是否具备进入临床试验的条件,即药效、毒性和作为一个药物所需的各种理化性质[3]。
需要注意的是,有2个药物处于Phase 0(0期临床试验)。0期临床试验是新药临床研究的新模式,其目的是为了减少西药研究开发过程中的风险,使更多的新药能尽快上市[4]。0期临床试验可花费少量资金收集到极有价值的新药在人体的安全性及药代动力学数据。如果新药在0期临床试验出现安全问题,新药研制者便可及时调整甚至放弃Ⅰ期临床试验,从而减少不必要的浪费。
2.2 药物类型
抗HIV药物的具体分类有100多种,排名前10位的药物类型见表2,其中7个是生物制品,包括HIV疫苗(HIV Vaccines)、多肽(Polypeptides)、重组载体疫苗(Recombinant Vector Vaccines)、DNA 疫苗(DNA Vaccines)、重组蛋白(Recombinant Proteins)、肽疫苗(Peptide Vaccines)和寡肽(Oligopeptides);3 个是化学药,包括前药(Prodrugs)、类固醇(Steroids)和氮杂糖(Iminosugars)。
生物制品占据重要地位,是抗HIV药物的研发重点。在排名前10位的药物类型中,超过200项的药物类型只有4种,生物制品3种,化学药只有1种。数量最多的是HIV疫苗,有625项,占绝对优势,被认为是预防AIDS的最有效工具。此外,也有较多研究集中在多肽和重组载体疫苗上,分别有291项和215项,但远不及HIV疫苗的研究多。从1987年第1种HIV候选疫苗投入临床试验至今,相继有数百种HIV疫苗投入临床前和临床试验,但迄今仍无1种被证实有效[5]。HIV疫苗的研究仍有很大的发展空间。唯一一个超过200项研究的化学药是“前药”,有214项。前药是指药物经过化学结构修饰后得到的在体外无活性或活性较小、在体内经酶或非酶的转化释放出活性药物而发挥药效的化合物,是药物发展的重要方向。

表2 排名前10位的抗HIV药物类型
2.3 作用靶点
抗HIV药物的作用靶点有100个,排名前10位的作用靶点见表3。其中超过1 000项的有5个,分别为HIV整合酶(HIVIntegrase)、HIV聚合酶(HIV pol)、HIV-1蛋白酶(HIV-1 Protease)、逆转录酶(Reverse Transcriptase)和逆转录酶(病毒)(Reverse Transcriptase viral)。可见,抗HIV药物作用靶点大多是通过阻断HIV复制周期中的3个关键酶(逆转录酶、整合酶、蛋白酶)达到抑制HIV复制的目的。这些作用于HIV关键酶的药物是比较传统的抗HIV药物,虽然起到了很大的作用,但仍存在一些问题。因此,对其他作用靶点的研究非常必要。

表3 排名前10位的抗HIV药物作用靶点
趋化因子受体也是抗HIV药物的重要靶点。排名前10位的作用靶点中,趋化因子受体CCR5(Chemokine CCR5 Receptor)有870项,作用于趋化因子受体CXCR4(Chemokine CXCR4 Receptor)的有327项。趋化因子受体CCR5和CXCR4在HIV-1病毒进入免疫细胞过程中起重要的作用,故趋化因子在HIV中的研究将为HIV感染开辟新的治疗途径。
2.4 天然来源分类
除寻找新的靶点外,研究人员还不断从动植物中提取到一些具有抗HIV活性的天然产物。天然来源的活性产物具有专一性、不良反应少、方便、有效等优点,越来越受到重视,成为抗HIV药物研究新的发展趋势。这些天然来源的活性产物主要以植物来源(Plants)为主,有161个;其次为动物来源(Animals)19个;此外,还有真菌来源(Fungi)14个、藻类来源(Algae)6个和细菌来源(Bacteria)5个。详见图1。

图1 抗HIV药物天然来源类型分布
植物来源的活性产物最多,传统中草药是其重要的组成部分,我国拥有丰富的中药资源,可以将今后的研究重点放在从中药中寻找抗HIV活性的有效成分,充分利用我国的资源优势。天然来源除了传统的中草药,海洋生物资源也是其重要组成部分。海洋生物资源因其生活的特殊生态环境,在生命过程中代谢产生一些结构特殊、生物活性显著的化学物质,且有更大的化学多样性,对人类很多疾病有很好的疗效。
由表4可见,在天然来源的活性成分中,以来源于Iotrochota baculifera(中国南海海绵)和 Nelumbo nucifera(中国莲)最多,各有8个。其中Iotrochota baculifera是一种热带海绵,海绵是最低等的多细胞代谢物。由于海绵中存在大量化学结构多样和生物活性广泛的天然产物,成为天然有机化学家的研究热点。此外,海绵中还含有很多结构罕见、具有抗癌或抗病毒活性的次生代谢产物,成为海洋药物开发最重要的生物资源之一。我国南海Iotrochota baculifera海绵资源丰富,已有研究表明,来源于该海绵的成分对HIV-1逆转录酶有一定的抑制作用[6]。这提示海绵生物资源的利用将是抗HIV药物的一个重要研究方向。有8个抗HIV药物来源于 Nelumbo nucifera(中国莲),Nelumbo nucifera(中国莲)为睡莲科莲属多年生大型水生草本植物,以藕或莲子为主产品,藕节、荷叶、莲芯(胚芽)、花、莲须(雄蕊)、莲梗等均可入药[7]。莲藕成分丰富,功能多样,但目前对莲藕资源的开发力度不够。有研究表明,荷叶95%乙醇提取物具有重要的抗HIV活性,说明莲藕也是寻找新的抗HIV药物的一个重要来源。这提示海洋生物资源和传统中药的开发是寻找抗HIV药物的重要方向。
3 结语
通过对抗HIV药物研发现状的分析,可得出以下结论:从研发阶段看,处于“生物测定”阶段的最多,其次是“临床前研究”。这是药物研发的重要环节,以此确定一个新的化合物是否具备进入临床试验的条件。从药物类型来看,生物制品占据绝对优势,远远领先于化学药。这是因为传统的化学药存在产率低、费用高等诸多缺点,使得抗HIV化学药的发展面临很多困难。由于没有针对HIV的特效治疗方法,研制安全、有效的疫苗是控制HIV传播的重要手段之一。此外,化学药中的前药也是抗HIV药物的重要发展方向。从作用靶点看,目前的抗HIV药物大多通过阻断HIV复制周期中的3个关键酶(逆转录酶、整合酶、蛋白酶)达到抑制HIV复制的目的。此外,趋化因子及其受体由于其广泛的细胞来源和生物学效应,受到越来越多的关注。从发展趋势看,天然产物结构新颖且具有多样药理活性,是国际药学领域关注的研究方向。药用植物、中草药及海洋生物资源是天然产物的重要来源和新药发现的重要途径,为抗HIV药物带来新的发展前景。
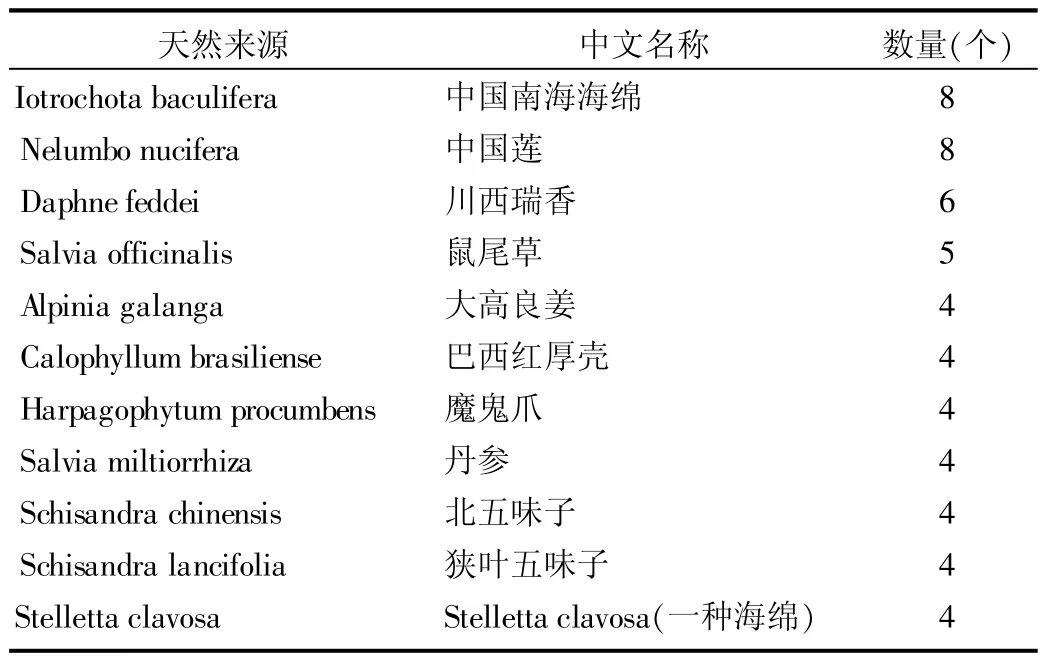
表4 排名前10位的天然来源的抗HIV药物
我国有着丰富的药用植物资源和海洋生物资源,要充分利用我国的资源优势,加大创新力度,提高我国在药物研发领域的地位。
参考文献:
[1]王 霞,马洪涛,温瑞兴.抗HIV药物及其靶点的研究进展[J].中国中药杂志,2009,34(11):1 454-1 459.
[2]盛 欣,李兰燕,毛雪石.创新药物研发信息资源:Thomson Reuters Integrity数据库[J].医学信息学杂志,2011,33(8):32-35.
[3]李 钧.最新药品注册技术精讲(第二版)[M].北京:化学工业出版社生物·医学出版分社,2008:83-85.
[4]张 骏,宋紫辉,蔡永明,等.0期临床试验:新药临床研究的新模式[J].首都医科大学学报,2011,32(4):581-585.
[5]孙 健,李 杰,吴南屏.HIV疫苗国内外研究进展[J].国际流行病学传染病学杂志,2009,36(3):183-187.
[6]林文瀚.南海海绵的结构多样性和生物活性[J].国际药学研究杂志,2011,38(1):1-11.
[7]周春华,陶 俊,李良俊,等.莲藕的化学成分与生物活性研究进展[J].氨基酸和生物资源,2007,29(4):63-69.

