基于HPR在线监测控制SBR曝气历时实现短程脱氮
张 欣,张代钧,张 天(1.重庆工业职业技术学院建筑与环境工程系,重庆 401120;2.重庆大学环境科学系,重庆 400030;3.重庆大学煤矿灾害动力学与控制国家重点实验室,重庆 400030)
基于HPR在线监测控制SBR曝气历时实现短程脱氮
张 欣1,2,张代钧2,3*,张 天1,2
(1.重庆工业职业技术学院建筑与环境工程系,重庆 401120;2.重庆大学环境科学系,重庆 400030;3.重庆大学煤矿灾害动力学与控制国家重点实验室,重庆 400030)
应用新型自动呼吸-滴定测量仪在线测量pH值、HPR等信号,进行了在 SBR内实现短程脱氮的研究.采用SBR处理人工合成废水,COD和NH4+-N浓度分别为360,40mg/L,温度稳定在20℃,DO低于2mg/L,基于HPR在线监测控制SBR曝气历时.运行约60d后,亚硝酸盐积累率达到 88%,COD和 NH4+-N去除率均在 90%以上,稳定实现了短程硝化反硝化.应用 HPR估计硝化过程的 NH4+-N浓度发现,NH4+-N实测值与基于HPR的计算值间存在良好的线性关系,相关系数为0.9722;计算值整体低于实测值,主要是由曝气初期的滴定启动滞后所致.
短程硝化反硝化;SBR;曝气历时控制;质子产生速率;在线监测
传统生物脱氮方法首先在硝化过程中利用氧作为电子受体将氨氧化成硝酸盐,然后在反硝化过程中利用有机碳源作为电子供体将硝酸盐还原成氮气从废水中去除,亚硝酸盐中间产物的形成和转化是完全硝化和反硝化过程的必经环节.在城市污水或工业废水处理中将硝化过程终止在亚硝酸盐阶段随后进行反硝化实现短程脱氮,将使生物脱氮的处理效率显著提高,降低处理成本[1].
短程脱氮的关键步骤是实现稳定的亚硝化,要在保持氨氧化菌(AOBs)正常生长和代谢的前提下,有效抑制亚硝酸盐氧化菌(NOBs)的生长,或者将其从活性污泥中淘洗去除.其主要途径有∶(1)采用污泥停留时间小于NOBs临界倍增时间的连续运行反应器将 NOBs从反应器中淘洗去除[2];(2)控制溶解氧在低浓度水平,AOBs利用其比 NOBs更高的氧亲合性竞争胜过 NOBs[3];(3)控制 pH值在较高水平,或采用高浓度游离氨基质抑制 NOBs的生长与代谢[4-5];(4)控制曝气历时,在氨氧化过程完成前或结束时停止曝气,阻止 NOBs的生长与代谢[6-7].在较高温度和适宜pH值下应用序批式生物反应器(Sequence Batch Reactor, SBR)处理高氨废水[8-10],是当前实现短程脱氮的主流.
近年来,有关氧利用速率(OUR)测量(呼吸测量)和质子产生速率(HPR)测量(滴定测量)的研究与开发日益受到青睐,开展了许多关于OUR、HPR单独或联合测量应用于废水生物处理的硝化过程监测[11-15]、强化生物除磷 EBPR过程监测[16-17]以及过程模拟[18-20]等工作.OUR 和 HPR作为过程监测变量能够反映过程动力学信息.截至目前,尚未见以HPR作为实时监测信号控制曝气历时实现短程硝化反硝化的报道,主要原因是受限于连续在线滴定测量仪的开发和应用.已经报道的滴定单元[12,21]、TOGA传感器[13,15]等只能用于批式试验或实验室分析,尚不能在现场进行连续在线测量. 本课题组自行开发了一种新型自动呼吸-滴定测量系统,能够同时连续测量 pH值、DO、OUR和HPR等信号[22-24].本文应用该新型自动呼吸-滴定测量仪在线监测实验室SBR曝气时段的pH值、DO、OUR和HPR等信号,基于HPR和pH值曲线上的转折点控制曝气历时,最终实现了稳定的短程硝化反硝化生物脱氮.
1 材料和方法
1.1 SBR试验装置
试验采用的SBR总有效体积8L,采用鼓风微孔曝气方式,用空气流量计调节曝气量,采用机械搅拌装置进行搅拌.采用恒温水浴循环确保 SBR内混合液温度稳定在20 .SBR℃ 运行过程中采用前置反硝化的运行方式,为方便操作,简化了控制策略,固定周期长度为4h(即1d 6个周期),且在每个周期内除了曝气时段根据在线监测结果灵活调整外,其他进水、缺氧搅拌、排泥和排水阶段均固定时间,因此,闲置时段依据曝气时段变化而变化.每个周期的具体运行工况见图 1∶进水 18min,并在进水时开始搅拌;进水结束后缺氧搅拌30min;曝气(碳化和硝化反应),根据在线监测pH值、DO和HPR值的变化确定好氧时段为t min;排泥,在曝气结束后继续搅拌几 min以方便排泥;沉淀约30min;出水18min;闲置.污泥泥龄为12d.
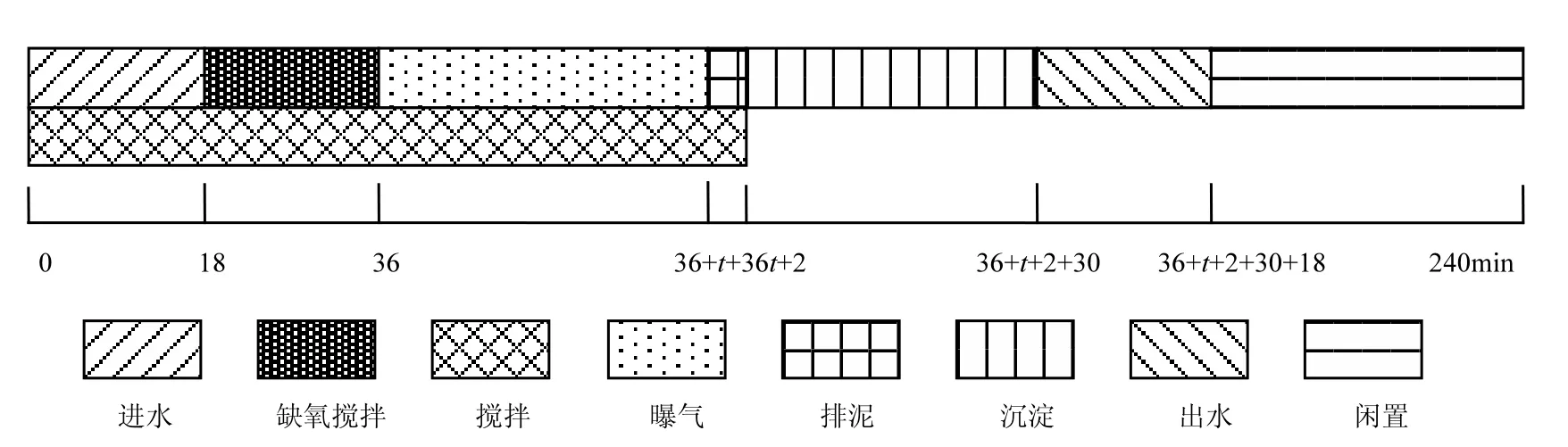
图1 SBR装置运行工况Fig.1 Operation mode in SBR
1.2 废水和污泥性质
启动SBR所使用的活性污泥取自重庆市大渡口区茄子溪污水处理厂曝气池,该污水处理厂采用具有脱氮功能的CAST工艺.试验用水采用人工合成废水,其主要组分及浓度均与城市生活污水接近.合成废水组成主要有 COD (CH3COONa⋅3H2O) 360mg/L、NH4+-N(NH4Cl)40mg/L、碱度(NaHCO3) 150mg/L、TP(KH2PO4)4.6mg/L和微量元素5mL/L等.微量元素营养液组成(g/L)为∶MgCl2⋅7H2O 3.6; CaCl2⋅7H2O 1.6;ZnSO4⋅7H2O 0.08;MnSO4·H2O 0.06; CuSO4·5H2O 0.04; H3BO30.01; Na2MoO4·2H2O 0.036; CoCl2·6H2O 0.09; EDTA 2.4.在SBR进水完毕后 COD 和 NH4+-N 测量值分别为 80.2, 12.23mg/L左右,均低于理论值 118.8,13.2mg/L(SBR体积交换比为0.33),这可能是因为活性污泥的吸附作用所致.
1.3 分析方法
COD采用标准重铬酸钾法测量,NH4+-N采用纳氏试剂分光光度法,NO2--N采用 N-(1-萘基)-乙二胺光度法,NO3--N采用酚二磺酸光度法,每3d测量1次. SV、SVI按国家环境保护部发布的标准方法测定.
1.4 在线控制策略
SBR混合液的DO、pH值、OUR和HPR等应用自动滴定-呼吸测量系统进行测量,分别在该测量系统测量室的进口和出口配备1个DO电极和1个pH电极以获取流入和流出测量室的混合液的DO和pH值(分别记为DO1、DO2和pH1、pH2),这使得测量完全独立于SBR运行装置[22].控制SBR曝气阶段的DO浓度低于2mg/L.当在线监测到的HPR开始从最高平台迅速下降时,计算机便输出一个控制信号停止曝气.
2 结果与分析
2.1 好氧过程的HPR变化规律
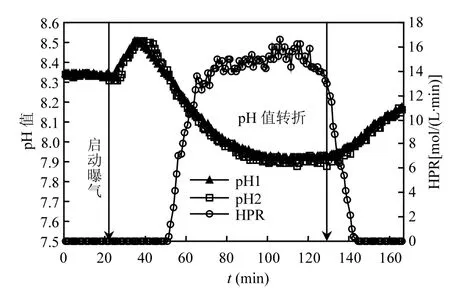
图2 SBR曝气阶段HPR、OUR、pH1、pH2响应曲线(实时控制策略前)Fig.2 Profiles of HPR, OUR, pH1and pH2 in the aerobic phase of SBR
由图 2可见,开始曝气后,pH值呈现快速上升趋势,直到约35min处,pH值转为下降,说明这段时间内微生物(异养菌和硝化菌)在大量耗氧,异养菌降解 COD活动占主导,至 pH值峰值时COD降解才基本完成.峰值之后,pH值迅速下降,说明硝化反应占了主导;由于混合液在测量室有一定的停留时间,对相同部分液体pH2读数略滞后于pH1,因此在pH值开始下降几min后滴定才开始,HPR从0上升到一个较高平台.pH值在约130min呈现由下降转为上升的转折点,该点被称为“氨谷”,即指示着氨氧化结束,已经被证实可用于生物短程脱氮曝气时段的控制[25];几乎与此同时,HPR开始从较高平台陡降,说明HPR陡降点亦指示着氨氧化结束.
2.2 基于HPR监测控制SBR曝气历时实现短程硝化反硝化
图3中,phaseI代表未进行实时控制,系统处于全程硝化反硝化段,由于曝气充分,COD和NH4+-N去除率几乎为100%,亚硝酸盐积累率接近0.
phaseII段为对处于全程硝化反硝化的SBR进行监测控制,逐步实现短程硝化反硝化的过程.约从第 16d开始,采用上述制定的启动方案,对 SBR进行监测控制.进行短程脱氮控制后,由于控制了曝气强度和时间,第21d时亚硝酸盐积累率快速增长至20%,至第40d左右时亚硝酸盐积累率上升到了 50%,进入了短程硝化状态;随后上升的速率基本保持稳定,直到上升至接近80%时上升速率明显变小,运行到约78d亚硝酸盐积累率达到88%并稳定下来.采取短程脱氮控制措施后出水NH4+-N浓度有所提高,可能是限制了DO导致少量NH4+-N没有降解完毕,但出水 NH4+-N仍在 4mg/L以下,去除率在90%以上;出水COD在6mg/L以下,其在全程脱氮和短程脱氮过程中的去除情况基本相同,去除率在 95%以上.在试验过程中发现,随着亚硝化积累率的逐渐提高,在曝气流量一定的情况下曝气时间逐渐缩短,这种情况的出现充分说明亚硝化细菌在总的硝化细菌中所占的比例逐渐增多.
在 SBR运行至约 100d时(进入图 3的phaseIII段),出水NH4+-N浓度有所升高,NH4+-N去除率有所下降,但COD去除率基本不变,NAR也基本维持在88%左右,污泥沉淀速率有所下降,但沉淀后上清液澄清,可以推断此时污泥发生了微膨胀.约至115d时,NH4+-N和COD去除率均明显下降,NAR也下降至73%,测试发现污泥SVI高达 198.6mL/g,污泥镜检发现存在大量丝状细菌,说明 SBR内发生了较严重的丝状菌膨胀.除了高污泥负荷、低DO浓度、偏低温度(16~20 )℃外,出水中较高的亚硝酸盐和硝酸盐浓度也是造成污泥膨胀的原因.Ma等[25]研究发现,亚硝酸盐积累会对污泥絮状结构造成有害影响,从而导致污泥沉淀性能恶化.通过采取添加新污泥、加大曝气量(DO在3~4mg/L)、改变体积交换比(VER在0.33~0.5间)及严格控制系统恒温等一系列措施,污泥膨胀得到了有效控制,约10d后亚硝酸盐积累率又回到了 80%以上,之后系统又运行了约30d,污泥沉淀性能没有再恶化,系统重新实现了稳定的短程硝化.
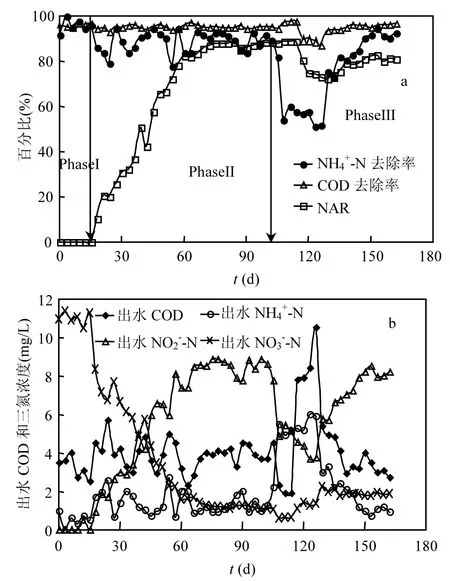
图3 SBR运行中NH4+-N、COD去除率和NAR曲线(a)和出水COD、NH4+-N、NO2--N和NO3--N变化曲线(b)Fig.3 Variations of NH4+-N, COD removal ratios and NAR of SBR (a) and variations of effluent COD, NH4+-N, NO2--N and NO3--N (b)
3 讨论
从pH值同HPR的对比中可以看出,两者均能作为氨氧化结束的指示信号. 氨氧化的结束点在pH曲线上表现为pH值由下降或稳定转为上升的极值点,在HPR曲线上表现为HPR由一个平台[约15μmol/(L⋅min)]向另一个平台(0)陡降的突跃,因平台的判断较之点的判断更加容易,显然,后者作为控制变量较前者更加灵敏,因此用HPR进行控制优于用pH值进行控制. HPR从一个较高水平快速下降到一个较低水平,意味着氨氧化(产生质子)速率快速降低,同时也说明混合液中NH4+-N快速下降到较低水平.从理论上讲,即使在 NH4+-N浓度较低时,氨氧化反应仍将继续,同时其产物亚硝酸盐氧化速率将加速上升;所以,只要在 HPR发生陡降时就停止曝气,就能有效实现短程硝化.虽然,Blackburne等[7]通过在线测量OUR,当测量OUR低于初始设定值时停止曝气,在前置反硝化SBR处理城市污水时实现了短程硝化反硝化脱氮;但是,由于氨氧化和亚硝酸盐氧化均消耗氧气,在同时包含大量 AOBs和NOBs的常规活性污泥系统中,氨氧化结束并不会立即导致 OUR出现十分明显下降,除非系统中NOBs数量已经很少;所以当采用OUR作为过程监测变量时,AOBs的初始富集是稳定实现短程硝化反硝化的关键因素[7].2步硝化理论认为,氨氧化过程产生氢离子,而亚硝酸盐氧化不产生氢离子.因此,在氨氧化结束时 HPR会立即出现陡降转折点,采用HPR而不采用OUR作为过程监测变量来启动和稳定运行短程硝化反硝化更加具有优势.
对比分析得知,本论文中短程硝化反硝化的启动时间比Peng等[6]所报道的更长,原因可能与本文采用的 SBR是前置反硝化形式有关. Blackburne等[7]进行的模拟研究表明,仅基于曝气长度控制的前置反硝化SBR的短程硝化的启动比起后置反硝化SBR(在硝化之后进入缺氧段,并投加碳源)需要更长的时间,这是因为提供碳源的后置反硝化阶段能更迅速的去除积累的亚硝酸盐,从而消除或减轻亚硝酸盐对 AOB的抑制.与Peng等[6]和Lemaire等[26]在曝气停止后投加外部碳源或进污水不同,Blackburne等[7]在以OUR作为监测信号及时停止曝气后,让SBR直接进入沉淀之前的一个闲置状态,通过内源亚硝酸盐呼吸进行可忽略的反硝化,结果发现实现稳定短程硝化反硝化的时间明显长于前者.
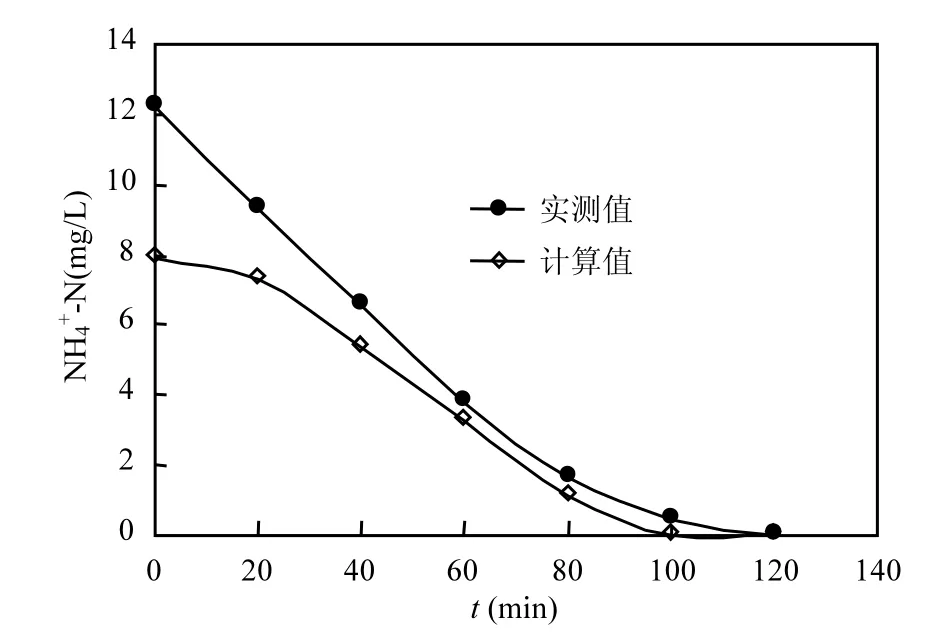
图4 SBR好氧阶段的NH4+-N实测值与基于HPR的估计值Fig.4 The measured value and estimated value based on HPR for process NH4+-N in the aerobic phase of SBR
HPR可用于氨氧化过程的动力学研究,这是pH值、DO和ORP等信号所不能实现的.图4中显示了 SBR好氧阶段 NH4+-N实测值与基于HPR的计算值的比较,计算值整体低于实测值,误差范围为-13.78%~-35.45%,平均误差为-24.19%.导致计算值低于实测值的结果主要与滴定测量系统的结构有关∶通过测量室获得的硝化过程质子产生速率信息始终滞后反应室Δt(混合液在测量室的停留时间),因此系统实际上是在硝化反应发生Δt时间后方才开始滴定,而在该段时间内NH4+-N已经部分降解,致使基于HPR所计算的初始 NH4+-N浓度遗漏了已经降解部分.另外,在曝气的初期,由于 DO水平不高,反硝化消耗质子仍在进行,此外氨氧化产生质子速率也较低,综合作用的结果是系统内基本无质子产生或消耗,这时的滴定测量不动作也将导致基于HPR的计算结果偏低.设硝化过程NH4+-N实测浓度为Y,基于HPR的NH4+-N计算浓度为X,Y同X的数学关系为一元线性方程Y=aX+b.对于不同的活性污泥等具体情况,a和 b可以通过具体试验进行校核.采用最小二乘法对试验数据进行拟合得到Y=1.3806X-0.0643,相关系数为0.9722.
4 结论
4.1 应用新型自动呼吸-滴定测量仪同时测量SBR曝气时段的pH值和HPR等信号,当pH值上的转折点“氨谷”出现时,HPR开始从较高平台陡降,证明HPR亦可作为氨氧化结束的指示信号,且比pH值信号更加灵敏.
4.2 基于 HPR在线监测,在出现平台陡降点时及时停止曝气,成功实现了短程硝化反硝化生物脱氮.经过约20d的运行SBR内的亚硝酸盐积累率上升到了 50%,进入了短程硝化状态. 实际运行约60d亚硝酸盐积累率达到88%并稳定下来,最终实现了短程硝化. COD和NH4+-N去除率均在90%以上.
4.3 HPR用于硝化过程的 NH4+-N浓度估计,NH4+-N实测值与基于HPR的计算值间的相关系数为 0.9722,总体趋势一致性较好. 计算值整体低于实测值,主要是因曝气初期的滴定滞后所致.
[1] Ruiz G, Jeison D, Rubilar O, et al. Nitrification—denitrification via nitrite accumulation for nitrogen removal from wastewaters. Bioresource Technol., 2006,97:330—335.
[2] Hellinga C, Schellen A A J C, Mulder J W, et al. The SHARON process: an innovative method for nitrogen removal from ammonium-rich waste water. Water Sci. Technol., 1998,37(9):135—142.
[3] Blackburne R, Yuan Z, Keller J. Partial nitrification to nitrite using low dissolved oxygen concentration as the main selection factor [J]. Biodegradation, 2008,19(2):303—312.
[4] Ciudad G, Gonzalez R, Bornhardt C, et al. Modes of operation and pH control as enhancement factors for partial nitrification with oxygen transport limitation [J]. Water Res., 2007,41(20):4621—4629.
[5] Vadivelu V M, Keller J, Yuan Z. Effect of free ammonia on the respiration and growth processes of an enriched nitrobacter culture [J]. Water Res., 2007,41(4):826-834.
[6] Peng Y Z, Chen Y, Peng C Y, et al. Nitrite accumulation by aeration controlled in sequencing batch reactors treating domestic wastewater [J]. Water Sci. Technol., 2004,50(10):35—43.
[7] Blackburne R, Yuan Z, Keller J. Demonstration of nitrogen removal via nitrite in a sequencing batch reactor treating domestic wastewater [J]. Water Res., 2008,42(8/9):2166-2176.
[8] Volcke E I P, Loccufier M, Noldus E J L, et al. Operation of a SHARON nitritation reactor,practical implications from a theoretical study [J]. Water Sci. Technol., 2007,56(6):145—154.
[9] Kim J H, Guo X, Park H S. Comparison study of the effects of temperature and free ammonia concentration on nitrification and nitrite accumulation [J]. Process Biochem., 2008,43(2):154—160.
[10] Pambrun V, Paul E, Sperandio M. Control and modelling of partial nitrification of effluents with high ammonia concentrations in sequencing batch reactor [J]. Chem. Eng. Process., 2008, 47(3):323—329.
[11] Gernaey K, Bogaert H, Vanrolleghem P, et al. A titration technique for on-line nitrification monitoring in activated sludge [J]. Water Sci. Technol., 1997,37(12):103-110.
[12] Massone A, Gernaey K, Rozzi A, et al. Measurement of ammonium concentration and nitrification rate by a new titrimetric biosensor [J]. Water Environ. Res., 1998,70(3):343-350.
[13] Pratt S, Yuan Z, Gapes D, et al. Development of a novel titration and off-gas analysis (TOGA) sensor for study of biological processed in wastewater treatment systems [J]. Biotechnol. Bioeng., 2003,81(4):482-495.
[14] Fiocchi N, Ficara E, Canziani R, et al. SBRs on-line monitoring by set-point titration [J]. Water Sci. Technol., 2006,53(4/5):541-549.
[15] Gapes D, Ptatt S, Yuan Z, et al. Online titrimetric and off-gas analysis for examining nitrification processed in wastewater treatment [J]. Water Res., 2003,37(11):2678-2690.
[16] Guisasola A, Pijuan M, Baeza J A, et al. Improving the start-up of an EBPR system using OUR to control the aerobic phase length: a simulation study [J]. Water Sci. Technol., 2006,53(4/5):253-262.
[17] Guisasola A, Vargas M, Marcelino M, et al. On-line monitoring of the enhanced biological phosphorus removal process using respirometry and titrimetry [J]. Biochem. Eng. J., 2007,35:371—379.
[18] Pratt S, Yuan Z, Keller J. Modeling aerobic carbon oxidation and storage by integrating respirometric, titrimetric and off-gas CO2Measurements [J]. Biotechnol. Bioeng., 2004,88(2):135-146.
[19] Jubany I, Baeza J A, Carrera J, et al. Respirometric calibration and validation of a biological nitrite oxidation model including biomass growth and substrate inhibition [J]. Water Res., 2005,39:4574-4584.
[20] Sin G, Vanrolleghem P A. Extensions to modeling aerobic carbon degradation using combined respirometric—titrimetric measurements in view of activated sludge model calibration [J]. Water Res., 2007,41:3345-3358.
[21] Gernaey K, Vanrolleghem P A, Verstraete W. On—line estimation of nitrosomonas kinetic parameters in activated sludge samples using titration in-sensor-experiments [J]. Water Res., 1998,32(1):71-80.
[22] Zhang X, Zhang D, Lu P, et al. Monitoring the nitrification and identifying the endpoint of ammonium oxidation by using a novel system of titrimetry [J]. Water Sci. Technol., 2011,64(11):2246-2252.
[23] 张代钧,卢培利,张 欣,等.污染物好氧生物降解呼吸测量方法及装置 [P]. 中国:ZL 2006 1 0054264.0.2006.11.29.
[24] 张代钧,张 欣,卢培利,等.废水生物处理中质子变化速率的在线滴定测量方法及装置 [P]. 中国:ZL 2009 1 0104312.6.2013. 3.27.
[25] Ma Y, Peng Y, Wang S, et al. Achieving nitrogen removal via nitrite in a pilot-scale continuous pre-denitrification plant [J]. Water Res., 2009,43(3):563—572.
[26] Lemaire R, Marcelino M, Yuan Z. Achieving the nitrite pathway using aeration phase length control and step-feed in an SBR removing nutrients from abattoir wastewater [J]. Biotechnol. Bioeng., 2008,100(6):1228—1236.
致谢:感谢重庆大学卢培利博士、蔡庆博士和白翠博士等在实验中给予的帮助.
Stable shortcut nitrogen removal performed in a SBR by controlling aeration duration based on HPR on-line monitoring.
ZHANG Xin1,2, ZHANG Dai-jun2,3*, ZHANG Tian1,2
(1.Construction and Environmental Engineering, Chongqing Industry Polytechnic College, Chongqing 401120, China;2.Department of Environmental Science, Chongqing University, Chongqing 400030, China;3.State Key Laboratory of Coal Mine Disaster Dynamics and Control, Chongqing University, Chongqing 400030, China). China Environmental Science, 2014,34(3):617~622
The hydrogen ion production rate (HPR) and the pH were measured by a novel automatically respirometrictitrimetric system, and shortcut nitrogen removal in an SBR was studied in the laboratory. An SBR was used to treat synthetic wastewater containing 360mg/L COD and 40mg/L NH4+-N at 20℃ with DO lower than 2.0mg/L. Controlling the aeration duration based on HPR online monitoring, shortcut nitrification-denitrification was successfully performed for approximately two months with a stable nitrite accumulation rate (NAR) above 88%, and the COD and NH4+-N removal ratios were both higher than 90%. Based on the HPR online monitoring data, the estimated NH4+-N concentrations in nitrification were closely related to the measured concentrations, with a correlation coefficient of 0.9722, and the estimated values were lower than the measured values mainly because of the titration delay at the beginning of the aeration phase.
shortcut nitrification-denitrification;sequence batch reactor;the control of aeration duration;hydrogen ion production rate;on-line monitoring
X703
:A
:1000-6923(2014)03-0617-06
张 欣(1983-),女,河南南阳人,讲师,博士,主要从事现代废水处理技术及污染控制研究.发表论文近10篇.
2013-06-25
重庆市自然科学基金(CSTC2013JJB20002)
*责任作者, 教授, dzhang@cqu.edu.cn

