基于纳米银/石墨烯/酪氨酸酶/聚酰胺-胺的双酚A传感器
郭倩琼,王炜祺,高佩怡,马腾飞,杨乐乐,黄杉生
(上海师范大学生命与环境科学学院,上海 200234)
基于纳米银/石墨烯/酪氨酸酶/聚酰胺-胺的双酚A传感器
郭倩琼,王炜祺,高佩怡,马腾飞,杨乐乐,黄杉生*
(上海师范大学生命与环境科学学院,上海 200234)
采用石墨烯纳米材料,并结合酪氨酸酶、聚酰胺-胺(PAMAM)和纳米银修饰玻碳电极研制了新型BPA生物传感器。运用循环伏安法和电化学交流阻抗考察了修饰电极的电化学行为。由于石墨烯独特的物理化学性质,结合聚酰胺-胺和纳米银的协同作用,该修饰电极对于BPA有较好的电流响应。在最佳条件下,该传感器对双酚A的线性检测范围为1.0×10-7~3.3×10-5mol/L,检测限为3.0×10-8mol/L(信噪比为3),相关系数为0.998。
石墨烯;酪氨酸酶;聚酰胺-胺;纳米银;双酚A传感器
0 引言
纳米银可通过光沉积或电沉积方法修饰在电极表面。纳米银具有强吸附能力和高比表面积,提高电化学有效表面积;并且对H2O2具有高催化作用,可用于H2O2的检测。Cui等[1]利用DNA在电极表面构建了网状结构,再在表面沉积纳米银,结合过氧化氢酶,制备了一种新型的过氧化氢传感器。Sun等[2]在TiO2包裹的压电石英电极上沉积纳米银构建了高灵敏度的DNA传感器检测大肠杆菌。Ting等[3]研发了阿霉素共轭银纳米粒子作为标记物的DNA传感器。
树状大分子是一类正在蓬勃发展的新型高分子材料,其特殊的结构特点引起了研究者的广泛关注,在催化剂、纳米复合材料、表面活性剂等领域有重要应用。聚酰胺-胺(PAMAM)是目前研究最为广泛的树状大分子之一,其特点是:分子形状和大小可控、分子内存在空腔、表面拥有大量羧基和胺基官能团、生物相容性好、粘度低且易修饰[4]。因此,PAMAM在光电传感器、基因载体、膜材料、药物载体、纳米复合材料等方面显示出广阔的前景[5]。近年来,PAMAM在电化学修饰上的优势逐渐显现出来。Algarra等[6]报道了利用PAMAM分子内空腔包裹CdTe量子点检测硝基芳香化合物的传感器。Qian等[7]研发了基于CdS-PAMAM纳米复合材料的光化学传感器检测细胞。
该文在玻碳电极上修饰纳米银、石墨烯、酪氨酸酶和聚酰胺-胺,研制新型双酚A生物传感器,该传感器制备方法简单,具有线性范围宽、检测限低、抗干扰能力强等特点。
1 实验部分
1.1 试剂与仪器
酪氨酸酶(提取自蘑菇,5370 U/mg)购自Sigma公司;聚酰胺-胺(G4)由上海师范大学生命与环境科学学院提供;石墨粉(颗粒度≤30μm)、硝酸、浓硫酸、硝酸钾、硝酸银、壳聚糖(Chits)购于上海化学试剂有限公司;双酚A(BPA)购于成都西亚化工股份有限公司;磷酸盐缓冲液(PBS)由0.1mol/LNa2HPO4和0.1mol/LNaH2PO4按不同的比例混合配制。实验中所有的试剂均为分析纯,未进一步纯化。实验用水为Milli-Q 18.2MΩ超纯水。所有的实验条件均在室温下进行。
循环伏安法(CV)、电化学阻抗谱图(EIS)和计时电流响应在CHI660B电化学分析仪(上海辰华仪器公司,中国)上进行,采用三电极体系:修饰电极为工作电极,铂丝电极为对电极,饱和甘汞电极为参比电极(SCE);电化学阻抗分析在1mmol/L[Fe(CN)6]4-/3-含有0.1mol/LKCl溶液中进行,频率范围是0.05 Hz到10 kHz;循环伏安实验在PBS中进行;计时电流响应的测试底液为0.1mol/L PBS(含0.1 mol/L KCl,pH7.0),所有的电化学测定都是在10mL的容器中进行的。
1.2 传感器的制备
1.2.1 石墨烯的制备
石墨烯的制备参照文献报道的方法进行[8]。在反应容器中加入浓硫酸和浓硝酸混合液(体积比为2∶1)用于氧化石墨,然后缓慢加入氯化钾,不断搅拌,冰浴反应120 h。在制得的混合物中加入去离子水清洗、过滤,重复几次,直至pH为7。将氧化态石墨烯溶于乙醇和水的混合溶液中,超声1 h使之分散均匀,然后加入肼还原氧化态石墨,反应20 h后,再离心、水洗和真空干燥。用TEM对所制得的石墨烯进行表征,结果见图1,制得的石墨烯为片状。将1mg石墨烯与1mL质量分数为0.5%的壳聚糖混合,修饰电极前超声1 h,形成均一溶液后备用。

图1 石墨烯的透射电子显微镜图Fig.1 SEM imageofgraphene
1.2.2 电极的制备
电极表面的组装过程见图2。玻碳电极(GCE,φ=3mm)依次用1.0、0.3、0.05mm的α-Al2O3粉末抛光,直至形成镜面。再分别用超纯水、HNO3-H2O(V/V=1∶1)、超纯水超声清洗电极3min,在0.5mol/LH2SO4中于-0.35~1.70 V的电位范围内,以100mV/s的速度循环扫描至电流稳定为止。用超纯水将电极冲洗干净后,用氮气将其表面吹干待用。
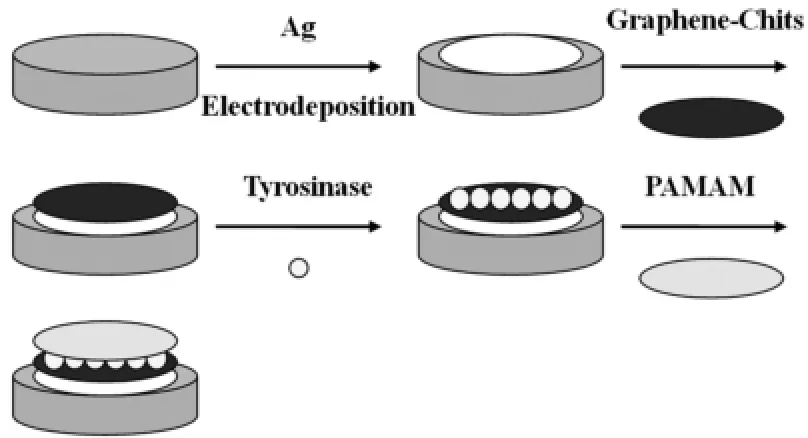
图2 电极的组装过程Fig.2 Assembly processof the eletrode
根据文献[9],将依前述方法处理干净的电极放入含有3.0mmol/L的0.1mol/LKNO3溶液中,在电压为-0.1 V下电沉积银120 s(电极记为Ag/ GCE)。将5μL 1mg/mLGraphene-Chits复合材料滴凃于电极表面,在空气中让其蒸干(Gra-Chits/ Ag/GCE)。再将10μL 5mg/mL的酪氨酸酶溶液(pH7.0 PBS)滴于Gra-Chits/Ag/GCE上,在空气中晾干(电极简记为Tyr/Gra-Chits/Ag/GCE)。最后,将5μLPAMAM滴于Tyr/Gra-Chits/Ag/GCE表面,晾干后用PAMAM/Tyr/Gra-Chits/Ag/GCE表示该修饰电极,电极不用时保存于4℃0.1 mol/LPBS(pH7.0)中。
2 结果与讨论
2.1 电极层层自组装过程的电化学阻抗谱图
图3为电极不同修饰层电化学阻抗图谱的Nyquist曲线。图中各曲线分别是裸玻碳电极、Ag/ GCE、Gra-Chits/Ag/GCE、Tyr/Gra-Chits/Ag/GCE、PAMAM/Tyr/Gra-Chits/Ag/GCE层层修饰电极在[Fe(CN)6]4-/3-(含有0.1mol/LKCl)溶液中的交流阻抗谱图。曲线a是裸玻碳电极的交流阻抗谱,阻抗值约为590Ω。当电沉积纳米银后,Ag/GCE的阻抗图的阻抗弧略微变小(曲线b),阻抗值为250Ω。表明银纳米颗粒具有良好的导电性,使得[Fe(CN)6]4-/3-在电极表面的电子转移阻力减小。当电极经Graphene-Chits复合材料修饰后,Gra-Chits/Ag/GCE(曲线c)的阻抗弧进一步变小,阻抗值降为150Ω。说明了壳聚糖的良好成膜性,以及石墨烯的良好导电性[10],证明Graphene-Chits复合材料已被修饰于Ag/GCE上。酪氨酸酶在pH7.0 PBS中带负电,可通过静电引力自组装固定于表面带有正电荷的Gra-Chits/Ag/GCE上。基于生物大分子导电性差的特性,Tyr/Gra-Chits/ Ag/GCE(曲线d)的阻抗值明显增大,为1 500Ω。当PAMAM修饰到Tyr/Gra-Chits/Ag/GCE之后,PAMAM/Tyr/Gra-Chits/Ag/GCE的阻抗值(曲线e)变为1 000Ω。PAMAM这一良好的纳米级树状分子,导电性能良好[11],从而使得电子转移变得容易。
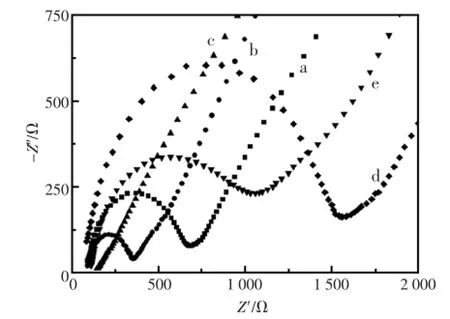
图3 不同修饰层电极的阻抗谱图(a)裸GCE;(b)Ag/GCE;(c)Gra-Chits/Ag/GCE;(d)Tyr/Gra-Chits/Ag/GCE;(e)PAMAM/Tyr/Gra-Chits/Ag/GCEFig.3 EIS imagesof different layersmodified electrodes
2.2 修饰电极在铁氰化钾中的电化学行为
图4为不同修饰电极在1mmol/L[Fe(CN)6]4-/3-(0.1mmol/LKCl)中的循环伏安图。在0.6到-0.2的电位范围内,裸玻碳电极在[Fe(CN)6]4-/3-溶液中的氧化还原电位是(ΔEp)75mV;当在裸玻碳电极(图4曲线a)表面覆盖一层Ag时,电极所产生的氧化还原峰电流增加(图4曲线b),这是因为纳米银作为一个良好的电子媒介体起到了增强电信号的作用。当电极表面修饰上一层Gra-Chits复合膜时,由于壳聚糖的良好成膜性,以及石墨烯的良好导电性,使得信号进一步增强(图4曲线c)。当电极表面覆盖一层Tyr膜后,峰电流(Ip)下降(图4曲线d),这是因为Tyr是一种生物大分子,它在电极表面的固定,阻碍了电极同电解液之间的电子转移。当电极表面修饰上一层PAMAM后,Ip也有一定程度的增大(图4曲线e)。实验结果与电化学阻抗的结果一致。
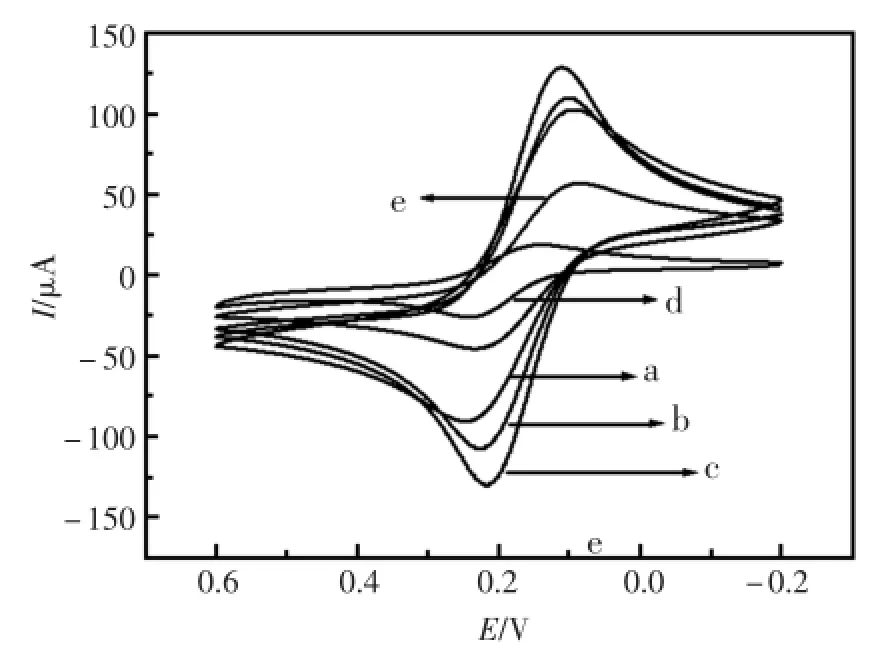
图4 不同修饰层电极在1mmol/L铁氰化钾+0.1 mmol/LKCl底液中的循环伏安图(a)裸GCE;(b)Ag/GCE;(c)Gra-Chits/Ag/GCE;(d)Tyr/ Gra-Chits/Ag/GCE;(e)PAMAM/Tyr/Gra-Chits/Ag/GCEFig.4 Cyclic voltammogramsofdifferent layersmodified electrodes in 1mmol/L[Fe(CN)6]4-/3-solution containing 0.1mmol/LKCl
2.3 BPA在修饰电极上的电化学行为
图5为不同修饰层电极在0.5μmol/L BPA(含有0.1mol/LKCl)中的循环伏安图。在0~0.8 V的电位范围内,0.5μmol/LBPA(含有0.1mol/L KCl)溶液中,裸的GCE(曲线a)、Ag/GCE(曲线b)、Gra-Chits/Ag/GCE(曲线c)均没有明显的氧化还原峰,说明在电极表面没有任何氧化反应发生,电极对BPA无响应。Tyr/Gra-Chits/Ag/GCE(曲线d)仅有一个较为微弱的氧化峰(Epa=0.523 V),说明BPA在Tyr/Gra-Chits/Ag/GCE的氧化较为微弱。究其原因,可能是酪氨酸酶作为生物大分子,导电性较差,响应信号较低。而对于PAMAM/Tyr/Gra-Chits/Ag/GCE(曲线e),可以观察到一个明显的氧化峰,(Epa=0.499 V),没有对应的还原峰,说明是一个不可逆电极反应。当修饰了PAMAM后,其分子内的空腔能固定已经修饰的Tyr;良好的生物亲和性[12]有效的保持了酪氨酸酶的生物活性;PAMAM作为良好的电子媒体[13],可以有效的增强电极的导电性;此外,PAMAM(G4)表面有大量的胺基,在待测溶液中带正电[14],使得更多的带负电的BPA能够与电极表面相接触[15],发生氧化反应,获得较强的电信号。
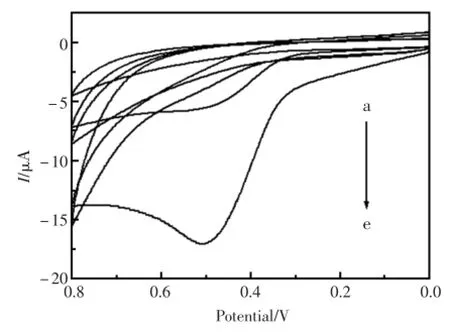
图5 修饰电极在0.5μmmol/LBPA(含有0.1mol/L KCl)中的循环伏安图(a)裸GCE;(b)Ag/GCE;(c)Gra-Chits/Ag/GCE;(d)Tyr/ Gra-Chits/Ag/GCE;(e)PAMAM/Tyr/Gra-Chits/Ag/GCEFig.5 Cyclic voltammogramsof different layersmodified electrodes in 0.5μmmol/LBPA solution containing 0.1 mol/LKCl
2.4 工作电位的影响
工作电位的选择对于修饰电极的电流响应有着较大的影响。图6显示了工作电位为0.4~0.9V的范围内,电极的氧化峰电流变化情况。在工作电位为0.5 V时,氧化峰电流达到最大值。所以,以下实验选择0.5V作为该修饰电极的工作电位。
2.5 溶液pH的影响
因为该电极修饰了酪氨酸酶,溶液的pH对于酶的电化学活性有着较大的影响。图7为在0.1 mol/L的PBS(含有0.1 mol/L KCl,pH4.0~pH10.0)中,溶液pH与氧化峰电流之间的关系图。如图所示,当pH的范围为4.0到7.0时,氧化峰电流的值随pH的增大而增大;当溶液的pH大于7.0以后,氧化峰电流的值逐渐变小。可能是当pH值从7.0继续增大至10.0时,酪氨酸酶的活性降低。与文献报道的酪氨酸酶保持最佳活性的pH范围基本一致。以下实验测试底液的pH值控制为7.0。
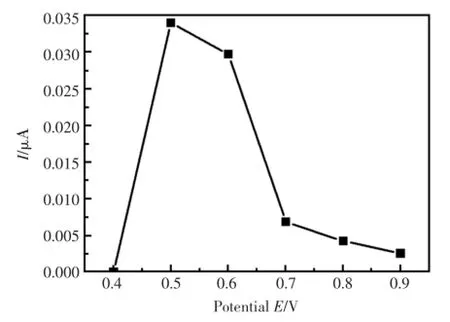
图6 工作电位对氧化峰电流的影响Fig.6 Effectofpotentialon the current response of modified electrodes
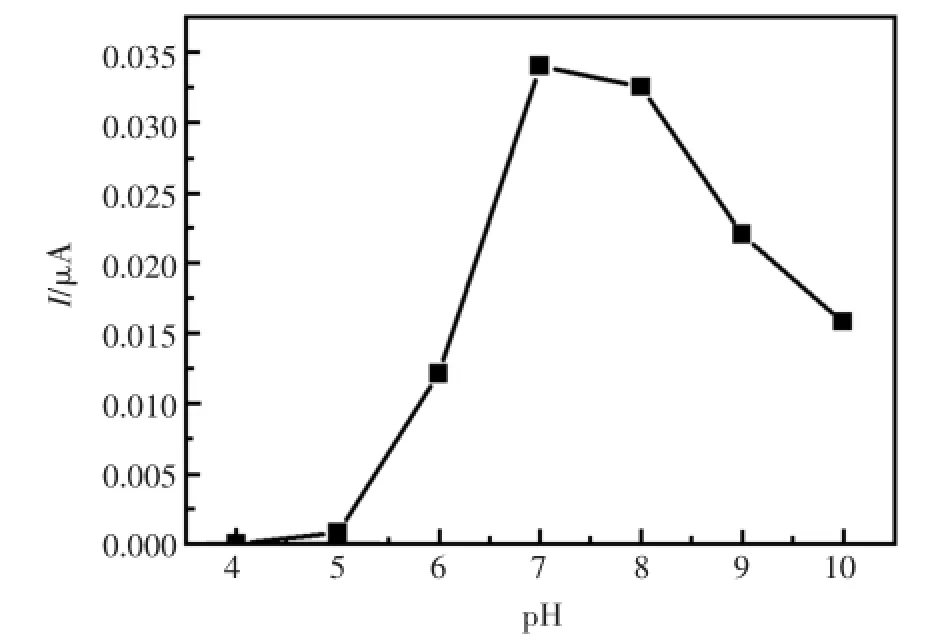
图7 不同pH值对传感器响应电流的影响Fig.7 EffectofpH on the currentresponseofmodified electrodes
2.6 计时库仑——电化学有效表面积
利用计时库仑法,通过Anson公式计算裸玻碳电极和PAMAM/Tyr/Gra-Chits/Ag/GCE的电化学有效表面积:
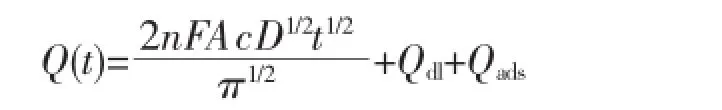
将Q对t1/2作图(图8),得到斜率值。计算得到裸玻碳电极和PAMAM/Tyr/Gra-Chits/Ag/GCE的电化学有效表面积分别为0.000 66 cm2和0.003 77 cm2。电化学表面积越大,电极表面的活性位置就越多。实验表明电极经过修饰后,电化学表面积明显增大,使得传感器能够获得更大的电流响应。
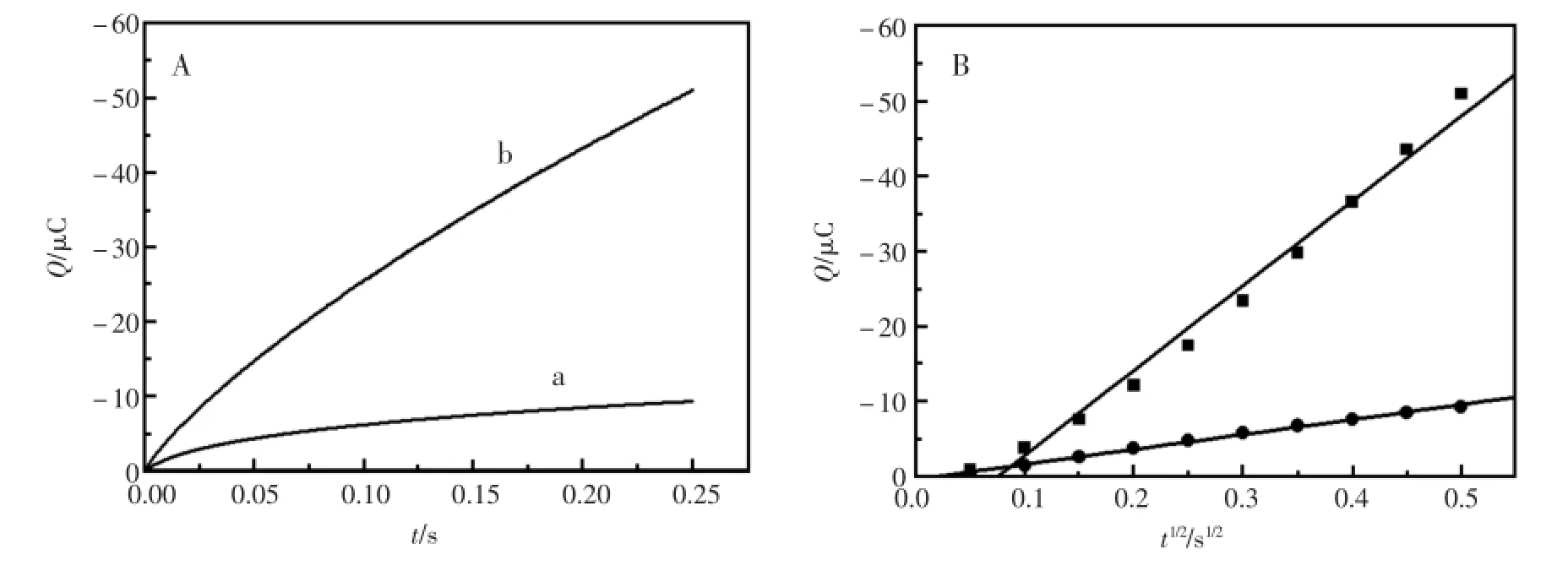
图8 计时库仑图(A)裸GCE和PAMAM/Tyr/Gra-Chits/Ag/GCE在1mmol/LK3[Fe(CN)6](含有0.1mol/LKCl)中的计时库仑图;(B)裸GCE和PAMAM/Tyr/Gra-Chits/Ag/GCE的Q与t1/2线性关系图Fig.8 chronocoulogram ofGCEand PAMAM/Tyr/Gra-Chits/Ag/GCE
2.7 计时电流响应
图9是PAMAM/Tyr/Gra-Chits/Ag/GCE在工作电位下,向PBS(pH7.0)中连续加入0.5mmol/L BPA的计时电流响应曲线。随着BPA的浓度不断增加,氧化电流逐级增加并在6 s内达到稳态电流。图9B为该传感器在不同浓度BPA下对响应电流的线性校正关系,HGNs-Chits/Tyr/Gra-Chits/PB/GCE对BPA的检测浓度范围为1.0×10-7~3.35×10-5,线性相关系数r=0.998,检测限为3×10-8mol/L(信噪比S/N=3)。
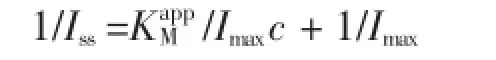
式中,Iss是加入底物后测得的稳态电流,c是底物浓度,Imax是底物达饱和后测得的最大电流。米氏常数可根据稳态电流的倒数和BPA浓度的倒数作图后,所得到的斜率和截距求得。按此公式测得PAMAM/Tyr/Gra-Chits/Ag/GCE的mmol/L,较低的说明通过该修饰方法固定的酪氨酸酶具有较高的活性。
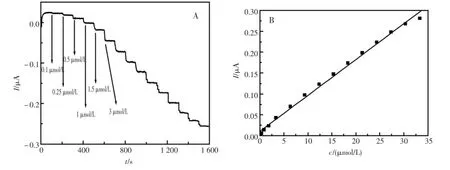
图9 计时电流响应曲线(A)PAMAM/Tyr/Gra-Chits/Ag/GCE在PBS(pH7.0)中连续加入不同浓度BPA的计时电流响应曲线(工作电位:0.5V);(B)响应电流与BPA浓度的校正曲线Fig.9 Amperometric current response curve ofmodified electrodes
2.8 电极的重现性、稳定性及干扰实验
在底液中维持BPA浓度为0.5μmol/L,连续测定7次,得到相对标准偏差(RSD)为5.8%;用3支不同的修饰电极分别检测,每支电极测3次,相对标准偏差(RSD)为2.5%,说明该传感器有较好的重现性。当该传感器不用时,置于4℃的PBS(pH=7.0)溶液中保存。一周后,该传感器响应电流为初始的95.5%,1个月后响应电流为原来的90.1%,说明此电极具有良好的稳定性。
考察了该传感器的抗干扰性,在0.5μmol/L的BPA溶液中分别加入一定浓度的KNO3、FeCl3、CuSO4、Na3PO4、ZnCl2、苯酚、间氨基酚、2,4-二氯苯酚、1-硝基-2-萘酚和邻氨基苯酚进行测定,以干扰物质造成的误差在5%之内作为干扰指标。结果发现,260倍浓度的苯酚、间氨基酚、2,4-二氯苯酚以及无机离子K+、Na+、Fe3+、Zn2+、Cu2+、NO3-、Cl-、SO42-和PO43-对BPA的测定基本不产生明显干扰,但是1-硝基-2-萘酚和邻氨基苯酚对BPA的测定有轻微影响(图10)。这表明该传感器的抗干扰性较好,能用于实际样品的检测。

图10 酚类有机物对PAMAM/Tyr/Gra-Chits/Ag/GCE测定BPA的电流干扰柱状图Fig.10 Currentinterference histogram of Phenolorganic matteron themodified electrodesdetermination of BPA
2.9 实际样品的测定及回收率
取日常生活用水,采用该方法测定其BPA含量。而后在试样中加入不同浓度的BPA,测定其回收率,结果见表1。该方法测定的回收率为97%~101%。表明此方法制备的BPA生物传感器为测定实际样品中BPA含量提供了一种可供选择的方法。
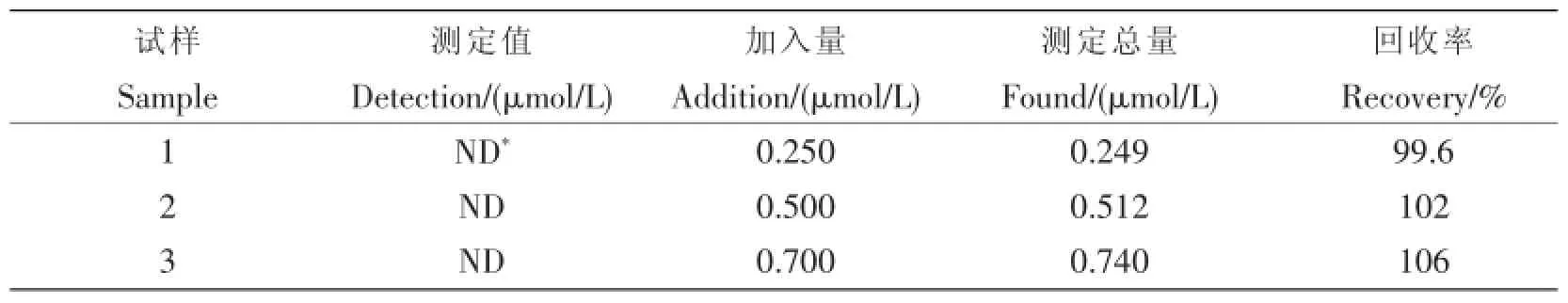
表1 标准加入法对实际样品的检测(n=3)Tab.1 The determ ination resultsof samples(n=3)
3 结论
在电极上修饰了具有良好导电性和生物亲和力的石墨烯和纳米银,结合PAMAM的卓越性质,以酪氨酸酶作为敏感元件,成功构建了一种新型BPA生物传感器。结果表明,石墨烯和纳米银能够促进电极表面的电子传递,PAMAM分子内的空腔能固定已经修饰的酪氨酸酶,且PAMAM的比表面积大,增加了电极的电化学有效表面积。该传感器表现出较好的稳定性、重现性和抗干扰性,为BPA的检测提供了一种可供选择的高灵敏度的方法。
[1]CuiK,Song Y H,Yao Y,etal.A novel hydrogen peroxide sensorbased on Ag nanoparticleselectrodeposited on DNA-networks modified glassy carbon electrode[J].Electrochemistry Communications,2008,10:663~667.
[2]Sun H,Choy TS,Zhu D R,etal.Nano-silver-modified PQC/DNA biosensor for detecting E.coliin environmentalwater[J].Biosens.Bioelectron,2009,24:1 405~1 410.
[3]Ting BP,Zhang J,Gao ZQ,etal.A DNA biosensor based on the detection of doxorubicin-conjugated Agnanoparticle labels using solid-state voltammetry[J].Biosens.Bioelectron.,2009,25:282~287.
[4]Venditto V J,Reqino CA,BrechbielMW.PAMAM dendrimer based macromolecules as improves contrast agents[J].Mol Pharm,2005,2(4):302~311.
[5]Wu LP,Zhang PZ,Guo Y,etal.Preparation of Hexanediamine-contained PAMAM Dendrimers Supported on Chitosan Microspheres and Their Application in the Adsorption of Bilirubin[J].Chemical Journal of Chinese Universities,2011,32(6):1 436~1 444.
[6]A lgarra M,Campos BB,Miranda M S,et.al.CdSe quantum dots capped PAMAM dendrimer nanocomposites for sensing nitroaromatic compounds[J].Talanta,2011,83(5):1 335~1 340.
[7]Qian Z,BaiH J,Wang G L,etal.A photoelectrochemical sensor based on CdS-polyamidoamine nano-composite film for cell captureand detection[J].Biosens.Bioelectron.,2010,25(9):2 045~2 050.
[8]Wang G X,Yang J,Park J,et al.Facile synthesis and characterization of graphene nanosheets[J].J.Phys.Chem.C,2008,112(22):8 192~8 195.
[9]Wu LP,Zhang PZ,Guo Y,etal.Preparation ofHexanediam ine-contained PAMAM Dendrimers Supported on Chitosan Microspheres and Their Application in the Adsorption of Bilirubin[J].Chemical Journal of Chinese Universities,2011,32(6):1 436~1 444.
[10]Ghosh S,Calizo I,Teweldebrhan D,etal.Extremely high thermal conductivity of graphene:Prospects for thermal management applications in nanoelectronic circuits[J].Appl.Phys.Lett.,2008,92:151 911~151 913.
[11]Huang JF,Luo H M,Liang CD,etal.Hydrophobic Brønsted Acid-Base Ionic Liquids Based on PAMAM Dendrimers with High Proton Conductivity and Blue Photoluminescence[J].J.Am.Chem.Soc.,2005,127(37):12 784~12 785.
[12]Yu Y Y,Sun Q,Zhou T S,et al.On-linemicrodialysis system with poly(amidoam ine)-encapsulated Ptnanoparticles biosensor for glutamate sensing in vivo[J].Bioelectrochemistry,2011,81(1):53~57.
[13]Kukhto A V,Kolesnikéé,Lappo A N,et al.Electrical and lum inescence properties ofa poly(amidoam ine)dendrimer containingnaphthalimide[J].Physicsof the solid state,2004,46:2 306~2310.
[14]El-Sayed M,KianiM F,Naimark M D,etal.Extravasation of Poly(amidoamine)(PAMAM)Dendrimers Across Microvascular Network Endothelium[J].Pharmaceutical Research,2001,18:23~28.
[15]Yin H S,Cui L,Chen Q P,etal.Amperometric determination of bisphenol A in milk using PAMAM-Fe3O4modified glassy carbon electrode[J].Food Chemistry,2011,125(3):1 097~1 103.
Bisphenol A biosensor based on glassy carbon electrodem odified w ith Ag nanoparticles,graphene,tyrosin aseand polyam idoam ine
GuoQian-qiong,WangWei-qi,Gao Pei-yi,Ma Teng-fei,Yang Le-le,Huang Sha-sheng*
(Life and EnvironmentalCollege,ShanghaiNormal University,Shanghai200234,China)
A bisphenol A biosensorbased on Agnanoparticles,graphene,tyrosinaseand polyamidoamine(PAMAM)modified electrode was prepared.The electrochemical behavior of the BPA biosensor was investigated by cyclic voltammetry and electrochemical impedance spectroscopy.Owning to the special physicochem ical characteristic of the nanomaterialsand the synergism between Ag nanoparticles and PAMAM,the sensor showed good amperometric response towards BPA.Under the optimal experimental conditions,the current is linear with the concentration of BPA in the range from 1.0×10-7to 3.3×10-5mol/L,with a detection limit of 3.0×10-8mol/L(S/N=3)and a correlation coefficientof0.998.
graphene;tyrosinase;PAMAM;Ag nanoparticles;bisphenol A sensor
*通讯联系人,E-mail:sshuang@shnu.edu.cn

