黄芩素PLGA纳米粒的制备及制剂学性质研究*
李 楠,范丽丽,刘志东,王爱潮,郭丽丽,周 沫
(1.天津中医药大学,天津市现代中药重点实验室-省部共建国家重点实验室培育基地,天津 300193;2.天津中医药大学,现代中药发现与制剂教育部工程研究中心,天津 300193)
黄芩素PLGA纳米粒的制备及制剂学性质研究*
李 楠1,2,范丽丽1,2,刘志东1,2,王爱潮1,2,郭丽丽1,2,周 沫1,2
(1.天津中医药大学,天津市现代中药重点实验室-省部共建国家重点实验室培育基地,天津 300193;2.天津中医药大学,现代中药发现与制剂教育部工程研究中心,天津 300193)
[目的]优化影响黄芩素聚乳酸/羟基乙酸共聚物(PLGA)纳米粒成型工艺参数,并评价优化工艺后所制纳米粒的制剂学性质。[方法]采用乳化-溶剂挥发法制备黄芩素PLGA纳米粒,以粒径、包封率为评价指标,单因素实验考察了聚乙烯醇(PVA)浓度、PLGA型号、PLGA分子量、PLGA浓度、水相与有机相体积比、丙酮与无水乙醇体积比、药物与PLGA的比例共7个参数对纳米粒成型工艺的作用规律。[结果]优化处方工艺制备的纳米粒包封率为(95.03±1.33)%、平均粒径为(126.80±4.50)nm、Zeta电位(-21.30±0.23)mV。[结论]乳化-溶剂挥发法制备的黄芩素PLGA纳米粒圆整,粒径均一。
黄芩素;乳酸/羟基乙酸共聚物;纳米粒;乳化-溶剂挥发法
黄芩的主要活性成分黄芩苷及其苷元黄芩素具有抗菌[1]、抗氧化[2]、抗病毒、抗辐射、抗肿瘤[3]等药理活性。黄芩苷对眼科疾病如角膜炎、结膜炎等的治疗作用已肯定[4]。但其自身理化性质以及普通滴眼液剂型的限制,使其滴眼后大量流失,药效维持时间短,生物利用度低。新型给药系统,如纳米粒[5-7]、脂质体、微乳、原位凝胶[8]等可以改善传统的眼用液体制剂的生物利用度较低的缺点。
聚乳酸/羟基乙酸共聚物(PLGA)是一种生物相容性好、可生物降解、安全性好、理化性能优异的医药用高分子材料,该材料进入人体后降解为人体内存在的乳酸和羟基乙酸,对人体无害[9-11]。本研究选用PLGA作为纳米粒载体材料,制备载黄芩素PLGA纳米粒,采用单因素试验优化制备工艺,考察了纳米粒的相关药剂学性质。
1 仪器和试药
高效液相色谱仪(Agilent 1200,美国);KQ-300B超声清洗器(天津Autoscience公司);Ap205电子天平(Mettler toledo,瑞士);电动搅拌(Ewka,德国);激光粒径测定仪(马尔文NanoZS,英国);超声波细胞粉碎机(JY92-IIN宁波新型生物科技股份有限公司);高速冷冻离心机(J-25Beckman美国)。
黄芩素对照品(中国药品生物制品检定所,批号111595-200905);黄芩素提取物(成都欧康医药有限公司,含量>95%);聚乙烯醇(PVA,天津市光复精细化工研究所);PLGA(济南岱罡生物科技有限公司);甲醇、乙腈(天津市康科德科技有限公司,色谱纯)磷酸(天津市化学试剂科贸有限公司,色谱纯);其他试剂均为分析纯。
2 方法与结果
2.1 纳米粒的制备 取适量黄芩素溶于无水乙醇、PLGA溶于丙酮,将两溶液混合得均一透明溶液作为有机相。取适量PVA溶于水中作为水相。在电动搅拌下,将有机相缓慢滴加到水相中。持续搅拌2~
4 h,直至丙酮完全挥干,将初乳于超声波细胞破碎仪中超声分散,经微孔滤膜过滤后,即得黄芩PLGA纳米粒混悬液。
2.2 包封率的测定
2.2.1 色谱条件 色谱柱:Diamonsil C18(200 mm×4.6 mm,5 μm),流动相∶甲醇-0.05%磷酸溶液(70∶30,V/V),波长:276 nm,柱温:35℃,流速:1.0 mL/min;进样:20 μL。
2.2.2 样品测定 精密移取0.5 mL黄芩素PLGA纳米粒于10mL量瓶中,2.5mL乙腈超声20min溶解纳米粒,无水乙醇定容,摇匀,经4℃下、2.0×104r/min超速冷冻离心20 min,取上清液适量稀释过微孔滤膜后进样20 μL,高效液相色谱(HPLC)法测定得药物总含量W总。另精密量取5mL黄芩素PLGA纳米粒胶体溶液,于4℃下、2.0×104r/min超速冷冻离心1h,取上清液,适量稀释过微孔滤膜后进样,HPLC测定得游离药物含量W游离。按下式计算包封率。包封率(EE%)=(W总-W游离)/W总×100%。
2.3 粒径、Zeta电位的测定 取黄芩素PLGA纳米粒,用纯化水稀释10倍,于25℃下用激光粒径测定仪中,测定其粒径分布及Zeta电位值。
2.4 处方筛选
2.4.1 PVA浓度的确定 分别配制出含有不同浓度PVA的溶液为水相,保持处方中其他组分的量不变,平行制备PLGA纳米粒。按2.3项测定纳米粒粒径,按2.2.3项测定包封率。结果见表1。
表1 PVA浓度对纳米粒包封率及粒径的影响(±s)Tab.1 Effect of PVA concentration on drug entrapment efficiency and size(±s)

表1 PVA浓度对纳米粒包封率及粒径的影响(±s)Tab.1 Effect of PVA concentration on drug entrapment efficiency and size(±s)
PVA浓度(%) 粒径(nm)0.5108.2±3.4 1 110.8±1.2 2 171.9±6.9 3 203.5±8.3 n 3 3 3 3包封率(%)74.72±0.77 90.55±0.71 77.45±1.11 78.50±1.07
由表1可知,PVA浓度对纳米粒粒径影响很大,PVA浓度为0.5%时纳米粒粒径最小。在实验范围内随PVA浓度增大,纳米粒包封率先增大后减小,PVA浓度为1%时,包封率最大,综合粒径及包封率结果最终确定PVA浓度为1%。
2.4.2 PLGA型号及重均分子质量的影响 固定PVA浓度为1%,保持处方中其他组分的量不变,选用PLGA(75/25)、PLGA(50/50)为聚合物材料,5 000、10 000及15 000三种不同重均分子质量的PLGA,平行制备PLGA纳米粒。按2.3项测定纳米粒粒径,按2.2.3项测定包封率。结果见表2。
表2 PLGA型号及重均分子量对纳米粒包封率及粒径的影响(±s)Tab.2 Effect of PLGA models and molecular mass on drug entrapment efficiency and size(±s)

表2 PLGA型号及重均分子量对纳米粒包封率及粒径的影响(±s)Tab.2 Effect of PLGA models and molecular mass on drug entrapment efficiency and size(±s)
PLGA型号 包封率(%) 粒径(nm)50/50 61.73±1.39 127.6±2.2 69.17±0.94 121.6±4.4 75.68±0.64 122.3±1.3 75/25 80.81±0.53 126.6±3.5 90.43±1.06 125.2±5.8 93.11±0.53 124.6±3.3 n 3 3 3 3 3 3分子量5 000 10 000 15 000 5 000 10 000 15 000
由表2可见,随着PLGA中乙交酯含量的增高,包封率降低。可能因为丙交酯含量降低,使PLGA的亲水性提高,增加了药物向外相的扩散。同一型号、不同重均分子质量PLGA制备的纳米粒,分子量较大时包封率较高;测定不同型号不同分子质量PLGA制备的纳米胶体溶液粒径大小均较接近,表明PLGA型号及重均分子量对纳米粒粒径影响不大。最终确定选用重均分子质量15000的PLGA(75/25)制备纳米粒。
2.4.3 PLGA浓度的影响 固定PVA浓度为1%,选用重均分子质量15 000万的PLGA(75/25)为聚合物材料,保持处方中其他组分的量不变,选择PLGA浓度为10、15、20、25、30 mg/mL,平行制备PLGA纳米粒。按2.3项测定纳米粒的粒径,按2.2.2项测定包封率。结果见表3。
表3 PLGA浓度对纳米粒包封率及粒径的影响(±s)Tab.3 Effect of PLGA concentration on drug entrapment efficiency and size(±s)

表3 PLGA浓度对纳米粒包封率及粒径的影响(±s)Tab.3 Effect of PLGA concentration on drug entrapment efficiency and size(±s)
PLGA浓度(g/h) 粒径(nm)10 106.2±2.4 15 110.8±1.2 20 123.2±5.4 25 172.5±4.1 30 204.9±6.3 n 3 3 3 3 3包封率(%)78.25±2.67 81.58±2.52 92.15±1.74 93.48±0.63 94.82±0.62
由表3可以看出,在实验范围内纳米粒包封率随着PLGA浓度增加而提高。分析原因可能为:1)聚合物浓度增高,可以加速纳米粒的固化,有效阻止了药物向外相扩散[13]。2)聚合物浓度增高,增加了有机相的黏度,减缓了小液滴中药物的扩散[14]。粒径结果显示随着PLGA浓度增加,纳米粒粒径也逐渐变大,最终PLGA浓度确定为20 mg/mL。
2.4.4 水相和有机相体积比的影响 PVA浓度为1%,PLGA(75/25)重均分子质量15 000,PLGA浓度20 mg/mL,保持处方中其他组分的量不变,选择水相和有机相的体积比为50∶1、20∶1、10∶1、5∶1,平行制备PLGA纳米粒的胶体溶液。按2.3项测定纳米胶体溶液的粒径,按2.2.2项测定包封率。结果见表4。
表4 水相与有机相体积比对纳米粒包封率及粒径的影响(±s)Tab.4 Effect of aqueous phase/organic phase volume ratio on drug entrapment efficiency and size(±s)

表4 水相与有机相体积比对纳米粒包封率及粒径的影响(±s)Tab.4 Effect of aqueous phase/organic phase volume ratio on drug entrapment efficiency and size(±s)
水相∶有机相50∶1 20∶1 10∶1 5∶1 n 3 3 3 3包封率(%) 粒径(nm)91.46±0.66 126.2±3.4 80.66±1.30 120.8±2.2 75.43±0.68 123.2±4.4 70.81±1.31 122.5±5.1
表4结果表明,随着水相与有机相比例的增大,纳米粒包封率逐渐增大。在使用乳化溶剂挥发法制备纳米粒时,有机相与水相的比例是影响纳米粒包封率的重要因素。文献报道,降低两相比例能显著增加纳米粒包封率,减少突释[15]。增大水相的量可稀释溶剂,使有机溶剂以高浓度梯度跨过相界面。不同体积比制备纳米粒的粒径测定结果相差不大,显示两相比例变化对纳米粒粒径影响不大。为使包封率最大化,最后选定水相∶有机相=50∶1。
2.4.5 丙酮和无水乙醇比例的影响 固定PVA浓度为1%,PLGA(75/25)重均分子质量15 000,PLGA浓度20 mg/mL,水相和有机相的体积比为50∶1,保持处方中其他组分的量不变,选择丙酮和无水乙醇的比例为7∶3、3∶1、4∶1,平行制备PLGA纳米粒。按2.3项测定纳米粒粒径,按2.2.2项测定包封率。结果见表5。
表5 丙酮与无水乙醇体积比对纳米粒包封率及粒径的影响(±s)Tab.5 Effect of acetone/ethanol volume ratio on drug entrapment efficiency and size(±s)

表5 丙酮与无水乙醇体积比对纳米粒包封率及粒径的影响(±s)Tab.5 Effect of acetone/ethanol volume ratio on drug entrapment efficiency and size(±s)
丙酮∶无水乙醇 粒径(nm)7∶3 162.2±1.4 3∶1 120.9±3.2 4∶1 111.2±7.4 n 3 3 3包封率(%)48.70±4.67 91.71±0.65 87.73±1.31
由表5可知,丙酮与无水乙醇的比例对纳米粒包封率及粒径均有较大影响,一定范围内,随着丙酮与无水乙醇比值的增大,纳米粒包封率逐渐增大,比值继续增大,包封率有所下降;纳米粒的粒径变化正好相反,随着二者比值的增大,纳米粒粒径逐渐减小。最终选定丙酮∶无水乙醇=3∶1。
2.4.6 药物与PLGA比例的影响 PVA浓度为1%,PLGA(75/25)分子质量15000,PLGA浓度20 mg/mL,水相和有机相的体积比为50∶1,丙酮和无水乙醇的比例3∶1,保持处方中其他组分的量不变,选择黄芩素的投药量为2、4、8、16 mg,平行制备PLGA纳米粒。按2.3项测定纳米粒的粒径,按2.2.2项测定包封率。结果见表6。
由表6可知随着药物与PLGA比例的增大,纳米粒包封率逐渐降低。主要是因为降低药物与PLGA比例可有效阻止制剂制备过程中药物向外相的渗漏,提高包封率。但药物与PLGA比例应控制在一定的范围内,若药物过多,PLGA不能完全将药物聚合包封,造成药物的损失,降低包封率。数据显示,当黄芩素∶PLGA=1∶40时纳米粒包封率最高,药物与PLGA不同比例对纳米粒的粒径基本无影响,所以最终选择黄芩素∶PLGA=1∶40。
表6 药物与聚乳酸-羟基乙酸共聚物(PLGA)比例对纳米粒包封率及粒径的影响(±s)Tab.6 Effect of Scutellarein/PLGA mass ratio on drug entrapment efficiency(±s)

表6 药物与聚乳酸-羟基乙酸共聚物(PLGA)比例对纳米粒包封率及粒径的影响(±s)Tab.6 Effect of Scutellarein/PLGA mass ratio on drug entrapment efficiency(±s)
药物量(mg) 包封率(%) 粒径(nm)2 98.07±1.36 119.2±1.4 4 90.71±0.96 120.9±3.2 8 81.07±0.78 123.2±7.3 16 43.40±1.97 121.2±5.4 n 3 3 3 3药物∶PLGA 1:40 1:20 1:10 1:5
2.5 处方的确定 根据实验结果,确定PVA浓度为1%,分子质量15 000 PLGA(75/25),PLGA浓度20 mg/mL,有机相中丙酮∶无水乙醇=3∶1,有机相与水相体积比为1∶50,药物与PLGA比例为1∶40,为最优处方。
2.6 优化处方纳米粒的表征
2.6.1 包封率的测定 按照2.2.2项下测定按照优化处方制备的3批纳米粒的包封率,结果见表7。
表7 不同批次黄芩素纳米粒包封率(±s)Tab.7 The drug entrapment efficiency in different batch of Scutellarein-PLGANP(±s)
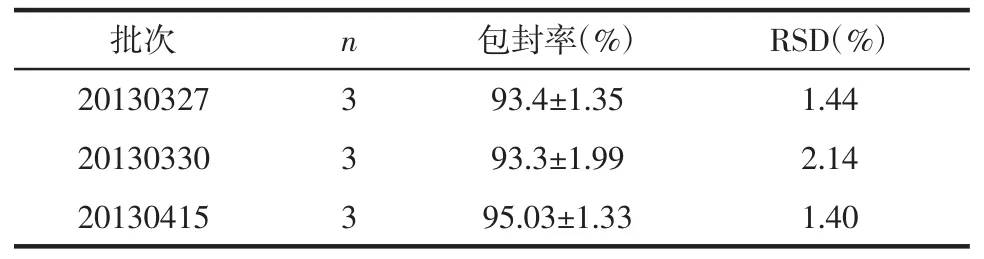
表7 不同批次黄芩素纳米粒包封率(±s)Tab.7 The drug entrapment efficiency in different batch of Scutellarein-PLGANP(±s)
批次 RSD(%)20130327 1.44 20130330 2.14 20130415 1.40 n 3 3 3包封率(%)93.4±1.35 93.3±1.99 95.03±1.33
2.6.2 粒径、Zeta电位的测定 取优化处方制备的黄芩素PLGA纳米粒,用纯化水稀释5倍,于25℃下用激光粒径测定仪中,测定其粒径分布及Zeta电位值(见图1,图2)。
3 讨论
有机相中加入无水乙醇,是由于前期只选用丙酮为有机相制备纳米粒的实验中发现当有机相滴入水相时,在生成纳米粒的同时会出现部分的聚合物聚集成团或在水相表面成膜的现象,严重影响了纳米粒的产率,PLGA浪费较多。加入一定量的无水乙醇后,再将其滴入到1%PVA水相中制备纳米粒时明显减少了PLGA团聚的量,纳米粒产率提高了,减少了浪费。分析原因可能是无水乙醇优先从有机相向水相扩散,从而使丙酮迅速地穿越相界面挥发除去,处于乳滴中的载体材料PLGA迅速析出并最终固化形成纳米粒。

图1 黄芩素PLGA纳米粒粒径图Fig.1 The submicron size of Scutellarein-PLGANP

图2 黄芩素PLGA纳米粒电位图Fig.2 The zeta potential of Scutellarein-PLGANP
PLGA纳米粒粒径小于微球,释药特性与微球相似。PLGA纳米粒因其特定的粒径范围具有特定的物理靶向性能,对特定部位的治疗效果显著。但与微球一样,如何提高纳米粒的包封率,是药剂工作者面临的一个亟待解决的问题[11]。
本研究初步考察了PLGA纳米粒制备过程中影响包封率的因素,成功制备了具较高包封率的载黄芩素的PLGA纳米粒,纳米粒的释放情况及体内生物利用还有待进一步的实验研究。
[1]华晓东,巩媛媛,芮 菁,等.黄芩素对皮肤过敏治疗作用的实验研究[J].天津中医药,2007,23(3):241-244.
[2] Rice-Evans C.Flavonoid antioxidants[J].Curr Med Chem,2001,8 (7):797-807.
[3] Lee MJ,Wang CJ,Tsai YY,et al.Inhitory effect of 12-Otetradecanoyphorbol-13-acetate caused tumor promotion in benzo pyreneinitiated CD-1 mouse skin by baicalein[J].Nutr Cancer,1999,34(2): 185-191.
[4]张 锐,赵海南,瞿继兰,等.聚乙二醇硬脂酸酯15对黄芩苷角膜透过性研究[J].天津中医药大学学报,2013,32(1):36-39.
[5]李佳玮,赵海南,郭秀君,等.盐酸小檗碱眼用固体脂质纳米粒的研究[J].天津中医药大学学报,2012,31(3):157-159.
[6] van Vlerken LE,Amiji MM.Multi-functional polymeric nanoparticles for tumour-targeted drug delivery[J].Expert Opin Drug Deliv, 2006,3(2):205-216.
[7] NieS,XingY,KimGJ,etal.Nanotechnologyapplicationsoncancer[J].Annu Rev Biomed Eng,2007,9:257-288
[8]李 琳,赵海南,李佳玮,等.盐酸小檗碱离子型眼用原位凝胶的研究[J].天津中医药大学学报,2011,30(4):229-231.
[9] Akan T,Kawabata K,Yanagisaun E,et al.Baicalin,the predominant flavone glucuronide of scutellariae radix,is absorbed from the rat gastrointestinal tract as the aglycone and restored to its original form[J].J Pharm armacol,2000,52(12):1563-1568.
[10]Sahoo SK,Panda AK,Labhasetwar V.Characterization of porous PLGA/PLA microparticles as a scaffold for three dimensional growth of breast cancercells[J].Biomacromolecules,2005,6(2):1132-1139.
[11]Kumari A,Yadav SK,Yadav SC.Biodegradable polymeric nanoparticles based drug delivery systems[J].Colloids Surf B Biointerf,2010, 75(1):1-18.
[12]饶卫兵,郝存江,魏 丽,等.膜-超声分散法制备川芎嗪固体脂质纳米粒[J].天津中医药,2009,24(6):503-505.
[13]符旭东,汤 韧,刘 宏.效应面法优化甲巯咪唑聚乳酸-羟基乙酸共聚物微球的处方工艺[J].广东药学院学报,2006,22(1):19-24.
[14]蒋朝军,杨清敏,胡筱菲,等.新型利培酮PLGA微球的制备及体外释放研究[J].中国药学杂志,2011,46(2):124-127.
[15]Mao SR,Shi Y,Li L,et al.Effects of process and formulation parameters on characteristics and internal morphology of poly(d,l-lactideco-glycolide)microspheres formed by the solvent evaporation method[J].Eur J Pharm Biopharm,2008,68(2):214-223.
Preparation and character in pharmacy of Scutellarein loaded PLGA nanoparticles
LI Nan1,2,FAN Li-li1,2,LIU Zhi-dong1,2,WANG Ai-chao1,2,GUO Li-li1,2,ZHOU Mo1,2
(1.Tianjin State Key Laboratory of Modern Chinese Medicine,Tianjin University of Traditional Chinese Medicine, Tianjin 300193,China;2.Engineering Research Center of Modern Chinese Medicine Discovery and Preparation Technique,Tianjin University of Traditional Chinese Medicine,Tianjin 300193,China)
[Objective]To optimize the processing parameters of Scutellarein loaded PLGA nanoparticles(PLGANP)and study the character in pharmacy of the optimal Scutellarein-PLGANP.[Methods]Seven processing parameters were assessed systematically to enhance the Scutellarein incorporation into PLGA nanoparticles and to minimize the particle size,including PVA concentration in the aqueous phase,PLGA models,PLGA molecular mass,PLGA concentration in the organic phase,aqueous phase/organic phase volume ratio,acetone/ethanol volume ratio,Scutellarein/PLGA mass ratio.[Results]The Scutellarein-PLGANP produced by the optimal formulation were submicron size of(126.80±4.50)nm and the zeta potential was(-21.30±0.23)mV,with the entrapment efficiency of(95.03± 1.33)%.[Conclusion]Scutellarein drug loaded PLGANP can be prepared by O/W emulsion solvent evaporation.
Scutellarein;PLGA;nanoparticle;emulsion solvent evaporation
R283.6
:A
:1672-1519(2014)03-0173-04
2013-07-07)
(本文编辑:高 杉,马晓辉)
10.11656/j.issn.1672-1519.2014.03.15
国家科技重大专项“重大新药创制”项目(2012 ZX09304007);教育部新世纪优秀人才支持计划(NCET-12-1068A);天津市自然科学基金项目(12JCYBJC18700)。
李 楠(1982-),女,博士,从事中药制剂研究。
刘志东,E-mail:lonerliuzd@163.com。

