垂盆草片提取工艺及制剂处方的研究
包汝泼, 梁 伟
(宁波天衡药业股份有限公司, 浙江 宁波 315201)
垂盆草片提取工艺及制剂处方的研究
包汝泼, 梁 伟
(宁波天衡药业股份有限公司, 浙江 宁波 315201)
目的 优化垂盆草片提取工艺及制剂处方。方法 采用正交设计法,以提取物中的槲皮素、山柰素和异鼠李素总量作指标,考察加水量、煎煮次数、煎煮时间对提取效果的影响;通过垂盆草中间体颗粒的引湿性和片剂的质量差异及崩解限度等质量指标选择制剂处方。 结果 优选的提取工艺为加 10 倍量水煎煮 3 次, 每次 60 min; 处方组成为浸膏粉、微晶纤维素、聚维酮、微粉硅胶和硬脂酸镁。结论 所选提取工艺及制剂处方科学合理,质量稳定。
垂盆草片;正交试验;槲皮素;引湿性
垂盆草片收载在 《中国药典》 1977 年版一部, 以景天科垂盆草经提取制备而成,具有清热解毒、活血利湿之功效[1]。 本公司生产该品 种多年, 但因 原有标准要求比较低,中间浸膏粉无有效成分的控制,生产处方和参数设置也以经验为主,没有具体的量化,为了更好保证质量,使工艺流程更趋科学合理,本实验对药材提取和处方工艺进行优化,获取最佳工艺条件。
1 仪器与试药
1.1 仪器 Agilent1260 高效液相色谱系统 ( 美国安捷伦科技有限公司), RE-85Z旋转蒸发仪 ( 上海医械专 机厂),SHL-3 型高速搅拌湿法造粒机 ( 上海美阳机械发展有限公司); ZPS008 旋转压片机 (上海天祥健台制药机械有限公司); AE240 型电子天平 (中国梅特勒-托利多仪器厂)。
1.2 试药 槲皮素对照品 (100081-200406)、 山柰素对照品 (0861-200002) 、 异 鼠 李 素 对 照 品 (110860-200205 ) 均为中国食品药品检定研究院提供,供含量测定用;垂盆草购自宁波市药材股份有限公司,经检验符合 《中国药典》2010 年版一部有关标准, 辅料购自正规医药企业, 乙腈等试剂符合色谱要求。
2 实验方法和结果
2.1 垂盆草浸膏和药材中成分测定[2]
2.1.1 色 谱条 件 diamonsil ODS 色 谱 柱 ( 250 mm×4.6 mm, 5 μm); 流动相为甲醇-0.4%磷酸 (48 ∶52); 检测波长 360 nm; 体积流量 1.0 mL/min; 柱温 30 ℃; 进样量 10 μL。 此条件下, 垂盆草片中3 种指标性成分达到较好的分离效果, 分离度大于 1.5, 理论板数按槲皮素峰计算不低于3 000, 典型图谱如图 1。

图1 混合对照品溶液 (A) 和样品溶液(B) 的 HPLC色谱图
2.1.2 对照品溶液的制备 取槲皮素、 山柰素、 异鼠李素对照品适量, 精密称定, 加甲醇制成每 1 mL各含 20 μg、 5 μg、 5 μg的混合溶液, 即得。
2.1.3 供试品溶液的制备 取浸膏或药材约 0.5 g, 精密称定, 加入甲醇-25%盐酸溶液 (4 ∶1) 混合溶液 25 mL,称定质量, 加热回流 1 h, 放冷, 再称定质量, 用甲醇-25%盐酸溶液 (4 ∶1) 混合溶液补足减失的质量, 摇匀,滤过,取续滤液,即得。
2.1.4 线性关系考察 分别取 18.22 μg/mL的槲皮素、4.805 μg/mL的山柰素和 4.628 μg/mL的异鼠李素对照品溶液各 2.0、 5.0、 10.0、 20.0、 50.0 μL注入液相色谱仪测定, 以峰面积 A为纵坐标, 进样量 C(μg) 为横坐标,求得槲皮素、山柰素和异鼠李素回归线性方程分别为:A槲皮素=4 250.4C-22.656 (r2=0.999 9), A山柰素=4 337.5 C-8.388 ( r2=0.999 5), A异鼠李素=4 156.5C-13.146(r2=0.997 1), 结 果表明槲 皮 素在进样量 为0.036 44 ~0.911 1 μg范 围 内 线 性 良 好、 山 柰 素 在 进 样 量 为0.009 610 ~0.240 2 μg范围内线性良好、 异鼠李素在进样量为0.009 256 ~0.462 8 μg范围内线性良好。
2.1.5 重复性试验 称取浸膏 (批号为 20120501) 样品 6份, 按 “2.1.3” 项下制备供试品, 分别测定, 计算 RSD,结果槲皮素质量分数为 1.47 mg/g(RSD=0.9%), 山柰素质量分数为 0.19 mg/g(RSD=1.3%), 槲皮素质量分数为0.090mg/g(RSD=2.9%), 说明方法重复性良好。
2.1.6 加样回收率试验 以浸膏粉为例, 取 6 份 0.25 g左右的浸膏 (批号为 20120501), 精密称定, 各加入槲皮素对照 品 (0.070 23 mg/mL)、 山 柰 素 对 照 品 (0.010 01 mg/mL) 和异鼠李素对照品 (0.004 628mg/mL) 混合液 5 mL, 混匀, 依法测定, 计算回收率和 RSD, 结果显示槲皮素的平均回收率为 97.7% (RSD=0.8%), 山柰素平均回收率为 101.87% (RSD=2.2%), 异鼠李素的平均回收率为98.8% (RSD=2.3%), 表明本法符合定量测定的要求。
2.1.7 样品的测定 按上述供试品制备方法制备后, 精密吸取溶液 10 μL, 注入液相色谱仪测定, 即得。
2.2 片重差异的测定 取药片 20 片, 精密称定, 求得平均片重后,再分别精密称定每片的质量,每片重与平均片重相比较,计算超出质量的最大限度。
2.3 崩解时限和引湿性试验的测定 参考 《中国药典》2010 年版一部附录崩解时限检查法 (附录 XIIA), 取素片6 片置吊篮玻璃管中, 于 (37 ±1)℃的恒温水中, 按每 1 min 作 30 ~32 次上下移动, 记录各片崩解成碎粒全部通过筛网的时间。
参考 《中国药典》 2010 年版二部附录引湿性试验指导原则 (附录 XIX J), 将混合好的粉末干燥至恒重后, 在已恒重的称量瓶底部放入厚约1 mm的粉末,放置在温度为(25 ±1)℃, 相对湿度为 64% ±2%的恒温培养箱中保持 24 h后取出称量,按该指导原则公式计算增重百分率。
2.4 提取工艺条件的筛选[3]
2.4.1 提取工艺的正交设计 根据大部分有效成分具有水溶性特点[4]及药品注册法规要求, 确定以水为提取溶媒,采用煎煮法提取, 并用 L9(34) 正交表安排试验, 因素水平见表1。

表1 因素水平
2.4.2 实验安排及结果 根据实验方案, 称取处方量药材, 先浸泡 30 m in, 然后按正交试验表项下设计的试验条件进行提取, 合并溶液, 减压浓缩至浸膏相对密度 1.08 g/mL, 静置 24 h, 离心, 取上清液浓缩至浸膏相对密度1.12 g/mL, 减压干燥, 再按 “2.1” 项方法测定槲皮素、山柰素、 异鼠李素量,计算得率 (得率为浸膏中总量占投料药材中总量的比例,按百分比计算),相同条件重复两次实验, 取平均值。 结果见表 2, 方差分析见表 3。
由方差分析表可知, 主次因素为 B>A>C,提取次数对成分提取有显著性影响, 提取效果 B3>B3>B1, 由直观分析得出最佳工艺为 A3B3C3, 考虑煎煮时间每次 80min 与每次 60min 相差不大, 煎煮时间太长一方面消耗能源, 一方面易破坏其他不稳定成分,所以最终确定提取工艺为A3B3C2, 即 加 10 倍量 水 , 提取 3 次, 每次煎煮 60 min。
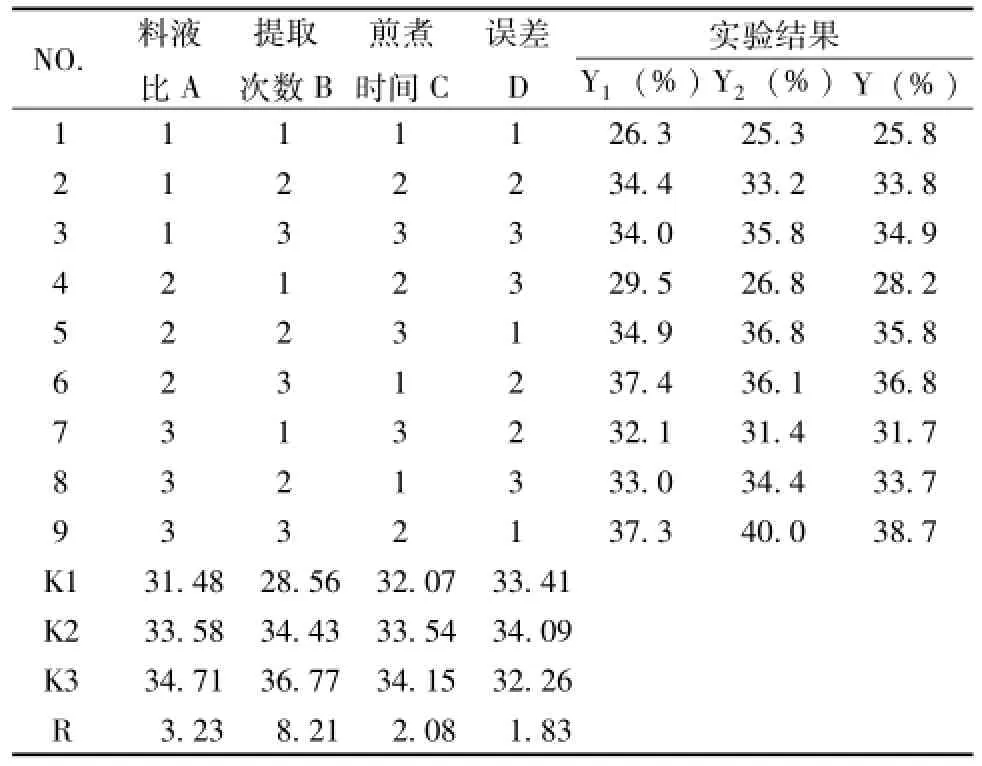
表2 提取工艺正交试验方案及结果

表3 结果的方差分析
2.5 设备的改造[5]垂盆草浸膏粉制粒时黏合剂加入过度集中易致局部过湿,会产生大量团块不能整粒过筛,如果通过加高乙醇体积分数,既提高了生产成本又降低了生产安全性,非最佳方法,本实验采用喷雾法造粒,将喷嘴安装到造粒锅顶部,用压力罐将黏合剂以喷雾形式喷入造粒锅中,溶液被雾化分散到物料上,制粒过程没有成团现象,颗粒的均匀性和流动性都有很大的改善。
2.6 处方的筛选[6]按表 4 处方比例称取浸膏粉与辅料共2 kg左 右 , 倒入 高 速搅拌湿 法 造 粒 机 中 混 匀, 加 入 80%乙醇的 PVP黏合剂, 按规定时间搅拌制软材, 20 目筛湿整,60 ℃烘箱干燥后整粒, 外加硬脂酸镁混合 (取一部分做引湿性实验) , 压片 ( 以 浸 膏 粉 计 算 为 0.32 g/片) , 检 查 素片的重量差异和崩解度, 记录数据, 统计结果见表5。

表4 不同处方组成

表5 不同处方的样品质量数据比较
从表5各组试验数据可见,处方1加了交联聚维酮增加了引湿性,并且在压片中出现了粘冲现象,不利于大规模生产, 处方2崩解时限最长, 易致崩解不合格, 处方3、4都符合质量要求,考虑到中药糖衣片服用量比较多,处方4在保证质量的前提下,相对片重比较轻,服用量小,生产成本也降低,因此确定处方4为最终处方。
2.7 工艺验证 根据试验筛选结果, 进行 3 批 40 万片规模的生产验证生产,结果3批浸膏的黄酮提取率分别为38.9%、 40.2%和 38.2%, 片剂生产过程中各项指标符合要求,没有出现粘冲和崩解不合格等现象,表明优化所得工艺稳定、可靠。
3 讨论
3.1 垂盆草苷具有明显的保肝作用, 常作为垂盆草质量指标成分[7], 本实验也曾以垂盆草苷作为含量测定成分, 但实践中发现其作为水溶性氰苷类化合物,极不稳定,受热易分解, 各批提取物中含量相差达10倍, 很难客观反映制剂的质量。 后据文献报道[8]垂盆草中黄酮类成分也有保肝作用,性质相对稳定,检测方法也被药典收录,所以采用黄酮成分作为质量控制指标。
3.2 在进行提取工艺优化时, 为了减少各种不明原因及仪器操作引起的误差,提高实验结果的精度和可信度,在尽量平衡的操作基础上各试验做两次,数据取两者均值。同时在实验中发现浸膏粉对片剂崩解影响也较大,主要是提取液浓缩时,表面产生的药液膜一定要过滤去除,否则易造成片剂崩解不合格。
3.3 制粒工序是中药片剂工艺的关键步骤, 粘冲、 崩解时限超标和压片顶裂等现象往往与制备的颗粒好坏有关[9],本实验对制粒的关键因素如黏合剂的种类、用量和搅拌时间等因素也进行了优化。
3.4 本品目前还是糖浆包衣, 生产工艺复杂, 操作过程中大多依赖操作者凭手感控制包衣质量, 与 GMP精神不符,糖衣中的蔗糖成分同时限制了一部分患者的服用[10], 本部门正在做相关研究拟用薄膜包衣来取代糖衣,以解决上述问题。
[ 1 ] 宋玉华, 李春雨, 郑 艳.垂盆草的研究进展[J].中药材, 2010, 33(12): 1973-1975.
[ 2 ] 国家药典委员会.中华人民共和国药典: 2010 年版一部[S].北京: 中国医药科技出版社, 2010: 198-199.
[3] 玄 律,倪 健.多指标优选醒目颗粒水提醇沉制备工艺[J].中成药, 2010, 32(7): 1238-1240.
[ 4] 邵成雷.垂盆草化学成分及其药理临床研究[D].济南:山东大学, 2006.
[5] 胡功允,彭俊清,余 慧.盐酸非索非那定盐酸伪麻黄碱缓释片处方工艺研究[J].中国现代应用药学, 2011, 28(9): 846-849.
[6] 孙淑萍,吴少云,李胜利,等.妇科复方抗菌消炎泡腾片的成型工艺研究[J].中成药, 2013, 35(2): 423-426.
[7] 潘金火,何满堂,罗 兰.垂盆草药材质量控制方法研究[J].成都中医药大学学报.2002, 25(1): 44-55.
[8] 潘金火, 潘 萍.垂盆草总黄酮中8种单体成分对肝细胞的保护作用[J].中国医院药学杂志, 2010, 30 (19):1621-1623.
[ 9 ] 高爱国.浅谈片剂制粒工艺控制[J].齐鲁药事, 2009,28(3): 187-188.
[10] 刘利清, 胡佳文.复方丹参片薄膜包衣工艺研究[J].中国药业, 2010, 19(5): 37.
R284.2
: B
: 1001-1528(2014)03-0646-04
10.3969/j.issn.1001-1528.2014.03.048
2013-04-12
包汝泼 (1976—) , 男, 硕士, 高级工程师, 从事新药研究。 E-mail: brp168@163.com

