地龙舒腰胶囊中有毒生物碱的检查
杨 骏, 张 彤, 李 婷*, 蔡贞贞, 陶建生
(1.上海中医药大学, 上海 201203; 2.上海市黄浦区香山中医医院, 上海 200020)
地龙舒腰胶囊中有毒生物碱的检查
杨 骏1,2, 张 彤1, 李 婷1*, 蔡贞贞1, 陶建生1
(1.上海中医药大学, 上海 201203; 2.上海市黄浦区香山中医医院, 上海 200020)
目的 地龙舒腰胶囊 (地龙, 穿山龙, 制川乌) 中有毒生物碱的检查。 方法 以制川乌中所含生物碱为研究对象, 采用 HPLC法, Xtimate C18色谱柱 (4.6 mm×250 mm, 5 μm) , 以 0.26% 醋 酸铵 ( 氨水 调 pH至 9.5 ) -乙腈(55 ∶45) 为流动相, 柱温为 30 ℃, 检测波长为 235 nm, 体积流量为 0.8 mL/min, 对方中双酯型生物碱进行含有量限度测定。结果 所建立方法专属性良好,新乌头碱、乌头碱、次乌头碱的稳定性、精密度、日间精密度良好,新乌头碱、 乌头碱、 次乌头碱的平均加样回收率在 90% ~110%之间, 而在胶囊中的 3 种有毒生物碱未检出。 结论 地龙舒腰胶囊中的有毒生物碱符合标准。
地龙舒腰胶囊;新乌头碱;乌头碱;次乌头碱
地龙舒腰胶囊处方源于已故全国名中医施维智先生的经验方,为上海市香山中医医院医院制剂(注册号 SYZ-ZF-088-2005)。 地龙舒腰胶囊的处方由地龙、穿山龙、制川乌三味药材组成,有抗炎、活血、止痛等作用,主治腰椎盘突出。该方临床使用数十年, 疗效确切, 深受患者欢迎[1]。 但是现行标准缺乏必要的质控指标,仅有一项地龙的薄层鉴别及水分等常规检查项目,目前已有对地龙舒腰胶囊的质量标准进行研究[2], 其中采用紫外法对其中酯型生物碱进行限度检查,但是由于紫外检测法专属性不强,故本研究拟参照 2010 年版 《中国药典》,结合大量文献调研,拟采用高效液相色谱法对地龙舒腰胶囊中制川乌所含毒性生物碱进行限度检查,为进一步评价和控制地龙舒腰胶囊的质量提供一定的依据。
制川乌为川乌的炮制加工品,辛、苦,热,有毒。具有祛风除湿,温经止痛的功效。乌头属主要成分是生物碱,包括双酯型生物碱,单酯型生物碱,氨醇型生物碱和其他类型化合物[3]。 双酯型生物碱既是有效成分,也是毒性较强物质。因此,对双酯型生物碱的含有量控制非常重要。 2010 年版 《中国药典》 一部中 “制川乌” 项下规定, 本品含双酯型生物碱以乌头碱 ( aconitine)、次乌头碱 (hypaconitine) 及新乌头碱 ( mesaconitine) 的总量计, 不得过 0.040%。 文献中一般对乌头碱或3 种生物碱进行测定, 方法有薄层色谱法[4], 高效液相法[5]等。 本实验选择 HPLC法测定地龙舒腰胶囊中的乌头碱、次乌头碱和新乌头,但这3种生物碱结构相似,分离有一定的难度,而许多文献中采用的条件不够理想或简便,如流动相添加离子对试剂[6],加入三氯甲烷[7]或四氢呋喃[8]。 本实验对HPLC的流动相进行了详细的摸索,以期建立更理想的色谱条件。
1 仪器与材料
Agilent 1200 高 效 液 相 色 谱 仪 ( G1314A 型VWD 检 测 器, Agilent ChemStation 工 作 站 );XS105DU电子天平 (瑞士梅特勒 -托利多公司);BS124S 型电子天平 (赛多利斯科学仪器北京有限公司); LXJ-IIB低速大容量多管离心机 (安亭科学仪器厂); WH-861 涡旋混合器 (上海环球物化仪器厂)。
制川乌饮片 (上海同济堂药业有限公司,批号 100801),乌头碱 (批号 110720-200410)、 新乌头碱 (批号 110799-200404)、 次乌头碱 (批号110798-200404) 均购自中国药品生物制品检定所, 纯度均不低于 98%; 地龙舒腰胶囊 (批号090704、 100802、 101101, 0.25g/粒, 上海市黄浦区香山中医医院研制); 乙腈为色谱纯 (Merck 公司), 水为双蒸水, 其余试剂均为分析纯 (国药集团化学试剂有限公司)。
2 方法与结果
2.1 川乌中有毒生物碱的 HPLC检查方法
2.1.1 色谱条件 Xtimate C18色谱柱 (4.6 mm× 250 mm, 5 μm); 以 0.26%醋酸铵溶液 (用氨水调 pH至 9.5) -乙腈 (55%∶45%) 为流动相; 柱温 30 ℃; 检 测 波 长 235 nm; 体 积 流 量 0.8 m L/min; 进样量 20 μL。
2.1.2 溶液制备
2.1.2.1 对照品溶液的制备 取 3 种生物碱对照品适量, 精密称定, 加入 0.02 mol/L硫酸溶液溶解并定容至 10 mL量瓶, 分别制成乌头碱 194 μg/mL, 新 乌 头 碱 589 μg/mL, 次 乌 头 碱 599 μg/mL的混合溶液。
2.1.2.2 供试品溶液的制备[9]取地龙舒腰胶囊(批号 090704) 40 粒, 取出内容物, 研磨混匀,取粉末约5 g, 精密称定, 置加盖离心管中, 加氨试液 8 mL,浸润 30 min, 加入乙醚 20 mL涡旋 2 min, 离心 (4 000 r/min,5 min)。 分取上层乙醚层, 下层再加乙醚 15 mL, 离心, 重复 3 次, 合并乙醚层, 少量乙醚洗涤沉淀。 40℃以下减压回收溶剂至干,残渣加入 0.02 mol/L硫酸溶液适量,超声使溶解, 分次洗涤残渣,转移至10 mL量瓶,以 0.02 mol/L硫酸定容, 摇匀, 精密量取 5 m L于10 m L离心管内。 加乙醚 1 mL, 涡旋 30 s, 离心(4 000 r/min, 2 min), 弃乙醚层, 取水层。 0.45 μm滤头过滤,即得。
2.1.2.3 阴性样品制备 按样品处方比例称取不含制川乌的药材适量,按成药的生产工艺制备缺制川乌的阴性样品,按供试品溶液制备方法制备阴性样品溶液。
2.1.3 专属性试验 分别精密吸取对照品溶液、供试品与阴性样品溶液各 20 μL, 注入液相色谱仪, 测定, 即得。色谱图见图1。
结果显示,阴性溶液在新乌头碱、乌头碱、次乌头碱的对照品溶液的相同保留时间未见色谱峰,说明杂质成分对测定无干扰。

图1 地龙舒腰胶囊高效液相色谱图Fig.1 HPLC chromatogram s of Dilong Shuyao CaPsules
2.1.4 线性关系的考察 分别精密称取新乌头碱、乌头碱、次乌头碱对照品适量于同一量瓶中,加0.02 mol/L硫酸溶液溶解并配制成一系列对照品溶液。 分别取表 1中不同质量浓度的对照品溶液 20 μL注入液相色谱仪, 测定, 记录峰面积积分值;以新乌头碱、乌头碱、次乌头碱对照品质量浓度(X) 对峰面积积分值 (Y) 绘制标准曲线, 并进行回归,计算标准曲线的回归方程及相关系数。结果见表1。
由表 1 可 见, 新 乌 头 碱 在 2.356 ~586.0 μg/mL, 乌头碱在 0.776 ~194.0 μg/mL, 次乌头碱在 2.396 ~599.0 μg/m L的范围内呈良好的线性关系。
2.1.5 日内精密度试验 精密吸取新乌头碱对照品溶液 (11.78、 47.12、 235.6 μg/m L)、 乌头碱对照品溶液 (3.88、 15.52、 77.6 μg/mL)、 次乌头碱对照品溶液 (11.98、 47.92、239.6 μg/mL)20 μL, 各连续进样 5 次,计算峰面积的相对标准偏差 (RSD), 结果新乌头碱峰面积的 RSD (n= 5) 分别为 1.16%, 0.48%, 0.18%; 乌头碱峰面积 的 RSD ( n=5 ) 分 别 为 1.42%、0.74%、0.20%; 次乌头碱峰面积的 RSD (n=5)分别为1.18%、 0.47%、 0.25%。

表1 线性关系Tab.1 Linear relationshiP
2.1.6 日间精密度试验 精密吸取新乌头碱对照品溶液 (11.78、 47.12、 235.6 μg/mL)、 乌头碱对照品溶液 (3.88、 15.52、 77.6 μg/mL)、 次乌头碱对照品溶液 (11.98、 47.92、 239.6 μg/mL)20 μL, 各连续进样 2 次, 计算峰面积的相对标准偏差 (RSD), 持续 5 d。 结果新乌头碱峰面积的RSD ( n=5) 分别为 1.74%、1.16%、 0.92%;乌头碱峰面积的 RSD ( n=5) 分 别 为 1.96%、1.45%、 1.14%; 次乌头碱峰面积的 RSD (n=5)分别为 1.93%、 1.49%、 0.92%。
2.1.7 溶液的稳定性试验 取对照品溶液 (新乌头碱 11.78 μg/m L、 乌头碱 3.88 μg/mL、 次乌头碱 11.98 μg/mL), 在 0、 2、 4、 8、 12、 24 h 分别进样 20 μL,计算峰面积的 RSD。结果新乌头碱、乌头碱、 次乌头碱峰面积的 RSD分别为 1.37%、1.30%、 1.42%。 表明新乌头碱、 乌头碱、 次乌头碱稳定性良好。
2.1.8 重复性试验 取地龙舒腰胶囊样品 (批号100802), 平行取样 6 次, 按照 “2.1.2.2” 项下方法处理, 制备样品供试品。 按 “2.1.1” 项下方法重复测定乌头碱、新乌头碱、次乌头碱的量,计算平均值和 RSD。 结果表明, 样品中乌头碱、 新乌头碱、次乌头碱的量极低以至于未检出。
2.1.9 加样回收率试验 取已知含有量的地龙舒腰胶囊样品9份,平均分为3组,分别精密加入乌头碱、新乌头碱、次乌头碱混合对照品适量,按供试品溶液的制备方法制成检测溶液,并按上述测定条件测定, 进样量 20 μL, 计算低、 中、 高 3 个加入量的平均回收率 (n=3), 结果见表 2。
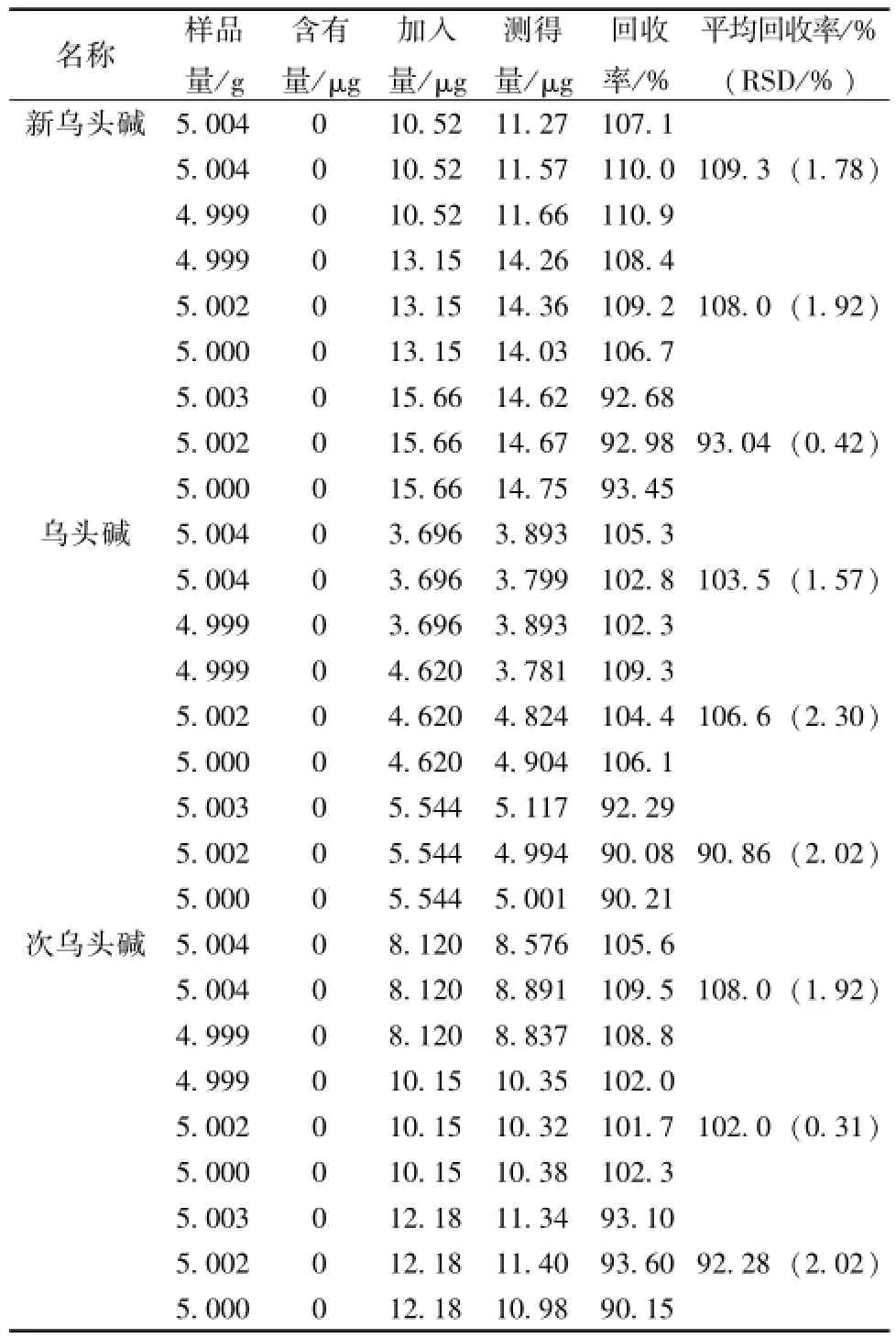
表 2 加样回收率试验 (n=9)Tab.2 Results of recovery tests(n=9)
结果表明, 平均加样回收率在 90% ~110%之间,回收率良好。
2.1.10 最低检测限确定 取混合对照品逐级稀释,测定信噪比,换算成信噪比为3时的对照品的进样量,结果新乌头碱、乌头碱、次乌头碱检测限分别为 6.68、 4.44、 2.07 μg。
2.1.11 样品测定 按供试品制备方法制备 3 批样品,分别进行检测,结果3批均未检测到新乌头碱、乌头碱、次乌头碱,表明3种成分在胶囊内含有量低于检测限。
3 讨论
乌头类生物碱是一类极性较强的生物碱,在实验中选择反相 C18柱作为分离乌头类生物碱的固定相,同时由于乌头类生物碱的碱性较强,在实验中需要加入一定碱来改善分离效果, 而一般的 C18柱pH的使用范围为 4 ~7, 不能满足实验需要, 因此, 选择了 pH的使用范围为 2 ~11 的 C18柱作为固定相。
新乌头碱、乌头碱、次乌头碱峰面积极小以至于无法积分,于是按照 “供试品溶液的制备” 方法处理处方中的制川乌饮片,测得其中乌头碱量为0.000 3%, 次乌头碱量为 0.006%, 新乌头碱未测出, 三者相加,符合 2010 年版 《中国药典》 一部中 “制川乌” 项下规定, 双酯型乌头碱未过0.04%。 地龙舒腰胶囊中未测到双酯型生物碱的原因可能是饮片中含有量过低,在制剂过程中双酯型生物碱水解为单酯型生物碱。
2010 年版 《中国药典》一部 “制川乌” 药材项下测定乌头碱的流动相, 采用四氢呋喃-乙腈-醋酸铵-冰醋酸系统, 即 0.1 mol/L醋酸铵为流动相 A(每 1 000 mL加 0.5 mL冰醋酸)、 乙腈-四氢呋喃(25 ∶15) 为流动相 B,检测波长为 235 nm,体积流量为 0.8 mL/min, 得到良好分离, 但是分离时间长,峰形不佳,理论塔板数低。考虑降低缓冲盐的浓度, 比较分别以 0.05 mol/L和 0.03 mol/L的醋酸铵为流动相,冰醋酸比例不变,前者按梯度洗脱的方法,结果出现前沿峰,仍然未得到良好的分离; 以 A-B (74 ∶26) 的比例洗脱, 虽分离良好,但峰形不佳, 对称性差。 改用 0.03 mol/L的醋酸铵时,峰形在前沿处过宽。
综合以上情况,对药典方法进行改良。查相关文献,乌头类生物碱的流动相多为添加了三乙胺[10]或醋酸铵缓冲盐[11]的体系, 胺类物质作为扫尾剂, 能有效改善生物碱类物质在 C18色谱柱中的峰形。同时,在流动相中加入少量酸,可使分离达到目的, 并使流动相的pH值在色谱柱的适合范围内。 本实验曾采用 0.2%冰醋酸-三乙胺[12]( 用三乙胺调 pH至 6.25)为流动相 A, 乙腈为流动相B, A-B (74 ∶26), 分离度良好, 峰形佳, 但是会出现柱压陡然增大,并且超过上限的现象,对仪器和系统伤害较大; 降低冰醋酸量为 0.1%,则基线不平。 以 0.04 mol/L三乙胺[13]( 用磷酸调 pH至3) 为流动相 A, 乙腈为 B, 检测波长为 235 nm,体积流量为 0.8 m L/min, A-B (71 ∶29) , 结果第1组峰 (即新乌头碱) 峰形过宽, 后两组峰 (乌头碱、次乌头碱)分离效果差,复方中其他成分对测定有干扰。 结合上述方法, 采用以 0.26%醋酸铵[14](氨水调 pH至 9.8) 为流动相 A, 乙腈为流动相 B,A-B (55 ∶45), 检测波长为 235 nm,柱温为 30 ℃,体积流量为 0.8 mL/min, 分析时间控制在 30 min 之内, 且分离度良好, 柱压稳定。实验中发现,流动相的碱性程度对出峰的时间有一定的影响,同时为了减少对柱子寿命的损耗,一般用氨水控制 pH在 10 以下。
乌头类生物碱在二氯甲烷中比较稳定,但在紫外检测时会影响目标成分的响应;在甲醇、乙腈中很不稳定, 但不影响乌头类生物碱的紫外吸收[15]。本实验中分别比较了用乙腈、 二氯甲烷[16]、 0.02 mol/L硫酸 溶 液[9]、 0.05% 盐酸-甲醇[17]作 溶 剂,结果二氯甲烷的峰形不佳, 0.05%盐酸-甲醇后两峰出峰时间晚于其他类别,考虑时间及环保因素,故选用 0.02 mol/L硫酸溶液作最终溶剂。
相关文献[18]比较了水提三氯甲烷萃取法、 酸提法、酸提乙醚萃取法、酸提三氯甲烷萃取法、氨水乙醚冷浸法、氨水乙醚超声法、酸超声提三氯甲烷萃取法7种方法。其中水提三氯甲烷萃取法效率最低,因为乌头类生物碱在水中的溶解度较低,不能全部被溶出;氨水乙醚冷浸法的提取率最高,这是由于乌头碱在乙醚中的溶解度高。酸提乙醚萃取法和酸提三氯甲烷萃取法由于在萃取过程中,可能乌头类生物碱被分配在水层一部分,导致提取不完全。 采用氨水乙醚提取法制备本胶囊样品, HPLC检测出杂质峰干扰过多,故在此基础上进行改善。
本实验采用高效液相色谱法同时测定地龙舒腰胶囊中乌头碱、次乌头碱和新乌头碱的量,方法专属性强、结果准确,能够对地龙舒腰胶囊提供有效的质量评价和质量控制,也为中药复方制剂中双酯型生物碱的质量标准研究提供了实验依据。
[1] 李麟平,吴云定,张伯禹,等.地龙舒腰汤为主治疗腰椎间盘突出症 236 例[ J].上海中医药杂志, 1997 (9):26-27.
[2] 杨 骏,李 婷,张 彤,等.地龙舒腰胶囊的质量标准研究[J].中国医药工业杂志, 2012, 43(6): 471-474.
[3] 李梦然 ,曲 玮,梁敬钰.乌头属化学成分和药理作用研究进展 [J].海峡药学, 2010, 22(4): 1-6.
[4] 郭廷东,唐志立,曹 阳,等.薄层色谱法检查姜红活血止痛酊中乌头碱限量[J].中国药业, 2011, 20 (17):29-30.
[ 5 ] 刘少静, 王小库, 朱改改, 等.RP-HPLC同时测定附子地上部分中新乌头碱和次乌头碱的含量[J].安徽医药, 2011,15(9): 1078-1079.
[6] 刘秀秀,晁若冰.反相离子对色谱法测定附子中生物碱成分[ J] .药学学报, 2006, 41(4) : 365-369.
[ 7 ] 朱俊访, 李卓亚, 沈志滨, 等.HPLC法测定不同地区制川乌中新乌头碱、 次乌头碱及乌头碱的含量[J].食品与药品, 2008, 10(9): 44-46.
[8] 张聿梅,鲁 静,蒋 渝,等.川乌和制川乌中单酯及双酯型生物碱成分的含量测定[J].药物分析杂志, 2005, 25(7): 807-812.
[ 9 ] 李丽敏, 王欣美, 王 柯, 等.RP-HPLC测定镇痛活络酊中 3 种乌头类生物碱含量[ J].中成药, 2008, 30 (12):1785-1788.
[10] 叶姣云, 赵 宁, 陈苹苹, 等.RP-HPLC梯度洗脱法测定四逆汤中乌头类生物碱的含量[J].浙江中医药大学学报,2011, 35(2): 289-291.
[11] 赵英永, 崔秀明, 戴 云, 等.高效液相色谱法测定草乌类药用植物活性成分含量[J].中国药学杂志, 2007, 42(11): 815-818.
[12] 黄建明.草乌标准提取物的研究 [D].上海: 复旦大学,2003: 18.
[13] 张洪超, 唐宇伟, 钱佳华.强力天麻杜仲胶囊中乌头类生物碱成分的含量测定[J].中国药业, 2008, 17(22): 33-34.
[14] 乔艳玲.两种常用中草药多成分快速分析方法的研究[D].北京: 中国协和医学院药物研究所, 2009: 36.
[15] 侯亚会, 陈永孝.HPLC测定小金胶囊中乌头碱的含量[J].成都中医药大学学报, 2009, 32(2): 90-91.
[16] 郑杭生, 冯年平.中药饮片制川乌、 制草乌中乌头碱、 次乌头碱的 HPLC测定[ J].药物分析杂志, 2005, 25 (1):34-36.
[17] 王 瑞, 孙毅坤, 王 耘, 等.高效液相色谱法测定附子及其炮制品中三种双酯型生物碱[J].现代生物医学进展,2007, 7(7): 1078-1080.
[18] 随志刚, 陈明玉, 刘志强, 等.草乌中乌头类生物碱提取方法 比 较 研 究 [ J].时 珍 国 医 国 药, 2009, 20 (3):513-514.
Toxical aconitum alkaloids in Dilong Shuyao CaPsules
YANG Jun1,2, ZHANG Tong1, LITing1*, CAIZhen-zhen1, TAO Jian-sheng1
(1.Shanghai University of Traditional Chinese Medicine, Shanghai201203, China; 2.Xiangshan Hospital of Traditional Chinese Medicine, Shanghai 200020, China)
Dilong Shuyao Capsules; mesaconitine; aconitine; hypaconitine
R927.2
: A
: 1001-1528(2014)01-0114-05
10.3969/j.issn.1001-1528.2014.01.028
2013-02-26
上海市卫生局 (2010Y009A); 卢湾区卫生系统学科带头人培养 (LWK0910); 上海市创新团队及重点学科 (J50302)
杨 骏 (1975—), 男, 副主任药师, 研究方向: 中医医院制剂。
*通信作者: 李 婷 (1984—) , 女, 实验师, 硕士, 研究方向: 中药制药与中药质量标准。 Tel:(021)51322323, E-mail: liting201304 @163.com

