苯与甲醇烷基化反应动力学
徐亚荣,董志新,徐新良,朱学栋
(1.华东理工大学化工学院,上海 200237;2.中国石油乌鲁木齐石化公司研究院,新疆 乌鲁木齐 830019)
近年来,随着下游产品对苯需求量的增长,国内苯产量大幅增加,而重整装置的规模扩大和乙烯产量的增长,使国内纯苯市场供应短缺的局面被打破, 必将导致苯的大量过剩,苯的综合利用将成为苯生产企业优先考虑的问题。甲醇作为一种廉价易得的优良试剂,是煤化工的重要产物之一,随着煤化工的迅猛发展,市场上甲醇必将迅速增多,甲醇在酯化、醚化、甲醇制烯烃等方面已得到广泛的研究及应用,如何将其充分合理利用也将会成为今后一段时期内研究的热点。通过苯与廉价的化工原料甲醇烷基化生产混合芳烃做为高辛烷值汽油调和组份,具有较强的社会和经济效益[1]。随着我国聚酯产能的增加,未来几年内对二甲苯(PX)和对苯二酸(PTA)供应仍将严重不足,因此通过苯增产二甲苯是解决苯有效利用的基本途径之一[2-4]。
本研究考察了固定床中苯与甲醇烷基化反应的影
响因素,并建立了苯与甲醇烷基化反应的动力学方程,以期为苯与甲醇烷基化工艺技术的进一步放大奠定技术基础。

图1 实验装置流程Fig.1 Flow of experiment installment 1-feedstock(methanol); 2-feedstock(benzene);3-mixer; 4-preheater; 5-reactor; 6-condenser
1 实验部分
模试实验的工艺流程装置如图1所示。反应在固定床反应炉中进行,自制催化剂装填量为30~50 mL,反应压力0.1~0.5 MPa,反应温度460~520 ℃。苯和甲醇的进料采用精密计量泵计量和控制。
采用GC-MS和GC联用分析产物。BetaDe120气相色谱柱 (60 m×0.25 mm),载气He流速为1.5 mL/min,检测室与汽化室温度均为300 ℃,起始柱温145 ℃ ,以1 ℃/min升温至190 ℃,并保持15 min。
苯甲醇烷基化反应中以苯的转化率(Xb)、甲苯的选择性(St)、二甲苯的选择性(Sx)以及甲苯和二甲苯的收率(Ytx)作为评价催化剂反应性能的指标,其计算公式分别为:

其中A为原料中苯的物质的量;C为产品中苯系物的物质的量;D为产品中甲苯的物质的量;E为产品中二甲苯的物质的量。
2 结果与讨论
2.1 反应温度对苯甲醇烷基化反应的影响
在甲醇与苯等物质的量进料,空速(WHSV)为8 h-1的条件下实验研究了反应温度对苯甲醇烷基化反应的影响,结果见图2。由图2所示,随着反应温度的增加,甲苯、二甲苯的选择性及其收率不断增加,其中在500 ℃时收率达到最高,此温度下苯的转化率也是最高的,高于500 ℃时,温度的升高对甲苯、二甲苯选择性的提高仍然有利,但影响不是很大。温度升高,工业化成本增加,且高温下催化剂稳定性下降,容易结焦生炭,降低催化剂寿命,经综合考虑,得出离子交换改性后的催化剂的较佳反应温度为500 ℃,此时苯的转化率达到了53.60%,甲苯、二甲苯的选择性为90.29%,甲苯、二甲苯的收率为48.39%。
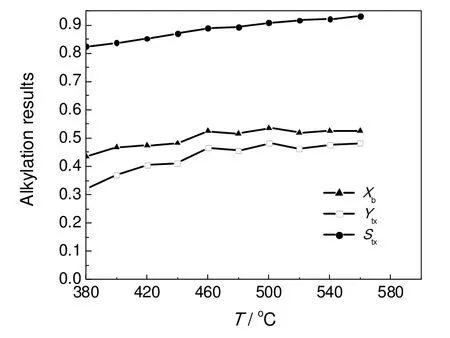
图2 反应温度对苯甲醇烷基化反应的影响Fig.2 Effect of temperature on alkylation of benzene and methanol

图3 空速对苯甲醇烷基化反应的影响Fig.3 Effect of space velocity on alkylation of benzene and methanol
2.2 不同空速对苯甲醇烷基化反应的影响
在反应温度500 ℃,甲醇与苯等物质的量进料条件下,不同空速对选择性和收率的影响如图3所示。由图3可知,随着反应空速的不断增加,甲苯、二甲苯的选择性基本不发生变化,说明苯甲醇烷基化反应为快速反应,可以很快达到反应平衡,其收率于空速为8 h-1时稍高是由于此点苯的转化率高,其余点收率也基本不发生变化,可见反应空速的不同对甲苯、二甲苯的选择性和收率均影响不大,考虑到催化剂的稳定性以及苯的转化率,反应空速选择为3~8 h-1。
2.3 苯和甲醇原料配比对烷基化反应的影响
在温度为500 ℃,压力为0.18 MPa,空速为8 h-1,N2流量为50 mL/min的反应条件下,苯和甲醇原料配比对烷基化结果的影响所图4所示。由图4可知,随着原料中甲醇与苯物质的量之比不断增加,苯的转化率也在不断升高,且基本成直线增加,说明甲醇量的不断增加,可以使原料苯反应得更为充分,从而提高苯的转化率,但甲醇量过大,则会造成甲苯、二甲苯的深度烷基化。在甲醇与苯物质的量比为0.25时,甲苯、二甲苯的总选择性达到了98.15%,但绝大多数均为甲苯,二甲苯含量仅为14.35%,此时没有C10存在,C9的量也仅仅为1.1%,然而在此配比下,苯的转化率极低,仅为17.30%,应用于工业生产时,需要循环回流的苯比较多,大大增加了设备的投资和能量的消耗,不利于工业化。当甲醇与苯物质的量比为1.2时,甲醇过量,苯不足,此时苯的转化率达到了56.67%,然而此时甲苯、二甲苯的转化率却下降到了87.57%,C9、C10的总量也达到了9.68%,选择性的降低,大大增加了分离设备的投资,也不利于工业化生产,考虑到工业化生产的影响,可认为甲醇与苯等物质的量为较佳配比,此时苯的转化率为46.72%,甲苯、二甲苯的选择性达到了90.79%。

图4 原料中苯和甲醇不同配比时的烷基化反应结果Fig.4 Alkylation results for different molar ratio of benzene and methanol in feedstock
2.4 苯甲醇烷基化反应动力学的研究
为了消除副反应和深度烷基化对苯甲醇烷基化反应动力学研究的影响,以及同时消除外扩散的影响,首先进行了实验条件的探索。
2.4.1 不同空速下的烷基化反应
实验设计在低温、高空速的条件下进行。反应温度为355~395 ℃,空速为25~125 h-1,N2流量为50 mL/min,甲醇与苯等物质的量进料。反应得到的产物中只有甲苯生成,苯的转化率随空速的变化趋势如图5所示。结果表明,苯的转化率随空速的增大而不断增加,苯的转化率也控制在了0~6%内,这样可以简化动力学方面的计算与分析。

图5 不同空速下苯的转化率Fig.5 Benzene conversion under different space velocities
2.4.2 反应物分压对烷基化反应的影响
保持通过反应器总气体流量以及其他变量不变的情况下,改变反应物的分压然后测定烷基化反应速率,反应温度为350 ℃时的结果如图6所示。可以看出,烷基化反应速率基本不随甲醇的分压而变化,但随苯分压的增加而线性加快。据文献报道[5],苯和甲醇烷基化反应的反应级数对苯是一级,对甲醇接近零级,与本实验结果一致。即:

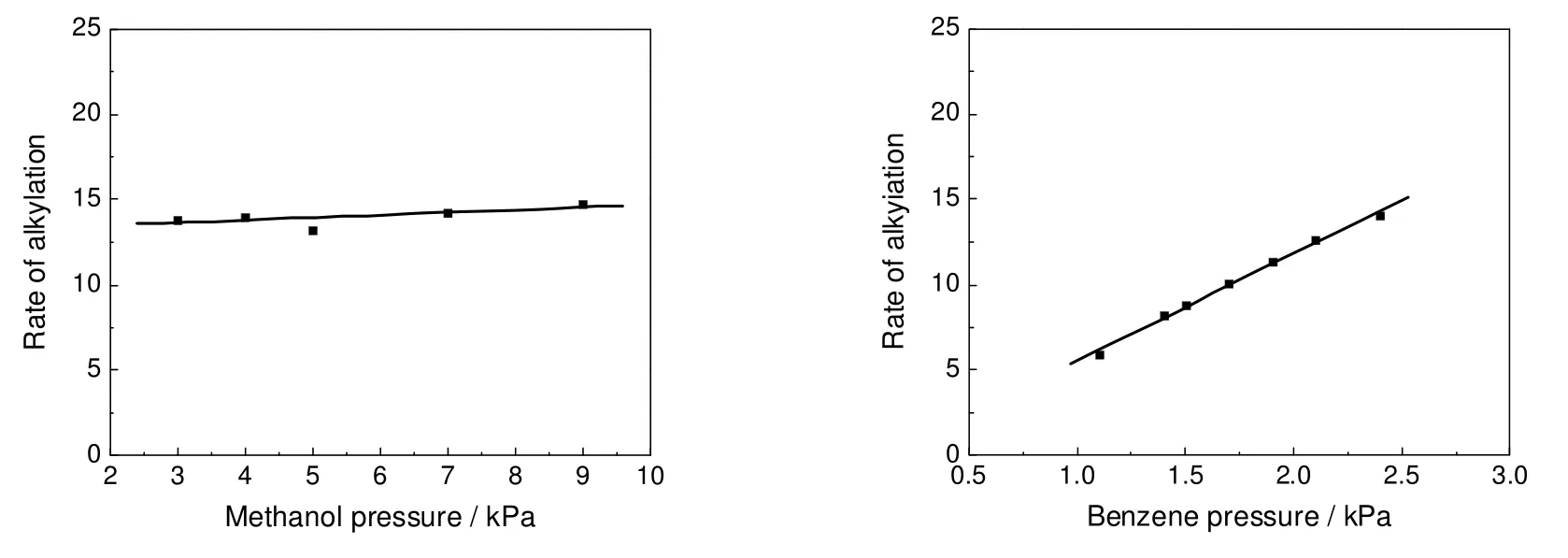
图6 分压对苯甲醇烷基化反应的影响Fig.6 Effect on alkylation for benzene and methanol to differential pressure
2.4.3 不同温度的烷基化反应
在空速为100 h-1,温度为355~395 ℃,其他参数不变的情况下,测定了不同反应温度下的烷基化反应速率。由于反应温度较低,且均在高空速下进行,使得烷基化的产物比较单一,只有甲苯生成,可以采用式(1)的动力学方程来描述。反应速率常数k与温度的关系符合Arrhenius方程,代入式(1)后并两边取对数得反应速率与温度的关系:
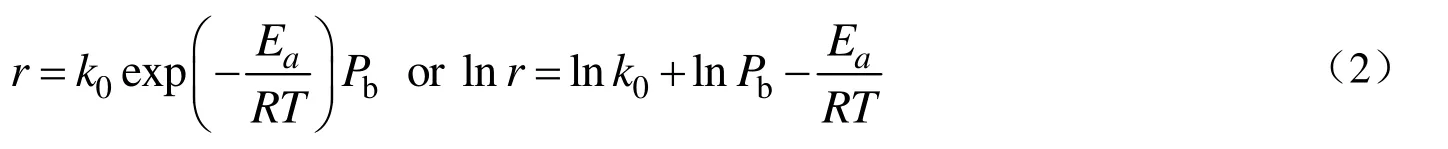

图7 烷基化反应速率与反应温度的关系Fig.7 Relation of rate of alkylation with temperature
将lnr与T-1作图可得图7所示的结果,可以看到两者的线性度较好,说明苯和甲醇的烷基化反应确实对苯为一级,对甲醇接近零级。由图7的斜率计算得出表观活化能为163.88 kJ/mol。在实验范围内,苯的分压变化也很小,可认为是一恒值(43.31大气压),由图7的截距和苯的分压值可得指前因子为7.1×106。所以单纯的苯和甲醇烷基化反应动力学方程为:

3 结 论
a)实验研究了反应温度和反应空速对苯甲醇烷基化反应的影响,当空速为8 h-1,甲醇与苯等物质的量时,随着反应温度的不断升高,苯的转化率也不断的增加,当温度升到500 ℃时,苯的转化率达到最大值;苯甲醇烷基化反应为快速反应,反应空速的增加对甲苯、二甲苯的选择性和收率均影响不大。
b)随着甲醇与苯物质的量比的不断增加,苯的转化率也在不断升高,甲醇与苯等物质的量时,苯的转化率为46.72%,甲苯、二甲苯的选择性达到了90.79%,符合工业化生产对目标产品的选择性。
c)苯与甲醇烷基化催化剂的本征动力学研究表明,苯的甲醇烷基化反应是连串反应,先生成甲苯再进一步烷基化生成二甲苯。苯甲醇烷基化反应的活化能较高(163.88 kJ/mol),需要较高的温度才能使反应进行。
[1] 曹劲松, 张军民. 甲苯甲醇烷基化制PX技术的开发优势 [J]. 石油化工技术与经济, 2010, 26(1):8-10.Cao Jinsong, Zhang Junmin. Technology advantage of para-xylene from alkylene with toluene and methanol [J]. Petrochemical technology and Economics, 2010, 26(1):8-10.
[2] 丁春华. 甲苯/甲醇选择烷基化催化剂的研制和催化性能的研究 [D]. 大连: 大连理工大学, 2007.
[3] 陈庆龄, 孔德金, 杨卫胜. 对二甲苯增产技术发展趋向 [J]. 石油化工, 2004, 33(10):909-914.Chen Qingling, Kong Dejin, Yang Weisheng. Tendency of technology development about para-xylene [J]. Petrochemical, 2004,33(10):909-914.
[4] David A S. A flexible approach for upgrading heavy aromatics [C]. San Antonio: National Petrochemical&Refiners Association NPRA Annual Meeting, 2000:23-27.
[5] Van Der Mynsbrugge J, Visur M, Olsbye U, et al. Methylation of benzene by methanol: single-site kinetics over H-ZSM-5 and H-beta zeolite catalysts [J]. Journal of Catalyst, 2012, 292:201-212.

