喜炎平注射液的安全性试验
杨海民
(河南省濮阳市食品药品检验所,河南 濮阳 457000)
喜炎平注射液的安全性试验
杨海民
(河南省濮阳市食品药品检验所,河南 濮阳 457000)
目的 评价喜炎平注射液的安全性。方法 采用静脉血管刺激试验、肌肉刺激试验、过敏试验观察喜炎平注射液的安全性。结果 喜炎平注射液对豚鼠未见明显过敏反应,肌肉刺激试验中亦未见病理性变化,静脉血管刺激试验中,未发现血管刺激反应。结论 喜炎平注射液在该条件下是安全的。
喜炎平注射液;静脉血管刺激试验;肌肉刺激试验;过敏试验
喜炎平注射液是从中药穿心莲全叶中提取的穿心莲内酯磺化物,为临床常用水溶性纯中药制剂,清热解毒,止咳止痢,具有广谱抗病毒和抗菌作用。临床上广泛应用于上呼吸道炎症、支气管炎、肺炎、脑炎及细菌性肠炎等,为了保证临床用药安全,本文对喜炎平注射液进行了有关药理学实验,报道如下。
1 材 料
1.1 药品与试剂:喜炎平注射液(规格:2 mL∶50 mg,江西青峰制药有限公司,批号:20120620);5%卵蛋白液(将新鲜鸡蛋取蛋清后用生理盐水按1∶20配制);0.9%氯化钠注射液(规格:100 mL∶0.9 g,石家庄四药有限公司,批号:120614168)。
1.2 实验动物:豚鼠,体质量300~400 g;兔,体质量2.0~3.0 kg,均购自河南康达实验动物有限公司。
1.3 实验条件:实验室通风、光照良好,温度为22~28 ℃,相对湿度为50%~70%。各种实验设施均达要求。
1.4 人与实验动物剂量换算:喜炎平注射液静脉滴注,每次300 mg,每天1次,滴速控制在每分30~40滴。公式(2)中d为欲求算的动物每千克体质量剂量,R为动物的体形系数[1]。
按公式1计算临床人用剂量(人以60 kg计):

2 方 法
2.1 静脉血管刺激试验[2]:取健康兔4只,雌雄各半。每只以无菌操作方法,左耳静脉滴注喜炎平注射液12.19 mg/kg体质量;右耳静脉滴注等容积0.9%氯化钠注射液,滴注时间要控制在40 min之内,连续3 d,每天给药一次。末次注射后5 h,由耳缘静脉注入空气处死2只,肉眼观察部位血管的局部反应,并取耳缘静脉血管组织做病理切片检查。其余2只兔继续给药至6 d后作上述处理。
病理检查:以注射针眼为中心向心、远心端各0.5 cm,为一段(B),然后依次向心端切(A)段、远心端(C)段,每段均为1 cm,经10%中性甲醛液固定,常规石蜡制片,每段切片3张,切片时血管横切,厚度约5 µm,苏木精-伊红染色,光学显微镜下观察。
2.2 肌肉刺激试验[2]:取兔2只,雌雄各半,剪去两侧后肢股四头肌部位的兔毛,以无菌操作方法分别于左侧股四头肌部位注射喜炎平注射液1 mL,右侧也注射1 mL 0.9%氯化钠注射液,48 h之后纵向切开皮肤,直接观察注射部位是否有水肿、充血、变性或坏死,并做病理切片检查。
2.3 过敏试验[3]:取健康豚鼠24只,分成药物组、生理盐水组和卵蛋白组3组,每组8只,雌雄各半。各组豚鼠按无菌操作隔日分别腹腔注射喜炎平注射液、0.9%氯化钠注射液和5%卵蛋白各0.5 mL,共3次。然后各组再分为两组,每组4只,雌雄各半,与首次注射后的14 d和21 d,由上肢外侧,再分别注射以上各药1.0 mL进行攻击,继续观察症状。
3 结 果
3.1 静脉血管刺激试验:试验中兔静脉连续静滴3 d后,兔耳静脉血管都无异常情况发生;镜检也均未见炎性反应或有血栓形成。连续静滴6 d后,镜检:A段、C段均无异常,而B段有炎性浸润,血管周围出现轻度水肿。病理结果见表1。
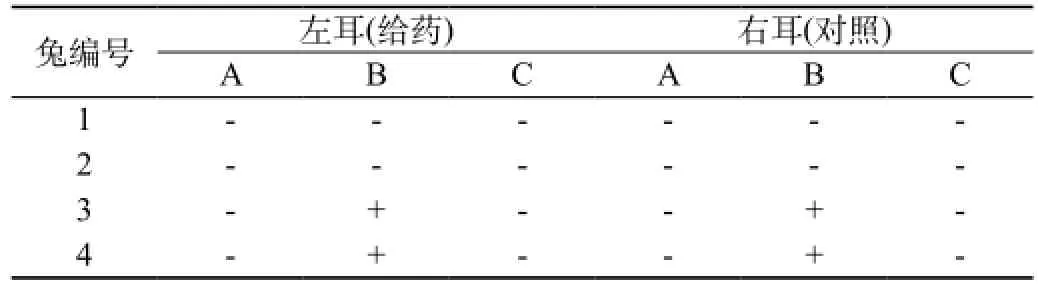
表1 血管刺激性试验病理检查结果
3.2 肌肉刺激试验:没有发现肌注局部异常,镜查未见炎症等病变。
3.3 过敏试验:药物组、生理盐水组豚鼠经攻击注射后无不良症状发生;而卵蛋白组出现烦躁不安、呼吸困难、喷嚏、抓鼻、痉挛等症状,并于5 d内陆续死亡。
4 讨 论
本次试验中,喜炎平注射液对豚鼠未见明显过敏反应,肌肉刺激试验中亦未见病理性变化,静脉血管刺激试验中,静脉注射3 d后,血管无刺激性变化,而6 d后注射部位B段有明显的血管刺激作用,而A段、C段均未发现血管刺激反应,有可能与针头的机械刺激有关。本实验说明了喜炎平注射液应用于临床是安全的。
[1] 徐淑云,卞如廉,陈修.药理实验方法学[M].3版.北京:人民卫生出版社,2002:203.
[2] 卫生部药品审评中心编.新药审批办法及有关法规汇编(二)[M].北京:卫生部药品审评中心,1993:86-87.
[3] 陈奇.中药药理研究方法学[M].2版.北京:人民卫生出版社,2006:157.
R282.710.2
:B
1671-8194(2014)33-0068-01

