测定空气中氧气含量实验的创新设计
◆王冰
作者:王冰,阜阳市第九中学,研究方向为中学化学教育教学(236400)。
1 问题的提出
实验是学习、体验和探究化学过程的重要途径。化学教材中安排的每一个化学实验,都是为化学教学服务的,实验的成败决定着化学教学整体的成败。初中化学教学的第一任务就是培养学生对化学的兴趣,只要学生在学习初期对化学有兴趣,学生学习化学的信心就会非常足。
测定空气中氧气含量实验是九年级化学中接触到的第一个定量分析实验,该实验对于学生认识空气的成分,了解空气中氧气的含量,有着重要的指导意义;对于激 发学生学习化学的兴趣,让学生主动地获取科学知识,学习科学探究的方法,有着非常重要的启蒙意义。
最早对空气成分中氧气含量的定量测定是由法国化学家拉瓦锡提出的:如图1所示,给密闭容器中少量的汞(即水银)连续加热12天之久,发现有一部分银白色的液态汞变成红色的粉末,同时容器里空气的体积差不多减少了五分之一;他将红色物质取出后加强热,发现红色物质分解成液态的汞和氧气,将氧气放入原密闭容器中,发现容器中的气体成分和空气的成分一样。于是,拉瓦锡得出空气中氧气的体积约占空气体积的1/5。这个实验显然在课堂上无法完成。为了给学生以直观的感受,加强学生对空气中氧气含量的认识,教材中设计了一个简易实验,以测定空气中氧气的含量。

在早期如二十世纪七八十年代的人民教育出版社出版的九年义务教育三年制初级中学教科书《化学》(全一册)课本上第7页有如图2所示的装置,其方法是将钟罩放入盛水的水槽中,以水面为基准线,将钟罩水面以上容积分为5等分,通过红磷燃烧消耗氧气,然后观察进入水的体积来测定(如图2所示)。

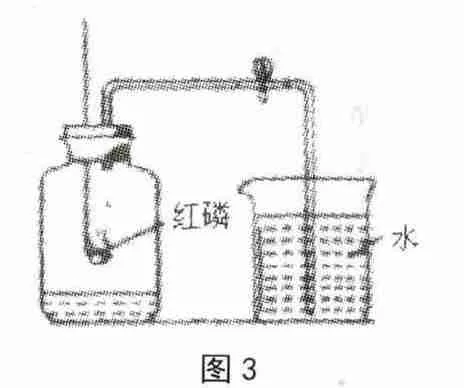
现在人民教育出版社出版的九年义务教育课程标准实验教科书《化学》上册第27页有图3所示实验装置,其方法是在集气瓶内加入少量水,将集气瓶水面以上容积划分为5等分,通过红磷燃烧消耗氧气,然后观察进入水的体积来测定(如图3所示)。
其实对于空气认识,人们是从身边生活的燃烧开始的。在小学自然科学常识教材中也有类似的实验,利用蜡烛的燃烧实验,了解认识空气中氧气的存在,主要目的是给学生一个定性的认识。
尽管九年制义务教育教材版本反复修订过多次,但空气成分中氧气含量的测定实验在九年级化学教材中并没有被删去,且实验的目的很明确:利用红磷的燃烧,消耗掉密闭容器内的氧气,从而使密闭容器内气体压强降低;利用大气压强原理,观察水的进入量,从而较准确地测定出空气中氧气的含量,给学生一个定量的认识。
多年的教学生涯中,笔者分别用图2和图3装置重复做过多次实验,但都很难达到理想的效果,相信很多同行在做该实验时都会有同感。因为实验时要在瓶外的酒精灯上加热引燃红磷,再伸入密闭容器内,并塞紧橡胶塞;燃着的红磷伸入容器的瞬间,容器内的空气受热会发生膨胀,部分空气被排出,特别是氮气的逸出,导致实验结果不够准确。其次,在酒精灯上点燃红磷时生成的五氧化二磷颗粒会以白烟的形式扩散到空气中,造成空气的污染。
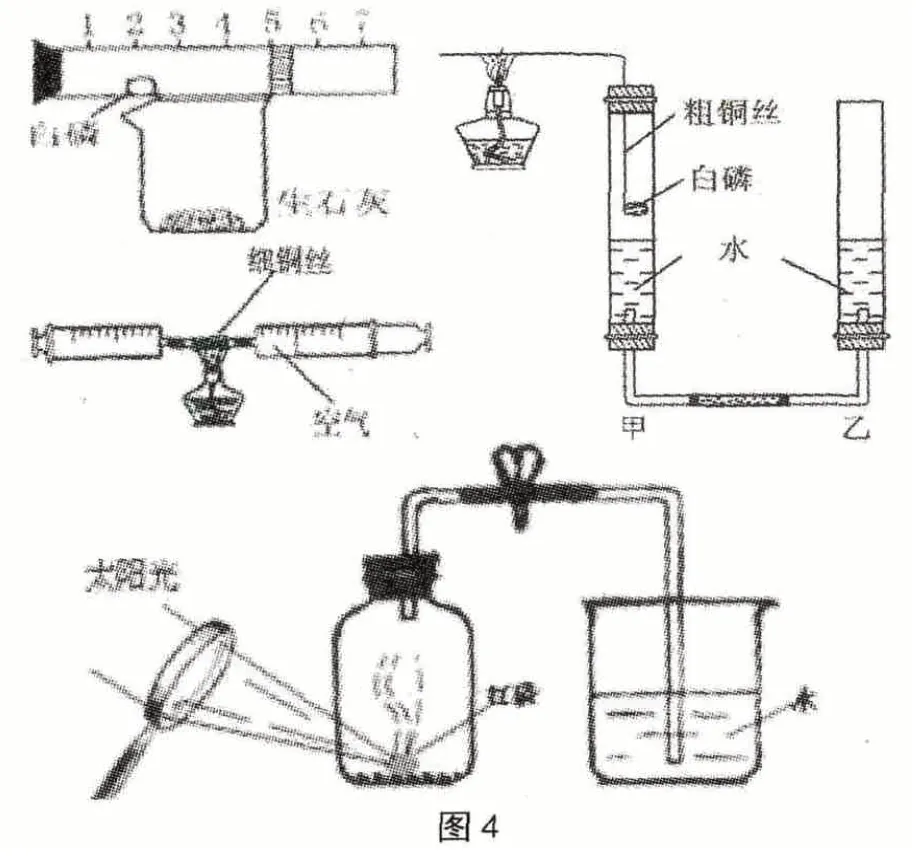
一些资料、杂志也介绍过一些测定空气中氧气含量的实验,装置大致见图4。从设计上说,这些思路都很有创意,但实际操作中却有很多困惑。有些实验的操作过于理论化,只能是纸上谈兵;有的实验甚至根本无法达到预期的效果或无法完成实验(如:有些实验设计用玻璃管内燃烧白磷观察活塞的移动,这种方式使用的白磷有剧毒,玻璃管也极易炸裂,存在安全隐患;有些实验设计利用加热的铜片或铜丝、铁丝的锈蚀消耗氧气,这种方式时间上具有不确定性,理论上也很难把氧气消耗完;有些实验设计用放大镜聚光来点燃红磷,这种方式要选择天气状况和教室的位置,同时也很难引燃红磷)。
空气中氧气含量的测定是初中化学中一个非常重要的探究实验,也是各种测试中的考查热点。为帮助学生更好地掌握相关知识,培养学生科学求实、一丝不苟的严谨学习态度,为此,特提出改进方案。
2 实验改进方案
实验仪器及药品 集气瓶(1个)、与集气瓶配套的橡胶塞(1个)、烧杯(1支)、燃烧匙(1个)、长约6厘米直径约1毫米粗铜丝2根、弹黄夹1个、乳胶管、导气管、红磷、水、导线3根、长约0.5厘米的废电炉丝一截、学生电源1个、电键开关1个(也可省去,因为学生电源中已含开关)、打孔机。
实验改进原理 在教材实验的基础上,开启学生电源,利用电流的热效应使电炉丝发热,引燃红磷,消耗掉密闭的集气瓶内的氧气,从而使甁内压强降低。
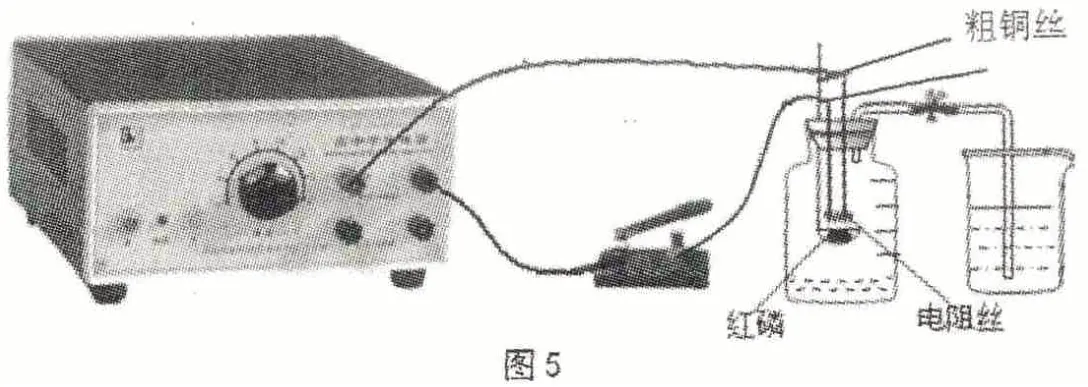
仪器的组装说明 按图5所示,先根据需要用打孔机给橡胶塞分别打4个小孔,安装好燃烧匙、铜丝、导气管;在2根铜丝的下端(伸入集气瓶部分剥去塑料皮)连接一段废电炉丝,调整与燃烧匙的距离,间隔大约0.2厘米;再把橡胶塞与集气瓶相连,并连接好导气管;最后在2根铜丝的上端再分别用导线与电源、开关相连。
实验仪器装置如图5所示。
实验操作及现象
步骤一:按图5,安装好仪器装置,并检查反应装置的气密性。
步骤二:如图5所示,在烧杯中放入足量水,燃烧匙内放入足量红磷,放入密闭的集气瓶中,在集气瓶中预先留置少量水,塞紧橡胶塞,用弹簧夹夹紧乳胶管。
步骤三:连接电源,闭合电键开关;引燃红磷后,断开电源开关,继续观察现象。
步骤四:待红磷熄灭后,冷却装置至室温,打开弹簧夹,观察现象。
结果表明,烧杯中的水立即进入集气瓶中,约为集气瓶剩余容积的五分之一(事先做好标记,以便观察),实验效果明显,效果良好。
3 实验的创新点及装置改进的意义
1)理化结合,利用物理知识来解决化学问题,加强学科间的联系。
2)操作简单易行。实验准备好后,只需开启、断开电源开关(或闭合电键开关),最后打开弹簧夹,观察现象即可,避免了以往按教材上的方法操作手忙脚乱的尴尬。
3)实验现象清晰明显,可视性强。
4)防止了环境污染。教材上的实验,在瓶外加热引烧红磷时有五氧化二磷白烟生成,逸散到空气中,会污染环境。
5)减少了实验误差,装置始终处于密封状态,实验数据准确。而教材上的实验,燃着的红磷伸入容器的瞬间,难免有少量空气特别是氮气逸出,增加了实验效果的不确定性。因为氮气的含量大于氧气,实验的结果可能会造成最后的进水量大于五分之一。
[1]九年义务教育三年制初级中学教科书:化学(全一册)[M].北京:人民教育出版社,1989:7.
[2]化学(上册)[M].北京:人民教育出版社,2006:27.

