碘催化合成对-正丁基苯胺的正交实验研究
马 琳
(1.宝鸡文理学院化学化工学院,陕西宝鸡721013;2.陕西省植物化学重点实验室,陕西宝鸡721013)
对-正丁基苯胺是重要的有机合成中间体之一,市场需求量较大。目前,工业化生产对-正丁基苯胺主要以苯胺和正丁醇为原料,采用ZnCl2作催化剂[1],存在腐蚀强、成本高的缺点。有研究报道,碘作为催化剂可用于多种有机反应[2-4]。作者以碘单质作催化剂合成对-正丁基苯胺[5],采用正交实验优化了合成工艺条件,并为解决单质碘升华附着设备问题,尝试以I2/Al2O3作催化剂合成对-正丁基苯胺。
1 实验
1.1 试剂与仪器
正丁醇、苯胺、Al2O3均为分析纯,碘(纯度≥99.8%)。
FYX0.2型高压釜(300mL),大连通产高压釜容器制造有限公司;GC900A型气相色谱仪,上海科创色谱仪器有限公司;GC6890型气相色谱仪、MS5973型质谱仪,美国安捷伦公司。
1.2 方法
1.2.1 单质碘作催化剂
将混合原料(正丁醇与苯胺物质的量比为0.8∶1,由工业生产条件确定[1])加入高压反应釜中,再加入催化剂碘。用氮气置换釜内空气3次,每次置换15 min。将反应釜温度升至180℃,恒温反应4h,然后将温度升至设定反应温度,恒温反应一定时间。反应结束后待气压表读数归零,从取液口取样,反应产物为淡棕红色。
首先进行单因素实验初步考察影响对-正丁基苯胺收率的主要因素,然后根据单因素实验结果[5],选择反应温度、反应时间、碘量和搅拌速度作为考察因素,以对-正丁基苯胺收率为考核指标,进行4因素3水平正交实验以优化合成条件[6],正交实验的因素与水平见表1。
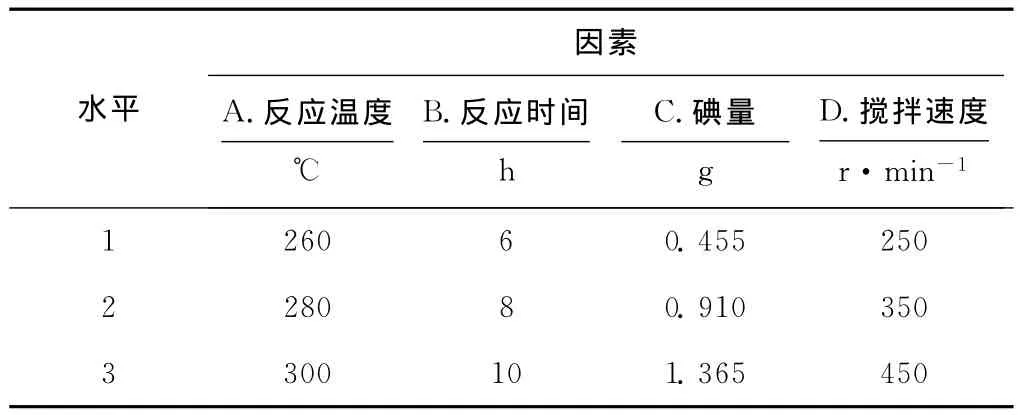
表1 正交实验的因素与水平Tab .1 The factors and levels of the orthogonal experiment
1.2.2 I2/Al2O3作催化剂
1)I2/Al2O3的制备:称取一定量烘干至恒质量的γ-Al2O3加入碘酒中,加热回流6h,冷却至室温后抽滤,用无水乙醇淋洗,重复3次,再用蒸馏水洗至中性,60℃干燥12h[7]后迅速放入干燥器中,自然冷却,即制得I2/Al2O3催化剂,称量,按下式计算碘负载量[8]:
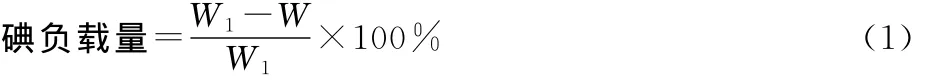
式中:W、W1分别为负载前、后活性炭的质量,g。
2)以I2/Al2O3代替单质碘作催化剂合成对-正丁基苯胺,反应条件选择正交实验确定的最优条件。
1.3 分析检测
首先对反应产物进行GC-MS分析确定产品峰位置,然后用气相色谱仪分析各峰产物,色谱定量采用峰面积归一法,按式(2)~(4)计算对-正丁基苯胺的收率[9]:

式中:npt为时间为t时目标产物的量;∑npt为时间为t时总产物的量;At为时间为t时反应物的GC峰面积;A0为初始反应物的GC峰面积。
2 结果与讨论
2.1 单质碘作催化剂
2.1.1 反应产物的确定
固定正丁醇与苯胺物质的量比为0.8∶1,在单因素实验确定的较优条件[5][反应温度280℃、反应时间8h、碘量0.455g(占苯胺质量的5‰)]下进行实验。用气相-质谱联用仪(GC-MS)检测反应产物,发现确有对-正丁基苯胺生成,并且确定目标产物的峰为峰3(图1a)。进一步测定产物的气相色谱,见图1b。

图1 单质碘作催化剂时,产物的GC-MS(a)和GC(b)图谱Fig.1 GC-MS(a)and GC(b)of the products using I2as catalyst
2.1.2 正交实验结果与分析(表2)
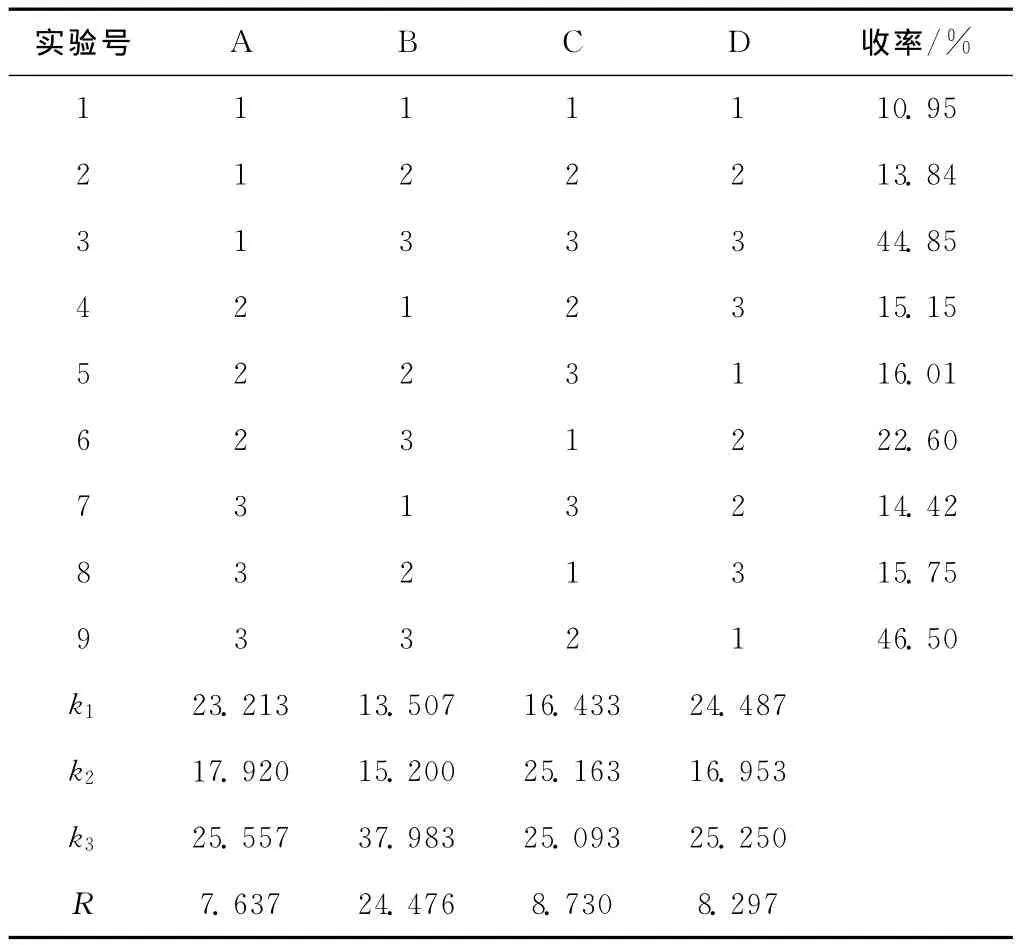
表2 正交实验结果与分析Tab .2 The results and analysis of the orthogonal experiment
由表2可知,各因素对对-正丁基苯胺收率的影响大小依次是:反应时间>碘量>搅拌速度>反应温度,最佳条件是A3B3C2D3,即反应温度300℃、反应时间10h、碘量0.910g、搅拌速度450r·min-1。
在优化条件下进行3次平行实验,对-正丁基苯胺收率分别为48.05%、50.12%、51.36%,平均收率49.84%,高于正交实验的最高收率,表明所确定优化条件可靠。
2.2 I2/Al2O3作催化剂
根据碘作催化剂合成对-正丁基苯胺的正交实验结果,在正丁醇与苯胺物质的量比为0.8∶1、反应温度为300℃、反应时间为10h、催化剂I2/Al2O3用量为4.51g(碘负载量20%)、搅拌速度为450r·min-1的优化条件下合成对-正丁基苯胺。气相色谱分析(图2)表明:以I2/Al2O3作催化剂确有对-正丁基苯胺生成,3次平行实验的结果见表3。
由表3可知,以I2/Al2O3作催化剂时,对-正丁基苯胺的收率达到55.51%。
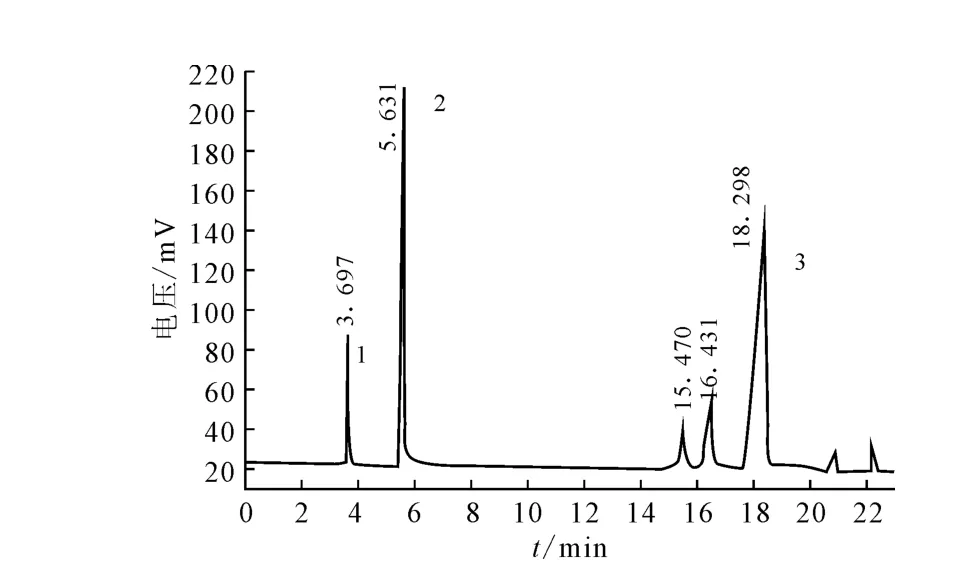
1.正丁醇 2.苯胺 3.对-正丁基苯胺图2 I2/Al2O3作催化剂时,产物的GC图谱Fig.2 GC of the products using I2/Al2O3as catalyst
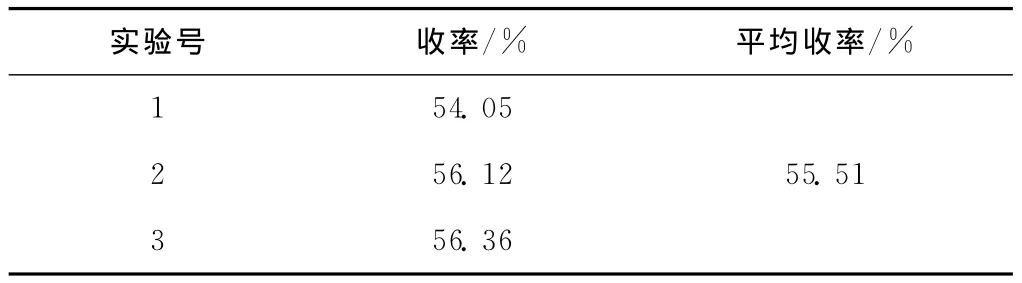
表3 I2/Al2O3作催化剂平行实验结果Tab.3 The parrel experiment results for catalyst I2/Al2O3
2.3 讨论
实验证明,以单质碘或I2/Al2O3作催化剂均可催化正丁醇和苯胺反应生成对-正丁基苯胺,且都不腐蚀反应器。实验结束后,打开高压反应釜观察发现:以单质碘作催化剂时,由于碘受热升华易附着在设备上难以清洗,催化剂不易回收;以I2/Al2O3作催化剂,Al2O3不但起到碘催化剂载体的作用,而且还能吸附回收碘,使碘在反应釜上的附着量大大减少,环境友好,催化剂亦可重复利用。比较单质碘作催化剂和I2/Al2O3作催化剂的合成结果,发现I2/Al2O3催化合成目标产物的收率高于单质碘。后续可进一步优化I2/Al2O3催化合成对-正丁基苯胺的条件,亦可尝试选用固定床反应器以进一步提高对-正丁基苯胺收率。
3 结论
以碘作催化剂、以正丁醇与苯胺为原料在高压反应釜内催化合成对-正丁基苯胺,用GC-MS和气相色谱对产物进行定性和定量分析。通过正交实验确定最佳反应条件如下:反应温度300℃、反应时间10h、碘量0.910g(占苯胺质量的10‰)、搅拌速度450r· min-1,在此条件下,对-正丁基苯胺收率为49.84%,并在以负载型催化剂I2/Al2O3代替单质碘时达到55.51%。
[1] 章思规.精细有机化学品技术手册[M].北京:科学出版社,1991:264-267.
[2] 王宏社,苗建英,赵立芳.碘作为催化剂在有机合成中的应用[J].有机化学,2005,25(6):615-618.
[3] 刘星明,袁先友.碘催化剂在精细有机物合成中的研究进展[J].湖南科技学院学报,2008,29(4):55-58.
[4] 沈舒苏,徐小平,纪顺俊.分子碘催化的有机反应研究进展[J].有机化学,2009,29(5):806-811.
[5] 马琳,张秀成,陈立宇.单质碘催化合成正丁基苯胺[J].重庆工学院学报(自然科学版),2008,22(2):52-54.
[6] 李云雁,胡传荣.试验设计与数据处理[M].北京:化学工业出版社,2008:128-142.
[7] 刘星明,袁先友.微波促进活性炭负载单质碘催化合成乙酰乙酸乙酯缩酮[J].湖南科技学院学报,2008,29(8):47-50.
[8] 田晓燕,胡奇林,田大年,等.活性炭负载单质碘催化合成季戊四醇双缩酮[J].宁夏工程技术,2006,5(2):137-139.
[9] 唐培堃.精细有机合成化学及工艺学[M].第十二版.天津:天津大学出版社,2007:40-41.

