两种交联氨基淀粉对水中Cu2 + 的吸附性能
韦晓燕,谭 军,欧阳玉霞,范举红,刘 锐
(1. 嘉兴学院南湖学院化学与纺织工程系,浙江嘉兴 314001;2. 浙江清华长三角研究院生态环境研究所,浙江嘉兴314006;3. 嘉兴学院生物与化学工程学院,浙江嘉兴 314001)
铜是一种地球上储量较为丰富的元素,广泛应用于现代工业生产,如电镀、化工、染料、纺织、冶炼、制药及食品等行业。这些行业产生的含铜离子废水若未经处理就排放会对动物及人体健康造成危害,我国已将铜及其化合物列入水体优先控制污染物的黑名单[1]。在畜禽养殖业中,代谢物的排放也会产生大量的Cu2+废水。常用的含Cu2+废水的处理方法有化学沉淀法、溶剂萃取法、膜分离法、电解法和离子交换法等,但这些方法或多或少都存在处理成本高、操作复杂、二次污染等问题[2]。吸附法是一种简单易行的处理含Cu2+废水的方法,寻找价廉易得且高效的吸附剂是吸附法的研究重点[3]。
许多天然多糖及其含有多功能基的衍生物,如壳聚糖、改性纤维素以及改性淀粉是近些年出现的一类重要的生物吸附剂。其中淀粉因其价廉、来源广泛,含有大量羟基易于进行化学改性而倍受关注[4]。不 溶 性 淀 粉 黄 原 酸 酯(insoluble starch xanthate,ISX)是研究较多并且应用效果较好的改性淀粉重金属吸附剂,但其不稳定、难于储存运输,因此使用受限[5]。为克服这一缺点,李义久等[6]采用交联、醚化和胺化工艺合成含C—N 的氨基淀粉(CAS),董爱琴等[7]则采用交联、氧化和胺化手段工艺合成含 ==C N 的氨基淀粉(DAS),两种氨基淀粉较ISX 的稳定性好,对Cu2+的吸附能力强,沉降效果更好。两者吸附Cu2+的功能基团同为氨基,但分子结构不同,究竟哪一种吸附效果更好,尚未有人对此研究报道。
为了验证及评价上述两类氨基淀粉对Cu2+的吸附性能,本文首先分别合成了两种氨基淀粉CAS和DAS,然后以CuSO4水溶液模拟含Cu2+废水,通过试验考察投加量、pH、吸附时间及温度对两种氨基淀粉去除Cu2+的影响,并且对两者的等温吸附特性、吸附动力学和吸附热力学进行了系统的对比研究,以期为氨基淀粉处理水中Cu2+的开发应用提供理论基础。
1 试验部分
1.1 试剂和仪器
玉米淀粉由上海福康食品厂提供,高氯酸、高碘酸钠、二乙烯三胺、环氧氯丙烷、乙二胺、丙酮、氢氧化钠、盐酸、硫酸铜,皆为分析纯。
DF-101S 集热式恒温水浴(杭州大卫科教仪器有限公司);JA50003N 电子天平、DELTA320A 型pH计(梅特勒-托利多国际股份有限公司);DZF 型真空干燥箱(上海精宏实验设备有限公司);AA800 型火焰原子吸收光谱仪(美国perkinelmer 公司);Flash EA-1112 型元素分析仪(意大利ThermoFingnigan 公司)。
1.2 交联氨基淀粉的制备
自制CAS(测得氨基含量1.65%),合成步骤及检测方法见参考文献[6];自制DAS(测得氨基含量2.32%),合成步骤及检测方法见参考文献[7]。
1.3 Cu2 +吸附试验
用CuSO4配制Cu2+浓度为30 ~200 mg/L 的溶液,用醋酸溶液或氨水调节溶液pH。将配制好的100 mL 一定浓度的Cu2+溶液分别置于250 mL 锥形瓶中,准确加入一定量的氨基淀粉CAS(或DAS),在一定温度和pH 下置于恒温振荡器中,在200 r/min下振荡一定时间后,静置,过滤。采用原子吸收法测定滤液中Cu2+浓度。用下式计算吸附容量和Cu2+去除率。
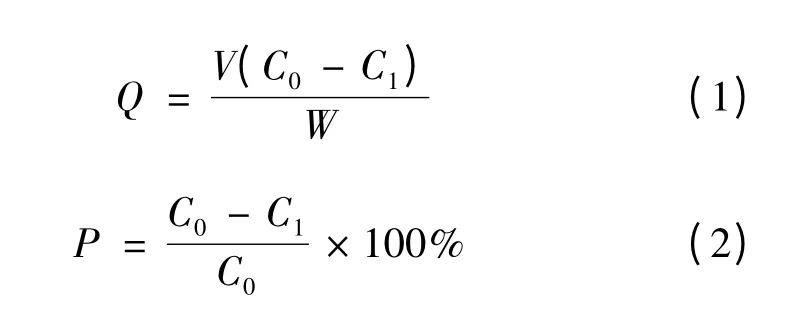
其中Q—吸附容量,mg/g;
V—含Cu2+溶液体积,L;
C0—吸附前溶液中Cu2+离子浓度,mg/L;
Cl—吸附后溶液中Cu2+离子浓度,mg/L;
W—吸附剂干重,g;
P—Cu2+去除率,%。
2 结果与讨论
2.1 吸附剂最佳用量的确定
于室温(25 ℃)下,称取不同质量的CAS 和DAS,分别加入到Cu2+浓度为30 mg/L 的CuSO4溶液中,测定两种氨基淀粉吸附剂投加量和溶液中Cu2+去除率的关系,结果如图1 所示。

图1 氨基淀粉用量对吸附效果的影响Fig.1 Effect of Two Adsorbents Dosage on Adsorption
由图1 可知两种氨基淀粉对Cu2+去除率都随投加量的增加而增大,这是因为随着吸附剂投加量增加,活性吸附位点也相应增加。当用量为0.01 g时,两者的去除率都达到最大,进一步增加投加量对去除率的影响已不明显,因此后续试验中CAS 和DAS 的投加量均为0.01 g;CAS 对Cu2+最大去除率为97. 92%,远高于DAS 对Cu2+最大去除率(70.4%)。从吸附容量看,最佳投加量时CAS 对Cu2+的吸附容量为294.34 mg/g(即4.59 mmol/g),DAS 的吸附容量为211.06 mg/g(即3.30 mmol/g),对应各自的氨基含量(1.01、1.45 mmol/g),两者吸附的铜氨络合比分别为4. 54 ∶1、2. 28 ∶1,说明CAS 的氨基对Cu2+具有更大的吸附量。另外,从分子结构角度分析,CAS 中C—N 键为σ 键,由于氮的电负性较大,其吸电子能力很强,造成氮原子周围电子云密度高,易受Cu2+的攻击;DAS 中 ==C N 的双键为σ-π 键,具有共轭效应,共轭效应可使氮原子上的电子云密度部分移向碳原子,从而降低了氮原子上电子云密度,使其与Cu2+结合的能力减弱[8]。
2.2 pH 的影响
介质的pH 对吸附过程有显著的影响,它不但直接影响溶液中离子的存在形态,还和吸附剂功能团的质子化有密切关系。故本文考察了pH 对两种氨基淀粉吸附性能的影响。于室温(25 ℃)下,投加量为0.01/100 mL,改变溶液pH 进行试验,结果如图2 所示。

图2 溶液pH 值对吸附容量的影响Fig.2 Effect of Solution pH on Adsorption
由图2 可知在pH 为3 ~5 时,CAS 对Cu2+吸附容量随pH 升高而迅速增大。这是因为氨基淀粉在酸性介质中,—NH2基会与H+结合,即质子化,形成—NH+3,失去吸附Cu2+的能力,所以H+浓度越大,介质酸性越强,CAS 越难与Cu2+结合。随pH 升高,质子化作用减弱,当pH 为5 ~7 时,氨基的质子化和吸附络合Cu2+反应达到平衡,CAS 吸附容量达最大。当pH >7.0 时[为避免铜离子与OH-生成Cu(OH)2沉淀,采用氨水调节溶液pH],其吸附容量又急剧下降,这是因为氨水中NH3与二价Cu2+形成可溶性的[Cu(NH3)4]2+的缘故。此时,OH-、NH3分子和吸附剂共同竞争Cu2+,CAS 吸附容量降低[9]。DAS 的吸附性能受pH 影响与前者相似,只是当pH 为4 ~4.5 时,吸附容量达最大。这可能是由于通过 ==C N 键的共轭效应可以降低氨基质子化后氨基上的正电荷密度,从而提高了DAS的抗酸性。
2.3 吸附平衡时间及吸附动力学
2.3.1 吸附时间与吸附性能的关系
一个性能优良的吸附剂不但要有较高的吸附容量,还要有较大的吸附速率。于室温(25 ℃)下,投加量为0.01 g/100 mL,考察吸附容量随时间的变化关系,结果如图3 所示。

图3 吸附时间对吸附效果的影响Fig.3 Effect of Contact Time on Adsorption
由图3 可知在前10 min 吸附反应进行得非常快,吸附容量已达到平衡吸附容量的90%。吸附时间增加,去除率缓慢增大,当吸附时间为90 min时,吸附达到平衡。反应初期的吸附速率大说明吸附剂表面有大量的吸附活性位点,反应中后期吸附速率减小则是由于剩余的活性位点减少、吸附在活性位点上的Cu2+对溶液中的静电排斥作用,以及吸附后液相中Cu2+浓度降低三者共同造成的。
2.3.2 吸附动力学和吸附活化能
分别采用拟一级和拟二级动力学模型[10-12]对吸附时间数据进行拟合,动力学方程如下。
拟一级:

拟二级:
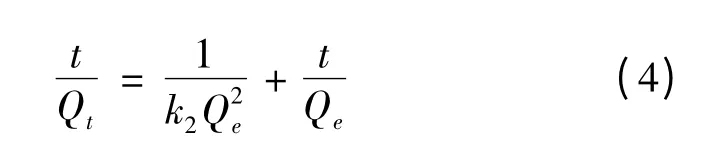
其中Qe、Qt——平衡时的平衡吸附容量和t 时刻的吸附容量;
k1、k2——拟一级和二级吸附速率常数。
拟一级动力学模型适合于传质扩散为控制步骤的吸附过程,拟二级则适用于化学吸附为控制步骤的吸附过程。Ho 等[10-12]成功运用拟二级动力学模拟吸附剂对水溶液中金属离子、染料、药物、有机物质的吸附过程,发现拟二级模型尤其适合描述带极性功能团的吸附剂对二价金属的化学吸附。两种动力学模型的拟合曲线(如图4)及相关性系数(如表1)。
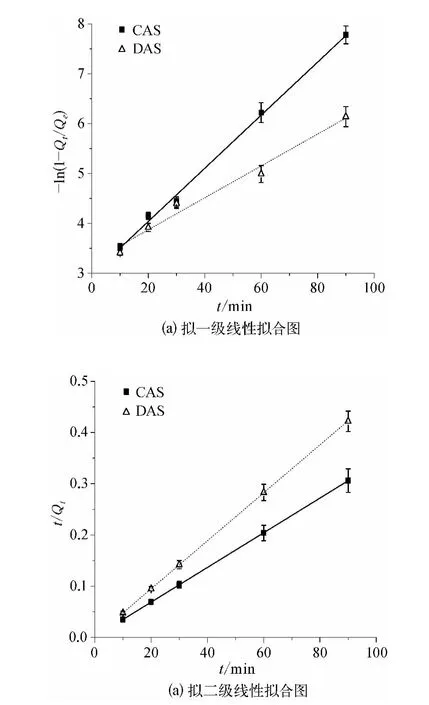
图4 吸附动力学曲线Fig.4 Curves of Cu2+Adsorption
由图4、表1 可知,两种氨基淀粉吸附Cu2+更符合拟二级动力学。根据二级动力学的t/Qt~t 曲线斜率,求出理论平衡吸附量Qe(cal.),理论值与试验测得的平衡吸附量一致,更加证明了两种吸附反应过程都属于拟二级反应。Cu2+在CAS(或DAS)上的吸附主要依靠Cu2+与氨基的化学键作用,属于化学吸附控制[12]。另外由表1 结果可知两种氨基淀粉对金属离子的吸附速率常数k2大小顺序为k2(CAS)>k2(DAS),因此CAS 对Cu2+的吸附速率比DAS 大。
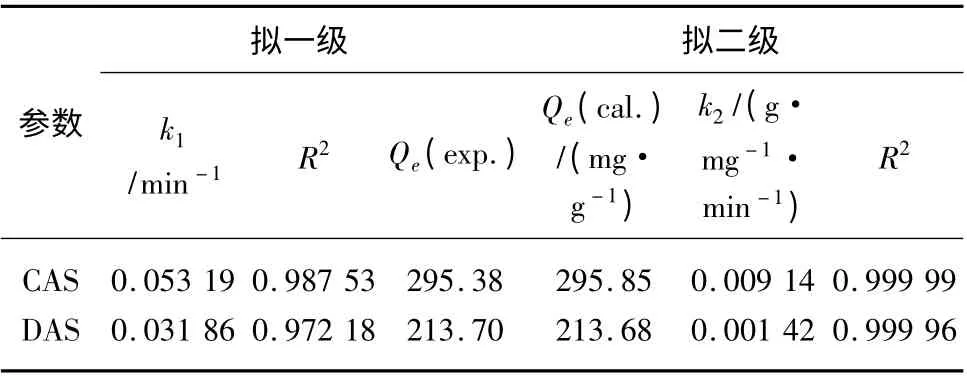
表1 两种氨基淀粉的拟一级及拟二级动力学线性分析Tab. 1 Kinetic Parameters of Pseudo-First-Order and Pseudo-Second-Order for Cu2+Adsorption
再分别测定288、308 K 下的DAS 和CAS 的吸附时间与吸附容量关系曲线(图略),采用拟二级反应动力学拟合得到反应速率常数值,通过Arrhenius方程计算吸附活化能。Arrhenius 方程的直线形式如下所示。

其中k2——拟二级动力学反应速率常数,g/mg·min;
Ea——吸附活化能,kJ/mol;
A——指前因子;
R——通用气体常数,8.314 J/mol·K;
T——开尔文温度。
根据不同温度下的ln k2与1/T 作图(如图5),得直线。由直线斜率(-Ea/R)可计算出两种改性氨基淀粉吸附Cu2+的吸附活化能Ea。

图5 CAS 和DAS 吸附活化能曲线Fig.5 Adsorption Activation Energy of CAS and DAS
由图5 可知DAS 的ln k2与1/T 的直线斜率大于CAS,根据直线斜率计算得出DAS 的吸附活化能Ea为65.06 kJ/mol,CAS 的Ea为29. 28 kJ/mol,即DAS 吸附活化能比CAS 吸附Cu2+活化能大,所以CAS 更容易吸附Cu2+且反应速度更快。
2.4 等温吸附研究
在室温条件下,0.1 g 氨基淀粉处理100 mL 不同浓度的Cu2+溶液(分别为30、60、90、180 mg/L),恒温振荡2 h 后,取样测定不同平衡浓度时两种氨基淀粉的平衡吸附量。分别采用Langmuir[13]和Freundlich[14]吸附等温式对等温吸附数据进行拟合,方程如下。
Langmuir 方程:
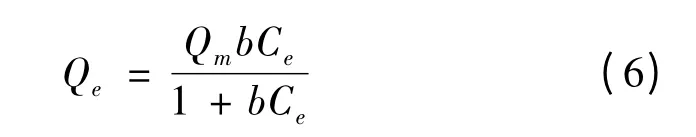
Freundlich 方程:

其中Qm、b——Langmuir 吸附常数,分别代表最大吸附量和吸附能;
Kf、n——Freundlich 吸附常数,分别代表键合力和非均相因子;
Qe——溶液达到平衡浓度Ce时的平衡吸附容量。
拟合的吸附等温线如图5 所示,相关参数如表2 所示。
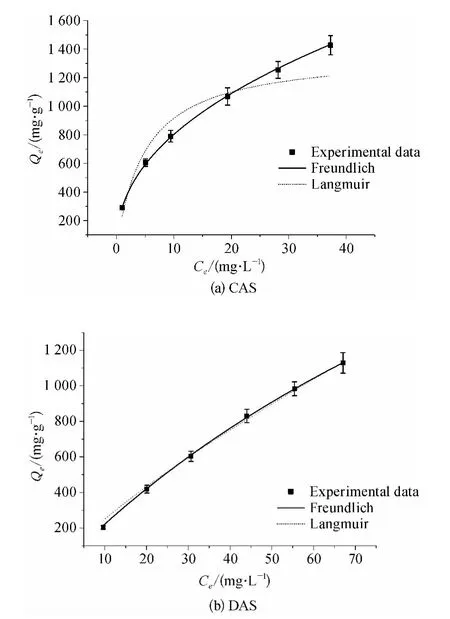
图6 等温吸附拟合曲线Fig.6 Adsorption Isotherm Curve
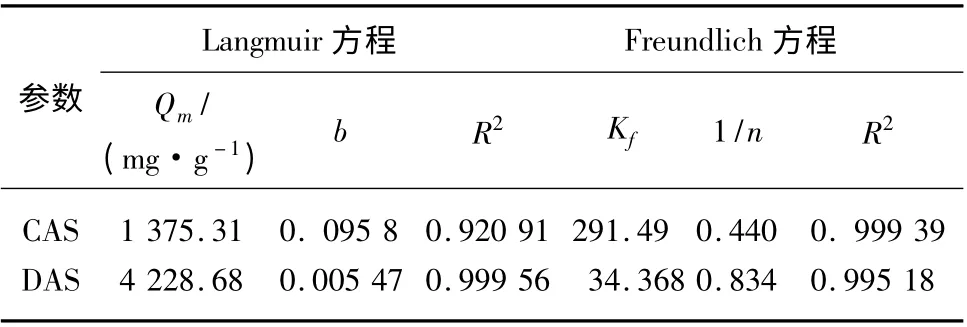
表2 氨基淀粉等温吸附曲线的相关参数Tab.2 Parameters of Adsorption Isotherm for Cu2+ Adsorption by CAS and DAS
由图6、表2 可知对CAS 而言,Langmuir 型拟合的相关系数只有0.920 91,而Freundlich 型的拟合相关系数则在0.99 以上,说明CAS 对Cu2+吸附等温特征更符合Freundlich 型,为非均匀表面吸附,这一结论与文献[6]的研究结果一致。DAS 对Cu2+的吸附数据采用Langmiur 模型拟合的相关系数为0.999 56,比Freundlich 型的0.995 18 更高,说明其对Cu2+的吸附属于均匀表面、单层吸附行为,该结果与文献[7]研究结果吻合。
根据前述2.1 的分析结果,Cu2+浓度为30 mg/L,投加量为0.01 g 时,CAS 和DAS 两者吸附的铜氨络合比分别为4.54 ∶1、2.28 ∶1,两种氨基淀粉中氨基与铜的络合比均大于铜氨络合物配位比0.5 ∶1,这可能是由于淀粉链上有部分羟基与Cu2+的配位,另外由于改性淀粉颗粒的多孔结构,一些Cu2+会在空隙表面发生物理吸附,因此吸附剂表面是非均匀的,CAS 这种吸附形式更为突出明显,这也是其等温吸附式拟合更符合Freundlich 型的原因。
2.5 温度对吸附的影响及热力学参数的测定
当温度为238.15 ~303.15 K 时测定了两种氨基淀粉吸附Cu2+的热力学参数。两者的吸附容量均随着温度的升高而增大,表明两种改性淀粉吸附铜离子均为吸热反应。通过方程(8)~(10)计算了吸附过程的热力学函数[15]:吉布斯吸附自由能(ΔG)、吸附焓(ΔH)和吸附熵(ΔS)。

其中D——热力学平衡常数;
R——理想气体常数,8.314 J/mol·K;
T——开尔文温度。
因为lg D 随1/T 变化的关系曲线为直线(图略),根据直线的斜率ΔH/(2. 303R)和截距ΔS/(2.303R)可确定得到ΔH、ΔS,再由式(10)计算ΔG,结果如表3 所示。

表3 氨基淀粉吸附Cu2+的热力学参数Tab.3 Thermodynamic Parameters for Cu2+Adsorption by CAS and DAS
由表3 可知ΔH >0,表明吸附反应为吸热反应。文献[16-19]中不同的改性天然高分子吸附重金属离子时,也有为吸热反应的结论。一个可能的原因是在水溶液中,由于水的溶剂化作用,金属离子以水合离子状态存在,要吸附到固体表面上,必须脱去金属离子表面的水合鞘,这个脱水过程需要消耗能量,当该能量大于Cu2+吸附于两种氨基淀粉表面放出的热量时,整个吸附过程表现为吸热反应[20]。另外ΔS >0 说明随着吸附反应进行,Cu2+在液相(溶液)和固相(吸附剂)间重新分配,无序性增强,所以是熵增的过程,并且随着温度升高,体系混乱度愈来愈大。ΔG <0,表明吸附反应是自发的过程,而且温度越高,ΔG 越小,说明温度越高越有利于吸附反应的进行,这一结论也符合吸热反应的基本特征。由以上计算结果可知两种氨基淀粉对铜离子的吸附都是自发、吸热、熵增过程。但CAS 吸附反应的焓变值、熵增值都远大于DAS;ΔG 更小,反应更容易进行,这和CAS 具有更大的吸附容量和吸附能力更强有关。
3 结论
本文从吸附剂用量、pH、吸附时间、溶液初始浓度、温度等方面对两种不同结构的氨基淀粉吸附Cu2+的性能进行了对比研究,并结合其结构特征和作用机理进行分析,得出以下结论:
(1)CAS(含C—N 键的氨基淀粉)对Cu2+吸附容量比DAS(含 ==C N 键的氨基淀粉)更大,吸附键合力更强;两种氨基淀粉对Cu2+的吸附均符合拟二级动力学,DAS 的吸附活化能大于CAS,CAS 的吸附速率大于DAS 的吸附速率;CAS 对Cu2+等温吸附符合Freundlich 型,为非均匀表面吸附,DAS 吸附则是均匀表面、单层吸附的吸附过程;两种氨基淀粉对Cu2+的吸附过程均为吸热、熵增、自发的过程;升高温度有利于其吸附。相比DAS,CAS 吸附Cu2+能力更强。
(2)溶液pH 对吸附影响较大。当pH 为5 ~7时,CAS 对Cu2+的去除效果最好;当pH 为4 ~4.5时,DAS 对Cu2+的吸附容量较大。
(3)通过对两种氨基淀粉去除Cu2+的比较,确定CAS 对Cu2+的吸附效果要比DAS 好。但值得一提的是,CAS 在合成的间接醚化阶段,反应含水率、醚化剂用量、引发剂用量、反应温度及反应时间等都会影响产物的纯度和产量,反应条件苛刻,难于控制,而DAS 的醛化则在室温下就可以顺利进行。所以,要推广应用CAS 必须对其醚化工艺进行改进,采用更好的醚化剂或引发剂可能是切实可行的办法。
[1]王秀玲.铜及其化合物对接触者健康的影响[J].工业卫生与职业病,1996,24(2):42-44.
[2]鲁栋梁,夏璐.重金属废水处理方法与进展[J].化工技术与开发,2008,37(12):32-35.
[3]黄君涛,熊帆,谢伟立,等. 吸附法处理重金属废水研究进展[J].水处理技术,2006,32(2):9-12.
[4]Wan Ngah W. S.,Hanafiah M. A. K. M. Removal of heavy metal ions from wastewater by chemically modified plant wastes as adsorbent:A review[J]. Bioresource Technology,2008,99(10):3935-3948.
[5]Wing R. E.,Doane W. M.,Russell C. R. Insoluble starch xanthate:use in heavy metal removal[J]. Journal of Applied Polymer Science,1975,19(15):847-854.
[6]Li Y. J.,Xiang B.,Ni Y. M. Removal of Cu (Ⅱ)from aqueous solutions by chelating starch derivatives[J]. Journal of Applied Polymer Science,2004,92(6):3881-3885.
[7]Aiqin Dong,Jie Xie,Wenmin Wang,et al. A novel method for amino starch preparation and its adsorption for Cu (Ⅱ)and Cr(Ⅵ)[J]. Journal of Hazardous Materials,2010,181 (9):448-454.
[8]徐寿昌.有机化学[M].北京:高等教育出版社,1993.
[9]Yin Q. F.,Ju B. Zh.,Zhang Sh. F.,et al. Preparation and characteristics of novel dialdehyde aminothiazole starch and its adsorption properties for Cu (Ⅱ)ions from aqueous solution[J].Carbohydrate Polymers,2008,72(5):326-333.
[10]Ho Y. S. Review of second-order models for adsorption systems[J]. Journal of Hazardous Materials,2006,36(1):681-689.
[11]Ho Y. S.,McKay G.. A comparison of chemisorption kinetic models applied to pollutant removal on various sorbents[J].Process Safety and Environment,1998,76(B):332-340.
[12]Ho Y. S.,McKay G.. Pseudo-second order model for sorption processes[J]. Process Biochemistry,1999,34(5):451-465.
[13]Langmuir I. The adsorption of gases on plane surfaces of glass,mica and platinum[J]. Journal of American Chemical Society,1918,40(9):1361-1378.
[14] Freundlich H. M. F. Über die Adsorption in Lösungen[J].Zeitschrift fur Physikalis-che Chemie,1906,57(A):385-470.
[15]冯媛,易发成.稻壳对铀吸附性能的研究[J].原子能科学技术,2011,45(2):161-167.
[16]Guoren Xie, Xiaoqin Shang, Rufeng Liu. Synthesis and characterization of a novel amino modified starch and its adsorption properties for Cd(Ⅱ)ions from aqueous solution. Carbohydrate Polymers,2011,84 (8):430-438.
[17]Wang X. S.,Qin Y.. Removal of Ni (Ⅱ),Zn (Ⅱ)and Cr(Ⅵ)from aqueous solution by Alternanthera philoxeroides biomass.Journal of Hazardous Materials,2006,138(6):582-588.
[18]Rakhshaee R.,Khosravi M.,Ganji M. T.. Kinetic modeling and thermodynamic study to remove Pb (Ⅱ),Cd (Ⅱ),Ni(Ⅱ)and Zn (Ⅱ)from aqueous solution using dead and living Azolla filiculoides[J]. Journal of Hazardous Materials,2006,134(2):120-129.
[19]H. Chen,G. L. Dai,J. Zhao,et al. Removal of copper (Ⅱ)ions by a biosorbent-Cinnamomum camphora leaves powder[J]. J.Hazard. Mater,2010,177(10):228-236.
[20]R. Donat,A. Akdogan,E. Erdem,et al. Thermodynamics of Pb2+and Ni2+adsorption onto natural bentonite from aqu-eous solutions[J]. Journal of Colloid and Interface Science,2005,286(7):43-52.

