咪唑型功能离子液体合成及其对铀(Ⅵ)的萃取
李宏宇,申利红,张 乐,李培佑
(1.邯郸学院 邯郸市有机小分子材料重点实验室,河北 邯郸 056005;2.核工业北京化工冶金研究院,北京 101149)
离子液体与传统的有机溶剂和电解质相比,具有一系列突出优点:1)几乎无蒸汽压、不挥发、无色、无味;2)有较大的稳定温度范围、较好的化学稳定性及较宽的电化学稳定电位窗口;3)通过阴阳离子的设计可调节其对无机物、有机物及聚合物的溶解性。由于离子液体具有以上优异性能,被视为“绿色”溶剂,可替代给大气带来污染的常规易挥发性有机化合物,用于有机合成反应和液-液萃取体系[1-2],极大地避免了因大量使用和挥发造成的资源浪费和环境污染问题。
铀水冶工艺中,萃取是主要的手段之一,疏水性室温离子液体代替煤油等挥发性有机溶剂作为稀释剂,用于铀酰离子萃取研究,近年来已有许多报道[3-4]:以烷基咪唑类疏水型室温离子液体为稀释剂,如[C8mim][PF6]或[C4mim][PF6]等,与铀萃取剂磷酸三丁酯(TBP)等复配用于萃取含铀水系中的铀,可得到较高的萃取效率[5-6]。在离子液体作为稀释剂的萃取体系中,萃取效果与离子液体本身的性能关系密切,离子液体与萃取剂、铀酰离子的相容性是一重要因素,大多情况下,离子液体对萃合物的溶解性不如常规有机溶剂,会存在萃取体系产生三相的问题,从而妨碍萃取过程的顺利进行,TBP与铀酰离子生成的萃合物与离子液体[C8mim][PF6]和[C4mim][PF6]体系,就存在此问题,在萃取过程中达到饱和,从而从有机相中析出而成为第三相。
本文利用特定功能离子液体(TSILs)的概念[7-9],将铀萃取剂功能基引入到离子液体阳离子结构中,设计合成一类新颖的TSILs,使离子液体既是稀释剂又是萃取剂,从而降低萃取体系中组分的复杂程度,可有效解决上述问题,有利于萃取工艺的优化[10]。
1 实验
1.1 仪器和试剂
BIO-RAD FTS-40傅里叶变换红外光谱仪,KBr压片;Bruker AC-E200型核磁共振光谱仪,CDCI3等作溶剂;PE-2400元素分析仪;732型可见分光光度计,上海精密科学仪器有限公司。
亚磷酸二正丁基酯,工业级,上海至鑫化工有限公司生产;六氟磷酸钾,分析纯,北京青鸿福科有限公司生产;N-甲基咪唑、四丁基溴化铵,分析纯,北京试剂公司;三氟甲基磺酰亚胺,分析纯,阿法埃莎天津化学有限公司提供;其他试剂均为分析纯,用前未作任何处理。
1.2 磷氧结构功能专一离子液体的合成
1)磷酸-溴代丙基-二正丁基酯的制备
向装有搅拌器、恒压滴液漏斗、温度计及导气管的250 mL 四口烧瓶中依次加入25%NaOH 水溶液(30mL)、3-溴丙醇(13.9g)、四氯化碳(25mL)、二氯甲烷(25mL)及四丁基溴化铵(TBAB,0.36g),冰水浴控制体系温度在10~15℃;搅拌下将亚磷酸二正丁基酯(24.3g)与四氯化碳(30mL)的混合溶液通过恒压滴液漏斗缓慢滴入上述体系中,滴加完毕后撤去冰水浴,室温下继续反应3h。然后用二氯甲烷(20mL)将体系稀释、过滤,母液依次用2%稀盐酸(20mL)洗涤3次、去离子水(20mL)洗涤3次,无水硫酸钠干燥过夜,减压除去四氯化碳和二氯甲烷,得到产品磷酸-溴代丙基-二正丁基酯(化合物Ⅰ),为无色透明液体,收率为72%。
2)1-(磷酸二正丁基正丙基酯)-3-甲基咪唑溴化物的制备
将3.31g化合物Ⅰ与0.82g N-甲基咪唑混合,搅拌下室温反应48h成盐,产物用乙酸乙酯洗涤纯化,真空干燥24h,得到无色透明黏稠液体,即1-(磷酸二正丁基正丙基酯)-3-甲基咪唑溴化物(化合物Ⅱ),收率为80%。
3)1-(磷酸二正丁基正丙基酯)-3-甲基咪唑六氟磷酸盐的制备
将4.13g化合物Ⅱ溶于30mL 去离子水中,与1.84g六氟磷酸钾的水溶液(20 mL 去离子水)混合,室温搅拌24h 进行离子交换。分液分离,有机相用去离子水反复洗涤至水相不含溴离子为止(硝酸银检验),真空干燥24h,得到浅黄色黏稠液体,即为1-(磷酸二正丁基正丙基酯)-3-甲基咪唑六氟磷酸盐(化合物Ⅲ),收率为73%。
4)1-(磷酸二正丁基正丙基酯)-3-甲基咪唑双三氟甲基磺酰亚胺盐的制备
将4.13g化合物Ⅲ溶于30mL 去离子水中,与2.87g双三氟甲基磺酰亚胺锂的水溶液混合(20mL 去离子水),室温搅拌反应24h。分液分离,有机相用去离子水反复洗涤至不含溴离子为止(硝酸银检验),真空干燥24h,得到无色透明液体,即为1-(磷酸二正丁基正丙基酯)-3-甲基咪唑双三氟甲基磺酰亚胺盐(化合物Ⅳ),产率为70%。
1.3 萃取试验及分析方法
向25mL分液漏斗中加入5mL本文制备的化合物Ⅳ和含60mg/L铀的硝酸溶液5mL,于室温下充分震荡30min,静置、分液分离,水相(萃余相)残余铀浓度用铀试剂进行比色分析。
萃取效果用分配比D(U)或萃取率E 表示,在相比1∶1的情况下,忽略平衡前后两相体积变化,计算公式如下:

式中,Ceq,o和Ceq,a分别 为 萃 取后 有 机 相 和 水 相中铀的平衡浓度。
2 结果与讨论
2.1 磷氧结构功能专一离子液体合成路线设计
为能达到硝酸环境下萃取铀酰离子,同时解决萃取体系复杂的问题,本文借助具有特定功能的离子液体的理念,将铀萃取剂功能结构引入到离子液体阳离子结构中,实现离子液体-萃取剂二组分合一,简化萃取体系成分,以期解决常规萃取体系存在的相关问题,如体系乳化、三相等。
TBP是常用的铀萃取剂,在硝酸体系中对铀酰离子有良好的萃取效果,同时,TBP 与咪唑型离子液体复配用于铀酰离子的萃取,已有相关文献报道[4-6,11],证明该复配体系对铀酰离子有良好的萃取效果。为此,本文以亚磷酸二丁酯和相应的溴代烷基醇为起始原料,首先合成了溴代烷基磷酸酯(化合物Ⅰ),然后与甲基咪唑成盐,将磷酸酯结构引入到咪唑环上,形成溴代咪唑型离子液体(化合物Ⅱ),再通过阴离子交换,设计合成了两种含不同阴离子类型的磷氧结构功能专一型咪唑离子液体(化合物Ⅲ和Ⅳ)。合成路线如图1所示。
2.2 中间产物及目标产物表征
1)磷酸-溴代丙基-二正丁基酯(Ⅰ)
元素分析:分子式,C11H24O4BrP(331.2);计算值,C 39.86、H 7.25、Br 24.12;实测值,C 39.17、H 7.78。测量误差为1.8%。
红外数据(FTIR):2 961(s)、2 933(s)、2 974(m)、1 466(m)、1 382(w)、1 279(s)、1 150(w)、1 072(s)、652(w)cm-1。
核磁 数据(1H NMR)(CDCl3):δ=0.87(t,6H)、1.33(m,4H)、1.60(m,4H)、2.13(t,2H)、3.44(t,2H)、3.99(m,4H)、4.11(m,2H)ppm。
上述数据与文献值[12]相符,证明得到了目标化合物Ⅰ。
2)1-(磷酸二正丁基正丙基酯)-3-甲基咪唑溴化物(Ⅱ)
元素分析:分子式,C15H30O4N2BrP(413.31);计算值,C 43.25、H 7.26、N 6.77、Br 19.33;实测值,C 41.44、H 7.34、N 7.43。测量误差为0.3%。
红外数据(FTIR):3 142(m)、3 061(s)、2 960(s)、2 873(s)、1 736(s)、1 572(m)、1 465(m)、1 373(m)、1 267(s)、1 170(m)、1 028(s)、906(w)、862(w)、756(w)、621(w)cm-1。

图1 1-(磷酸二正丁基正丙基酯)-3-甲基咪唑六氟磷酸盐和1-(磷酸二正丁基正丙基酯)-3-甲基咪唑双三氟甲基磺酰亚胺盐合成路线Fig.1 Synthetic routes of 1-dibutylphosphorylpropyl-3-methylimidazole hexafluorophosphate and 1-dibutylphosphorylpropyl-3-methylimidazole bis(trifluoromethanesulfonyl)imide
核磁数据(1H NMR)(D2O):δ=8.63(s,1H)、7.38(s,1H)、7.33(s,1H)、4.21~4.24(t,2H)、3.96~3.98(m,6H)、3.75(s,3H)、2.13~2.16(m,2H)、1.51~1.54(m,4H)、1.24~1.25(m,4H)、0.75~0.79(t,6H)ppm。
上述数据综合分析表明,得到了目标化合物Ⅱ。
3)1-(磷酸二正丁基正丙基酯)-3-甲基咪唑六氟磷酸盐(Ⅲ)
元素分析:分子式,C15H30O4N2BrP(477.8);计算 值,C 37.67、H 6.28、N 5.86;实 测 值,C 37.48、H 5.06、N 5.80。测量误差为0.4%。
FTIR数据:3 168(m)、3 122(m)、2 963(s)、2 875(s)、1 577(m)、1 466(m)、1 263(s)、1 171(s)、1 029(s)、840(s)cm-1。
1H NMR(CDCl3)数 据:δ=8.57(s,1H)、7.28(s,1H)、7.22(s,1H)、4.24~4.27(t,2H)、3.95~4.00(m,6H)、3.83(s,3H)、2.10~2.20(m,2H)、1.56~1.63(m,4H)、1.29~1.38(m,4H)、0.85~0.88(t,6H)ppm。
上述数据综合分析表明,得到了目标化合物Ⅲ。
4)1-(磷酸二正丁基正丙基酯)-3-甲基咪唑双三氟甲基磺酰亚胺盐(Ⅳ)
元素分析:分子式,C17H30N3O8S2F6P(613.6);计 算 值,C 33.25、H 4.89、N 6.85;实 测 值,C 33.32、H 5.006、N 6.688。测量误差为0.1%。
FTIR数据:3 157(m)、3 119(m)、2 965(s)、2 877(m)、1 576(m)、1 467(m)、1 431(w)、1 353(s)、1 264(s)、1 196(s)、1 138(s)、1 058(s)、1 031(s)、803(m)、789(m)、740(m)、653(m)、617(m)、570(m)cm-1。
1H NMR(CDCl3)数据:δ=8.85(s,1H)、7.44(s,1H)、7.21(s,1H)、4.29~4.32(m,2H)、3.96~4.01(m,6H)、3.88(s,3H)、2.18~2.19(m,2H)、1.58~1.61(m,4H)、1.31~1.36(m,4H)、0.87~0.89(t,6H)ppm。
上述数据综合分析表明,得到了目标化合物Ⅳ。
2.3 硝酸环境下对铀酰离子萃取初步研究
1)不同硝酸浓度下对铀酰离子的萃取行为
图2示出化合物Ⅲ在不同硝酸浓度下对铀酰离子的萃取行为(曲线1)。由图可看出:由于离子液体阳离子结构中引入了磷酸酯功能基团,对铀酰离子具有明显的萃取效果,特别是高酸度环境,D(U)可达10 以上,E 达90%左右。而常规的离子液体([C8mim][PF6]、[C4mim][PF6]),若无外加萃取剂对铀酰离子是不萃取的。
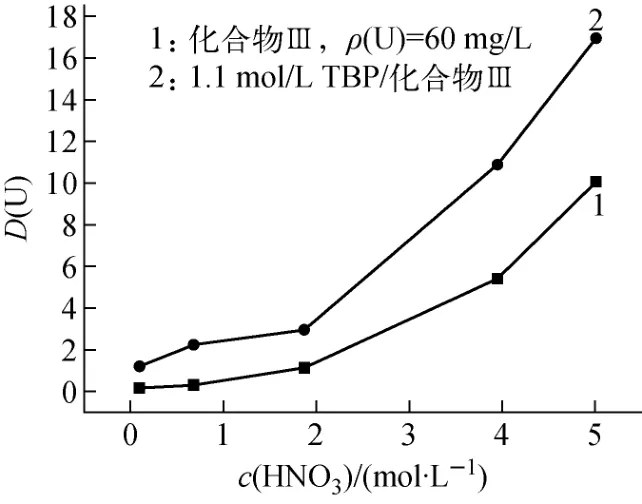
图2 硝酸浓度对D(U)的影响Fig.2 Effect of nitrate concentration on D(U)
曲线2是在化合物Ⅲ中补加少量萃取剂TBP后对铀酰离子的萃取行为,发现萃取效果变化明显,萃取效率提高、萃取相稳定,萃取分配比可接近20。这是由于TBP本身作为萃取剂,能从硝酸体系中有效地萃取铀酰离子,与化合物Ⅲ复配后产生了协萃效应,进一步优化了萃取效果。

图3 离子液体的阴离子结构对D(U)的影响Fig.3 Effect of ion liquid anion structure on D(U)
2)不同阴离子结构对铀酰离子的萃取行为图3示出两种不同阴离子结构的特定功能离子液体(Ⅲ和Ⅳ)对铀酰离子的萃取行为。从图3可看出,在高酸度(HNO3在0.7mol/L 以上)条件下,具有磷酸酯结构的两种离子液体对铀酰离子的萃取效果相同,分配比均随水相的初始酸度增加而增大;但在水相呈低酸度时,两种离子液体表现出不同的萃取效率,对化合物Ⅵ(即阴离子为[CF3SO3)2N]-型)萃取体系(曲线1),分配比随酸度的增大而降低。这可能是由于低酸度下化合物Ⅵ表现出了不同的萃取机理。有研究[8]表明,低酸度条件下,在研究离子液体对Hg2+和Cd2+的萃取行为时,发现[CF3SO3)2N]-型离子液体中的阳离子结构,易与水相中的金属离子发生离子交换,导致相应的金属离子被交换到离子液相中,所以产生了萃取分配比较高的现象。
3 结论
1)利用特定功能离子液体的概念,将TBP的功能基引入到离子液体阳离子结构中,设计合成了两种具有不同阴离子结构的咪唑型功能专一的离子液体:1-(磷酸二正丁基正丙基酯)-3-甲基咪唑六氟磷酸盐(Ⅲ)和1-(磷酸二正丁基正丙基酯)-3-甲基咪唑双三氟甲基磺酰亚胺盐(Ⅳ),并通过元素分析、傅里叶红外光谱和核磁共振等手段进行了结构确认。
2)利用所制备的特定功能的离子液体,对铀酰离子在硝酸介质中的萃取行为进行了初步研究,结果表明:室温条件下,所合成的离子液体可在硝酸介质中萃取铀酰离子,单独使用时,铀酰离子在两相中的萃取分配比D(U)可达10,与TBP复配使用D(U)接近20,萃取率E 可达90%以上。因此,在实际应用时,可考虑复配体系,利用TBP的协萃效应提高萃取效率。
3)该特定功能离子液体由于具有萃取剂功能基团,使得离子液体既是稀释剂又是萃取剂,从而降低了萃取体系中组分的复杂程度,可有效地解决萃取体系乳化、出现三相等问题。
[1] WELTON T.Room temperature ionic liquids solvents for synthesis and catalysis[J].Chem Rev,1999,99(8):2 071-2 083.
[2] 李汝雄.绿色溶剂——离子液体的合成与应用[M].北京:化学工业出版社,2004:35-95.
[3] 沈兴海,徐超,刘新起,等.离子液体在金属离子萃取分离中的应用[J].核化学与放射化学,2006,28(3):129-138.SHEN Xinghai,XU Chao,LIU Xinqi,et al.Ionic liquids used in extraction and separation of metal ions[J].J Nucl Radiochem,2006,28(3):129-138(in Chinese).
[4] 李宏宇,刘正平.室温离子液体用于放射性核素分离研究中的进展[J].铀矿冶,2008,27(2):86-91.LI Hongyu,LIU Zhengping.Progress in separation of radioactive isotopes by room temperature ionic liquids[J].Uranium Mining and Metallurgy,2008,27(2):86-91(in Chinese).
[5] GIRIDHAL P,VENKATESAN K P,SRINIVASAN T G,et al.Effect of alkyl group in 1-alkyl-3-methylimimdazolium hexafluorophosphate ionic liquids on the extraction of uranium by TBP diluted with ionic liquids[J].J Radioanal Nucl Chem,2004,5(1):21-26.
[6] GIRIDHAL P,SRINIVASAN T G,VASUDEVA RAO P R,et al.Extraction of uranium(Ⅵ)from nitric acid medium by 1.1 mol/L TBP in ionic liquid diluent[J].J Radioanal Nucl Chem,2004,265(1):31-38.
[7] VISSER A E,SWATLOSKI R P,REICHERT W M,et al.Task-specific ionic liquids for the extraction of metal ions from aqueous solutions[J].Chem Commun,2001(1):135-136.
[8] VISSER A E,SWATLOSKI R P,REICHERT W M,et al.Task-specific ionic liquids incorporating novel cations for the coordination and extraction of Hg2+and Cd2+:Synthesis,characterization,and extraction studies[J].Environ Sci Technol,2002,36(11):2 523-2 529.
[9] WHITEHEAD J A,LAWRANCE G A,MCCLUSKEY A.Green leaching:Recyclable and selective leaching of gold-bearing ore in an ionic liquid[J].Green Chem,2004,6(7):313-315.
[10]李宏宇,刘浩,刘正平,等.一种含磷氧结构的功能化离子液体及其制备方法和应用:中国,CN 101838290A[P].2010-09-22.
[11]褚泰伟,秦丽,刘新起,等.离子液体用于萃取铀酰离子的初步研究[J].核化学与放射化学,2007,29(3):146-150.CHU Taiwei,QIN Li,LIU Xinqi,et al.Extraction of uranium from nitric acid medium by TBP in roomtemperature ionic liquids[J].J Nucl Radiochem,2007,29(3):146-150(in Chinese).
[12]GHEORGHE I,ADRIANA P,SMARAANDA I,et al.Synthesis of mixed alkylphosphites and alkylphosphates[J].Phosphorus,Sulfur,and Silicon and the Related Elements,2003,178(7):1 513-1 519.

