体外膜肺氧合在成人心外科术后心源性休克应用早期死亡率及临床结果危险因素分析
杜中涛,杨 峰,江春景,邢家林,缪 娜,刘 锋,杨晓芳,江 瑜,李 蛟,侯晓彤
·临床研究·
体外膜肺氧合在成人心外科术后心源性休克应用早期死亡率及临床结果危险因素分析
杜中涛,杨 峰,江春景,邢家林,缪 娜,刘 锋,杨晓芳,江 瑜,李 蛟,侯晓彤
目的 探讨体外膜肺氧合(ECMO)对心脏手术后难治性心源性休克提供临时机械循环支持的应用效果及早期死亡率危险因素分析。方法 回顾分析本院2012年1月至2012年12月期间,6 986名成人心脏术后患者中有54例(0.77%)患者因为术后心源性休克而应用静脉动脉(VA)ECMO支持。使用指证包括:心脏术后难以脱离体外循环,容量合适的情况下大剂量的血管活性药物应用和/或者应用主动脉内气囊反搏(IABP)仍难以维持血流动力学稳定。其中有11例(20%)患者因为各种原因支持时间少于24 h未纳入统计分析。结果 43例患者平均年龄为59.0岁,男性30例,女性13例。ECMO平均支持时间是5.1 d。31例(72.1%)患者成功脱离ECMO辅助。30 d及1年死亡率分别为60.5%(27/43)和69.8%(30/43)。ECMO患者院内死亡率为65.1%(28/43)。对出院患者进行门诊随访,ECMO患者1年生存率为30.2%(13/43)。Logistic回归分析发现患者应用ECMO后72 h左室射血分数(LVEF)≤30%和ECMO应用3 d内悬浮红细胞输入量是院内死亡率的重要预测因子(OR=14.76,95%CI=2.34-93.25,P=0.004;OR=0.60,95%CI=0.38-0.94,P=0.03)。结论 ECMO为心脏术后严重心源性休克患者提供了一个有效的临时心肺支持。辅助期间较低的LVEF和较多的悬浮红细胞输入量是影响死亡率的危险因素。在ECMO辅助支持期间,应该每日监测LVEF变化及悬浮红细胞的输入量。
机械循环辅助;体外生命支持;心脏外科;心源性休克;危险因素
心外科术后约有3%~5%的患者发生心功能不全[1],其中大部分患者在正性肌力药物以及主动脉内气囊反搏(intra-aortic balloon pump,IABP)的帮助下可以成功脱离体外循环(extracorporeal circula⁃tion,ECC)。但仍有约1%的患者因为心脏或肺脏的问题进展为难治性心源性休克需要机械循环的支持[2-3]。体外膜肺氧合(extracorporeal membrane ox⁃ygenation,ECMO)作为一种短期的体外生命支持辅助装置于1972年在一例创伤患者中得到成功应用以来,有越来越多的研究报道ECMO在复杂心力衰竭中能提供有效的循环支持[4-7],本研究就本中心心脏术后应用ECMO的患者进行总结分析,评估早期以及中期的临床结果,预测影响死亡率的危险因素,为提高ECMO患者救治成功率提供经验总结。
1 资料与方法
1.1 患者入选及排除标准 2012年1月至2012年12月份,本院成人心外科一共进行了6 986例手术,其中有54例(0.77%)因为心脏术后低心排综合征应用ECMO进行循环支持辅助。54例中有11例因各种原因辅助时间<24 h未纳入统计。余43例患者的心脏手术为:冠状动脉旁路移植术(coronary artery bypass graft,CABG)11例,非体外循环下冠状动脉旁路移植术(off-pump CABG,OPCABG)14例,瓣膜手术9例,瓣膜手术+CABG 7例,肺动脉栓塞取栓术2例。ECMO应用指证有:心脏手术期间体外循环后并行阶段大剂量正性肌力药物以及IABP应用仍难以脱离ECC、在监护室或者病房发生难以复律的恶性心律失常、心脏骤停、药物及IABP难以维持有效循环(平均动脉压<60 mm Hg)、乳酸持续的升高。
1.2 ECMO环路组建 ECMO环路由离心泵、膜肺、肝素化涂层管路及动静脉插管组成,套包有美敦力(CB1Q91R,Medtronic,US)及迈科维(PLS2050,MAQUET,Germany)两种规格,插管采用美敦力Car⁃meda涂层插管。43例患者中有42例采用周围血管置管,1例采用正中切口右房升主动脉置管。股动静脉采用切开直视下的Open-Seldinger方法置入动静脉插管[8]。
1.3 ECMO患者管理 初始的ECMO流量以维持患者平均动脉压在60~70 mm Hg以上为标准设置,但一般不超过4~4.5L/min以降低对红细胞的破坏。气流量及氧浓度设置一般使膜肺后氧分压达到300 mm Hg左右,二氧化碳分压维持在正常范围(35~45 mm Hg)。如果发生膜肺血浆渗漏或者明显血栓形成时,及时更换膜肺。
没有明显外科出血时,静脉持续泵入肝素以维持全血激活凝固时间(ACT)在180~220 s之间。手术当天(外科手术期间安装的ECMO,ECC结束时可以全量鱼精蛋白应用)及术后第一天一般不应用肝素以避免难以控制的外科出血发生,当血小板低于50×109时,根据情况输注血小板。
当周围循环稳定时,可以逐渐降低正性肌力药物的应用至基础需要量以降低心脏后负荷,同时使心肌得到一定的休息。当左心功能很差(脉压差很低)时,可以据情况使用IABP降低左室后负荷同时改善冠脉供血,如果存在严重的左心衰竭时,为保证左心能有效减负荷可以增加左心引流(一般采用左室心尖置管或者左房、肺静脉置管)连接入ECMO静脉端使左心得到休息。
日常监测超声评估心功能变化及患者血气情况调整ECMO流量,当ECMO流量调到1.5 L/min时如果在患者循环稳定、血管活性药物药量不大的情况下,在ECMO动静脉环路间接入一“桥”连接管用以试停ECMO后的装置系统自循环,全身应用肝素(100 U/kg)后试停ECMO治疗。试停成功后拔除动静脉插管结束ECMO治疗。
1.4 数据收集 回顾性分析ECMO患者资料,包括患者基本信息,心功能状态,化验检查,血制品应用,辅助期间并发症,辅助时间,住院期间生存状态,一年生存率等临床数据。患者基本信息及术前状态见表1,根据患者心脏手术种类的不同将患者分为5个亚组。
1.5 统计分析 采用SPPSS 19.0对所有数据进行统计分析,计数数据采用百分率表示,使用卡方检验,计量数据采用均数±标准差(±s)表示,采用独立样本t检验。对影响院内死亡率的危险因素分析采用逐步logistic回归分析,使用Kaplan-Meier生存曲线对一年生存率进行生存分析,P<0.05有统计学意义。
2 结 果
43例患者ECMO辅助结果见表2,ECMO平均支持时间(5.1±4.1)d,31例(72.1%)患者成功脱离ECMO辅助支持,15例(34.9%)患者成功出院,其中13例(30.2%)患者在一年随访时健康存活。在不同手术中,瓣膜疾病及肺栓塞患者年龄(平均年龄46岁、47.5岁)较冠脉疾病患者年轻(平均年龄63岁),CABG同时进行瓣膜手术ECC及主动脉阻断时间偏长,瓣膜疾病相对于冠脉患者ECMO辅助后死亡率较高(66.7%vs 45.5%),同时ECMO辅助时间也延长(9.0 d vs 3.5 d)。ECMO辅助期间肺部感染8例(18.6%)、神经系统损伤4例(9.3%)、插管侧下肢缺血3例(7.0%)、消化道出血和血尿各1例(2.3%)。
表1 患者一般资料(±s)

表1 患者一般资料(±s)
注:BMI:体重指数;LVEF:左室射血分数;NYHA:纽约心脏协会。瓣膜手术包括:二尖瓣置换2例,二尖瓣修复1例,二尖瓣+主动脉瓣置换3例,二尖瓣置换+三尖瓣修复2例,二尖瓣+主动脉瓣置换+三尖瓣修复1例。其他:肺动脉栓塞取栓术2例。
项目 合计 OPCABG CABG 瓣膜手术 CABG+瓣膜 其他例数 43 14 11 9 7 2男性(%) 30(69.8) 8(57.1) 11(100) 4(44.4) 5(71.4) 2(100)年龄(岁) 59±12.2 64±8.9 63±11 46±10.6 61±14.4 47.5±14.8 BMI(kg/m2) 23.9±3.7 24.0±3.6 25.6±3.8 20.7±3.1 24.7±2.8 24.5±0.7 LVEF(%) 58.0±12.0 53.5±11.1 58.5±14.6 63.6±8.0 56.1±13.1 67.5±2.1心功能NYHA 2.9±0.7 2.6±0.6 2.9±0.7 3.1±0.78 3.3±0.76 3±1.4
表2 ECMO不同组别之间临床结果(±s)

表2 ECMO不同组别之间临床结果(±s)
项目 合计 OPCABG CABG 瓣膜手术 CABG+瓣膜 其他例数 43 14 11 9 7 2 ECC时间(min) 135.2±121.7 0 190.8±100.8 174.2±102.1 261.7±58.7 157.0±7.1阻断时间(min) 47.3±54.4 0 35.7±56.5 82.2±43.1 107.0±34.5 75.5±2.1 ECMO时间(d) 5.1±4.1 4.3±1.8 3.5±1.1 9.0±7.1 4.2±2.9 4.9±1.5 ICU时间(d) 9.2±6.3 7.4±3.7 8.1±4.4 15.4±9.5 7±4.3 8.5±5.0住院时间(d) 28.4±14.6 23.4±11.7 32.6±17.7 34.3±16.6 23.1±10.2 31.5±9.2 ECMO脱机率(%) 31(72.1) 9(64.3) 10(90.9) 5(55.6) 5(71.4) 2(100)30天死亡率(%) 27(60.5) 11(78.6) 5(45.5) 6(66.7) 4(57.1) 1(50)住院死亡率(%) 28(65.1) 11(78.6) 5(45.5) 7(77.8) 4(57.1) 1(50)1年死亡率(%) 30(69.8) 11(78.6) 6(54.5) 8(98.9) 4(57.1) 1(50)
对于可能影响患者生存率的相关因素(包括术前及ECMO期间的生化、心功能、是否应用IABP等指标)进行分析发现,ECMO第三天患者的LVEF及ECMO应用三天内的悬浮红细胞输入量在院内存活组与死亡组之间具有统计学差异。笔者将这两个因素与院内死亡率进行Logistic回归分析发现ECMO第三天的LVEF<30%及红细胞输入量是院内死亡的独立危险因素,见表4。根据ECMO应用第三天的LVEF结果将患者又分为LVEF≤25%、26%~29%、≥30%三组,利用Kaplan-Meier生存曲线绘制生存曲线。LVEF≥30%组一年生存率为50%,LVEF 26%~29%组0%,LVEF≤25组10%(P=0.001)见图1。所有患者的30 d生存率和一年生存率分别为39.5%、30.2%,见图2。43例患者中30例患者联合应用了IABP,存活出院的患者中10例(66.7%)联合应用了IABP,院内死亡的患者中有20例(71.4%)应用了IABP,通过卡方检验P=0.75,见表3。
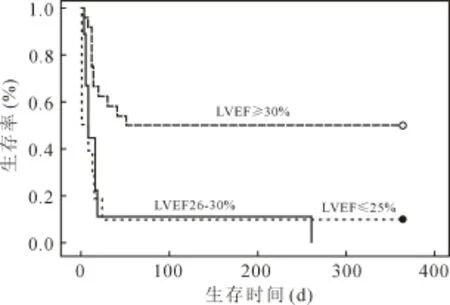
图1 应用ECMO后第3天时不同LVEF患者一年生存率对比

图2 Kaplan-Meier生存曲线
表3 ECMO患者院内生存与死亡相关因素分析(±s)

表3 ECMO患者院内生存与死亡相关因素分析(±s)
因素 生存组(n=15) 死亡组(n=28) P值术前 白蛋白(G/L) 40.7±5.9 40.3±5.2 0.83总胆红素(umol/L) 14.0±6.1 18.2±11.2 0.18 LVEF(%) 58.4±12.3 57.7±12.1 0.86 ECMO前 pH 7.4±0.1 7.3±0.1 0.29乳酸(mmol/l) 11.8±5.4 13.9±4.7 0.20 ECMO后24 h pH 7.5±0.1 7.5±0.1 0.96乳酸(mmol/l) 4.8±3.8 6.8±5.3 0.19 ECMO后3 d 白蛋白(G/L) 36.3±5.6 34.3±4.6 0.23总胆色素(umol/L) 33.5±28.6 40.1±35.4 0.55 LVEF(%) 43.8±11.3 34.35±13.6 0.03细胞3 d内输入量(U) 8.1±7.3 14.4±9.8 0.03应用IABP(%) 10(66.7) 20(71.4) 0.75

表4 院内ECMO患者死亡率危险因素分析
3 讨 论
心源性休克是心脏外科术后主要并发症之一,尤其多在术前心功能不良或存在心源性休克的患者中发生[4-7]。在本中心,心外科手术后发生严重的低心排血流动力学不稳定而患者心功能有可能恢复时,VA-ECMO是比较常用的治疗手段。ECMO能提供短期的循环辅助,部分患者经过ECMO的辅助能过渡到自身恢复或心室辅助装置状态,为下一步治疗提供时间[9]。由于目前国内没有注册的心室辅助装置及心脏移植供体的短缺,在过渡到心脏移植及心室辅助装置等方面应用较少。
心脏外科手术后,部分患者因为再血管化心肌梗死以及心肌顿抑等原因表现为低心排综合征,ECMO能为这部分患者提供短时有效的循环支持以满足患者的全身器官灌注。临床上,目前没有明确的教科书定义ECMO的应用标准,除非有明确应用禁忌(比如难以控制的外科大出血),一般建议早期应用ECMO以保证重要脏器在低心排期间能得到及时有效的灌注。在本组辅助的患者中,CABG患者的生存率明显高于瓣膜手术患者,冠脉疾病患者的ECMO平均支持时间也较瓣膜疾病患者明显缩短,这可能是因为CABG患者术后出现的低心排,一般是由于围手术期心梗或者缺血再灌注损伤导致,而瓣膜疾病患者多因本身心肌功能存在一定问题引起。这部分瓣膜病患者出现的低心排在短期内(5~7 d)难以恢复,及早过渡到心室辅助装置可能是比较好的选择[7]。
ECMO辅助期间肺部感染、神经系统损伤及插管侧下肢缺血是比较严重的并发症。针对这种情况,团队加强了ECMO辅助期间患者护理的无菌操作及抗生素的严格应用,制定了每日早交班期间患者唤醒制度,以便及早评估患者精神状态。对于周围血管插管建立的ECMO常规置入远端灌注插管改善下肢供血[8]。
在这些患者中,大部分在ECMO应用之前都已安装了IABP辅助治疗以降低心室后负荷增加冠脉供血,但是近来有临床报道IABP并没有提高ECMO患者的生存率[10],其产生的搏动灌注也没有明显改善患者的微循环[11]。本研究中院内生存组与死亡组中的IABP比例分别为66.7%和71.4%,通过检验两组不具有统计学差异,与之前的报道结果相同。而且在低心排下,IABP能够阻挡一部分股动脉来的ECMO血流[12],因此,在后续的临床实践中IABP与ECMO联合应用的价值及时机尚需进一步研究。
笔者统计分析了白蛋白、胆色素、乳酸、pH值、LVEF动态变化、红细胞输入量等指标与院内死亡率之间的关系,如表4所示。研究发现白蛋白、胆色
素、乳酸、pH值在生存组与死亡组之间没有明显统计学差异,而之前的许多研究证实ECMO前的pH值及乳酸水平等与死亡率具有明显的相关性[13-14]。这可能是因为本组患者中有很大一部分是在心脏外科手术中因为不能脱离ECC而安装的ECMO,在ECMO之前患者一直处在ECC下,机体的灌注能得到一定保证且酸碱平衡紊乱不会太严重。在本研究中,ECMO后3 d的LVEF值及3 d内的红细胞输入量这两个指标在存活组与死亡组之间具有统计学差异。本研究根据LVEF的差异绘制生存曲线发现LVEF≥30%组一年生存率能达到50%,利用LVEF≥30%及红细胞输入量分级作为统计指标与院内生存率进入logistic回归分析,发现这两个指标可以作为患者院内生存率的预测因素。ECMO后3 d的LVEF值≥30%,其院内存活率是未达到者的17.4倍。ECMO后3 d内输血总量每增加一个等级(多输4 U)的院内存活的比数比例是60%。ECMO患者3 d后心功能如果能恢复,能够顺利脱离ECMO并出院的机会明显增高,这也正是ECMO作为一种短期心肺支持设备所发挥的作用,如果这部分患者经过ECMO的辅助3 d后仍然不能恢复的话,心室辅助装置可能是一种比较好的应用选择。
本研究仅回顾分析了一年间的临床数据,具有一定的局限性。在目前状态下,ECMO对于心外科术后心源性休克是一种比较好的支持治疗手段,虽然具有较高的死亡率,但是仍挽救了部分患者(一年生存率30.2%)。随着国内ECMO团队的逐渐成熟,对于ECMO的认识不断强化,术后合理的患者管理监测,并发症预防措施的完善及设备的更加优化,ECMO在重症患者的治疗中一定能取得比较满意的结果。
[1] Golding LA.Postcardiotomy mechanical support[J].Semin Tho⁃rac Cardiovasc Surg,1991,3(1):29-33.
[2] Hsu PS,Chen JL,Hong GJ,et al.Extracorporeal membrane oxy⁃genation for refractory cardiogenic shock after cardiac surgery.Eu⁃ropean[J].Eur J Cardiothorac Surg,2010,37(2):328-333.
[3] Smith C,Bellomo R,Raman JS,et al.An extracorporeal mem⁃brane oxygenation-based approach to cardiogenic shock in an older population[J].Ann Thorac Surg,2001,71(5):1421-1427.
[4] Doll N,Kiaii B,Borger M,et al.Five-year results of 219 con⁃secutive patients treated with extracorporeal membrane oxygenation for refractory postoperative cardiogenic shock[J].Ann Thorac Surg,2004,77(1):151-157.
[5] Smedira NG,Moazami N,Golding CM,et al.Clinical experience with 202 adults receiving extracorporeal membrane oxygenation for cardiac failure:survival at five years[J].J Thorac Cardiovasc Surg,2001,122(1):92-102.
[6] Doll N,Fabricius A,Borger MA,et al.Temporary extracorporeal membrane oxygenation in patients with refractory postoperative car⁃diogenic shock—a single center experience[J].J Card Surg,2003,18(6):512-518.
[7] Bakhtiary F,Keller H,Dogan S,et al.Venoarterial extracorpore⁃al membrane oxygenation for treatment of cardiogenic shock:clini⁃cal experiences in 45 adult patients[J].J Thorac Cardiovasc Surg,2008,135(2):382-388.
[8] 杜中涛,邢家林,侯晓彤,等.经股动脉插管建立体外膜肺氧合严重下肢缺血危险因素分析[J].中国体外循环杂志,2013,11(3),150-153.
[9] Lafc G,Budak AB,Yener Au,et al.Use of extracorporeal mem⁃brane oxygenation in adults[J].Heart Lung Circ,2014,23(1):10-23.
[10] Park TK,Yang JH,Choi SH,et al.Clinical impact of intra-aor⁃tic balloon pump during extracorporeal life support in patients with acute myocardial infarction complicated by cardiogenic shock[J].BMC Anesthesiology,2014,14:27.
[11] Petroni T,Harrois A,AmourJ,et al.Intra-Aortic Balloon Pump Effects on Macrocirculation and Microcirculation in Cardiogenic Shock Patients Supported by Venoarterial Extracorporeal Membrane Oxygenation[J].Crit Care Med,2014,42(9):2075-2082.
[12] Yang F,Jia ZS,Xing JL,et al.Effects of intra-aortic balloon pump on cerebral blood flow during peripheral venoarterial extra⁃corporeal membrane oxygenation support[J].J Transl Med,2014,12:106.
[13] Combes A,Leprince P,Luyt CE,et al.Outcomes and long-term quality-of-life of patients supported by extracorporeal membrane oxygenation for refractory cardiogenic shock[J].Crit Care Med,2008,36(5):1404-1411.
[14] Cheung PY,Etches PC,Weardon M,et al.Use of plasma lactate to predict early mortality and adverse outcome after neonatal extra⁃corporeal membrane oxygenation:a prospective cohort in early childhood[J].Crit Care Med,2002,30(9):2135-2139.
Extracorporeal membrane oxygenation for refractory cardiogenic shock after cardiac surgery:risk factors of early mortality and outcome
Du Zhong-tao,Yang Feng,Jiang Chun-jing,Xing Jia-lin,Miao Na,Liu Feng,Yang Xiao-fang,Jiang Yu,Li Jiao,Hou Xiao-tong
Department of Extracorporeal Circulation,Center for Cardiac Intensive Care,Beijing Anzhen Hospital,
Capital Medical University,Beijing,China
Objective Analysis of risk factors of early mortality and outcome during extracorporeal membrane oxygenation(ECMO)support for those with refractory cardiogenic shock after cardiac surgery.Methods Between January 2012 and December 2012,6986 patients underwent cardiac surgery in our adult cardiac critical care unit.Among those,54 patients(0.77%)were suppor⁃ted with veno-arterial ECMO for cardiac support because of refractory postcardiotomy cardiogenic shock.Indications for ECMO support included:failure to wean from cardiopulmonary bypass,or refractory cardiogenic shock development despite adequate filling volumes,large-dose inotropes and/or intra-aortic balloon pump support.11 patients(20%)were excluded because the support time was less than 24 hours.The short-term and medium-term results of these patients were analyzed,and in addition,the prognostic factors of sur⁃vival were predicted.Results Patients'average age was 59.0±12.2 years.There were 30 male and 13 female patients.Overall mean support time was 5.1±4.1 days.Thirty-one(72.1%)patients could be successfully weaned from ECMO.The 30-day and 1-year mor⁃talities were 60.5%(27/43)and 69.8%(30/43),respectively.The in-hospital mortality was 65.1%(28/43).Thirteen(30.2%)patients were still alive at 1-year out-patient follow up.Stepwise logistic regression identified left-ventricular ejection fraction(LVEF)≤30%at 72 h after ECMO initiation and number of packed red blood cells(PRBCs)transfused during ECMO as significant predictors of mortality[odds ratio(OR)=14.76;95%confidence interval(CI)=2.34-93.25;P=0.004 and OR=0.60;95%CI=0.38-0.94,P=0.03,respectively].Conclusion ECMO provides a good temporary cardiopulmonary support in patients with postcardiotomy
Mechanical circulatory assistance;Extracorporeal membrane oxygenation;Cardiacsurgery;Cardiogenic shock;Risk factors
100029北京,首都医科大学附属北京安贞医院心脏外科危重症中心,体外循环及机械循环辅助科
通讯作者:侯晓彤,Email:xt.hou@ccmu.cn
2014⁃09⁃18)
2014⁃09⁃23)
10.13498/j.cnki.chin.j.ecc.2014.04.05
cardiogenic shock.The risk factor of mortality is poor LVEF after ECMO support,so the LVEF should be strictly monitored everyday during ECMO support.

