心室跨壁复极离散度预测心脏再同步治疗除颤器术后快速室性心律失常的风险*
何静, 严激, 徐健, 孙贤林 ,苏浩 ,宇霏 ,陈康玉
心室跨壁复极离散度预测心脏再同步治疗除颤器术后快速室性心律失常的风险*
何静, 严激, 徐健, 孙贤林 ,苏浩 ,宇霏 ,陈康玉
目的:心脏再同步治疗除颤器(CRT-D)增加了心室复极离散度(TDR),本研究旨在评价心肌跨壁复极离散度指标中的QTc间期,T波顶点(T p)T波终点(Te)之间的时限(TpTe)和TpTe /QTc是否与CRT-D患者需治疗的快速室性心律失常相关。
TpTe间期;跨壁复极离散度;心脏再同步化除颤器
(Chinese Circulation Journal, 2014,29:791.)
对于合并心脏不同步的进展性心力衰竭患者,接受心脏再同步治疗(CRT)的益处包括提高射血分数和生活质量,降低心衰住院率和死亡率[1,2]。研究发现,CRT虽然能够降低总死亡率,但室性心律失常的死亡风险并没有降低[3]。分析COMPANION试验中患者的死亡原因,CRT患者仍存在突发心源性猝死的风险[4],其室速风暴的发生率在4%~7%[5、6]。CRT左心室导线的植入增加了心肌跨壁复极离散度(TDR),而TDR是多种恶性室性心律失常,尤其是多形性室速、尖端扭转性室速的发生基础。电生理的基础实验证明,当同步记录心电图和内、中、外三层心肌的单相动作电位时,体表心电图T波顶点(T p)与心外膜心肌复极的终点对应,T波终点(Te)与M细胞的复极终点对应,在正常情况下,心外膜心肌的复极时间最短, M细胞的复极时间最长。因此Tp与T e之间的时限(TpTe )就可以代表心外膜心肌(最短)与中层心肌(最长)复极时间的差异,此即TDR。对于植入左心室电极的患者T波波峰可看做心肌表面细胞的复极,T波波谷可看做心肌完成复极的标志,因此可以把植入心脏再同步治疗除颤器(CRT-D)患者的心肌复极离散度看做T峰至T谷的间期即TpTe[7、8]。为排除心率对QT间期的影响,TpTe 与QTc间期之比(TpTe/QTc)亦是重要指标。CRT-D植入对反映TDR的上述指标是否产生影响,后者能否预测室性心律失常的发生,目前尚不明确。本文通过前瞻性的随访研究,探讨上述指标预测CRT-D术后室性心律失常的有效性。
1 资料和方法
病例资料:连续选取2011-01至2013-01安徽省立医院行CRT-D植入的患者,所入选的患者需符合如下条件,窦性心律或心房颤动(房颤),QRS波时限≥0.12 s,左心室射血分数(LVEF)≤0.35,NYHA心功能III或IV级的患者,在优化药物治疗的基础上行CRT-D治疗,以改善症状和预后。共入选160例患者, 在术后留取即刻12导联心电图,并详细记录V5导联的变化情况。
CRT-D植入:所有患者均采用经静脉途径植入CRT-D装置。左锁骨下静脉穿刺或头静脉切开,穿刺成功后行冠状静脉窦插管和逆行造影,充分显示冠状窦及各属支,将左心室导线植入靶静脉。测试无误后,应用常规方法将右心室导线置于右室心尖部或间隔部,右心房导线置于右心耳处。所有测试完毕后,连接脉冲发生器,逐层缝合切口。
心电图的测量及计算:本研究的心电图均取自CRT-D植入后的即刻心电图,所记录的心电图均采用走纸为25 mm/s,振幅为10 mm/mV,取V5导联做为数据分析,当V5导联的T波小于1 mm或者T波中隐含着一个巨大的U波,II导联的T波做为数据分析,QTc间期的测量以QRS起始到T波终点为准。起始点以Q( 或R) 波起点为准。T 波终点一般以T 波下降支与等电位线的交点或T 波和U波之间的最低点为准,校正QTc间期采用Bazett公式[9]. TpTe的选择为当T波为正时取自T波峰顶至T波终点的间期,当T波为倒置时取其谷底至T波终点的间期,所选择的患者的心电图均测量并计算其TpTe /QTc。所有的心电图测量数据均在术后分别由两位临床医师完成,当测量数据不一致时取其平均值,但当两者测量数据差距大于10 ms时,其测量数据由第三位临床医生评价准确性 。
随访:所有植入CRT-D的患者术后随访均在我中心起搏器随访门诊进行,随访包括术后常规按时随访和不适随访,即患者自觉不适时及时接受随访,随访设备均为CRT-D的常规随访设备,随访的主要终点为持续性室性心动过速或心室颤动,起搏器需抗心动过速起搏(ATP)和(或)放电治疗。随访的次要终点心力衰竭住院和全因死亡。随访时间(20±10)个月。
统计学分析 :数据分析由SPSS 16.0统计软件包完成,计量资料表示为平均值±标准差。两组间均数的差异用独立样本t检验,P<0.05被认为有统计学意义,受试者工作曲线(ROC)用于评估最适当的指标预测范围,受试者生存曲线(Kaplan-Meier curves) 用于检测预测指标意义。
2 结果
160名接受CRT-D患者,随访(20±10)个月(中位数为19个月)。其中发生室性心律失常需要CRT-D治疗的患者30例(治疗组),未发生者130例(未治疗组)。两组的基线资料差异无统计学意义(表1)。

表1 两组入选患者基线资料(%)
治疗组的患者较未治疗组TpTe/QTc ( 0.24±0.05 vs 0.20±0.04, P<0.001) 、TpTe[ (119±30) ms vs(95±20) ms, P<0.001]明显增加,差异有统计学意义;两组的QTc间期差异无统计学意义[(480±60)ms vs (470±70) ms,P=0.6),QTc间期的增加与放电治疗的风险无统计学相关性。
治疗组与未治疗组患者的多因素回归分析发现:TpTe≥120 ms、TpTe/QTc≥0.25、术前患者的室性心律失常病史、术后患者的心功能分级、术后患者的左心室的大小是CRT-D患者发生术后室性心律失常的危险因素,胺碘酮的使用是CRT-D术后室性心律失常的保护因素(P<0.05),β受体阻滞剂的使用在本研究中对于术后室性心律失常的发生无明显相关性(表2)。 在受试者工作曲线(ROC)中,TpTe/QTc ≥ 0.25 预测CRT-D患者室性心律失常风险的敏感性和特异性分别为47%和91%(图1),而TpTe≥120 ms预测CRT-D患者室性心律失常风险的敏感性和特异性分别为40%和95%(图2)。预测CRT-D术后患者生存曲线(Kaplan-Meier curves)分析表明,TpTe/QTc和TpTe均能有效预测患者的预后情况(P均<0.001,图3、4)。
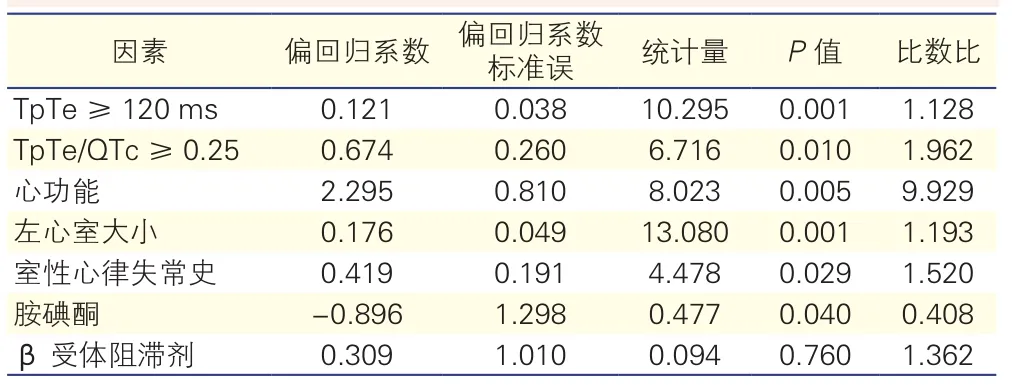
表2 心脏再同步治疗除颤器患者术后室性心律失常相关的多因素回归分析结果
3 讨论
目前室性心律失常风险的发生已被报道和TDR的增加存在相关性,对于存在快速室性心律失常风险的长QT综合征[10],Brugada综合征和肥厚性心肌病的患者[11、12],TDR预测室性心律失常发生具有相对较佳的敏感性及特异性。符合CRT-D植入适应症的患者同时也是快速室性心律失常发生的高危人群,本研究以CRT-D术后即刻心电图上TDR作为预测需治疗的室性心律失常的指标,结果表明QTc间期的差异与放电治疗无明显的相关性,TpTe和TpTe/QTc 与室性心律失常的发生和预后显著相关,即TpTe和TpTe/QTc的增加预示着CRT-D患者室性心律失常风险的增加。
Fish等[7]采用动脉灌注的犬左心室楔形标本同步记录了在心外膜与心内膜起搏时的跨壁心电图和内、中、外三层心肌细胞的跨膜动作电位。当由心内膜起搏调整至心外膜起搏时,TDR均显著增加,且同质心肌与异质心肌的跨室壁传导明显不同,异质化心肌(包括心内膜、心外膜及M心肌细胞) 的跨室壁激动会导致TDR延长,即心外膜除极和复极均比中层M细胞要早。心衰患者的心肌异质化非常明显,而部分缺血性心肌病患者在发展至心衰时,其心肌异质化更为明显[13]。有文献报道深层心外膜下存在阻抗屏障[14],导致心外膜起搏时心外膜与M区域额外的传导阻滞,并进一步导致TDR的增加。其机制在于,激动在心外膜与M细胞之间传递的时间在心外膜起搏时较心内膜起搏时更长,进一步导致M细胞复极延迟并致TDR增加。早先的相关研究预测TDR与CRT-D患者的放电治疗无明确的联系,目前已被证实是不准确的[15],TDR的延长和室性心律失常的发生存在着正相关性。本研究以走纸为25 mm/s的术后心电图的V5导联的数据分析确定了TpTe、TpTe/QTc对于预测放电治疗的预测价值,论证了TpTe≥120 ms及TpTe/QTc ≥ 0.25对于预测术后放电的价值,在以往的相关研究中,对于CRT-D患者中术后心电图中的V5导联的TpTe大于或等于其QTc间期的四分之一被认为是预测术后放电风险增加的较简单和直接的指标,但其准确性较差。本研究中TpTe与TpTe/QTc的预测价值虽然其敏感性并不是很高,但对于其较高的特异性预测价值可用于对CRT-D患者放电风险的评估参考。
TDR预测CRT-D术后快速室性心律失常的风险是否具有临床实用价值,能否在术后参数程控时进行优化,以减小TDR,降低快速室性心律失常的风险。Turkoglu等[16]的一系列报道阐明了上述可能性,对CRT-D 患者程控最优化的心室间期,也即最小化的TpTe,报道了两例以最优化TpTe间期治疗患者起搏器致室颤。但其临时实际应用价值有待更进一步的研究来明确。
总的来说,TpTe 和TpTe/QTc作为TDR在心电图上的指标,可有效预测CRT-D术后患者治疗风险,TpTe≥120 ms、TpTe/QTc ≥0.25均可作为需治疗的室性心律失常的危险因素。
局限性:首先,治疗组30例与未治疗组130例比较,表明QTc差异两组无显著性,可能与研究样本量偏小,随访时间相对较短有关,有待进一步研究明确。 其次,缺乏对患者植入CRT-D的应答性的亚组分析,相关研究发现对CRT-D应答的心衰患者,发生室性心律失常的风险明显减少,因此应对CRT-D有效患者进行亚组分析。
[1] Cazeau S, Leclercq C, Lavergne T, et al. Effects of multisite biventricular pacing in patients with heart failure and i ntraventricular conduction delay. N Engl J Med, 2001,344: 873-880.
[2] 李小鹰. 2010年慢性心力衰竭治疗进展. 中国循环杂志, 2011, 26: 81-83.
[3] Bradley DJ, Bradley EA, Baughman B, et al. Cardiac resynchronization and death from progressive heart failure: A meta-analysis of randomized controlled trials. JAMA, 2003, 289: 730-740.
[4] Carson P, Anand I, O' Connor C, et al. Mode of death in advanced heart failure the Comparison of Medical, Pacing, and Defibrillation T herapies in Heart Failure (COMPANION) Trial. J A m Coll C ardiol, 2005, 46: 2329-2334.
[5] Gasparini M, Lunati M, Landolina M, et al. Electrical storm in patients with biventricular implantable cardioverter defibrillator: Incidence, predictors, and prognostic implications. A m H eart J, 2008, 156: 847-854.
[6] Nayak HM, Verdino RJ, Russo AM, et al. Ventricular tachycardia storm after initiation of biventricular pacing: I ncidence, clinical characteristics, management, and outcome. J Cardiovasc Electrophysiol, 2007, 19: 708-715.
[7] Fish JM, DiDiego JM, N esterenko VV, et al. Epicardial activation of left ventricular wall prolongs QT interval and transmural dispersion of repolarization: Implications for biventricular pacing. Circulation, 2004, 109: 2136-2142.
[8] Medina-Ravell VA, Lankipalli RS, Yan GX, et al. Effect of epicardial or biventricular pacing to prolong QT interval and increase transmural dispersion of repolarization. Does resynchronization therapy pose a risk for patients predisposed to long QT or torsade de pointes? C irculation, 2003, 107: 740-746
[9] Bazett HC. An analysis of the time-relations of electrocardiograms. Heart J, 1920, 7: 353-370.
[10] Yamaguchi M, Shimizu M, Ino H, et al. T wave peak-to-end interval and QT dispersion in acquired long QT syndrome: A new index f or arrhythmogenicity. Clin Sci (Lond), 2003, 105: 671-676.
[11] Castro Hevia J, Antzelevitch C, Tornes B, et al. Tpeak-Tend and T peak-Tend dispersion as risk factors f or ventricular tachycardia/ ventricular fibrillation in patients with the Brugada syndrome. J Am Coll C ardiol, 2006, 47: 1828-1834.
[12] Shimizu M, Ino H, Okeie K, et al. T -peak t o T -end interval may be a better predictor of high-risk patients with hypertrophic cardiomyopathy associated with a cardiac troponin I mutation than QT dispersion. Clinical Cardiology, 2002, 25: 335-339.
[13] 毋健, 王坷. 左心室形态改变对心脏电机械同步性的影响. 中国循环杂志, 2007, 22: 133-135
[14] Fish JM, Brugada J, Antzeleviteh C. Potential proarrhythmie effects ofbiventrieular pacing. J Am Coll Cardiol, 2005, 46: 2340-2347.
[15] Dilaveris P, Giannopoulos G, Synetos A, et al. Effect of biventricular pacing on ventricular repolarization and functional indices in patients with heart failure: Lack of association with arrhythmic events. Europace, 2009, 11: 741-750.
[16] Turkoglu C, Aliyev F, Celiker C, et al. Optimization of repolarization during biventricular pacing: A new target in patients with biventricular devices? Ann Noninvasive Electrocardiol, 2010, 15: 36-42.
Predictive Value of Ventricular Transmural Dispersion of Repolarization on Rapid Ventricular Tachycardia Risk in Patients After Resynchronization
HE Jing, YAN Ji, XU Jian, SUN Xian-lin, SU Hao, YU Fei, CHEN Kuang-yu.
Department of Cardiology, Anhui Medical University Aff i liated Provincial Hospital, Hefei (230001), Anhui, China Corresponding Author: YAN Ji, Email: yanji111111@126.com
Objective: Cardiac resynchronization therapy defibrillator (CRT-D) increases ventricular transmural dispersion of repolarization (TDR). Our work evaluated the relationship between QTc interval of TDR indicators, TpTe, TpTe/QTc ratio and rapid ventricular arrhythmia in patients with CRT-D.Methods: A total of 160 consecutive patients who received CRT–D implantation in our hospital from 2011-01 to 2013-03 were studied. The immediate post operative ECG was collected to analyze lead V5QTc interval, TpTe and TpTe/QTc ratio for assessing its TDR. The patients were divided into 2 groups: Treatment group, the patients with ventricular tachycardia or ventricular fi brillation received CRT-D, n=30 (18.7%) and Non-treatments group, n=130 (81.3%). All patients were followedup for (20 ± 10) months and the rapid ventricular arrhythmia was recorded by CRT-D devices.Results: The patients in Treatment group had increased TpTe/QTc (0.24 ± 0.05) vs (0.20 ± 0.04, and TpTe (119 ± 30) ms vs (95 ± 20) ms, both P<0.001. The QTc interval was similar between 2 groups (480 ± 60) ms vs (470 ± 70) ms, P=0.6 and QTc interval was not related to the risk of CRT-D requirement. The sensitivity and specif i city for TpTe/QTc ≥ 0.25 predicting the risk of ventricular arrhythmia in CRT-D patients were at 47% and 91%, while TpTe ≥ 120 ms were at 40% and 95% respectively. The post CRT-D surviving curve analysis indicated that TpTe/QTc ratio and TpTe could predict the prognosis inrelevant patients, P<0.001.Conclusion: The elevated TpTe and TpTe/QT ratio may increase the incidence of CRT–D requirement in patients with ventricular arrhythmia after resynchronization.
Tp-Td interval; Transmural dispersion of repolarization; Cardiac resynchronization therapy def i brillator
2014-04-22)
(编辑:常文静)
2010年安徽省卫生厅医学科研重点项目(2010A002)
230001 安徽省合肥市,安徽医科大学附属省立医院 心血管病内科
何静 硕士研究生 研究方向为心律失常与心内电生理学 Email:282643224@qq.com 通讯作者: 严激 Email:yanji111111@126.com
R54
A
1000-3614(2014)10-0791-05
10.3969/j.issn.1000-3614.2014.10.009
方法:2011-01至2013-01连续选取160例于我院行CRT-D植入的患者,所选资料为术后即刻心电图,分析其V5导联的QTc间期,TpTe,TpTe/QTc值以评估其TDR,所有植入CRT-D患者均于我中心常规随访,随访时间为(20±10)个月。快速室性心律失常的发生均采自程控仪调取的CRT-D记录。
结果: 其中因持续性室性心动过速、心室颤动接受CRT-D治疗的患者为30例(治疗组,18.7%),未治疗的患者为未治疗组(130例,81.3%)。治疗组的TpTe/QTc ( 0.24±0.05 vs 0.20±0.04, P<0.001) 和 TpTe [(119±30) ms vs (95±20) ms, P<0.001 ]较未治疗组明显增加,但两组间QTc间期差异无统计学意义[(480±60)ms vs (470±70) ms,P=0.6]。QTc间期与CRT-D治疗的风险无相关性。TpTe/QTc ≥ 0.25 预测CRT-D患者室性心律失常风险的敏感性和特异性分别为47%和91%,而TpTe≥120 ms预测CRT-D患者室性心律失常风险的敏感性和特异性分别为40%和95%。CRT-D术后患者生存曲线分析表明,TpTe/QTc和TpTe均能有效预测患者的预后情况(P<0.001)。
结论:TpTe和TpTe/QTc 的增加显著增加再同步治疗除颤器患者术后需CRT-D治疗的风险。

