氧氟沙星混配金属配合物的合成与抑菌活性
张淑源,张 欣,张 华
(天津师范大学化学学院,天津300387)
喹诺酮类药物是应用于临床的一大类广谱、高效、低毒性的抗菌药物,该类药物以喹诺酮母核作为基本骨架.随着喹诺酮类药物的广泛应用,细菌对这类药物的耐药性也迅速产生并提高.20世纪无机药物的复兴,使得金属离子在病理过程中的作用倍显重要.目前对喹诺酮类药物金属配合物的研究是无机化学领域的重点,对该类化合物的生物活性进行研究,了解其在体内运输、转化和代谢的规律具有一定的应用价值[1].喹诺酮药物按照母环的不同进行分类,可以分为喹啉类(诺氟沙星)、吡啶并嘧啶类(吡哌酸)、1,8-萘啶类(萘啶酸、依诺沙星)、曾啉类(西诺沙星)等;按照喹诺酮构架中稠合环数目的不同进行分类,可分为二元环、三元环(如氧氟沙星)和多元环类[2-4].喹诺酮药物除了有抗菌活性外,有些喹诺酮药物还有其他功效,如抗肿瘤作用[5]和抗病毒作用[6],以及对心血管方面的活性[7]等.金属离子对喹诺酮类药物在体内的生物活性有重要影响,因此,近年来许多学者对喹诺酮与金属离子配位形成配合物的合成、结构、生物活性等进行了研究报道[8-10].
本课题组以氧氟沙星为母体,以吡啶衍生物(邻菲啰啉、2,9-二甲基-1,10-邻菲啰啉、2,2′-联吡啶、4,4′-二甲基-2,2′-联吡啶、8-羟基喹啉) 为辅助配体,合成了一些新的喹诺酮金属配合物.用红外光谱推测了配合物可能的结构.利用琼脂扩散法,在不同浓度下测定配体及其过渡金属配合物的抑菌活性.这些工作可以为进一步了解喹诺酮及其金属配合物的作用机制、药物的耐药性和毒性等提供参考.
1 实验
1.1 仪器与试剂
仪器:FT-IR型红外光谱仪(KBr压片法),由美国Varian公司生产.
试剂:2,2′-联吡啶、8-羟基喹啉,由天津市光复精细化工研究所生产;氧氟沙星,由上海楷洋生物技术有限公司生产,其基本骨架如图1所示;4,4′-二甲基-2,2′-联吡啶,由上海晶纯实业有限公司生产;邻菲啰啉,由北京芳草医药化工研制公司生产;2,9-二甲基-1,10-邻菲啰啉,由百灵威科技有限公司生产.所有试剂均为分析纯,高氯酸盐自制.
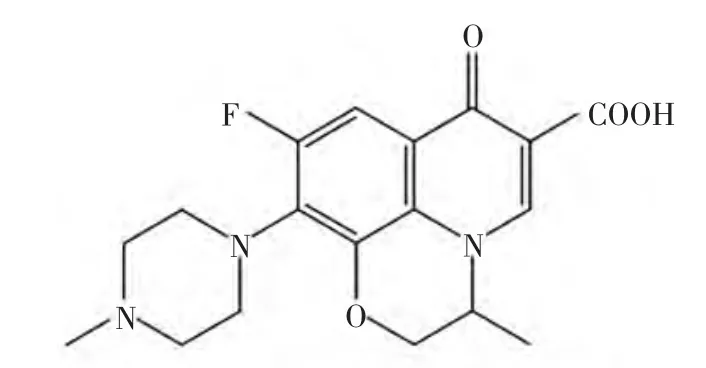
图1 氧氟沙星分子结构的基本骨架Fig.1 Basic skeleton of ofloxacin
1.2 实验方法
1.2.1 氧氟沙星和邻菲啰啉(8-羟基喹啉)金属配合物的合成
将金属高氯酸盐(1mmol)、氧氟沙星(1mmol)、邻菲啰啉(1mmol)或 8-羟基喹啉(1mmol)、氢氧化钠(1mmol)、乙醇和水(各12mL)放入25mL反应釜中,在温度为393 K下反应4d,然后缓慢冷却至室温.过滤后静置,有沉淀或晶体产生.用去离子水洗涤、干燥.
1.2.2 氧氟沙星和 2,9-二甲基-1,10-邻菲啰啉(2,2′-联吡啶、4,4′-二甲基-2,2′-联吡啶)金属配合物的合成
用少量蒸馏水溶解1mmol的金属高氯酸盐,用乙醇溶解 1mmol的 2,9-二甲基-1,10-邻菲啰啉(2,2′-联吡啶、4,4′-二甲基-2,2′-联吡啶),然后将二者混合,调pH至9.0左右.再用少量氢氧化钠溶液溶解1mmol氧氟沙星,将其缓慢滴入前者中,反应30min.调pH至6.0左右,加热回流8h,过滤,室温下静置挥发.有沉淀或晶体产生.用去离子水洗涤、干燥.
1.2.3 氧氟沙星混配金属配合物抑菌活性的测定
将保存于-80℃的大肠杆菌(Escherichia coli)(革兰氏阴性菌)和枯草芽孢杆菌(Bacillus subtilis)(革兰氏阳性菌)菌种接种于营养肉汤管内,37℃培养24h.将培养物接种于琼脂平板,从平板中挑选典型的单个菌落,接种于琼脂斜面,37℃培养24h.再转种斜面1次(37℃,24h).用生理盐水将菌落洗下,制成所需浓度的均匀菌液.
待测化合物配成质量浓度分别为20、40、60mg/L的溶液(用DMF[11]作溶剂),用注射器吸取配好的药液0.2mL,放入装有10个滤纸片的磨口称量瓶中(每个滤纸片上沾有药液0.02mL),于(37±1)℃恒温培养箱放置2d后取用.
将药皿片平铺于涂有菌液的培养皿上,每个三分线内加1个药皿片,平行3次.倒置培养皿于(37±1)℃恒温培养箱内,1d后用直尺量取抑菌环直径.
2 结果与讨论
2.1 氧氟沙星、辅助配体及金属配合物的红外光谱分析
为便于对结果进行描述,分别将氧氟沙星-邻菲啰啉金属配合物记为配合物Ⅰ,氧氟沙星-2,9-二甲基-1,10-邻菲啰啉金属配合物记为配合物Ⅱ,氧氟沙星-2,2′-联吡啶金属配合物记为配合物Ⅲ,氧氟沙星-4,4′-二甲基-2,2′-联吡啶金属配合物记为配合物Ⅳ,氧氟沙星-8-羟基喹啉金属配合物记为配合物Ⅴ.
配体氧氟沙星和配合物的红外光谱差异显著。氧氟沙星中1709cm-1处有一个=很强的吸收峰,该峰归属于氧氟沙星3位羧基上ν(C O)的吸收峰,在金属配合物中出现了2个强吸收峰(配合物Ⅰ为1622cm-1和 1474cm-1,Ⅱ为 1623 cm-1和 1476cm-1,Ⅲ为1628cm-1和 1473 cm-1,Ⅳ 为 1627cm-1和 1464cm-1,Ⅴ为 1623 cm-1和 1466cm-1),这 2个峰是 ν(COO-)的不对称伸缩振动吸收峰和对称伸缩振动吸收峰,其差值Δ约为148cm-1,表明羧基与=金属离子参与配位[12-13]。母环4位上酮基振动峰ν(CO)P发生转移,配合物Ⅰ中从氧氟沙星中的1621cm-1转移至1579cm-(1Ⅱ为1577cm-1、Ⅲ为1592cm-1、Ⅳ为1586cm-1、Ⅴ为1580cm-1),这是酮基与金属离子配位的结果。这些红外光谱数据的改变充分说明了氧氟沙星的3位羧基和4位酮基的氧与金属离子发生配位[14]。配合物Ⅰ的红外光谱在3 435cm-(1Ⅱ为3 421cm-1、Ⅲ为3 360cm-1、Ⅳ为 3 403 cm-1、Ⅴ为 3 427cm-1)处有一个宽并强的吸收峰,为配合物结晶水ν(O—H)的伸缩振动吸收峰[15]。
自由配体(邻菲啰啉、2,9-二甲基-1,10-邻菲啰啉、2,2′-联吡啶、4,4′-二甲基-2,2′-联吡啶、8-羟基喹啉)的面外弯曲振动峰位于853 cm-1和732cm-1附近,在配合物中辅助配体的环振动峰移至1517cm-1附近,为一强吸收峰,C—H面外弯曲振动峰在844cm-1和729cm-1附近处,这表明辅助配体参与配位[16]。在配合物的红外光谱中观测到自由ClO4-的特征振动峰(1102cm-1),未观察到ClO4-参与配位所显示的特征峰。这些结果与本课题组所做的晶体结构解析结果(待发表)一致。
2.2 抑菌活性的测定结果
以大肠杆菌和枯草芽胞杆菌为测试菌种,测定配体氧氟沙星、5种辅助配体及其过渡金属配合物在质量浓度分别为20、40、60mg/L时的抑菌能力.不同化合物在各浓度下的抑菌环直径如表1所示.
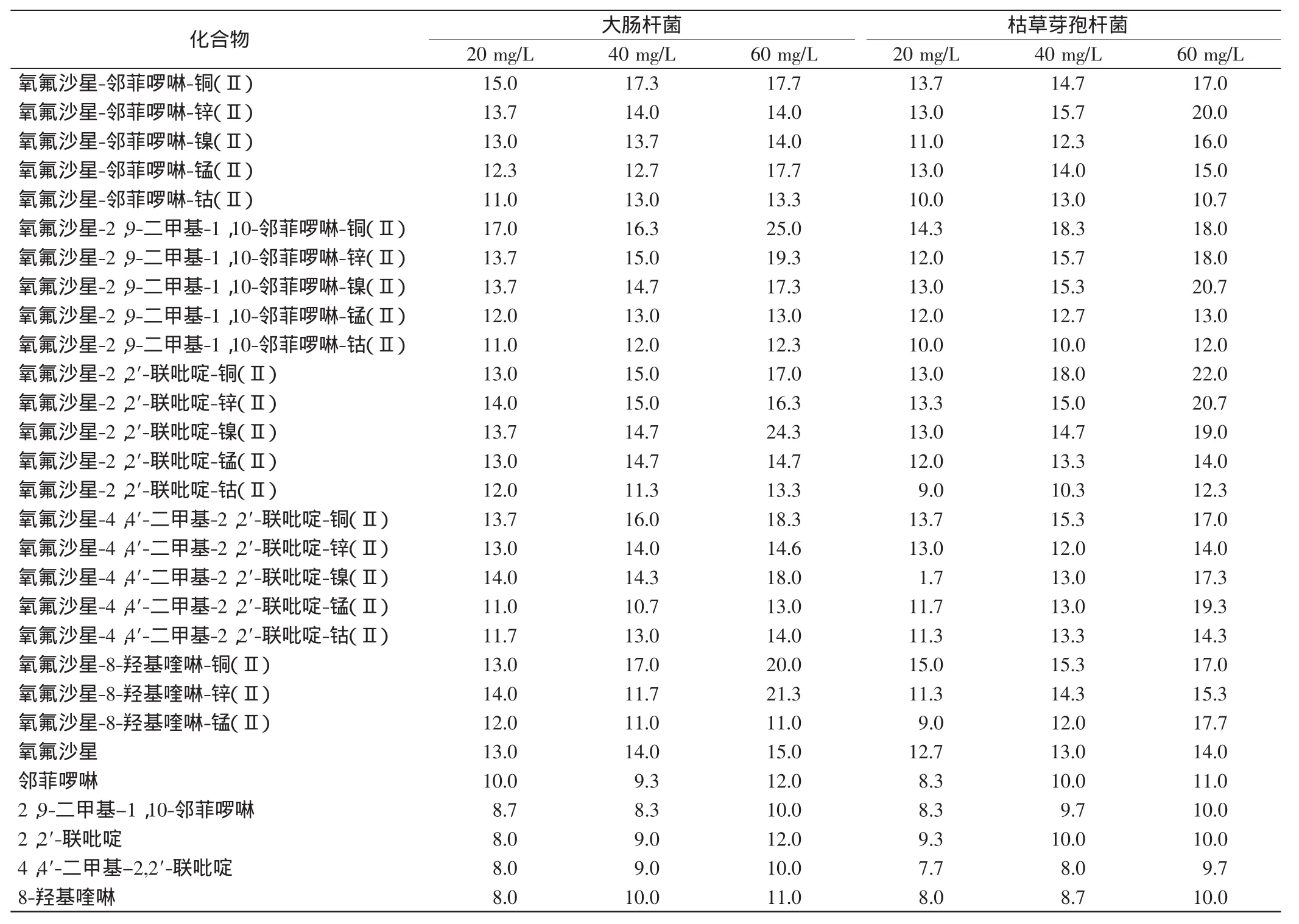
表1 化合物的抑菌活性Tab.1 Antibacterial activity of compounds mm
从表1可以看出,氧氟沙星、辅助配体及其过渡金属配合物对大肠杆菌和枯草芽孢杆菌的生长均有一定的抑制作用.总体上,随着浓度的增加化合物的抑菌效果增强.比较氧氟沙星的不同金属配合物,金属铜(Ⅱ)配合物对大肠杆菌和枯草芽孢杆菌的抑制作用普遍强于其他金属的配合物;其次是锌(Ⅱ)配合物.5种辅助配体对大肠杆菌和枯草芽孢杆菌的抑制作用相对较弱.化合物对大肠杆菌的抑制作用总体上强于枯草芽孢杆菌.
3 结论
本研究以氧氟沙星为母体,选择共面性好并能进行螯合的吡啶衍生物邻菲啰啉、2,9-二甲基-1,10-邻菲啰啉、2,2′-联吡啶、4,4′-二甲基-2,2′-联吡啶、8-羟基喹啉为辅助配体,合成了23种新的喹诺酮金属配合物,通过红外光谱方法推测了配合物可能的结构.利用琼脂扩散法,在不同浓度下对所有配体及配合物的抑菌活性进行测定.结果表明:氧氟沙星与其辅助配体形成的混配化合物对大肠杆菌和枯草芽孢杆菌均有一定的抑制作用,其中铜(Ⅱ)、锌(Ⅱ)和镍(Ⅱ)的金属配合物对这2种细菌的抑菌活性明显强于配体氧氟沙星,并且铜(Ⅱ)配合物的抑菌作用最强;而锰(Ⅱ)和钴(Ⅱ)的配合物对2种细菌的抑菌活性普遍等于或弱于氧氟沙星.在20、40、60mg/L这3个质量浓度下,大部分配合物随着浓度的增大抑菌活性增强.
[1] 冯连顺,刘明亮.喹诺酮类药物的结构修饰及“非经典”生物活性研究进展[J].国际药学研究杂志,2010,37(2):139-143.
[2]仉文升,李安良.药物化学[M].北京:高等教育出版社,2004.
[3] 李涛,颜少勇,陈伟进,等.抗肿瘤喹诺酮类药物的发现及其进展[J].国外医药:抗生素分册,2001,22(1):15-27.
[4] LIU Y J,CHAO H,TAN L F,et al.Interaction of polypyridyl ruthenium(II)complexcontainingasymmetricligandwithDNA[J].JInorg Biochem,2005,99(2):530-537.
[5]吕凯,冯连顺,刘明亮,等.喹诺酮抗肿瘤活性及构效关系研究进展[J].中国医药工业杂志,2010,41(6):456-463.
[6]刘又宁.氟喹诺酮类药物的临床应用价值[J].中华结核和呼吸杂志,2008,31(10):722-723.
[7]袁瑾懿,王明亮.氟喹诺酮类和严重心律失常危险:基于人群的研究[J].中国感染与化疗杂志,2013(6):449.
[8] 姜至杰,高春.降低喹诺酮类药物抗菌活性的金属离子筛选[J].西北药学杂志,2013,28(1):69-72.
[9] 郑智昌,雷霆雯.不同金属离子对洛美沙星吸收度的影响[J].国外医药:抗生素分册,1996,17(2):158.
[10]王国平,傅旭春,朱龙观.双核铜(Ⅱ)-氟喹诺酮-邻菲咯啉混配配合物的合成、晶体结构和抗肿瘤活性[J].无机化学学报,2003,19(9):1001-1005.
[11]王卫东,华雍.CuCl2在混合溶剂(DMF-H2O)中的热力学性质[J].吉首大学学报:自然科学版,2006,27(5):98-101.
[12]傅楚瑾,肖莹,吴凡.间-(β-羧基丁内酸胺)苯酚甲醛树脂对混合金属离子体系中Hg(Ⅱ)鳌合性能的测定[J].上海师范学院学报:自然科学版,1983(2):70-73.
[13]樊聪,华敏,陈争艳,等.间苯二甲酸和邻菲罗啉与Cd(Ⅱ)配位聚合物的合成、表征及晶体结构[J].化工技术与开发,2013,42(8):13-16.
[14]秦琳琳,阎雁.Meso-四(4-羧基苯基)卟啉及其金属配合物的合成及光谱性质研究[J].广东化工,2013,40(9):21-22.
[15]林国良,江智渊,洪满水.含羧基聚硅氧烷去除金属离子的研究[J].成都科技大学学报,1995(4):52-55.
[16]TARUSHI A,POLATOQLOU E,KLJUN J,et al.Interaction of Zn(Ⅱ)with quinolone drugs:structure and biological evaluation[J].Dlton Transactions,2011,40(37):9461-9473.

