石墨烯在化学储能中的研究进展
黄 澍,王 玮,王康丽,蒋 凯,程时杰
(1武汉工程大学材料科学与工程学院,湖北 武汉430073;2强电磁工程与新技术国家重点实验室,华中科技大学电气与电子工程学院,湖北 武汉430074;3材料成型与模具技术国家重点实验室,华中科技大学材料科学与工程学院,湖北 武汉430074)
在化石资源日渐减少、环境问题日益严重的今天,能源问题成为现阶段制约人类社会可持续发展的关键因素。实现可替代传统化石能源的可再生能源(如风能、太阳能等)的有效利用,是解决能源危机的重要手段。而大规模储能技术的引入将有效提高可再生能源发电的入网效率。同时,混合动力车和电动汽车的逐步市场化以及各种便携式用电装置的快速发展,均需要高效实用的电能存储系统。
优异的储能材料是储能系统的核心部分,而具有特殊结构的碳材料一直是储能材料大家族的重要成员,特别是2004年发现的石墨烯[1],它是一种由碳原子构成的单层片状结构的新材料,具有许多特殊的性质[2-3]。石墨烯强度达130 GPa,比钢高100倍,是目前强度最高的材料;热导率可达500 W/(m·K),是金刚石的3倍;载流子迁移率高达15000 cm2/(V·S),是商用硅片的10倍以上;石墨烯具有超大的比表面积(2630 m2/g)、室温量子霍尔效应和良好的铁磁性,是目前已知的在常温下导电性能最好的材料,电子在其中的运动速度远超过一般导体,达到了光速的1/300。石墨烯一经发现即毫无疑问地成为目前材料科学界的研究热点。它的出现彻底颠覆了70年前由Landau 和Peierls 提出的绝对二维晶体是热力学不稳定的且不可能存在的传统理论[4-5]。
石墨烯是由碳原子以sp2杂化连接的单原子层构成的新型二维原子晶体,其基本结构单元为有机材料中最稳定的六元环,理论厚度仅为0.34 nm,是迄今为止发现的最薄的二维材料,由于石墨烯结构的片段可以卷曲得到富勒烯、碳纳米管或者堆叠形成石墨,因此被认为是构建石墨、富勒烯、碳纳米管和石墨等碳材料的基本结构单元(图1)[6]。
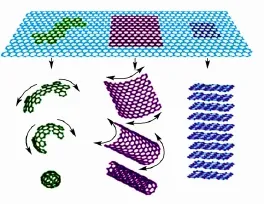
图1 石墨烯作为基本结构单元构成富勒烯、碳纳米管和石墨等碳材料的示意图[6]Fig.1 Schematic of graphene as the basic structural element of some carbon allotropes including fullerenes,carbon nanotubes and graphite[6]
目前,石墨烯制备的主要方法有机械剥离法[1]、晶体外延生长法[7]、化学气相沉积法[8]、氧化还原法[9]、碳纳米管剖开法[10]、电化学剥离法[11]。机械剥离法和化学气相沉积法可以获得有良好微观形貌的单层石墨烯,但制备方法复杂且仅能获得少量石墨烯,不适合石墨烯的大规模生产和应用。晶体外延生长法能够根据不同的条件制备得到单层或多层的石墨烯,但缺点在于对反应温度要求比较严格,并且较难将石墨烯片层转移到其它基体。氧化还原法成本低、产率高、利于工业化生产,但以有毒的肼作还原剂对环境有害。电化学剥离法可以快速、低成本制备石墨烯,但得到的产物绝大多数为多层结构,不易得到单层石墨烯。研究人员也在不断地对各种方法进行改进,或探索新的方法以期制备出质量更好且适合工业生产的石墨烯。
石墨烯是真正的表面性固体,理想的单层石墨烯具有超大的比表面积,是目前世界上最薄但也是最坚韧的纳米导电材料,其每个碳原子均为sp2杂化,并贡献剩余一个p 轨道上的电子形成大π键,π电子可以自由移动,这赋予石墨烯良好的导电性。在室温下石墨烯传递电子的速率比普通的导电材料快得多。这为其在储能领域的应用奠定了基础,近年来人们对它在多个化学储能领域中的应用进行了研究,如储氢、超级电容器、锂离子电池、锂硫电池和锂-空气电池等。
1 石墨烯在储氢中的应用
氢能以其资源丰富、零污染、可再生、热效率高等优点成为未来能源结构中最具发展潜力的能源载体,被誉为21世纪的绿色能源[12-13]。氢能的利用需要能量密度大、能耗少、安全性高的储运技术,其中衡量储氢性能的标准主要包括质量储氢密度和体积储氢密度。此外,充放氢的速率、可逆性以及循环使用寿命等参数也同样重要。
氢在常规条件下以气态形式存在,且易燃、易爆、易扩散,使得人们在实际应用中要重点考虑氢储存和运输过程中的安全、高效和无泄漏损失,这就给储存和运输带来很大的困难。吸附储氢是近年来出现的新型储氢方法。由于其具有安全可靠、储存容器重量轻、形状选择余地大和储存效率高等特点而成为当前储氢材料开发和研究的热点。碳质材料,尤其是具有大的比表面积、大的孔隙率的活性炭、碳纳米纤维、富勒烯及碳纳米管等,一直是储氢技术研究和开发的热门材料[14-17]。但已有的研究结果证明,活性炭、碳纳米纤维和富勒烯等碳材料在中高压、室温下的储氢性能均达不到美国能源部所提出的质量储氢密度不低于6.5%(质量分数)的目标[18]。碳纳米管虽然达到要求,但由于制备方法的多样、结构形貌的差异、处理方法和测试手段的不同,得到的实验数据离散性很大[19]。
在石墨烯出现之前,研究者一般认为碳基材料在室温、10 MPa 环境下实际储氢能力远低于1%(质量分数)。石墨烯问世以来,作为碳质材料的基本组成单元,相对于其它的储氢材料(如石墨、碳纳米管及传统的金属/合金等)而言,展现出更优异的储氢性能,众多国内外科学家都在积极发掘石墨烯及其复合结构的储氢潜能。Serguel 等[20]通过计算表明:具有多层和较大片层间距的石墨烯结构更有利于储氢。当石墨烯的片层间距达到6 Å(1Å=0.1nm)时,一层氢气分子可以安插在片层之间,形成“三明治”结构,可以达到2%~3%(质量分数)的储氢量。
Lin 等[21]采用从头算法在考虑化学吸附的情况下得到石墨烯的储氢量为7.7%(质量分数)。Ataca等[22]采用第一性原理平面波法计算得到掺入Ca 后,石墨烯的储氢量可达8.4%(质量分数)。Dimitmkakis等[23]利用石墨烯和碳纳米管设计了一个三维储氢模型,如果这种材料掺入Li+(图2),其在常压下储氢能力可以达41 g/L,数倍于一般碳材料。
目前,有关石墨烯储氢的实际研究结果与理论容量仍有一定距离。Chen 等[24]利用二维石墨烯片掺杂钯纳米颗粒后再混合活性炭受体,用作储氢材料。实验证明,这种材料在10 MPa 下储氢量为0.82%(质量分数),比不含石墨烯的钯材料提升了49%,而且此材料的吸附是高度可逆的。
石墨烯储氢性能好坏与其实际的比表面积大小和活性掺杂物等密切相关。探索不同的石墨烯制备工艺,对石墨烯进行有效掺杂/复合是以后石墨烯基储氢材料研究的重要方向。

图2 模拟锂离子掺杂3D 柱状结构石墨烯吸附氢分子(绿色代表氢原子,紫色代表锂原子)[23]Fig.2 Snapshot from the simulations of lithium dopedpillaredstructure(Hydrogen molecules are represented in green while lithium atoms are in purple)[23]
2 石墨烯在超级电容器中的应用
超级电容器按储能机理可分为双电层电容器和赝电容电容器。双电层电容器通过电极与电解质之间以静电方式聚集电荷形成的双电层来储存电能,电极材料主要是碳材料(如碳纳米管、碳气凝胶等);而赝电容电容器主要是在电极材料表面发生高度可逆的法拉第氧化还原反应,产生与电极充电电位有关的电容。赝电容电容器一般具有更大的比容量,主要电极材料为金属氧化物和导电聚合物。超级电容器功率密度大、循环寿命长、操作安全,是优秀的功率型储能系统[25-27]。
超级电容器的独立支撑电极需具有较高的力学强度和大的电容。如前所述,过渡金属氧化物、导电聚合物和具有高比表面积的碳基活性材料为常用的电极材料。而如表1所示,石墨烯与其它碳材料相比,比表面积大、电导率高、化学稳定性好,这些优良的性能使石墨烯及石墨烯基材料成为超级电容器电极材料有力的竞争者。石墨烯是完全离散的单层石墨材料,其整个表面可以形成双电层,但是在形成宏观聚集体过程中,石墨烯片层之间互相杂乱叠加,使得形成有效双电层的面积减少。如果其表面可以完全释放,则将获得远高于多孔炭的比容量。在石墨烯片层叠加而形成宏观聚集体的过程中,通过控制条件使其形成的孔隙集中在2.0 nm 以上,有利于电解液的扩散。而且其独特的二维结构使其不需要添加剂或黏结剂就能够通过控制微观结构自组装成三维宏观结构而直接用于超级电容器[28]。
石墨烯超级电容器的比容量与石墨烯材料的有效比表面积和孔径分布有关。纯石墨烯在无机电解液中的比容量一般为100~200 F/g,在有机电解液和离子液体中则相对偏低。通过适当的活化改性处理,可以改善石墨烯的电化学性能。单一石墨烯制成的电极材料往往很难将它的优异性能完全体现[29-30],因此研究者们还将导电聚合物[31]、金属氧化物[32]、其它碳材料[33]等均匀分散于石墨烯表面,在石墨烯片层间形成阻隔,防止其重新聚集,从而提高石墨烯的有效比表面积和比容量。
Li 等[34]在石墨烯片上进行原位阳极电聚合生成聚苯胺,得到的复合材料抗张强度达到12.6 MPa,有高而稳定的电化学电容(质量比容量为233 F/g,体积比容量为135 F/cm3),超过现在许多其它可用的碳基柔性电极,因此在柔性超级电容器方面有很大应用前景。
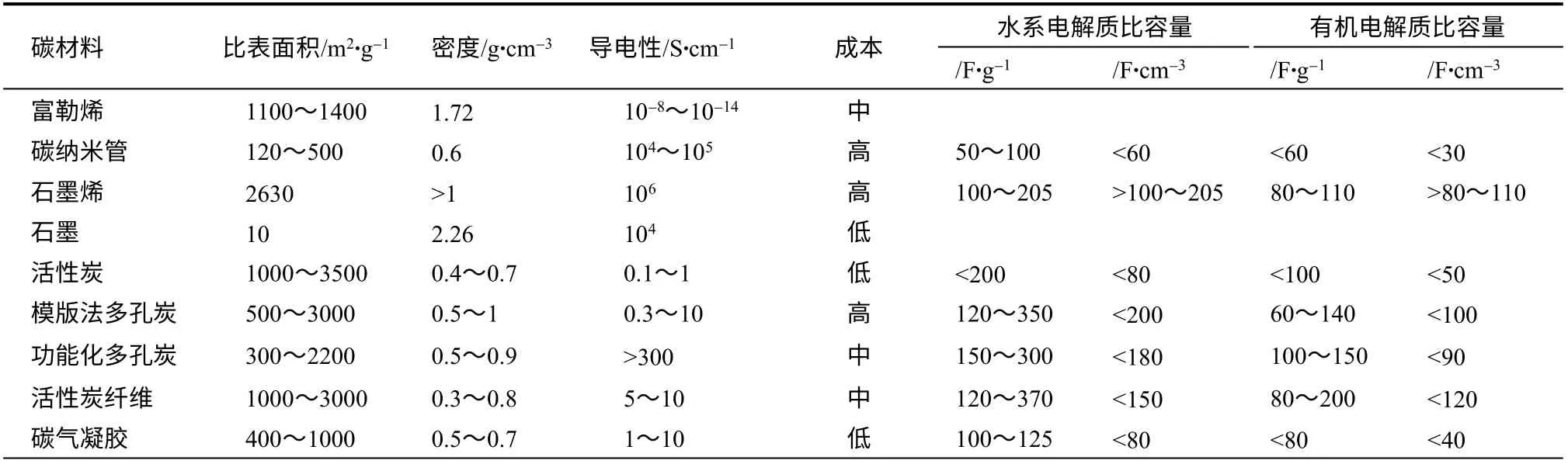
表1 超级电容器各种碳材料的比较[36]Table 1 Comparison of various carbon electrode materials for supercapacitors[36]
MnO2作为一种价格低、可广泛采用的金属氧化物材料,不需要使用强酸强碱电解质,中性电解质即可,因而环境友好、安全方便;此外,纳米MnO2电化学活性较高,因此石墨烯与MnO2复合材料的研究获得大量关注。Fan 等[35]将KMnO4与石墨烯混合,利用微波辐射的方法将KMnO4还原成MnO2,还原成的MnO2沉积在石墨烯表面,这样的复合材料作阳极,活性炭作阴极得到比容量为114 F/g 的超级电容器。利用微波辐射的方法,Yan等[37]把MnO2自沉积在石墨烯表面形成MnO2/石墨烯复合材料。在2 mV/s 下比容量达到310 F/g,是纯石墨烯的3倍。而且在比较大的扫描速率范围内仍能保持很高的电容保留率(在100 mV/s 下达到88%,500 mV/s 下达到74%)。Peng 等[38]则在这些基础上将MnO2纳米片与石墨烯混合制成柔性平面超级电容器(图3)。这种平面结构不仅引入更多的电化学表面吸附/解析电解液离子,而且提供更多的界面用于充放电过程中电荷的传输。其电化学比容量可达到233 F/g,7000 次充放电循环后仍可保持92%的容量。
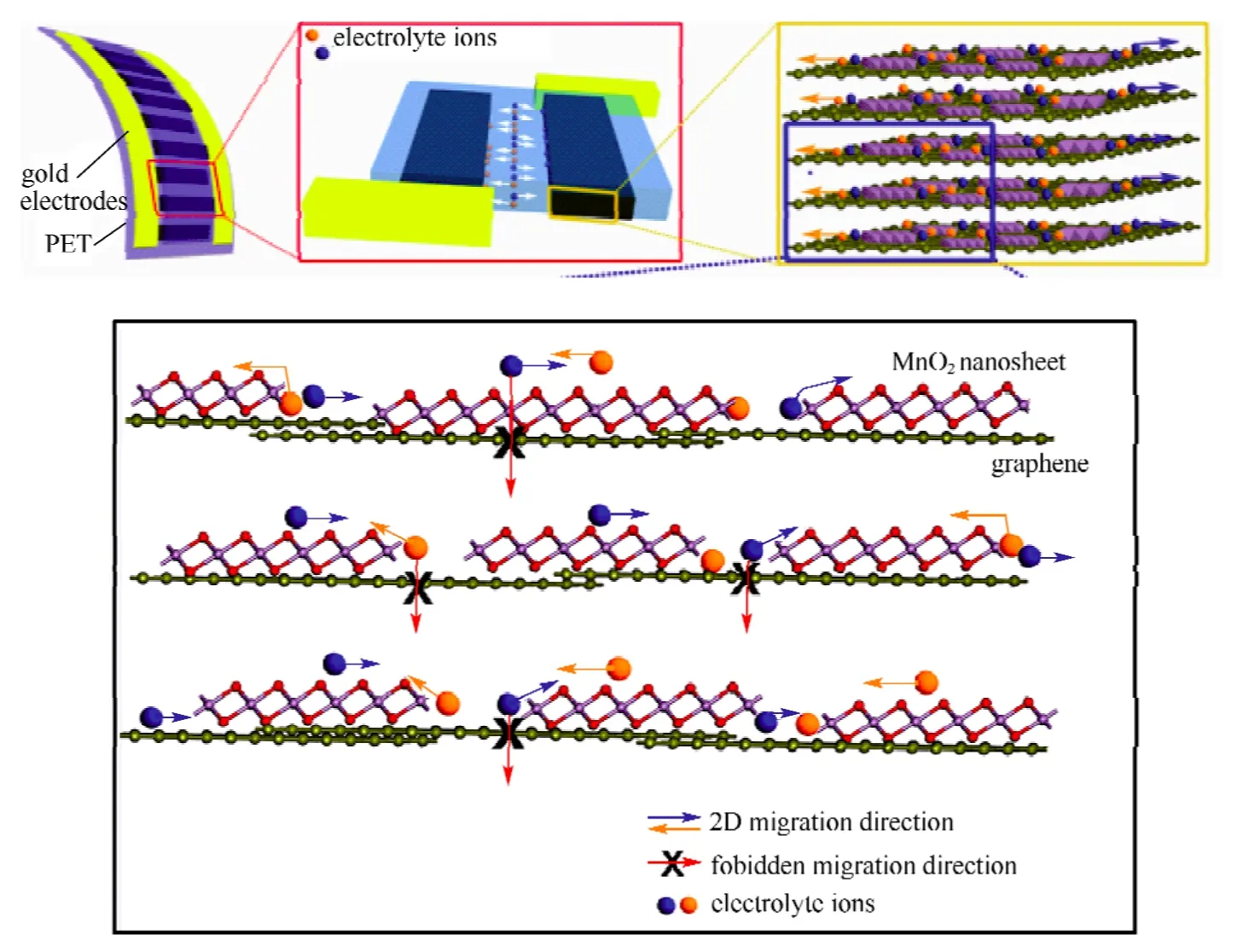
图3 以δ-MnO2/石墨烯混合结构为基础的柔性平面超级电容器[38]Fig.3 Design of hybrid δ-MnO2/graphene structures based flexible planar supercapacitors[38]
石墨烯以其独特的二维结构可与其它材料组成三维导电网络。Fan 等[39]利用CVD 法将石墨烯和碳纳米管成功合成了Dimitmkakis 等[23]所模拟的三维结构并用于超级电容器中。虽然存在石墨层与催化剂表面的润湿性较差导致碳纳米管在石墨上生长的一致性较差的问题,但在扫速10 mV/s 下最大比容量仍能达到385 F/g。这种结构不但能在氧化还原过程中提供巨大的缓冲空间,同时能增加石墨烯表面的扩散路径,形成电子传输的三维网络。
石墨烯本身有很强的团聚趋势,会影响电容器的能量储存和循环寿命。Dong 等[40]制备出分层结构的石墨烯材料用于改善超级电容器的性能,其比容量接近单层石墨烯理论值。将其与聚苯胺纳米棒复合后复合电极比容量高达763 F/g。
目前,大多数观点认为化学法还原氧化石墨烯都需要在高温环境下进行,但Lü等[41]成功地在真空环境中、远比理论临界剥离温度[42]低的温度(200℃)下制得石墨烯,原理如图4所示。这种方法得到的石墨烯比高温法制得的石墨烯比容量更高,达到了279 F/g。
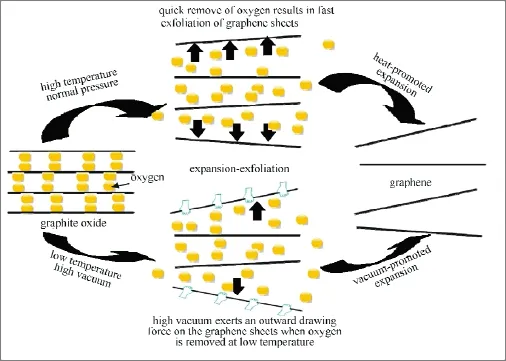
图4 石墨烯化学剥离示意图[41][(顶部)大气压下高温(约1000 ℃)剥离;(底部)低温(约200 ℃)高真空剥离]Fig.4 Schematic representation of chemical exfoliation of graphenes. High-temperature(above 1000 ℃)exfoliation under an atmosphericpressure (top);Low-temperature(as low as 200 ℃)exfoliation under high vacuum(bottom)[41]
石墨烯是制作高效、高能、柔韧和微型超级电容器很有潜力的材料。实现石墨烯高的有效比表面积和优良导电性能是实现其在超级电容器中应用的前提。目前,石墨烯和金属氧化物、导电聚合物复合材料的研究进展迅速,但仍限于实验室研究,还没有理想的大规模制备高质量石墨烯及其复合材料的方法,也较少考虑石墨烯基超级电容器的体积比性能,对其元件性能的研究和报道尚未形成统一的标准。
3 石墨烯在锂离子电池中的应用
锂离子电池具有电压高、比能量高、无记忆效应、循环寿命长、无环境污染等特点,被广泛应用于移动电话、笔记本电脑和其它便携式电子设备中[43-44]。碳/石墨材料是最早应用于锂离子电池的材料,也是目前已经商业化使用的负极材料,其价格便宜、来源丰富、能提供低而平稳的工作电压且性能稳定[45-46]。但其比容量较小,每6个C 与1个Li+形成LiC6结构存储Li+,理论比容量为372 mA·h/g。为了满足对锂离子电池能量密度越来越高的要求,人们一直在尝试寻找新的电极材料。自石墨烯被成功制备以来,与石墨、炭黑、碳纳米管等其它碳基材料相比,其片层具有的柔性和可控性,为构筑新的纳米结构提供了机会,能够更有效地改善活性材料的电化学性能[47]。石墨烯以无序松散的方式聚集,这种结构有利于Li+的插入,在片层两面都能储存Li+,形成Li2C6结构,理论容量(744 mA·h/g)明显提高[48-49]。研究者通过分子轨道理论计算发现,0.7 nm 的石墨片层间距是储Li 的最佳层间距,该层间距也能有效防止电解质进入片层间而发生形成SEI 膜(固体电解质界面膜)的不可逆反应。同时,石墨烯自然聚集形成的皱褶表面也为Li+提供了额外的存储空间。此外,采用电导率很高的石墨烯作为锂离子电池负极材料时,Li+在石墨烯材料中的扩散路径比较短,可以很大程度地提高其倍率性能。因此,石墨烯是一类具有应用前景的锂离子电池负极材料[50]。但石墨烯负极材料受到首周库仑效率低、充放电平台较高等缺点的制约[51-52],导致其并不能替代传统石墨直接作为负极材料使用。如何有效地调控石墨烯的组装与立体结构[53],使其形成良好的电子与离子传输通道将是构建高性能电极材料的关键。与此同时,通过化学方法在石墨烯结构中引入其它的活性位点或活性物质,进而实现化学储锂与物理储锂的有机结合则是另一个有前景的研究方向。
许多金属和金属氧化物具有很高的理论比容量,是锂电池负极材料的研究热点。借助石墨烯的高电子导电性和高力学强度,将石墨烯与金属或金属氧化物复合,有望克服这类材料充放电过程中体积变化大和导电性差的缺点,实现锂离子电池负极材料的变革。石墨烯复合电极负极材料中,有关Sn[54]、Sb[55]、Si[56]、Co3O4[57]、Fe3O4[58]、TiO2[59]、SnO2[60]、Mn3O4[61]的研究成果显著。
Sn 的金属氧化物SnO2因具有较高的理论容量(790 mA·h/g)成为研究石墨烯包覆金属氧化物的热点材料之一。为了改善纳米颗粒在石墨烯表面的分散情况,Wang 等[62]利用SnCl2与氧化石墨烯之间的原位氧化还原反应,结合喷雾干燥法制备SnO2/石墨烯复合材料。通过该方法制备的石墨烯含量仅为2.4%(质量分数)的复合材料,具有良好的分散效果,在67 mA/g 电流密度下脱Li,比容量可稳定在840 mA·h/g。
Wang 等[63]为了定向控制纳米颗粒在石墨烯表面的排布,利用三元自组装技术,以石墨烯为基底,表面活性剂作为分子模板,构造指定的金属氧化物/石墨烯复合材料,获得了稳定的、有序交替堆叠的纳米金属氧化物与石墨烯的复合材料,如图5所示。这种方法获得的SnO2与石墨烯的复合电极能达到760 mA·h/g,接近理论能量密度,且在120个循环后基本没有容量损失。
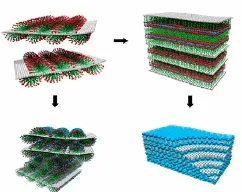
图5 表面活性剂辅助石墨烯-SnO2 层自组装制备三元有序纳米复合材料[63]Fig.5 Schematic illustrations of the ternary self-assembly approach to ordered graphene-tin oxide nano-composites[63]
Wang 等[64]结合水热合成的两步法将Mn3O4与石墨烯有效复合,所得的复合材料在低电流密度下(40 mA/g)脱Li 比容量约为900 mA·h/g,接近理论容量936 mA·h/g,并且材料的高倍率性能好,电流密度达到1600 mA/g 时,比容量仍保持在390 mA·h/g左右。
以多孔MgO 为模板,Fan 等[65]利用CVD 的方法合成出多孔石墨烯。此材料Raman 峰强度比ID/IG明显大于其它已知的大部分石墨烯材料,具有高度无序结构[66],所以该复合材料作为锂离子电池负极材料具有较高的可逆容量及较好的倍率特性。
为了改善Fe3O4的循环性能,Wei 等[67]利用石墨烯与Fe3O4纳米微球交联在一起形成3D 石墨烯泡沫结构,把Fe3O4用石墨烯片包裹起来抑制其在充放电过程中的体积形变。85 次循环后容量达到1060 mA·h/g,在150个循环后容量仍保持在1059 mA·h/g。
Sn 基、Si 基和过渡金属类负极材料与石墨烯的复合材料已得到广泛深入研究。制备方法也由最初的简单机械混合发展到能很好地控制材料微观形貌结构的原位反应、界面反应等方法。但为了能够满足在实际运用中对电池循环寿命、快速大电流充放电、高比容量等的需求,研究出能获得微观形貌良好可控的复合材料的简便制备方法,是石墨烯在锂离子电池中进一步应用的关键。
就锂离子电池体系而言,正极材料的导电性是限制电池性能的重要因素。许多正极材料的实际容量远低于理论容量,特别是在大电流充放电时其比容量迅速下降。加入电子导电性强的石墨烯,减少了电极活性材料与电解质之间的界面电阻,有利于Li+传导[68];同时,石墨烯片层包覆在电极材料表面抑制了金属氧化物的溶解和相变,保持了充放电过程中电极材料的结构稳定[69]。因此将石墨烯引入到正极材料中作为正极集流体的涂覆层以及正极的导电添加剂,既保证了电极材料高的活性表面积,又可提高电极的导电性,从而有效改善倍率性能,具有很好的应用前景。
4 锂硫电池
锂硫电池是目前锂电池中的研究热点。由于单质硫具有多电子还原反应的电化学性能,而且硫元素的相对原子质量较小,因此其理论比容量可达到1675 mA·h/g,与锂组装成电池,理论比能量可达2600 W·h/kg,它的工作电压在2.1 V 左右,能满足多种场合的应用需求,符合电动汽车对电池的要求,也符合便携式电子产品对电池“轻、薄、小”的要求,而且S 具有来源广泛(成本低)、无毒(无污染)、耐过充能力强等特点。但S 自身导电性差,反应会产生聚硫化物,聚硫化物在充放电过程中很容易溶解到有机电解液中,导致在循环过程中活性材料不可避免地损失,充放电中S 与Li6S 体积的形变破坏电极结构的稳定性,从而使其循环寿命不尽人意。
为了达到锂硫电池应用的目标,一要提高正极材料的导电性;二要控制材料容量的衰减,改进电池的循环性能。研究者发现石墨烯的加入可以很好地改善锂硫电池低导电性、体积膨胀和聚硫产物流失的问题。石墨烯可以有效地固定住S 以降低穿梭效应,在大电流放电时,可以为电极的体积膨胀提供缓冲,从而提升锂硫电池的循环效率和大电流放电性能[70]。
Wang 等[71]为了将石墨烯用于提升锂硫电池硫正极的电化学性能,他们将石墨烯纳米片与单质硫混合后加热制得硫/石墨烯复合材料。通过 SEM 和EDS 测试分析发现,硫颗粒均匀包覆在石墨烯片层表面。循环充放电测试表明,含有硫/石墨烯复合材料的正极放电比容量和循环稳定性均高于普通硫正极。Cao 等[72]合成了一种层状石墨烯/硫复合材料作为锂硫电池的正极材料。这种复合材料是由一层石墨烯一层硫层状堆积起来的三维三明治结构。该复合材料在1 C 的放电倍率下可逆比容量约为 505 mA·h/g。在它的外层包覆一层全氟磺酸薄膜能吸附反应生成的聚硫化物,提高电池的循环稳定性,循环100 次后电池的比容量保持在75%以上,而且此复合材料硫含量高达70%(质量分数)。
Zhou 等[73]尝试在S 的表面涂覆石墨烯做成正极材料,以改善锂硫电池的性能。比较如图6所示的4 种电极材料后发现,用石墨烯/硫+石墨烯-隔膜的组合在1.5 A/g的电流密度下能达到1000 mA·h/g 的容量,并且在300 次循环后电池容量仍能保持在97%。
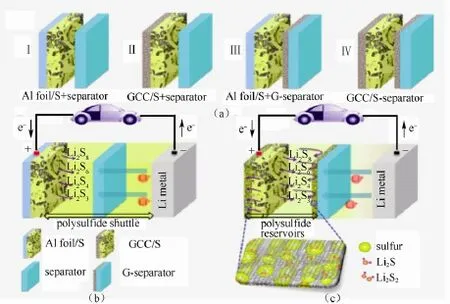
图6 (a)复合电极示意图;(b)用I 复合电极的锂硫电池示意图;(c)用IV 复合电极的锂硫电池示意图[72]Fig.6 (a)Schematic of electrode configurations;(b)Schematic of a Li-S battery with electrode configuration I;(c)Schematic of a Li-S battery with electrode configuration IV[72]
锂硫电池在低温环境下性能会受到极大影响,Huang 等[74]利用分层多孔石墨烯作为骨架包裹S 制备的锂硫电池在-40 ℃时仍能保持386 mA·h/g 的放电性能,其原理如图7所示。
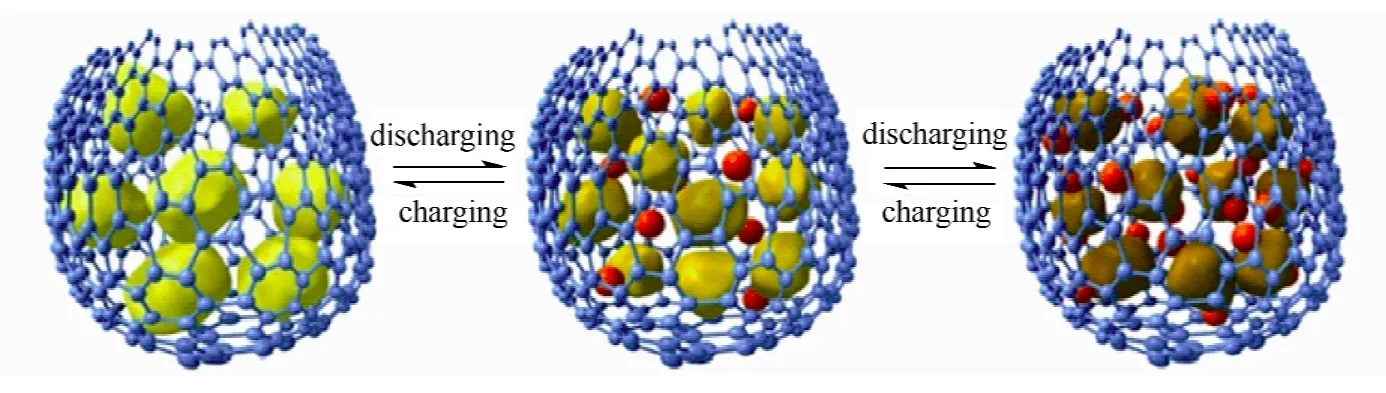
图7 石墨烯作为骨架截留硫的锂硫电池充放电过程示意图[73]Fig.7 Schematic illustration of entrapment of sulfur in graphene support for lithium-sulfur batteries during the charging-discharging processes[73]
Zhou 等[75]用纤维混合石墨烯和S 制备的锂硫电池电极是极高的多孔结构,并且可以利用切片的方式直接获得锂硫电池电极。为了减少聚硫物质溶解造成硫电极的损耗,Ji 等[76]把S 涂覆在氧化石墨烯的表面,在155 ℃烧结12 h,S 熔化并且扩散到氧化石墨烯的孔内,容量达到950~1400 mA·h/g,在50 次充放电循环后容量仍能保持在95%。
锂硫电池虽然获得一定的进展,但仍面临许多挑战,提高电极中含S 量和振实密度是实现高能量密度的基础,但S 和石墨烯的密度都较低,对体积能量密度影响不利。而且相对于传统电池材料,硫电极反应更为复杂,目前锂硫电池的反应机理仍不明确,石墨烯在锂硫电池中所能扮演的角色仍需要进一步地探索。
5 锂-空气电池
锂-空气电池作为理想的高比能量化学电源,成为近年来的研究热点。锂空电池[77]具有极高的理论比容量3828 mA·h/g 和理论比能量11425 W·h/kg(有机体系,不含氧气质量)。
Abraham 等[78]于1996年报道了非水溶性电解质锂-空气电池。有别于常规的水溶性电解质电池体系,使用有机电解液或全固态电解质的锂-空气电池是一种全新的金属空气电池,其反应机理如下。
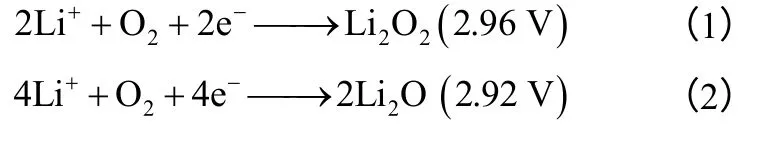
但目前该电池的研究工作正处于起步阶段,有许多基础问题需要研究。其中,适合长寿命高功率锂-空气电池使用的高效空气电极的开发,是发展锂-空气电池的重要课题。
空气电极作为锂-空气电池的研究热点,不仅是因为它主要贡献着电池的能量密度,也因为它直接影响了电池的输出电压/输出功率。早期开发出的混合电解液的锂-空气电池一直使用固定了催化剂的空气电极,这种空气电极是以高温烧结制作出来的贵金属或贵金属合金等的超微颗粒催化剂为基础,由具有高比表面积的碳材料用黏结剂粘结的混合催化剂层及疏水处理过的空气扩散层组成,其制作工艺非常复杂,成本很高。用性能相当或更好的廉价材料取而代之是空气电极走向实用化的关键,而石墨烯的发现给空气电极材料带来了新的选择[79]。石墨烯具有将空气中的氧还原的催化效果,以此特征为出发点,以石墨烯作为空气电极,金属Li 为负极,使用混合电解液(有机电解液/固体电解质/水溶性电解液)进行组合,开发出具有金属Li/有机电解液/固体电解质/水溶性电解液/石墨烯空气电极结构的锂-空气电池。结构如图8所示[80]。
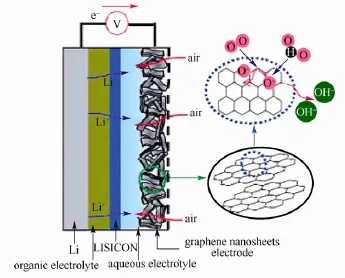
图8 石墨烯电极用于锂-空气电池的结构和实验原理图[79]Fig.8 Schematic showing the structure of a rechargeable Li-air cell based on a GNSs electrode[79]
目前,石墨烯电极用于锂-空气电池领域的研究已经取得了一定的进展。石墨烯作为催化剂或催化剂基底在锂-空气电池中表现出良好的潜能,其巨大的比表面积提升了锂-空气电池的放电容量。作为催化剂使用可以有效提升锂-空气电池的循环性能;作为催化剂基底,可以在其表面牢固黏附催化剂。石墨烯同时还可以有效地降低锂-空气电池的过电位。
Sun 等[81]把石墨纳米片作为阴极催化剂加入锂-空气电池中,发现这种电极比伏尔甘XC-72 碳材料拥有更好的循环性能和更低的过电位。Zhang 等[82]制备一种石墨烯泡沫作为锂-空气电池的空气电极。首先通过电化学法由石墨纸得到表面缺陷的石墨烯泡沫,然后在惰性气氛中退火以修复石墨烯泡沫结构的表面缺陷。这种石墨烯泡沫由1~10 μm 宽、1~2 nm 厚的巨大超薄石墨烯片层3D 堆叠组成。测试其在锂-空气电池中20 圈后循环效率能达到80%,放电电压稳定在2.8 V。
Xiao 等[83]制备的分层次多孔石墨烯,利用其独特的多孔结构,提高了电极中O2扩散,从而获得15000 mA·h/g 的优良性能。为了探讨石墨烯在锂-空气电池中的作用机理,Yoo 等[84]分别将石墨烯纳米片和热处理后的石墨烯纳米片用于锂-空气电池中的电极,发现热处理后的石墨烯展现出更稳定的循环性能。分析其原因可能是由于热处理后石墨烯表面的结晶化造成sp3/sp2比例的降低,减少了石墨烯的缺陷,或是由于热处理去除了石墨烯表面的官能团从而阻止了其在放电过程中被氧原子氧化。
随着储能领域的发展(如电动汽车和智能电网),锂-空气电池以其巨大的潜力被认为是下一代新电池技术,我们需要深入探索石墨烯在锂-空气电池中的应用及其作用机制,进一步提高锂-空气电池的效率和循环性能,推动其实用化。
6 结 语
新型储能材料的研究和开发是发展高效储能技术的关键。石墨烯是以sp2杂化为基元结构的真正表面性固体碳质材料,具有优异的储能性质,展现出良好的应用前景。
目前,石墨烯的应用可以分为两类:石墨烯的直接应用和石墨烯复合材料的应用,有关石墨烯基储能材料的研究尚待深入。现阶段,有关石墨烯储能材料的研究重点将集中在以下几个方面。
(1)探索操作简单、产量较高和成本低廉的高质量石墨烯制备方法,并实现对石墨烯的可控制备。
(2)研究石墨烯的尺寸、结构、缺陷以及孔径等对(电)化学性能的影响。通过对石墨烯进行有效地掺杂和化学修饰功能化,优化与其它类型的电极材料的复合,进一步提高石墨烯基电极材料的性能。
(3)在对石墨烯材料一系列重要物性进行研究的基础上,设计和开发新构型、新理念的高性能石墨烯基储能元件。
[1] Novoselov K S,Geim A K,Morozov S V,et al.Electric field effect in atomically thin carbon films[J].Science,2004,306:666-671.
[2] Lee C G,Wei X D,Kysar J W,et al. Measurement of the elastic properties and intrinsic strength of monolayer graphene[J]. Science,2008,321:385-388.
[3] Balandin A A,Ghosh S,Bao W Z,et al. Superior thermal conductivity of single-layer graphene[J]. Nano Lett.,2008,8:902-907.
[4] Peierls R E. Quelquesproprietiestypiques des corpses solides[J]. Ann.Inst.Henri Poincare,1935,5:177-222.
[5] Landau L D. Zur theorie der phasenumwandlungen II[J]. Phys. Z.Sowjetunion,1937,11:26-35.
[6] Geim A K,Novoselov K S. The rise of graphene[J]. Nat. Mater.,2007,6:183-191.
[7] Berger C,Song Z M,Li X B,et al. Electronic confinement and coherence in patterned epitaxial graphene[J]. Science,2006,312(5777):1191-1196.
[8] Wei D,Liu Y,Zhang H,Huang L,Wu B,Chen J,Yu G.Scalable synthesis of few-layer graphene ribbons with controlled morphologies by a template method and their applications in nanoelectromechanical switches[J]. J. Am. Chem. Soc.,2009,131(31):11147-11154.
[9] Dreyer D R,Park S,Bielawski C W,et al.The chemistry of graphene oxide[J].Chem.Soc.Rev.,2010,39(1):228-241.
[10] Xu E,Wei J,Wang K,et al.Doped carbon nanotube array with a gradient of nitrogen concentration[J]. Carbon,2010,48(11):3097-3102.
[11] Wei D,Grande L,Chundi V,et al.Graphene from electrochemical exfoliation and its direct applications in enhanced energy storage devices[J].Chem.Commun.,2012,48(9):1239-1241.
[12] Schlapbach L,Zuttel A. Hydrogen-storage materials for mobile application[J]. Nature,2001,414:353-358.
[13] Turner J A.Sustainable hydrogen production[J]. Science,2004,305(5686):972-974.
[14] Zhou L,Zhou Y P,Sun Y. A comparative study of hydrogen adsorption on super activated carbon versus carbon nanotubes[J]. Int.J.Hydrog.Energy,2004,29(5):475-479.
[15] Frost H , Snurr R Q. Design requirements for metal-organic frameworks as hydrogen storage materials[J]. J. Phys. Chem. C.,2007,111(50):18794-18803.
[16] Li Q,Park O K,Lee J H.Positive temperature coefficient behavior of HDPE/EVA blends filled with carbon black[J]. Adv. Mater. Res.,2009,79(1/2):2267-2270.
[17] Yildirim T,Ciraci S. Titanium-decorated carbon nanotubes as a potential high-capacity hydrogen storage medium[J]. Phys. Rev.Lett.,2005,94(17):175501-175504.
[18] DOE targets for onboard hydrogen storage systems for light-duty vehicles[EB/OL].http://www.eere.energy.gov/hydrogen and fuel cells/storage/pdfs/targets on board hydro storage explanation.pdf,2009,09.
[19] Zhou L,Zhou Y,Sun Y. Enhanced storage of hydrogen at the temperature of liquid nitrogen[J]. Int.J.Hydrog.Energy,2004,29:319-322.
[20] Serguel P,Tse J S,Yurchenko S N,et al.Graphene nanostructures as tunable storage media for molecular hydrogen[J]. Acad. Sci.USA,2005,102(30):10439-10444.
[21] Lin Y,Ding F,Yakobson B I. Hydrogen storage by spillover on grapheneasa phase nucleation process[J]. Physical Review B,2008,78:041402(R).
[22] Ataca C,Aktürk E,Ciraci S. Hydrogen storageof calcium atoms adsorbed on graphene:First-principles plane wave calculations[J].Physical Review B,2009,79(4):041406(R).
[23] Dimitrakakis G K,Tylianakis E,Froudakis G E,et al. Pillared graphene:A new 3-D network nanostructure for enhanced hydrogen storage[J]. Nano Lett.,2008,8(10):3166-3170.
[24] Chen C H,Chung T Y,Shen C C,et al. Hydrogen storage performance in palladium doped graphene/carbon composites[J]. Int.J.Hydrog.Energy,2013,38:3681-3688.
[25] Simon P,Gogotsi Y.Materials for electrochemical capacitors[J]. Nat.Mater.,2008,7:845-854.
[26] Sharma P,Bhatti T S. A review on electrochemical double-layer capacitors[J].Energy Conv.Manag.,2010,51(12):2901-2912.
[27] Inagaki M,Konno H,Tanaike O.Carbon materials for electrochemical capacitors[J].J.Power Sources,2010,195(24):7880-7903.
[28] Chen J,Li C,Shi G Q. Graphene materials for electrochemical capacitors[J].J.Phys.Chem.Lett.,2013,4:1244-1253.
[29] Stolter M D,Park S,Zhu Y,et al.Graphene-based ultracapacitors[J].Nano Lett.,2008,8:3498-3502.
[30] Vivekchand S R C,Route C S,Subrahmanyam K S,et al.Graphene-based electrochemical supercapacitors[J]. J. Chem. Sci.,2008,120(1):9-13.
[31] Li J,Xie H Q,Li Y,et a1.Electrochemical properties of graphene nanosheets/polyaniline nanofibers composites as electrode for supercapacitors[J].J.Power Sources,2011,196(24):10775-10781.
[32] Wu Z S,Wang D W,Ren W C. Anchoring hydrous RuO2on graphene sheets for high-performance electrochemical capacitors[J].Adv.Funct.Mater.,2010,20:3595-3603.
[33] Rakhi R B,Alshareef H N. Enhancement of the energy storage properties of supercapacitors using graphene nanosheets dispersed with metal oxide-loaded carbon nanotubes[J]. J. Power Sources,2011,196:8858-8865.
[34] Wang D W,Li F,Zhao J,et al.Fabrication of graphene/polyaniline composite paper via in situ anodic electropolymerization for high-performance flexible electrode[J]. ACS Nano,2009,3:1745-1752.
[35] Fan Z,Yan J,Wei T,et al.Asymmetric supercapacitors based on graphene/Mno2and activated carbon nanofiber electrodes with high power and energy density[J]. Adv. Funct. Mater.,2011,21:2366-2374.
[36] Zhang L L,Zhou R,Zhao X S,et al.Graphene-based materials as supercapacitor electrodes[J]. J.Mater.Chem.,2010,20:5983-5992.
[37] Yan J,Fan Z J,Wei T,et al. Fast and reversible surface redox reaction of graphene-MnO2composites as supercapacitor electrodes[J].Carbon,2010,48(13):3825-3833.
[38] Peng L L,Peng X,Liu B R,et al. Ultrathin two-dimensional MnO2/graphene hybrid nanostructures for high-performance,flexible planar supercapacitors[J]. Nano Lett.,2013,13(5):2151-2157.
[39] Fan Z J,Yan J,Zhi L J,et al. A three-dimensional carbon nanotube/graphene sandwich and its application as electrode in supercapacitors[J]. Adv.Mater.,2010,22(33):3723-3728.
[40] Dong L,Chen Z X,Yang D,et al. Hierarchically structured graphene-based supercapacitor electrodes[J]. RSC Adv.,2013,3:21183-21191.
[41] Lü W,Tang D M,He Y B,et al. Low-temperature exfoliated graphenes:Vacuum-promoted exfoliation and electrochemical energy storage[J].ACS Nano,2009,3(11):3730-3736.
[42] McAllister M J,Li J L,Adamson D M,et al. Single sheet functionalized graphene by oxidation and thermal expansion of graphite[J].Chem.Mater.,2007,19(18):4396-4404.
[43] Tarascon J M,Armand M.Issues and challenges facing rechargeable lithium batteries[J]. Nature,2001,414:359-367.
[44] Fergus J W. Recent developments in cathode materials for lithium ion batteries[J]. J.Power Sources,2010,195(4):939-954.
[45] Armand M,Tarascon J M.Building better batteries[J]. Nature,2008,451(7179):652-657.
[46] Ishihara T,Kawahara A,Takita Y,et al. Effects of synthesis condition of graphitic nanocarbon tube on anodicproperty of Li-ion rechargeable battery[J].J.Power Sources,2001,97&98 :129-132.
[47] Dunn B,Kamath H,Tarascon J M.Electrical energy storage for the grid:A battery of choices[J]. Science,2011,334(6058):928-935.
[48] Zhi L J,Hu Y S,Hamaoui B E. Precursor-controlled formation of novel carbon/metal and carbon/metal oxide nanocomposites[J]. Adv.Mater.,2008,20:1727-1731.
[49] Wang D H,Choi D W,Li J,et al.Self- assembled TiO2-graphene hybrid nanostructures for enhanced Li-ion insertion[J]. ACS Nano,2009,3:907-914.
[50] Wang C,Li D,Too C O,et al. Electrochemical properties ofgraphene paper electrodes used in lithium batteries[J]. Chem. Mater.,2009,21(13):2604-2606.
[51] Xue D J,Xin S,Yan Y,et al.Improving the electrode performance of Ge through Ge@C core-shell nanoparticles and graphene networks[J]. J.Am.Chem.Soc.,2012,134(5):2512-2515.
[52] Yang X W,Qiu L,Cheng C,et al.Ordered gelation of chemically converted graphene for next-generation electroconductive hydrogel films[J].Angew.Chem.Int.Edit.,2011,50(32):7325-7328.
[53] Su F,He Y B,Li B H,et al.Could graphene construct an effective conducting network in a high-power lithium ion battery?[J]. Nano Energy,2012,1:429-439.
[54] Wang G X,Wang B,Wang X L,et al.Sn/graphene nanocomposite with 3D architecture for enhanced reversible lithium storage in lithium ion batteries[J].J.Mater.Chem.,2009,19(44):8378-8384.
[55] Kwon Y J,Kim H,Doo S G,et al. Sn0.9Si0.1/carbon core-shell nanoparticles for high-density lithium storage materials[J]. Chem.Mater.,2007,19(5):982-986.
[56] Yang S B,Feng X L,Zhi L J,et al.Nanographene-constructed hollow carbon spheres and their favorable electroactivity with respect to lithium storage[J].Adv.Mater.,2010,22(7):838-842.
[57] Wang G X,Shen X P,Yao J,et al. Graphene nanosheets for enhanced lithium storage in lithium ion batteries[J]. Carbon,2009,47(8):2049-2053.
[58] Behera S K. Enhanced rate performance and cyclic stability of Fe3O4-graphene nano composites for Li ion battery anodes[J]. Chem.Commun.,2011,47(37):10371-10373.
[59] Liang M H , Zhi L Z. Graphene-based electrode materials for rechargeable lithium batteries[J]. J. Mater. Chem.,2009,19:5871-5878.
[60] Paek S M,Yoo E J,Honma I. Enhanced cyclic performance and lithium storage capacity of SnO2/ graphene nanoporous electrodes with three-dimensionally delaminated flexible structure[J]. Nano Lett.,2009,9(1):72-75.
[61] Lee J W,Hoo A S,Kim J D,et al. A facile and template-free hydrothermal synthesis of Mn3O4nano rods on graphene sheets for supercapacitor electrodes with long cycle stability[J]. Chem. Mater.,2012,24:1158-1164.
[62] Wang X Y,Zhou X F,Yao K,et al.A SnO2/graphene composite as a high stability electrode for lithium ion batteries[J]. Carbon,2011,49:133-139.
[63] Wang D H,Kou R,Choi D,et al.Ternary self-assembly of ordered metal oxide-graphene nanocomposites for electrochemical energy storage[J]. ACS Nano,2010,4:1587-1595.
[64] Wang H L,Cui L F,Yang Y,et al. Mn3O4-graphene hybrid as a high-capacity anode material for lithium ion batteries[J]. J. Am.Chem.Soc.,2010,132(40):13978-13980.
[65] Fan Z J,Yan J,Ning G Q,et al.Porous graphene networks as high performance anode materials for lithium ion batteries[J]. Carbon,2013,60:558-561.
[66] Pan D Y,Wang S,Zhao B,et al.Li storage properties of disordered graphene nanosheets[J]. Chem.Mater.,2009,21(14):3136-3142
[67] Wei W,Yang S,Zhou H,et al.3D graphene foams cross-linked with pre-encapsulated Fe3O4nanospheres for enhanced lithium storage[J].Adv.Mater.,2013,25(21):2909-2914.
[68] Rao C V,Reddy A L M,Ishikawa Y,et al. LiNi1/3Co1/3Mn1/3O2-graphene composite as a promising cathode for lithium-ion batteries[J]. ACS Appl.Mater.& Interfaces,2011,3(8):2966-2972.
[69] Liu H D,Gao P,Fang J,et al.Li3V2(PO4)3/graphenenanocomposites as cathode material for lithium ion batteries[J]. Chem. Commun.,2011,47(32):9110-9112.
[70] Wang H L,Yang Y,Liang Y Y,et al. Graphene-wrapped sulfur particles as a rechargeable lithium-sulfur battery cathode material with high capacity and cycling stability[J].Nano Lett.,2011,11(7):2644-2647.
[71] Wang J Z,Lu L,Choucair M,et al.Sulfur-graphene composite for rechargeable lithium batteries[J]. J.Power Sources,2011,196(16):7030-7034.
[72] Cao Y L,Li X L,Aksay I A,et al. Sandwich-type functionalized graphene sheet-sulfur nanocomposite for rechargeable lithium batteries[J]. Phys.Chem.,2011,13(17):7660-7665.
[73] Zhou G M,Pei S F,Li L,et al.A graphene-pure-sulfur sandwich structure for ultrafast, long-life lithium-sulfur batteries[J]. Adv.Mater.,2013,doi:10.1002/ adma.201302877.
[74] Huang J Q,Liu X F,Zhang Q,et al.Entrapment of sulfur in hierarchical porous graphene for lithium-sulfur batteries with high rate performance from-40 ℃to 60 ℃[J].Nano Energy,2013,2:314-321.
[75] Zhou G M,Yin L C,Wang D W,et al.Fibrous hybrid of graphene and sulfur nanocrystals for high-performance lithium-sulfur batteries[J]. ACS Nano,2013,7(6):5367-5375.
[76] Ji L W,Rao M M,Zheng H M,et al. Graphene oxide as a sulfur immobilizer in high performance lithium/sulfur cells[J].J.Am.Chem.Soc.,2011,133:18522-18525.
[77] Kowalczk I,Read J,Salomon M.Li-air batteries:A classic example of limitations owing to solubilities[J]. Pure Appl. Chem.,2007,79(5):851-860
[78] Abraham K M ,Jiang Z. A polymer electrolyte-based rechargeable lithium/oxygen battery[J].J.Electrochemi.Soc.,1996,143 (1):1-5.
[79] Cao R G,Lee J S,Liu M L,et al.Recent progress in non-precious catalysts for metal-air batteries[J]. Adv.Energy Mater.,2012,2(7):816-829.
[80] Kim H,Lim H D,Kim J,et al. Graphene for advanced Li/S and Li/air batteries[J]. J.Mater.Chem.A,2014,1(2):33-47.
[81] Sun B,Wang B,Su D W,et al. Graphene nanosheets as cathode catalysts for lithium-air batteries with an enhanced electrochemical performance[J]. Carbon,2012,50(2):727-733.
[82] Zhang W Y,Zhu J X,Ang H X,et al.Binder-free graphene foams for O2electrodes of LiO2batteries[J].Nano Scale,2013,5:9651-9658.
[83] Xiao J,Mei D,Li X,et al. Hierarchically porous graphene as a lithium-air battery electrode[J].Nano Lett.,2011,11:5071-5078
[84] Yoo E,Zhou H S. Li-air rechargeable battery based on metal-free graphene nanosheet catalysts[J]. ACS Nano,2011,5(4):3020-3026.

