6-羟基-2-萘磺酸铜、镁、锌、钴、镍配合物的合成和结构表征
王高峰,孙述文
(运城学院应用化学系,山西运城 044000)
6-羟基-2-萘磺酸铜、镁、锌、钴、镍配合物的合成和结构表征
王高峰,孙述文
(运城学院应用化学系,山西运城 044000)
6-羟基-2-萘磺酸钠分别和CuSO4,MgSO4,ZnSO4、Co(phen)3Cl2反应,物质的量比为5∶1,得到一系列铜、镁、锌、钴、镍配合物并通过红外和元素分析确定结构。测定了钴的配合物的单晶结构,结果表明,钴配合物1属于三斜晶系,P-1空间群,a=12.4120(15)Å,b=12.4711(16)Å,c=20.090(2)Å,α=90.0450(10)°,β=103.161(2)°,γ=113.519(2)°,V=2761.9(6)Å3,Z=2。
铜;钴;6-羟基-2-萘磺酸;配合物
近年来,有机磺酸根的配位行为引起了人们越来越多的关注[1-8]。与有机膦酸不同的是,有机磺酸的配位方式对于所处的环境比较敏感,稍微改变其周围的化学环境,就会产生其配位方式的改变[1-2]。研究表明,磺酸化合物可以具有与金属膦酸类似的结构与功能[2-4],且和金属膦酸相比,─S03─基团可用1个、2个或3个氧原子与金属配位,其配位方式更加多样化,具有很大的灵活性,从而使得金属磺酸盐的配位结构更加丰富。当有机配位体中含有多个磺酸根配位体时,它们与金属离子反应可以和多羧酸配体一样,形成高维的更稳定结构[5-8]。6-羟基-2-萘磺酸钠是很经典的配合物,但是应用6-羟基-2-萘磺酸作为配体的其他化合物很少见报道。本文用6-羟基-2-萘磺酸钠盐和不同的其他金属盐反应,得到了相应的铜、镁、锌、钴、镍的配合物。
1 实验部分
1.1 主要仪器与试剂原料
Bruker Vector 22红外光谱仪,Elementar Vario ELIII元素分析仪,Bruker Smart Apex II CCD单晶衍射仪。
硫酸,氯化钠,2-萘酚,硫酸铜,硫酸镁,硫酸锌,氯化钴,氯化镍,甲醇,邻菲罗林等均为市售分析纯试剂。6-羟基-2-萘磺酸钠按照文献方法合成[9]。
1.2 实验方法
1.2.1 6-羟基-2-萘磺酸铜(1)的合成
6-羟基-2-萘磺酸钠(15 mmol)溶于5 mL水中,搅拌5 min溶解,加入CuSO4·5H2O(5 mmol)固体,继续搅拌10 min,加热至溶液澄清,冷却,得到浅棕色晶状物。产率46%。
IR(KBr,cm-1):3237,1624,1599,1471,1393,1349,1216,1155,1096,1029,900,861。
元素分析:计算值(%)C,38.86;H,4.24。实测值(%)C,38.81;H 4.20。
1.2.2 6-羟基-2-萘磺酸镁(2)的合成
合成方法同6-羟基-2-萘磺酸铜类似,只是将硫酸铜换成硫酸镁。产率42%。
IR(KBr,cm-1):3393,1624,1437,1394,1168,1098,1030,903,874,823,661,485。
元素分析:计算值(%)C,41.50;H,4.53。实测值(%)C,41.46;H,4.51。
1.2.3 6-羟基-2-萘磺酸锌(3)的合成
合成方法同6-羟基-2-萘磺酸铜,只是将硫酸铜换成硫酸锌。产率38%。
IR(KBr,cm-1):3429,1625,1394,1168,1097,1030,902,874,681,626。
元素分析:计算值(%)C,38.75;H,4.23。实测值(%)C,38.71;H,4.22。
1.2.4 [双(6-羟基-2-萘磺酸)][三(邻菲罗林)钴](4)的合成
氯化钴(2.5 mmol)溶于20 mL甲醇中,加入6-羟基-2-萘磺酸钠5 mmol,微热至全部溶解后,加入邻菲罗林7.5 mmol,继续并搅拌10 min。室温放置5 h后,有大量橙红色块状晶体析出,产率76%。
IR(KBr,cm-1):3421,1625,1517,1425,1183,1093,1027,842,724,672,620。
元素分析:计算值(%)C,64.30;H,3.66。实测值(%)C,64.26;H,3.62。
1.2.5 [双(6-羟基-2-萘磺酸)][三(邻菲罗林)镍](5)的合成
合成方法同[双(6-羟基-2-萘磺酸)][三(邻菲罗林)钴]类似,将氯化钴换成氯化镍。红色晶体,产率72%。
IR(KBr,cm-1):3422,1623,1518,1426,1180,1130,1094,1030,848,751,726,675,623。
元素分析:计算值(%)C,64.32;H,3.66。实测值(%)C,64.30;H,3.65。
1.3 单晶结构分析
适合X-射线测定的钴配合物在甲醇溶剂中缓慢挥发得到。测定了配合物4的单晶结构,其分子结构见图1。该配合物的晶体学数据见表1。配合物的主要键长键角见表2。在配合物中,6-羟基-2-萘磺酸配体无序。
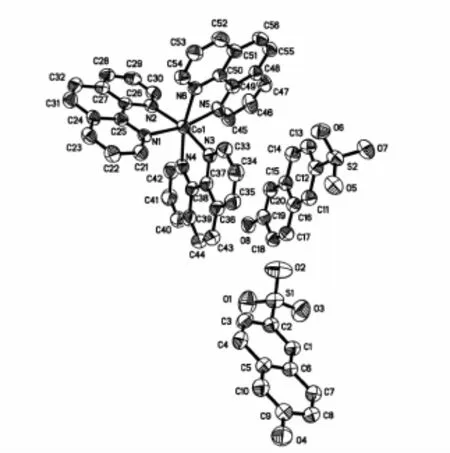
图1 配合物4的分子结构图Figure 1 Molecular structure of complex 4

表1 配合物4的晶体学数据表Table 1 Crystallographic data of complexes 4

表2 配合物4的部分键长键角Table 2 Bond lengths and angles of complex 4
2 结果与讨论
利用6-羟基-2-萘磺酸钠盐和不同的其他金属盐反应,顺利得到了相应的金属配合物,并通过红外和元素分析表征。在配合物1~5中,分别在1155,1096,1029;1168,1098,1030;1168,1097,1030;1183,1093,1027和1180,1094,1030 cm-1处出现了一组磺酸基的特征伸缩振动和变形振动吸收[10]。元素分析表明,配合物1~3中金属离子周围有6个配位水。而配合物4~5元素分析表明,邻菲罗林配体参与了金属离子的配位。
单晶结构分析进一步确证了结构。单晶结构分析表明,配合物4的晶体由[Co(phen)3]2+阳离子、两个6-羟基-2-萘磺酸阴离子组成和6.5个游离水组成。Co2+为六配位,配位原子分别来自3个phen的N原子。所有的键长键角都在合理的范围内。在配合物中,磺酸根没有参与配位,仅以抗衡离子存在。
3 结论
1)用6-羟基-2-萘磺酸钠盐和不同的其他金属盐反应,合成了一系列铜、镁、锌、钴、镍的配合物,方法简便,操作简单。
2)在配合物4中,磺酸根阴离子仅仅以抗衡离子的形式存在,在配合物4~5中,引入phen作为第二配体,金属离子和6个N原子以6配位的形式存在。
[1]Shimizu G K H,Enright G D,Ratcliffe C I,et al.A Layered Silver Sulfonate Incorporating Nine-coordinate AgI in a Hexagonal Grid[J].Chem.Commun,1999,(16),1485-1486.
[2]Shimizu G K H,Enright G D,Ratcliffe C I,et al.Silver Sulfonates:?An Unexplored Class of Layered Solids[J].Chem.Mater,1998,10(11)3282-3283.
[3]Gunderman B J,Squattrito P J.Synthesis and Structures of Potassium and Rubidium Arenesulfonates[J].Inorg.Chem,1994,33(13):2924-2931.
[4]Smith G,Cloutt B A,Lynch D E,et al.Nitrogen Base Adducts with Silver(I)p-Toluenesulfonate:Syntheses and Single Crystal X-ray Characterizations of the Adducts with Pyridine(1:1),2-Aminopyridine(1:2),2-Aminopyrimidine(1:1),4,6-Dimethyl-2-aminopyrimidine(2:3),and 3-Aminobenzoic Acid (1:2)and the Crystal Structure of the Parent Silver (I)p-Toluenesulfonate[J].Inorg.Chem,1998,37 (13):3236-3242.
[5]Orr G.W,Barbour L J,Atwood J L.Controlling Molecular Self-Organization:Formation of Nanometer-Scale Spheres and Tubules[J].Science,1999,285,1049-1052.
[6]Johnson C P,Atwood J L,Steed J W,et al.Transition Metal Complexes of p-Sulfonatocalix[5]arene [J].Inorg.Chem,1996,35(9):2602-2610.
[7]Atwood J L,Orr G W,Means N C,et al.Metal Ion Complexes of Water-soluble Calix[4]arenes[J].Inorg.Chem,1992,3l(4),603-606.
[8]Hardie M J,Johnson J A,Raston C L,et al.Cooperative Hydrogen Bonding and Yttrium(III)Complexation in the Assembly of Molecular Capsules[J].Chem.Commun,2000,(10),849-850.
[9]韩广甸,赵树森,李述文.有机制备化学手册(上)[M].北京:化学工业出版社,1980.
[10]隋爱香.金属磺酸盐配合物的合成、性质和结构表征[D].西安:西北大学,2007.
Synthesis of Copper,Magnesium,Zinc and Cobalt Complexes Containg 6-Hydroxynaphthalene-2-sulfate Ligands
WANG Gao-feng*,SUN Shu-wen
(Department of Applied Chemistry.Yuncheng University,Yuncheng 044000,China)
The reaction of sodium 6-hydroxynaphthalene-2-sulfate with CuSO4,MgSO4,ZnSO4and CoCl2/phen,NiCl2/phen respectively gave the corresponding sulfate complexes.These obtained complexes were characterized by elemental analysis,and IR spectra.The X-ray crystal structure of cobalt complex 1 is also reported.The single crystal of complex 1 is triclinic,has space group P-1,with a=12.4120(15)Å,b=12.4711(16)Å,c=20.090(2)Å,α=90.0450(10)°,β=103.161(2)°,γ=113.519(2)°,V=2761.9(6)Å3,Z=2.
copper;cobalt;6-hydroxynaphthalene-2-sulfonate;complexes
O614
A
1004-275X(2014)02-0010-03
12.3969/j.issn.1004-275X.2014.02.004
收稿:2013-10-17
运城学院博士科研启动基金(YQ-2013012)
王高峰(1979-),男,博士,主要从事配合物的合成和结构研究。

