献血者HBV、HCV、HIV检测模式探讨
陈红,刘春兰,王亚彬,倪龙凤
(九江市中心血站,江西九江332000)
·调查报告·
献血者HBV、HCV、HIV检测模式探讨
陈红,刘春兰,王亚彬,倪龙凤
(九江市中心血站,江西九江332000)
目的对献血者样本进行HBV、HCV、HIV的ELISA检测、NAT检测和确证试验,在保证血液安全的前提下,选择最佳的献血者HBV、HCV、HIV的检测模式。方法2003年9月1日至2014年8月31日九江血站采集的无偿献血样本共43473例,用两种ELISA试剂进行HBV、HCV和HIV检测,检测阴性样本和单试剂阳性的样本进行NAT检测,单试剂样本分别进行确证试验。结果42161例ELISA阴性样本有75例NAT阳性,阳性率0.18%;45例HBV单试剂阳性样本有7例NAT阳性,有2例确认试验阳性(其中1例NAT阳性);18例HCV单试剂阳性样本NAT未检出阳性,确证试验5例不确定;15例HIV单试剂阳性样本NAT未检出阳性,确证试验1例不确定,追踪为阴性。结论开展NAT检测十分必要,但NAT检测不能完全代替ELISA检测,献血者的HBV、HCV、HIV检测模式选用一种ELISA试剂加一种NAT试剂检测能最大限度地防止阳性样本的漏检,更好地保障血液安全。
ELISA检测;核酸检测;确证试验;血液安全
DOI∶10.3969/j.issn.1674-1129.2014.06.053 2012年6月
卫生部颁布了新的《血站技术操作规程》[1],献血者乙型肝炎病毒(HBV)感染标志物、丙型肝炎病毒(HCV)感染标志物和人类免疫缺陷病毒(HIV)感染标志物的检测方法可以用两种不同生产厂家的酶联免疫(ELISA)试剂或一种ELISA试剂加一种核酸扩增(NAT)试剂检测。我国从2010年开始在血站进行病毒核酸检测的试点工作,目前关于我国献血者核酸检测的功效仍在研究中[2]。现在很多血站在采用两次ELISA后再加做一次NAT,检测成本巨大。本站通过对献血者样本进行HBV、HCV、HIV的ELISA检测、NAT检测和确证试验,在保证血液安全的前提下,选择最佳的献血者HBV、HCV、HIV的检测模式。
1 材料与方法
1.1 材料2013年9月1日-2014年8月31日九江地区无偿献血者共计43473例,体检合格后采血,同时留取2管5±1ml样本,其中1管用EDTAK2抗凝的真空采血管,用于ELISA检测,1管用无菌、无DAN酶、无RNA酶、带分离胶的EDTA-K2抗凝BD真空采血管,用于核酸检测。所有样本在2~8℃保存,1600g离心20min,48h内完成ELISA和NAT检测。
1.2 试剂与仪器
1.2.1 ELISA试验乙型肝炎病毒表面抗原诊断试剂(英科新创科技有限公司、北京万泰生物药业股份有限公司、珠海丽珠试剂股份有限公司)、丙型肝炎病毒抗体诊断试剂(英科新创科技有限公司、北京万泰生物药业股份有限公司)、人类免疫缺陷病毒HIV1/2抗体诊断试剂(上海实业科华生物技术有限公司),人类免疫缺陷病毒HIV1/2抗原抗体诊断试剂盒(珠海丽珠试剂股份有限公司),试剂均通过中国药品生物制品检定所批批检合格,且在有效期内使用;检测用澳斯邦全自动加样仪STAR和全自动酶免仪FAME完成,在校验期内使用。
1.2.2 核酸试验乙型肝炎病毒、丙型肝炎病毒、人类免疫缺陷病毒(1+2型)核酸联合检测试剂(罗氏诊断产品有限公司),在有效期内使用;检测用美国罗氏Cobas S201全自动核酸检测系统(包括Hamilton STAR全自动混样仪、Cobas Ampilprep核酸提取仪和Cobas Taqmen Analyzer核酸扩增检测仪)完成,在校验期内使用。
1.2.3 确认试验乙型肝炎病毒表面抗原确认试剂(珠海丽珠,批号2014060248)、丙型肝炎病毒抗体确证试剂(北京万泰,批号RC20140101)、人类免疫缺陷病毒HIV1/2抗体确证试剂(MP生物医学亚太有限公司,批号AE3031),在有效期内使用。
1.3 方法
1.3.1 ELISA试验用2种ELISA试剂进行HBV、HCV、HIV检测,每次检测严格按试剂说明书操作,阴阳性对照成立,室内质控在控。任何1种试剂S/ CO值≥1.0为反应性,0.85≤S/CO值<1.0为灰区,任一种试剂检测为反应性或灰区的,则重取血袋导管血双试剂双孔平行复试,复试后任1种试剂任1孔呈反应性或灰区的,判为阳性。
1.3.2 核酸试验淘汰ELISA试验双试剂阳性的样本,阴性和HBV、HCV、HIV单试剂阳性的样本由全自动混样仪自动混样,每6份样本(167μl/份)混合成1份(1ml)作为一级混样池(pool)样本,由全自动核酸提取仪和全自动核酸扩增检测仪采用核酸定性筛查试剂进行HBV-HCV-HIV NAT检测。每批检测均设置1个阴性质控和5个阳性质控,每个pool均含内对照。pool检测为阴性,6份样本合格;pool检测为反应性,对该pool中的6份样本进行单份拆分检测,拆分试验为阴性判定为NAT检测阴性,反之拆分试验为反应性判定为NAT检测阳性。阳性的样本委托罗氏公司做鉴别试验。
1.3.3 确认试验HBV单试剂阳性的样本进行确认检测(中和试验),样本的抑制率≥50%,判为阳性;HCV单试剂阳性的样本进行确证检测(重组免疫印迹法RIBA),至少出现2种HCV抗体特异条带(Core、NS3、NS4、NS5)强度1+及以上判为阳性,仅出现1种HCV抗体特异条带强度1+及以上判为不确定;HIV单试剂阳性的样本进行确证检测(免疫印迹法WB),至少有2条ENV带(gp160/gp41和gp120),或1条env带和p24带同时出现判为阳性,出现HIV抗体特异带,但不足以判阳性的则判为不确定[3]。
2 结果
2.1 43473例样本经ELISA检测有42161例阴性样本和78例单试剂阳性样本,其中HBV单试剂样本45例,HCV单试剂样本18例,HIV单试剂样本15例。
2.2 核酸检测42161例阴性样本拆分后有75例阳性,经鉴别试验有44例为HBV阳性,无HCV和HIV阳性;78例HBV、HCV、HIV单试剂阳性样本,拆分后有7例阳性,经鉴别试验有6例为HBV阳性,无HCV和HIV阳性。
2.3 78例单试剂阳性样本NAT或确认试验阳性判为阳性结果见表1。
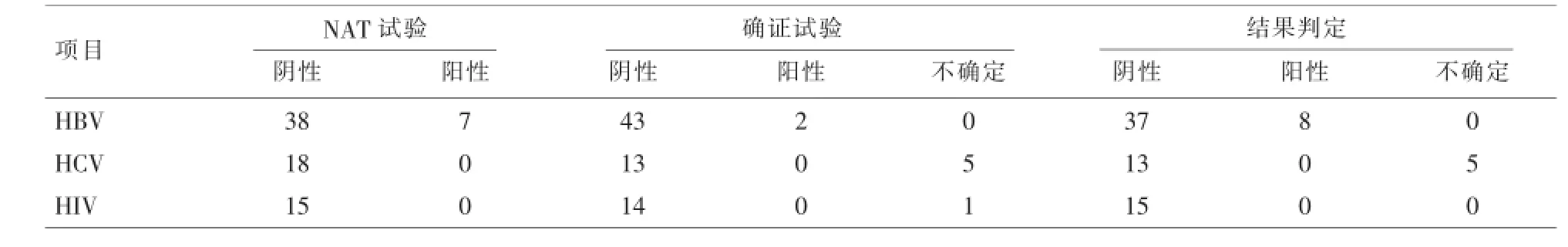
表1 78份单试剂阳性结果
3 讨论
42161例ELISA检测阴性样本,经核酸检测,检出75例阳性样本,阳性率为0.18%,高于德宏地区0.098%[4]和常州地区(0.1%)[5],但低于龙岩地区0.24%[6]。45例HBV单试剂阳性样本,核酸检测7例阳性,18例HCV单试剂阳性样本和15例HIV单试剂阳性样本,核酸未检出阳性。核酸检测阳性样本共82例经核酸鉴别试验,有51例为HBV阳性,未检出HCV和HIV阳性,阳性率为62.2%,与济南地区63.86%[7]和东莞地区65.38%[8]相近。分析原因,可能是:(1)我国是HBV高流行国家,虽然HBV计划免疫在我国取得了重大成效,但HBsAg在1~59岁普通人群中的流行率仍高达5.84%[9],所以HBV的检出率较高;(2)HBV是DNA病毒,对于外界环境的抵抗力较强,而HCV和HIV均是RNA病毒,对温度较敏感,相对稳定性差,易降解,造成HCV和HIV无法检出;(3)在核酸检测过程中由于扩增产物、气溶胶、人为操作等原因造成核酸检测结果的假阳性;(4)由于我们样本数量不够大,所以未检出HCV-RNA和HIV-RNA阳性的样本。以上数据说明由于“窗口期”、灵敏度、亚型、病毒变异以及免疫静默感染等方面原因,ELISA检测存在局限性,NAT检测能有效缩短病毒检测窗口期,检测隐匿性的病毒感染及病毒变异株等,弥补ELISA检测的不足。
我们对HBV、HCV、HIV单试剂阳性样本分别用中和、RIBA和WB试验确证。45例HBV单试剂阳性样本有2例阳性,其中1例核酸检测阳性;18例HCV单试剂阳性样本有5例不确定,核酸未检出;15例HIV单试剂阳性样本有1例不确定,核酸未检出,经追踪此样本检测结果同前,因此可以排除HIV阳性。结果表明,NAT试验虽能检出部分ELISA漏检的样本,但由于检测系统灵敏度、样本病毒载量低、病毒在样本中的不规则分布和核酸检测抓取病毒的随机性等原因,有可能导致NAT检测存在假阴性,所以NAT检测不能完全代替ELISA检测,同时核酸实验室的规范化、标准化和精细化管理是十分重要的[10]。
综上所述,笔者认为开展NAT检测十分必要,献血者的HBV、HCV、HIV检测模式选用一种ELISA试剂加一种NAT试剂检测能最大限度地防止阳性样本的漏检,更好地保障血液安全,这与江西省血液中心的相关报道一致[11]。但任何的检测试剂都存在灵敏度和特异性的问题,如何选择最佳的ELISA试剂和NAT试剂的组合,将是我们下一步需要研究的。
[1]卫生部.血站技术操作规程[S].卫医政发[2012]1号.2012∶13.
[2]李金明.我国血站核酸检测及质量管理的现状与展望[J].中国输血杂志,2012,25(10)∶933-934.
[3]叶应妩,王毓三,申子瑜.全国临床检验存在规程[M].第3版.南京∶东南大学出版社,2006∶623-628.
[4]郭兆富,陈天鹏,尹以靖,等.NAT技术在德宏地区献血标本输血传染病筛检中的应用[J].临床输血与检验,2013,15(3):247-248.
[5]何亚琴,张建伟,杨爱龙,等.核酸检测技术在常州地区献血筛查中的应用[J].中国输血杂志,2011,24(7)∶560-562.
[6]黄丽平.核酸技术在龙岩地区献血者血液筛查中的应用[J].中国输血杂志,2013,26(6)∶575-576.
[7]朱永宝,张妍,李英莲,等.2010-2012年济南地区无偿献血者核酸检测结果分析[J].中国输血杂志,2013,26(8)∶722-724.
[8]师玲玲,刘赴平,王德文,等.核酸检测技术在献血者血液筛查中的初步应用[J].中国输血杂志,2010,23(1)∶11-13.
[9]Lu J,Zhou Y,Lin X,et al.General epidemiological parameters of viral hepatitis A,B,C,and E in six regions of China∶a crosssectional study in 2007[J].PloS One,2009,4(12)∶8467.
[10]陈红,王亚彬,倪龙凤,等.核酸与ELISA检测联合应用于血液筛查的结果分析[J].中国输血杂志,2014,27(8)∶847-848.
[11]钱榕,方昌志,熊丽红,等.南昌地区献血者HBV感染隐匿风险与基因型调查分析[J].实验与检验医学,2014,32(4)∶386-388.
R193.3,R446.62,R512.91,R512.63,R512.62
A
1674-1129(2014)06-0778-02
2014-09-15;
2014-10-24)
江西省九江市科技局课题项目(编号∶[2013]50-19)

