调温和油脂组成对巧克力原料油及其应用性能的影响
沈海燕,张 虹*,谢仕潮,胡 鹏,王兴国
(1.江南大学食品学院,江苏 无锡 214122;2.丰益(上海)生物技术研发中心有限公司,上海 200137)
调温和油脂组成对巧克力原料油及其应用性能的影响
沈海燕1,2,张 虹2,*,谢仕潮2,胡 鹏2,王兴国1
(1.江南大学食品学院,江苏 无锡 214122;2.丰益(上海)生物技术研发中心有限公司,上海 200137)
研究调温和油脂组成对巧克力油脂(可可脂与全氢化棕榈仁油硬脂混合物)的相容性、巧克力的质构以及在20 ℃贮藏3个月过程中起霜稳定性的影响。结果表明:可可脂与全氢化棕榈仁油硬脂混合物未调温时随可可脂含量增加有明显的稀释作用,经调温后可可脂含量在30%~50%之间出现明显共晶;巧克力硬度受调温和巧克力油脂相容性影响显著。当巧克力油基中可可脂含量<50%,巧克力硬度随可可脂增加而降低;当可可脂含量>50%,经调温巧克力硬度显著增加而未经调温巧克力硬度较为恒定。20℃贮藏实验发现:未调温,巧克力可可脂含量越高,起霜越显著;调温 后,样品可可脂含量在10%~50%范围内起霜程度降低,当可可脂含量>50%及纯全氢化棕榈仁油硬脂时,产品得到明显改善而无起霜现象。从巧克力的熔化特性和巧克力表层的脂肪酸组成分析发现,当可可脂含量>50%时,未调温巧克力引起起霜的机制是不稳定晶体向稳定晶体转化;当可可脂含量≤50%时,引起起霜的机制是可可脂与全氢化棕榈仁油硬脂较差的相容性,导致部分油脂迁移至表面重结晶。
可可脂;全氢化棕榈仁油硬脂;调温;等固相图;起霜;硬度
自从奥尔梅克文明第1次将可可豆制成了巧克力[1],巧克力开始走进了人们的生活。巧克力独特的硬脆而不油腻的质构,以及只熔于口不熔于手的熔化特性提供了巧克力良好的口感和风味,而逐渐被大众喜爱。巧克力中常用的油脂是可可脂(cocoa butter,CB),而它主要产于热带地区,受地理位置和气候的影响,其产量远远不能满足食品工业的需求。为解决供需矛盾,可可脂代用品的研制和生产一直是世界食品工业的研究热点。按原料和特性基本上可以分为三类[2]:可可脂类似物(cocoa butter equivalent,CBE)、非月桂酸型代可可脂(cocoa butter replacer,CBR)和月桂酸型代可可脂(cocoa butter substitute,CBS)。但巧克力在贮藏过程中极易出现起霜的现象[3],常常会导致产品品质急剧下降,最显著的是巧克力表面出现白色的霜花。因此研究起霜的原因对巧克力工业具有很大的意义[4],而起霜是个很复杂的过程,近30多年来关于引起巧克力起霜的原因,发现影响起霜的因素很多,包括基料油脂的相容性[1,5-6]、乳化剂[7]、加工条件(调温[8]和冷却速率[9-10])、贮藏条件(贮藏温度湿度[11]和温度波动[12])等。调温是巧克力加工过程的重要环节。调温的目的是为了形成适当数量、大小和晶型的晶种[11]。因此调温过程对基料油脂相容性评价和巧克力的品质有直接影响[5]。合适调温的巧克力,其产品的脱模性好、表面光亮。若未经调温,油脂冷却过程中将极易形成不稳定晶型,使得产品在贮藏过程中发生重结晶,而导致巧克力起霜。若调温过度,脱模面光泽度则会消失而且会影响到口感。CBS是国内常用的CB代用品。它一般以富含月桂酸的植物油,如棕榈仁油为基础原料,经过适度氢化或结晶分提而得到的。然后在将与CB混合时常常会出现不相容的情况,这对巧克力口感、产品稳定性、加工性能等都会产生重要的影响[2]。然而目前对于调温对CB与全氢化棕榈硬脂(full hydrogenated palm kernel stearin,FHPKS)混合物相容性评价以及其制成的巧克力的起霜情况与原因还存在很大的不确定性。因此本实验通过研究是否调温对不同配比CB与FHPKS相容性评价,以及是否调温和不同油脂组成对巧克力的质构、起霜稳定性影响,同时结合熔化特性和脂肪酸组成变化,探索调温与基料油脂相容性引起起霜原因的差异。从而为巧克力加工工业以及起霜机理的研究提供参考。
1 材料与方法
1.1 材料与试剂
全棕榈仁油硬脂、可可脂 益海嘉里上海研发中心;大豆卵磷脂 秦皇岛金海食品工业有限公司;可可粉、糖粉、脱脂乳粉 市售。
1.2 仪器与设备
TA-XT Plus型质构仪 中国北京微讯超技仪器技术有限公司;Bruker minispec Mq20型脉冲核磁共振仪(p-NMR) 德国Bruker公司;DSC1.823e型差示扫描量热仪 瑞士Mettler-Toledo公司;Wiener-1-S型球磨机澳大利亚Wiener公司。
1.3 方法
1.3.1 脂肪酸组成
气相色谱法,样品采用三氟化硼甲酯化方法处理。色谱条件:CP-Si188毛细管柱(100 m×0.25 mm,0.2 μm);升温程序:120 ℃保持3 min,以8 ℃/min升温到175 ℃,175 ℃保持28 min,以3 ℃/min升温至215 ℃,215 ℃保持30 min;FID检测器,检测器温度250 ℃;进样温度250 ℃;载气N2,压力200 kPa;H2压力60 kPa;空气压力50 kPa。根据标样保留时间定性,用面积归一化法定量。
1.3.2 示差扫描量热法(differential scanning calorimetry,DSC)测定
精确称量约5 mg左右样品,放入专用铝盒内,压紧密封,进行检测。检测时以空铝盒做参比,液氮为冷却介质。CB与FHPKS混合物及巧克力产品表层熔化特性测定如下:1)未调温:将样品从室温下迅速加热到80 ℃稳定5 min(消除结晶记忆),然后以5 ℃/min的速率降温至-40 ℃并保持5 min,然后以5 ℃/min的速率升温至80 ℃。2)调温:样品的调温参照美国油脂化学协会(American Oil Chemists Society,AOCS)方法进行调温,25 ℃常温进样,以5 ℃/min的速率升温至80 ℃。3)巧克力贮藏过程的熔化特性:取样位置为巧克力表面,25 ℃稳定5 min,然后以5 ℃/min的速率升温至80 ℃。以上其熔化过程中的熔化曲线及焓值被记录。
1.3.3 固体脂肪含量(SFC)
SFC由差式量热扫描仪的熔化曲线,经数学计算获得,即[9]:
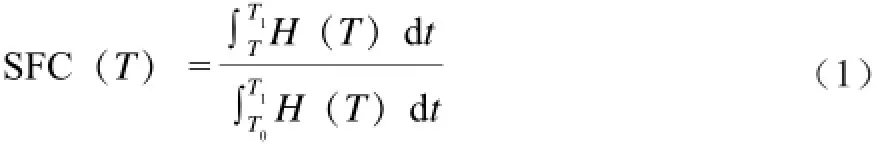
式中:T0、T1、T分别表示DSC熔化曲线中起始点、终止点以及测定点温度;H(T)表示DSC熔化曲线。
1.3.4 CB与FHPKS混合体系相容性分析
将CB和FHPKS以质量比100∶0、90∶10、80∶20、70∶30、60∶40、50∶50、40∶60、30∶70、20∶80、10∶90、0∶100的比例混合。通过DSC的熔化曲线获得上述混合样品在10、20、25、30、35、40 ℃条件下的SFC。
双相混合物的相容性用等固相图来评价。经DSC获得的SFC参照Lambelet等[13]的方法作出等固相图,即以混合物中CB含量为横坐标,温度为纵坐标,以5%、10%、20%、30%、40%、60%、80%的固脂含量为系列曲线的相图。
1.3.5 巧克力的制备与贮藏
巧克力配方:42%糖、13%可可粉、7%脱脂乳粉、38%油(CB与FHPKS混合,0%~100%,10%为间隔)。
巧克力制备:所有原料混合并在球磨机中研磨1.5 h。然后将巧克力浆料分为2部分,一部分浆料在40 ℃浇膜,另一部分经调温(调温方法:样品完全融化(40 ℃保持30 min),冷却至27~28 ℃至巧克力出现黏黏的厚重感,立即升温至31~32 ℃[14])后浇膜。冷却脱模后装入透明塑料袋中密封。
巧克力的贮藏:巧克力在(20±2) ℃条件下贮藏,其相对湿度为60%,观察其起霜情况,典型样品热力学分析,及起霜表层及内部油脂脂肪酸组成分析。并用ΔI表示脂肪酸组成的变化,按照公式(2)计算[15]。

式中:I*为巧克力表面某一脂肪酸组成/%;I为巧克力块指定某一脂肪酸组成/%。
1.3.6 硬度测试
脱模后在20 ℃保持1 h的巧克力样品,其硬度的测试采用质构仪(P/2探头),测试前速率:10.0 mm/s;测试中速率:0.5 mm/s;测试后速率:10.0 mm/s;刺入深度:6.0mm。每个样品平行测定3次,取平均值作为最终硬度值。
1.3.7 图像观察
贮藏过程的巧克力表面形态采用佳能相机拍摄记录。
2 结果与分析
2.1 原料油组成及相容性分析
2.1.1 脂肪酸组成

表1 FHPKS与CB的脂肪酸组成Table 1 Fatty acid profile of CB and FHPKS
利用气相色谱法对CB与FHPKS的脂肪酸组成进行分析,其结果见表1。CB中主要含长碳链脂肪酸(C16∶0、C18∶0、C18∶1),约占总脂肪酸含量的96%。而FHPKS的中碳链脂肪酸(C10∶0、C12∶0、C14∶0)约占78%,而长碳链脂肪酸(C16∶0、C18∶0、C20∶0)仅约为20%。从不饱和脂肪酸的含量上分析,CB与FHPKS的差异也非常明显,CB中不饱和脂肪酸含量约为36%,而FHPKS经全部氢化后不饱和程度几乎为0。
2.1.2 相容性分析
CB与FHPKS混合后经调温与非调温两种不同处理获得不同的等固相图,如图1a、b所示。

图1 CB和FHPKS混合物的等固相图Fig.1 Isosolid phase diagram for mixture of CB and FHPKS
由图1a可见,随着CB含量增加,固脂量降低,混合物出现明显的稀释作用,且低温(高固脂量)时更显著,并伴随有轻微的共晶。由图1b可见,经调温后,固脂量在5%~10%时,仅30%~80% CB有轻微的共晶。固脂量在20%~40%时,10%~90% CB有共晶,固脂量50%时CvB共晶程度最大。固脂量继续增加,各个比例均有不同程度的共晶,固脂量50%时CB共晶程度仍为最大。
综上所述,未调温样品随CB含量的增加有明显的稀释作用;而调温样品在40%~70% CB范围显著的共晶现象,且温度越低,其相互作用及共晶现象越显著。结合脂肪酸组成来看,CB是以长碳链饱和酸为主,而FHPKS则以中碳链饱和酸为主,CB和FHPKS共同结晶能力较弱,因此未调温时出现明显的稀释作用,且低温更显著;而经调温后,CB形成3倍链长的β型而FHPKS为2倍链长的β’[16-17],晶体结构的差异可能是引起调温后混合物共晶的主要原因,低温时共晶更显著,恰好验证了这一点,且该结论与其他学者的一致[1,15]。
2.2 调温对巧克力物理特性的影响
2.2.1 调温对巧克力硬度的影响
巧克力的硬度是影响巧克力感官品质以及贮藏稳定性的重要指标,利用质构仪分析经不同处理(经调温与非调温)后的浆料,经浇膜,成型后对巧克力的硬度的测试结果如图2所示。
由图2可知,当CB含量<50%时,未调温和经调温巧克力的硬度均随着CB含量的增加而逐渐降低,同比例时未调温样品硬度较高,这主要是由于FHPKS比例占优势,未调温仍迅速结晶形成了稳定的β’,并形成坚固的网络结构[18],而CB结晶缓慢形成细小的晶体[18],未形成完整的网络结构而是零散的分散在FHPKS的坚固结构中,因此该范围内样品的硬度主要受FHPKS的影响;而经调温后,β型的CB形成了坚固的网络结构,与FHPKS形成的结构因晶体差异显著存在相斥作用反而导致硬度降低[1]。而当CB含量>50%后,未调温的巧克力硬度维持在相对稳定的状态;调温巧克力的硬度随着CB含量的增加而显著增加,这与此时CB已占优势,经调温形成坚固的网络结构使硬度显著提高。且发现巧克力硬度随CB含量的变化趋势与CB与FHPKS的未调温和经调温相图中等固曲线变化趋势一致。Timms[18]、Bigalii[19]等提出混合物出现共晶作用或稀释作用时常常会引起熔点降低,硬度下降。油基中CB含量为50%在经调温与非调温处理均具有最低的硬度,与该比例的严重共晶密切相关。由此可见,调温以及CB和FHPKS之间相互作用对巧克力的硬度影响极为显著。
2.2.2 调温对巧克力贮藏过程稳定性的影响
调温是巧克力加工生产的重要环节,对巧克力的品质以及运输、贮藏过程中其产品的稳定性有很大的影响。通过对不同处理(经调温与非调温)获得的巧克力进行20 ℃贮藏实验观察其起霜情况,研究调温环节对巧克力贮藏稳定性的影响,图3用图像记录了上述巧克力贮藏过程中表面的变化情况。贮藏0 d(浇膜后),未调温(图3A)和调温样品(图3B)均有较好的光泽,且CB含量>70%的样品经调温后,其光泽有所提高。贮藏1周后,未调温样品表面出现不同程度的起霜,尤其是CB含量>80%的样品,其表面出现均匀的大理石斑纹,这与Yasuyoshi等[20]在研究未调温巧克力起霜现象一致,是由大量次生晶体的生长所引起的。CB含量在30%~70%的样品表面光泽消失,有轻微的起霜痕迹。CB含量<20%的样品表面仍具有较好的光泽;调温样品经贮藏1周后,CB含量>60%以及<20%的样品仍保持较好的光泽,而CB含量为30%~50%的样品光泽消失,出现明显的起霜痕迹。随着贮藏时间的延长(4周后),未调温样品均出现了不同程度的起霜(除CB含量为0%~10%的样品),且随着CB含量增加,起霜程度加大;而调温样品,CB含量在30%~50%之间的样品起霜程度继续加大,且20% CB样品也出现了起霜痕迹,其他比例仍具有较好的光泽。贮藏至12周时,CB含量为0%时表面光泽消失,有起霜痕迹。该样品出现起霜的时间与王风艳等[17]研究纯棕榈仁油基代可可脂巧克力制品表面光泽消失时间是一致的。其他比例全部起霜且程度均有进一步的增加;调温样品中CB含量为10%~20%表面有起霜痕迹。CB含量>50%表面光泽略有消失。而30%~50%起霜程度继续加大。综上所述,贮藏至12周时,未调温样品已基本全部起霜且随着CB含量的增加以及贮藏时间延长,起霜程度更显著。而CB未获得稳定的晶型是引起未调温巧克力起霜最主要原因;经调温后,CB含量>50%的巧克力起霜情况明显改善。而CB含量≤50%时的巧克力仍出现起霜且50%最显著,由CB与FHPKS的相图可知共晶范围为40%~70% CB,50%共晶最严重,而温度较低时大部分比例均出现共晶。由此可CB含量>50%或100% FHPKS时,调温改善了的巧克力起霜;CB含量≤50%时,虽经调温,巧克力受CB与FHPKS较差的相容性影响仍会出现起霜,这与其他学者的研究结论也是一致的[1,15]。

图3 调温对不同配比CB和FHPKS巧克力20 ℃贮藏过程起霜的影响Fig.3 Effect of tempering on the bloo ming of compound chocolate with various CB/FHPKS ratios during storage at 20 ℃
2.2.3 调温对贮藏过程熔化特性的影响
贮藏过程中巧克力的熔化特性,特别是巧克力表面霜的熔化特性以及表面组分的改变,常用来揭示引起巧克力起霜的原因,如晶型转化[21]、油脂迁移[22]等。巧克力贮藏过程中两种典型基料油比例(CB含量分别为100%和50%)熔化特性及相关比例表面组分变化分别如图4和表2所示。
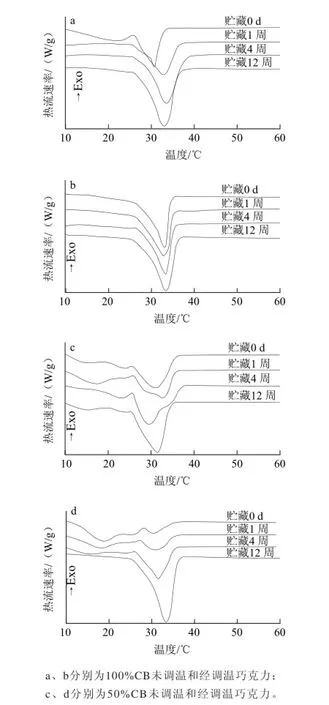
图4 20 ℃贮藏过程中典型比例巧克力DSC熔化曲线Fig.4 Differential scanning calorimetry melting curves of typical ratio of compound chocolate during storage at 20 ℃
由图4a可知,贮藏0 d时,熔化曲线有2个峰(峰值为22 ℃和31 ℃左右)。贮藏1周后,较低温度的熔化峰消失,较高温度的熔化峰的峰值显著升高,形成一个单峰(峰值为33 ℃左右)。随着贮藏时间继续延长,峰型更加尖锐。图4b中贮藏0 d的峰值温度与文献报道的βV的峰温一致,可见经过调温后已达到稳定的βV,随着贮藏时间的延长峰型、峰值均无显著变化。由图4c可知,贮藏0 d样品未经调温有很宽的融程。贮藏1周后形成2个主要的峰(峰值温度分布在15、30 ℃),可见贮藏1周后仅存在峰型的变化。贮藏4周后,低温处熔化峰消失,形成了一个单峰(峰值温度为30 ℃),巧克力表面光泽完全消失,已部分起霜。而贮藏12周后在32 ℃形成了一个尖锐的峰。经调温后(图4d)贮藏0 d形成2个明显的峰。随着时间的延长低温部分向高温转移。贮藏12周后形成一个的主要峰(峰温在33 ℃左右)。

表2 20 ℃贮藏过程中典型比例巧克力DSC焓值的变化Table 2 Change in enthalpy of typical ratio compound chocolate during storage at 20 ℃J/g
由表2可知,100% CB未调温巧克力样品贮藏0 d时,焓值约为23 J/g。随着贮藏时间的延迟,焓值逐渐增加。100% CB经调温后巧克力随着贮藏时间的延迟,焓值无显著差异。50% CB未调温样品贮藏1周内焓值无明显差异,可见贮藏1周后仅存在峰型的变化,这与CB与FHPKS相容性差有关,出现了严重相分离,焓值有部分被抵消导致总体变化不显著。贮藏4周后,焓值小幅度增加,贮藏12周时,焓值显著增加至79.38 J/g。50% CB经调温样品贮藏过程焓值变化趋势和未调温相似,但贮藏12周时焓值较未调温低,为60.79 J/g。
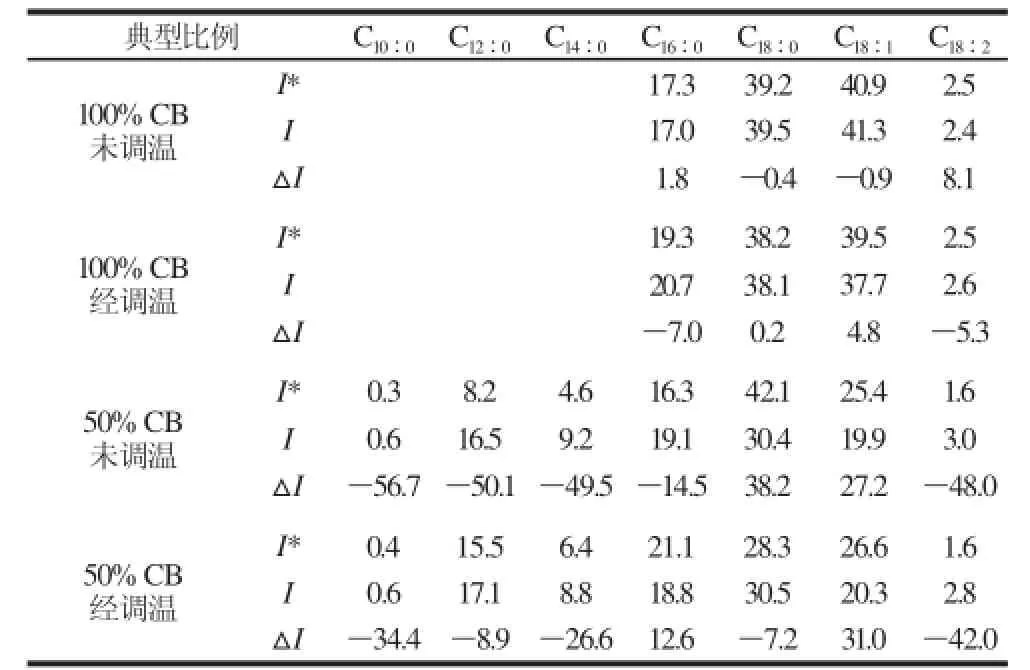
表3 贮藏4周巧克力以及霜的脂肪酸组成Table 3 Fatty acid composition of bloo ming and chocolate after fourweek storage %
表3为贮藏12周时巧克力表面和巧克力块的脂肪酸变化情况,可见100% CB未调温样品脂肪酸组成未发现明显变化。此期间未调温巧克力样品大量起霜且随着贮藏时间的延长而加剧,相应焓值随着贮藏时间逐渐增加,这显示样品的大量起霜是由晶型从不稳定转变成稳定的晶型[23],从而导致了高熔点物质的生成和焓值的增加。这结果与Yasuyoshi等[20]结论一致。100% CB经调温样品脂肪酸组成无显著差异,且焓值无显著变化且与文献报道的βV的焓值相同。Cebula等[24]认为βV至βVI转化是经调温后的纯CB巧克力起霜原因,可见贮藏12周内未发生该转变。50% CB未调温巧克力表面霜较巧克力块硬脂酸C18∶0(+38.2%)和油酸C18∶1(+27.2%)明显增加。结合焓值变化可见贮藏1周内主要为相分离,继续贮藏出现油脂迁移至表面,随着贮藏时间的增加,油脂迁移程度显著增加,而迁移至表面的油脂重结晶形成高熔点物质导致相应焓值在12周时显著增加。可见调温和共晶共同作用[25]导致了非调温(CB<50%)巧克力的起霜。50% CB经调温后巧克力表面霜较巧克力块棕榈酸C16∶0(+12.6%)、油酸C18∶1(+30.9%)明显增加,部分甘三酯迁移至表面重结晶形成更高熔点的物质,从而峰值与焓值均增加。可见CB与FHPKS间较差的相容性是引起50% CB经调温巧克力的起霜[1,15]。
3 结 论
CB与FHPKS混合物未经调温随CB含量增加有明显的稀释作用,经调温后CB含量在30%~50%有明显的共晶,且低温时大部分比例均出现共晶。巧克力硬度受调温和巧克力油脂相容性影响显著,当巧克力油基中CB含量<50%,巧克力硬度随CB含量增加而降低;当CB含量>50%,经调温巧克力硬度显著增加而未经调温巧克力硬度较为恒定。20 ℃贮藏实验发现:未调温,巧克力CB含量越高,起霜越显著;调温后,样品在CB含量10%~50%范围内起霜程度降低,当CB含量>50%及纯FHPKS时,产品得到明显改善而无起霜现象。从巧克力的熔化特性和巧克力表层的脂肪酸组成分析发现,调温(CB含量>50%)和油脂组成(CB含量≤50%)引起起霜的主要原因不同,前者是不稳定晶体向稳定晶体转化,后者是CB与FHPKS较差的相容性,导致部分油脂迁移至表面重结晶。
[1] LONCHAMPT P, HARTEL R W. Fat bloom in chocolate and compound coatings[J]. European Journal of Lipid Science and Technology, 2004, 106(4): 241-274.
[2] HUI Y H, 徐生庚, 裘爱泳. 贝雷: 油脂化学与工艺学[M]. 5版. 北京:中国轻工业出版社, 2001.
[3] 王风艳, 王兴国, 陶冠军, 等. 巧克力起霜研究进展[J]. 食品科学, 2011, 32(5): 301-305.
[4] 华聘聘. 巧克力制品起霜的主要原因[J]. 食品科学, 1994, 15(6): 20-23.
[5] WILLIAMS S, RANSOM-PAINTER K. Mixtures of palm kernel oil with cocoa butter and milk fat in compound coatings[J]. Journal of the American Oil Chemists’ Society, 1997, 74(4): 357-366.
[6] ALI A, DIMICK P S. Melting and solidification characteristics of confectionery fats: anhydrous milk fat, cocoa butter and palm kernel stearin blends[J]. Journal of the American Oil Chemists’ Society, 1994, 71(8): 803-806.
[7] WALTER P, CORNILLON P. Influence of thermal conditions and presence of additives on fat bloom in chocolate[J]. Journal of the American Oil Chemists’ Society, 2001, 78(9): 927-932.
[8] AFOAKWA E O, PATERSON A. Effects of tempering and fat crystallization behavior on microstructure, mechanical properties and appearance in dark chocolate systems[J]. Journal of Food Engineering, 2008, 89(2): 128-136.
[9] TEWKESBURY H, STAPLEY A G F, FRYER P J. Modeling temperature distributions in cooling chocolate moulds[J]. Chemical Engineering Science, 2000, 55(16): 3123-3132.
[10] CAMPOS R, NARINE S. Effect of cooling rate on the structure and mechanical properties of milk fat and lard[J]. Food Research International, 2002, 35: 971-981.
[11] ALI A, SELAMAT J. Effect of storage temperature on texture, polymorphic structure, bloom formation and sensory attributes of fi lled dark chocolate[J]. Food Chemistry, 2001, 72(4): 491-497.
[12] WALTER P, CORNILLON P. Influence of thermal conditions and presence of additives on fat bloom in chocolate[J]. Journal of the American Oil Chemists’Society, 2001, 78(9): 927-932.
[13] LAMBELET P, RAEMY A. Iso-solid diagrams of fat blends from thermal analysis data[J]. Journal of the American Oil Chemists’Society, 1983, 60(4): 845-847.
[14] LUCCAS V, PAULO C, EFRAIM P, et al. Food compositions, process for preparing food compositions and products: US, 0311409[P]. 2009-11-17.
[15] WILLE R, LUTTON E. Polymorphism of cocoa butter[J]. Journal of the American Oil Chemists’ Society, 1966, 43(8): 491-496.
[16] D’SOUZA V, DEMAN J. Short spacing and polymorphic forms of natural and commercial solid fats: a review[J]. Journal of the American Oil Chemists’ Society, 1990, 67(11): 835-843.
[17] WANG Fengyan, LIU Yuanfa, SHAN Liang. Blooming in cocoa butter substitutes based compound chocolate: investigations on composition, morphology and melting behavior[J]. Journal of the American Oil Chemists’ Society, 2010, 87(10): 1137-1143.
[18] TIMMS R E. Phase behavior of fats and their mixtures [J]. Progress in Lipid Research, 1984, 23: 1-38.
[19] BIGALII G L. Practical aspects of the eutectic effect on confectionery fats and their mixtures[J]. Manuf Confect, 1988, 68: 65-80.
[20] YASUYOSHI K, TAMAO H. Composition and structure of fat bloom in untempered chocolate[J]. Sensory and Nutritive Qualities of Food, 2005, 70(7): 450-452.
[21] BRICKNELLJ, HARTEL R. Relation of fat bloom in chocolate to polymorphic transition of cocoa butter[J]. Journal of the American Oil Chemists’ Society, 1998, 75(11): 1609-1615.
[22] WILLE R, LUTTON E. Polymorphism of cocoa butter[J]. Journal of the American Oil Chemists’ Society, 1966, 43(8): 491-496.
[23] SATO K, ARISHIMA T. Polymorphism of POP and SOS. I. occurrence and polymorphic transformation[J]. Journal of the American Oil Chemists’ Society, 1989, 66(5): 664-674.
[24] CEBULA D, ZIEGLEDER G. Stuidies of bloom formation using X-ray diffraction from chocolate after long-term storage[J]. Fat Science Technology, 1993, 95: 340-343.
[25] ROSSELL J B. Interaction of triglycerides and of fats containing them[J]. Chemistry and Industry, 1973(9): 832-835.
Effects of Tempering and Fatty Acid Composition on the Compatibility and Applicability of Chocolate Fats
SHEN Hai-yan1,2, ZHANG Hong2,*, XIE Shi-chao2, HU Peng2, WANG Xing-guo1
(1. School of Food Science and Technology, Jiangnan University, Wuxi 214122, China; 2. Wilmar (Shanghai) Biotechnology R&D Center Co. Ltd., Shanghai 200137, China)
The effects of tempering and fatty acid composition on the compatibility of chocolate fats, i.e., cocoa butter (CB) blended with fully hydrogenated palm kernel stearin (FHPKS), the hardness of chocolate and chocolate blooming during storage at 20 ℃ for 12 weeks were evaluated. Without tempering, the isosolid phase diagram showed a dilution effect with increasing proportion of CB. With tempering, an eutectic behavior occurred when the mixtures contained 30%?50% CB. Tempering and compatibility of chocolate fats had a signifi cant effect on the hardness of chocolate. The hardness was decreased with increasing CB from 0 to 50%. When the content of CB was higher than 50%, two different trends occurred, i.e., the hardness of the tempered chocolate increased obviously whereas the hardness of the non-tempered one kept constant. During storage of chocolate at 20 ℃ for three months, it was found that tempering was an important factor affecting chocolate blooming. All the non-tempered chocolate had bloom within 3-month storage tests, and the degree of bloomingfor non-tempered chocolate was positively correlated to the CB content. After tempering, 10%?50% CB had less bloom formation than the non-temper ones whereas the products containing 60%?100% CB kept glossy. The results of DSC and fatty acid compositions indicated that polymorphic transformation from the unstable to the stable state was the reason for the bloom of non-tempered chocolate containing > 50% CB, and the mechanism for bloom formation of chocolate with ≤50% CB may mainly be attributed to the lipid migration due to the incompatibility between CB and FHPKS .
cocoa butter; fully hydrogenated palm kernel stearin; temper; isosolid diagrams; bloom; hardness
TS225.6
A
1002-6630(2014)03-0037-06
10.7506/spkx1002-6630-201403008
2012-11-09
“十二五”国家科技支撑计划项目(2011BAD02B04);国家自然科学基金青年基金项目(31201382)
沈海燕(1988—),女,硕士研究生,研究方向为油脂结晶和食品质构。E-mail:shenhaiyan881002@163.com
*通信作者:张虹(1965—),女,博士,研究方向为油脂和食品质构、结构酯及乳化体系。E-mail:zhanghongsh@wilmar-intl.com

