对二甲氨基苯甲醛比色法测定溶液中的尿素
周 佳,孙 勇,唐传球,饶贞学,甘 露
(郧阳师范高等专科学校生物化学与环境工程系,湖北 十堰442000)
尿素是一种无色或白色的棒状结晶体,有刺激性气味,广泛应用于工农业生产。目前国内外有多种测定尿素浓度的方法,使用最多的有分光光度法[1-2]、红外光谱法[3]和尿素酶法[4],其中分光光度法又具有简便、快捷的特点,包括硫胺脲二乙酰一肟显色测定法[5-6]和对二甲氨基苯甲醛(PDAB)显色测定法[7],但前者显色产物不稳定、操作复杂,而对二甲氨基苯甲醛显色测定法操作简捷、准确度较高,国内对其报道[8-10]较多,但大多只对影响尿素浓度测定的单因素进行研究,对于各因素之间的相互影响未作探讨。
作者以对二甲氨基苯甲醛与尿素反应生成显色物,利用分光光度计在不同的波长下对该显色物进行测定确定最佳波长,然后通过单因素实验确定影响测定的主要因素,在此基础上设计正交实验优化尿素浓度的测定条件,并绘制测定溶液中尿素浓度的标准曲线。
1 实验
1.1 试剂和仪器
尿素、浓硫酸、无水乙醇、对二甲氨基苯甲醛,均为分析纯。
721型可见分光光度计,上海精密科学仪器有限公司;1cm玻璃比色皿;BS225S型电子天平,北京赛多利斯科学仪器有限公司;HWS-28型恒温水浴箱,上海齐新科学仪器有限公司。
1.2 溶液的配制
(1)尿素标准溶液:称取0.5000g尿素,用少量蒸馏水溶解后转移至100mL的容量瓶中定容,即得浓度为5.00g·L-1的尿素标准溶液。分别量取该标准溶液2mL、4mL、6mL、8mL、10mL、12mL、14mL、16mL,依次加入到100mL的容量瓶中定容,得到浓度(mg·L-1)分别为100、200、300、400、500、600、700、800的系列尿素标准溶液。
(2)对二甲氨基苯甲醛溶液:称取2.5000g对二甲氨基苯甲醛,溶解于500mL无水乙醇中。
1.3 反应机理
对二甲氨基苯甲醛与尿素在浓硫酸作催化剂和无水乙醇作溶剂条件下,反应生成黄棕色的有机化合物。其反应方程式如下:
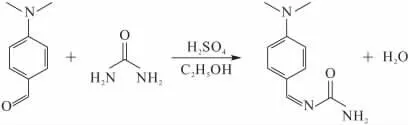
1.4 测定方法
1.4.1 最佳波长的确定
称取2.0000g对二甲氨基苯甲醛固体溶解于48 mL无水乙醇中,加入2mL浓硫酸,置于棕色瓶中备用。量取10mL蒸馏水、10mL 100mg·L-1尿素标准溶液和10mL 200mg·L-1尿素标准溶液,依次加入3支圆底试管中,分别向试管中加入1mL配制好的对二甲氨基苯甲醛溶液,摇匀后静置10min,以空白试液调零,置于1cm的比色皿中,对两组尿素标准溶液在412~460nm波长范围内进行测定。
1.4.2 单因素实验
取2支圆底试管,一支试管中的液体作为参比溶液,依次加入0.6mL浓硫酸、10mL对二甲氨基苯甲醛溶液和10mL蒸馏水;另一支试管中的液体作为测试溶液,依次加入0.6mL浓硫酸、10mL对二甲氨基苯甲醛溶液和10mL 200mg·L-1的尿素标准溶液。一定温度下反应一定时间,测定所测试溶液的吸光度(基于参比溶液)。
1.4.3 正交实验
波长为426nm时,以反应得到的黄棕色溶液对应的吸光度为考核指标,以200mg·L-1尿素溶液用量、对二甲氨基苯甲醛用量、反应温度和浓硫酸用量为考察因素,每个因素选取3个水平,设计L9(34)正交实验,实验的因素和水平见表1。

表1 正交实验的因素与水平Tab.1 Factors and levels of orthogonal experiment
1.4.4 标准曲线的绘制
将配制好的100mg·L-1、200mg·L-1、300mg·L-1、400mg·L-1、500mg·L-1、600mg·L-1、700mg·L-1、800mg·L-1的尿素标准溶液在426 nm处按正交实验选出的最优条件进行测定,确定尿素浓度与吸光度之间的线性关系。
2 结果与讨论
2.1 最佳波长的选择
测得100mg·L-1、200mg·L-1尿素标准溶液的吸光度与吸收波长的关系曲线见图1。
由图1可以看出,尿素溶液与对二甲氨基苯甲醛反应得到的产物在426nm处有最大吸收峰。因此,选择426nm作为测定尿素浓度的最佳波长。
2.2 单因素实验结果
2.2.1 反应时间的影响
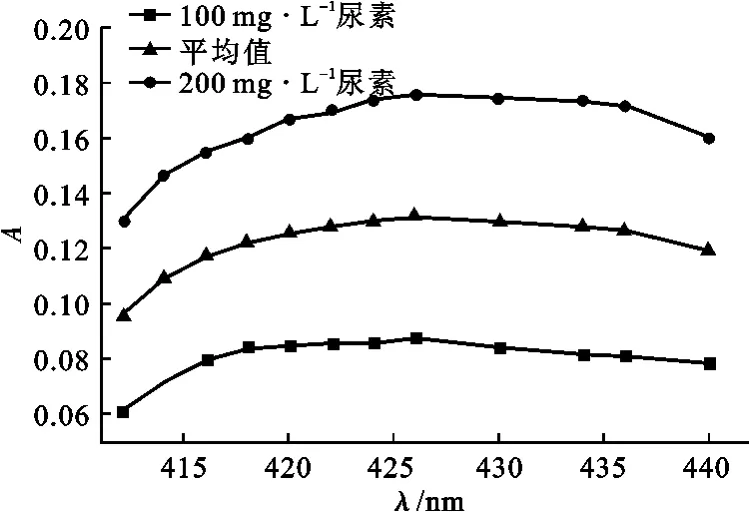
图1 尿素溶液吸光度与吸收波长关系曲线Fig.1 The relationship curves of absorbance and absorption wavelength for urea solutions
固定其它条件不变,常温下反应3min、6min、8min、10min、15min后进行测定,对应溶液的吸光度分别为0.1195、0.1196、0.1197、0.1198、0.1198。表明,当反应时间超过8min时,显色反应基本完成。这与文献[1,9]所得结论基本一致。
2.2.2 对二甲氨基苯甲醛用量的影响
固定其它条件不变,改变对二甲氨基苯甲醛的用量(3mL、6mL、10mL、14mL、18mL),常温下反应10min后进行测定,结果见图2。

图2 对二甲氨基苯甲醛用量对吸光度的影响Fig.2 Effect of PDAB amount on absorbance
由图2可知,当对二甲氨基苯甲醛用量为10mL时,吸光度最大。
2.2.3 浓硫酸用量和尿素用量的影响
固定其它条件不变,于40℃水浴中反应10min后进行测定,测得浓硫酸用量为0.4mL、0.6mL、1.0mL、1.2mL时对应溶液的吸光度分别为0.1153、0.1261、0.0842、0.0736,表明,随着浓硫酸用量的增加,吸光度先升后降,浓硫酸用量为0.6mL时吸光度最大;测得200mg·L-1尿素用量为5mL、10mL、15mL、20mL时对应溶液的吸光度分别为0.0973、0.1242、0.1049、0.1076,表明,随着尿素用量的增加,吸光度先升后降,200mg·L-1尿素用量为10mL时吸光度最大。
2.2.4 反应温度的影响
固定其它条件不变,在温度为25℃、30℃、40℃、50℃的水浴中反应10min后进行测定,结果见图3。

图3 反应温度对吸光度的影响Fig.3 Effect of reaction temperature on absorbance
由图3可知,反应温度为30℃时,对应溶液的吸光度最大。
2.3 测定条件的优化
根据单因素实验结果可知,反应时间对测定影响较小,其它因素影响较大。据此进行正交实验(表1),结果见表2。
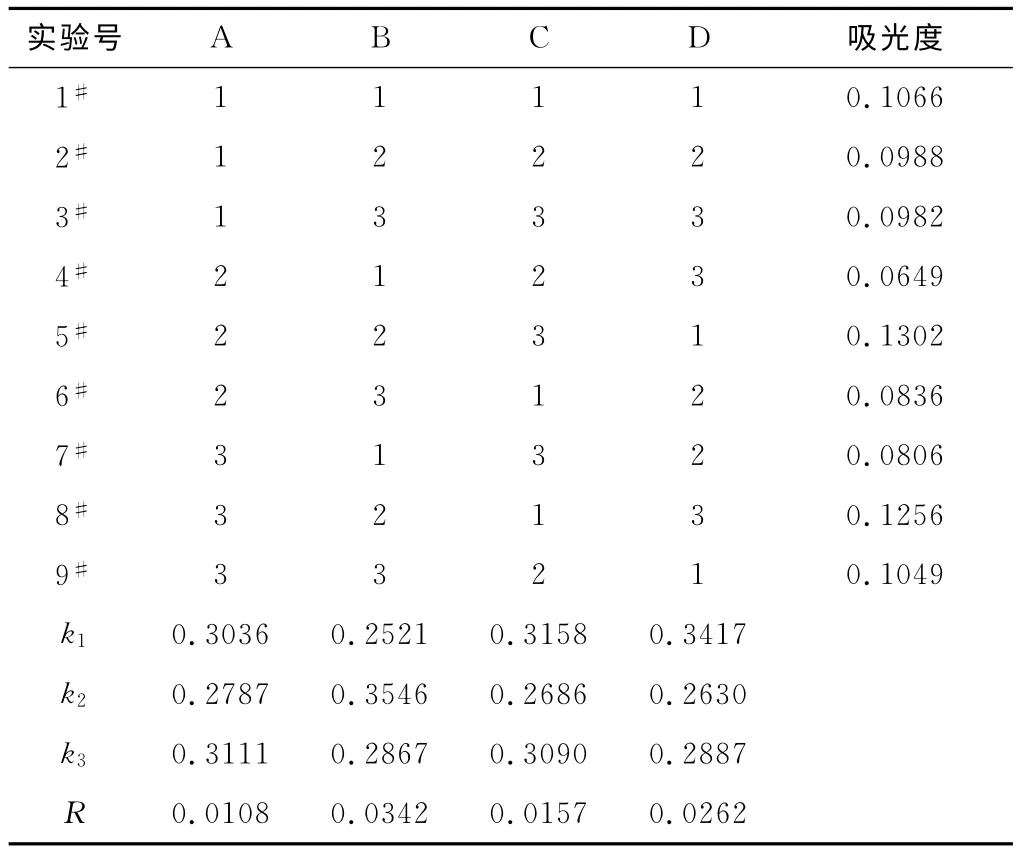
表2 正交实验结果与分析Tab.2 Result and analysis orthogonal experiment
由表2可以看出,各因素对吸光度的影响大小为:对二甲氨基苯甲醛用量>浓硫酸用量>反应温度>尿素用量。测定尿素浓度的最优组合为A3B2C1D1,即200mg·L-1尿素溶液用量为14mL、对二甲氨基苯甲醛用量为10mL、反应温度为30℃、浓硫酸用量为0.4mL。
2.4 重复性实验
取200mg·L-1尿素标准溶液,在两台分光光度计上按确定的最佳测定条件进行测定,每台分光光度计做4个重复实验,计算相对标准偏差,结果见表3。
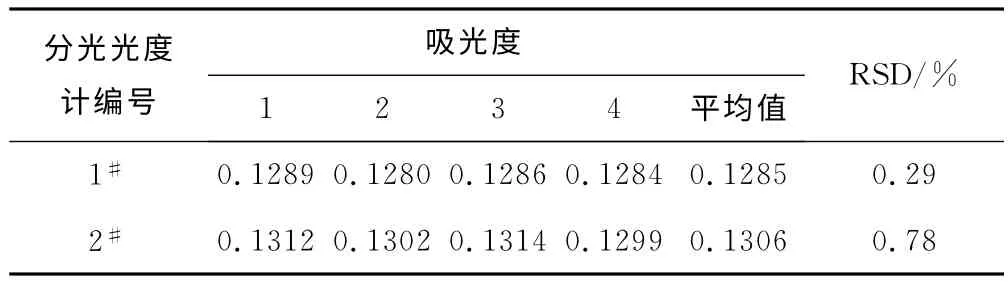
表3 重复性实验的测定结果Tab.3 Determination results of repetitive experiment
由表3可以看出,测定结果与正交实验结果基本吻合,相对标准偏差分别为0.29%和0.78%,说明本方法有较好的重复性。
2.5 标准曲线
绘制尿素浓度(c)与对应生成物的吸光度(A)的标准曲线,如图4所示。
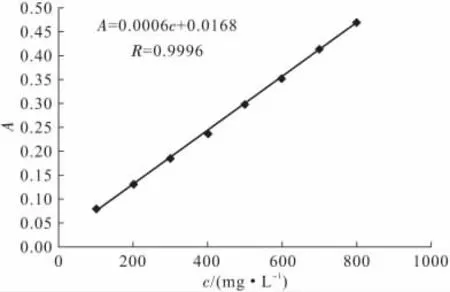
图4 尿素浓度与吸光度关系标准曲线Fig.4 Standard curve of relationship between urea concentration and absorbance
由图4可以看出,以426nm作为测定波长,尿素在100~800mg·L-1浓度范围内符合朗伯-比尔定律,计算得到尿素浓度与对应生成物的吸光度的线性回归方程:A=0.0006c+0.0168,相关系数R=0.9996,表明尿素浓度与吸光度具有良好的线性关系。
3 结论
运用对二甲氨基苯甲醛比色法测定溶液中尿素的浓度。通过单因素实验确定了主要的影响因素,并通过正交实验对尿素测定条件进行优化。结果表明:测定尿素的最佳波长为426nm;在该波长下,最优测定条件为:200mg·L-1尿素溶液用量14mL、对二甲氨基苯甲醛用量10mL、反应温度30℃、浓硫酸用量0.4mL。尿素浓度在100~800mg·L-1范围内与吸光度呈现良好的线性关系,线性回归方程为A=0.0006c+0.0168,相关系数R=0.9996。该方法操作方便、快速、准确度高、重现性好,能够用于溶液中尿素浓度的测定。
[1]苗晓杰,蒋恩臣,王佳,等.对二甲氨基苯甲醛显色分光光度法检测水溶液中常微量尿素[J].东北农业大学学报,2011,42(8):87-92.
[2]翟少伟.二乙酰一肟法测定乳尿素氮的研究[J].湖北农业科学,2010,49(3):686-687,691.
[3]杨仁杰,刘蓉,徐可欣.基于中红外光谱检测牛奶中掺杂的尿素[J].光谱学与光谱分析,2011,31(9):2383-2385.
[4]杜昌文,周健民.水溶液中微量尿素的测定[J].土壤肥料,2002,(4):41-43.
[5]施伟红.改良二乙酰一肟-安替比林法测定游泳池水中尿素[J].中国卫生检验杂志,2008,18(7):1319-1320.
[6]唐明江,刘宗林,王剑.游泳池水中尿素测定方法的研究[J].中国卫生检验杂志,2008,18(4):641-642.
[7]武金凤,郭志刚,郝美艳.饲料中尿素测定方法的研究[J].中国农业科技导报,2008,10(增2):87-93.
[8]刘志刚,赵庆良,孙丽欣,等.PDAB比色法直接测定液相中的常量尿素[J].哈尔滨工业大学学报,2008,40(8):1214-1217.
[9]李敏,郑长立,张勇.对二甲氨基苯甲醛比色法测定解析废液中的微量尿素[J].化工技术与开发,2005,34(3):42-43.
[10]陈录华.对二甲氨基苯甲醛法测定常量尿素[J].大氮肥,1998,21(6):422-424.

