血清视黄醇结合蛋白4与2型糖尿病视网膜病变的相关性
赵丽君,王薇
(哈尔滨医科大学附属第二医院内分泌代谢病科,黑龙江哈尔滨 150086)
糖尿病视网膜病变(diabetic retinopathy,DR)是糖尿病患者最常见、最严重的并发症之一,也是患者生活质量下降和致盲的重要原因之一,发病率高,但其发病机制和影响因素多而复杂。血清视黄醇结合蛋白4(RBP4)是一种由肝脏合成的分泌性视黄醇结合蛋白,新近发现其还可以由脂肪细胞分泌而被称为脂肪细胞因子[1]。RBP4可以转运血循环中的视黄醇,与视网膜上的RBP4受体结合后释放视黄醇进入视网膜,推测RBP4也有引起视网膜血管内皮细胞功能紊乱的可能,从而参与视网膜病变的发生发展。我们对2型糖尿病(type 2 diabetes,T2DM)患者是否合并有视网膜病变进行病例对照研究,现报道如下。
1 资料与方法
1.1 一般资料
选择2010年9月至2012年6月间我院内分泌代谢病科住院的T2DM患者192例和我院体检中心正常糖调节者59例。将受试对象分为健康对照组(N组,n=59)和2型糖尿病组,后者再根据是否合并糖尿病视网膜病变分为糖网组(DR组,n=103)和非糖网组(NDR组,n=89)。检测各对象空腹血糖(fasting blood sugar,FBS)、糖化血红蛋白(glycosylated hemoglobin A 1 c,HbA1c)、空腹胰岛素(fasting insulin,FINS)、甘油三酯(triglyceride,TG)、总胆固醇(total cholesterol,TC)、低密度脂蛋白胆固醇(low-density lipoprotein cholesterol,LDL-C)、高密度脂蛋白胆固醇(highdensity lipoprotein cholesterol,HDL-C)、尿微量白蛋白(microalbuminuria,mALB)、尿肌酐(urine creatinine,UC)、尿微量白蛋白/肌酐(microalbuminuria/creatinine,A/C)和血清RBP-4水平;采集收缩压(systolic blood pressure,SBD)、舒张压(diastolic blood pressure,DBP)、体质量指数(body mass index,BMI)、腰臀比(waist hip ratio,WHR)、体脂数(body fatter ratio,BFR)和稳态模型下的胰岛素抵抗指数(HOMA-IR)。
1.2 方法
1.2.1 化验检查 全自动生化仪检测RBP-4、FBS、TCH、TG、HDL-C、LDL-C;高压液相层析法检测 HbA1c;化学免疫发光法检测FINS、F-C肽、mALB、UC。根据公式计算稳态模型胰岛素抵抗指数(HOMA-IR)=FBS ×FINS/22.5,BMI=体质量/身高2。
1.2.2 DR的诊断 入院后给予散瞳后眼底全方位彩色摄像并储存,最后由本院眼科的一名主任医师根据存储图像采用1985年中华医学会眼科学会全国统一的诊断标准做出诊断。
1.3 统计学处理
2 结 果
2.1 实验各组的一般资料比较
见表1。

表1 3组对象一般临床资料的比较Tab 1 Commparison of clinical data of three groups
N组与NDR组及DR组相比,在年龄、病程、BMI、WHR、SBP、DBP、HbA1c、FBS、FINS、HOMA-IR、T-CH、TG、HDL-C、RBP4、mALB和尿A/C上的差异均有统计学意义(P<0.05),在BFR和LDL-C上差异无统计学意义(P>0.05);NDR组与DR组相比,在年龄、病程、RBP4、mALB和尿 A/C上差异有统计学意义(P<0.05);N组的UC水平与NDR组相比差异有统计学意义(P<0.05),而DR组与NDR组相比,UC水平的差异无统计学意义(P>0.05)。
2.2 多因素分析
见表2。
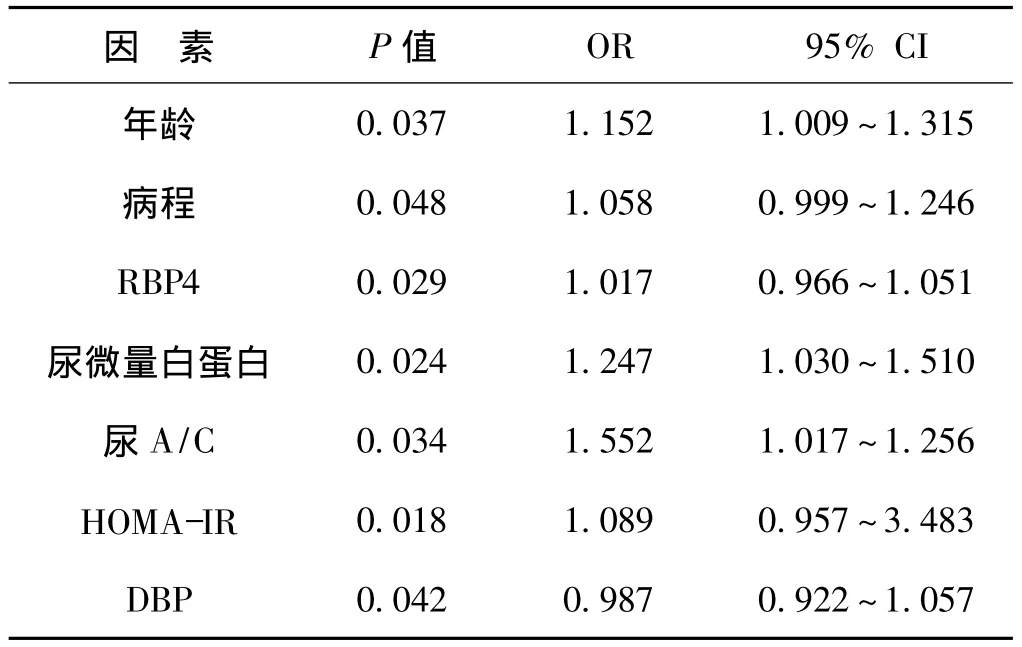
表2 Logistic多元回归分析结果Tab 2 Results of Logistic multiple regression
Logistic多元回归分析结果显示,年龄、病程、RBP4、mALB、尿A/C、HOMA-IR是T2DM患者发生DR的独立危险因素,DBP是T2DM患者DR发生的保护性因素。
3 讨 论
本研究显示,T2DM患者不管是否合并 DR其HOMA-IR、RBP4、mALB和尿A/C均高于正常健康者;更重要的是合并有DR患者的年龄、病程、RBP4、mALB和尿A/C水平明显高于未合并DR患者。经过Logistic多元回归分析后发现,年龄、病程、RBP4、mALB、尿A/C、HOMA-IR是T2DM患者发生DR的独立危险因素,DBP和体脂数是T2DM患者DR发生的保护性因素。DR的病理生理改变主要为基底膜增厚、微血管瘤形成、内皮细胞增生、血-视网膜屏障破裂、毛细血管闭塞、新生血管形成等[2]。目前具体的发病机制未明,主要学说有非酶性糖基化蛋白终产物沉积学说、氧化应激学说、生长因子学说、多元醇代谢旁路及内质网应激学说和炎症学说等[3]。RBP4是2005年发现的一种新型脂肪细胞因子,研究发现其参与了代谢综合征、IR和T2DM及其并发症的发生发展[1]。RBP4的生理功能是在体内运输维生素A的特异运载蛋白,从而在协助维生素A发挥生理作用的过程中起着重要作用[4]。DR患者与非DR患者相比,增殖性视网膜病变的患者较背景性视网膜病变的患者血清RBP4水平显著升高,随着2型糖尿病患者病程进展,血清RBP4水平逐渐增高,推测RBP4不仅参与了DR的发生发展,而且可能成为诊断DR和治疗方面的新指标[5]。也可能是因为RBP4浓度过高导致视网膜微血管内皮功能紊乱,其机制可能是通过抑制血管内皮细胞中胰岛素活性,加上患者胰岛素抵抗,血管舒张因子NO释放减少,影响血管功能状态[6]。血清RBP4的水平与IR成正比[7],因此RBP4与高胰岛素对视网膜微血管的共同作用就促进着DR的进展。mALB和尿A/C是糖尿病肾病早期诊断的有效指标,糖尿病肾病也属于微血管病变,因此可以通过检测mALB和尿A/C以早期发现和诊断DR。最近研究表明挪威和亚洲等地相似,mALB水平与DR有着密切联系,并且低水平的mALB就具有预测DR发生和进展的作用,检测 mALB 安全便宜[8]。
综上所述,DR逐渐成为多发病,临床表现反应时间缓慢,早期诊断困难,临床治疗效果不满意,若不有效控制危险因素,可反复发作直至失明。除了积极控制血糖、血脂、血压等高危因素之外,血清 RBP4、HOMA-IR、mALB和尿A/C对DR发生发展可能的负面作用也应受到重视,并且这些指标的出现往往早于临床表现,因此可能成为DR检测的指标。本研究的结果尚须大样本的前瞻性研究来进一步证实。
[1]YANG Q,GRAHAM T E,MODY N,et al.Serum retinal binding protein 4 contributes to insulin resistance in obesity and type 2 diabetes[J].Nature,2005,436(7049):356-362.
[2]罗利彬,潘佳秋,于学静,等.2型糖尿病视网膜病变患者血清RBP4水平变化及其与胰岛素抵抗的关系研究[J].黑龙江医药科学,2012,35(2):7-8.
[3]李朝辉,吕林,马玲.糖尿病视网膜病变中细胞凋亡的研究进展[J].现代生物医学进展,2009,9(21):4158-4160.
[4]TRAYHURN P,WOOD I S.Adipokines:inflammation and the pleiotropic role of white adipose tissue[J].Br J Nuti,2004,92(3):347-355.
[5]LI Z Z,LU X Z,LIU J B,et al.Serum retinol-binding protein 4 levels in patients with diabetic retinopathy [J].J Int Med Res,2010,38(1):95-99.
[6]PARK S E,KIM D H,LEE J H,et al.Retinol-binding protein-4 is associated with endorthelial dysfunction in adults with newly diagnosed type 2 diabetes mellitus[J].Atherosclerosis,2009,204(1):23-25.
[7]KOTNIK P,FISCHER-POSOVSKY P,WABITSCH M.RBP4:a controversial adipokine[J].Eur J Endocrinol,2011,165(5):703-711.
[8]BERTELSEN G,PETO T,LINDEKLEIV H,et al.Tromso eye study:prevalence and risk factors of diabetic retinopathy[J/OL].Acta Ophthalmologica,2012,doi:10.1111/J.1755-3768.2012-2542.x

